Изучение токсического действия на организм белых крыс и кроликов композиции лечебных средств
Автор: Идиятов И.И., Галяутдинова Г.Г., Халикова К.Ф., Ямалова Г.Р., Маланьев А.В.
Статья в выпуске: 1 т.245, 2021 года.
Бесплатный доступ
В статье представлены материалы по изучению токсичности комплекса лечебнопрофилактических средств, включающего холин хлорид, янтарную кислоту, ксимедон, сорбитол, суспензию молочно и пропионовокислых микроорганизмов, на организм лабораторных животных в опыте на белых крысах и кроликах. На основании результатов первичного скрининга средство рекомендуется для устранения последствий токсикозов животных, гепатопротекции и коррекции обмена веществ. По результатам проведенных исследований было установлено, что данная композиция в соответствии с существующей классификацией является малотоксичной, местного раздражающего действия на слизистые оболочки глаз и кожу не оказывает, кумулятивными свойствами не обладает, следовательно, имеет перспективы для дальнейшего исследования.
Композиция, острая токсичность, белые крысы, кролики
Короткий адрес: https://sciup.org/142229114
IDR: 142229114 | УДК: 619:616-099-02:632 | DOI: 10.31588/2413-4201-1883-245-1-55-60
Study of the toxic effect on the organism of white rats and rabbits of the composition of medicines
The article presents materials on the study of the toxicity of a complex of therapeutic and prophylactic agents, including choline chloride, succinic acid, xymedon, sorbitol, a suspension of lactic and propionic acid microorganisms, on the organism of laboratory animals in the experiment on white rats and rabbits. Based on the results of primary screening, the agent is recommended for eliminating the consequences of animal toxicosis, hepatoprotection and metabolic correction. According to the results of the studies, it was found that this composition, in accordance with the existing classification, is low-toxic, does not have a local irritating effect on the mucous membranes of the eyes and skin, does not possess cumulative properties, therefore, has prospects for further research.
Текст научной статьи Изучение токсического действия на организм белых крыс и кроликов композиции лечебных средств
Интенсификация промышленности приводит к росту воздействия на окружающую среду различных физических, химических, биологических и других факторов. При этом в кормах и пищевых продуктах появляются токсичные соединения, которые в дальнейшем проникают во внутреннюю среду организма [4].
Центральным органом, нейтрализующим токсические вещества и выводя- щим их из организма является печень. Являясь самой крупной железой, данный орган выполняет огромное количество различных физиологических функций. Печень способна восстанавливать свои пораженные клетки, путем регенерации и замещения новыми, сохраняя при этом свои основные функции. Однако и эта совершенная система подвержена поражениям [1]. Механизмы ее повреждения многообраз- ны, но приводят к повреждению гепатоцитов, что сопровождается цитолизом, воспалительной реакцией и развитием фиброза [7]. Токсиканты могут проявлять как прямое токсическое действие на печень и организм в целом, так и оказывать пагубное воздействие, претерпевая изменения в процессе метаболизма. При поражении печени под угрозу ставится функционирование всего организма, поэтому своевременное лечение и профилактика заболеваний печени являются очень важными. Актуальность проблемы разработки комплекса лечебно-профилактических средств для лечения патологии печени продиктована разнообразием форм и факторов воздействия на орган, а также постоянным возникновением новых видов опасных патогенов [2, 3, 4].
По результатам первичного отбора компонентов средства для устранения последствий токсикозов, гепатопротекции и коррекции обмена веществ был сформирован комплекс, включающий холин хлорид, янтарную кислоту, ксимедон, сорбитол, суспензию молочно- и пропионовокислых микроорганизмов [7, 8, 9].
Целью работы явилось изучение общего токсического действия средства, рекомендуемого для устранения последствий токсикозов, гепатопротекции и коррекции обмена веществ, на организм лабораторных животных.
Материал и методы исследований. Исследования проведены в отделении токсикологии ФГБНУ «ФЦТРБ-ВНИВИ» в соответствии с нормативными документами [5].
Острую токсичность лечебнопрофилактической композиции оценивали в опыте на 25 белых крысах массой тела 190-220 г, из которых было сформировано 5 групп по 5 животных в каждой. Крысам опытных групп однократно перорально вводили препарат в виде суспензии на 0,9 % растворе натрия хлорида: первой группе животных в дозе 500 мг/кг массы тела (в объеме 5 мл/кг массы тела), второй группе – 1000 мг/кг (10 мл/кг), третьей – 1500 мг/кг (15 мл/кг), четвертой – 2000 мг/кг (20 мл/кг). Крысам контрольной группы однократно перорально вводили
0,9 % раствор натрия хлорида в объеме 20 мл/кг массы тела. Животные содержались в контролируемых условиях вивария с соблюдением санитарно-гигиенических требований, имели свободный доступ к воде и корму. После проведения манипуляций за подопытными крысами вели наблюдение по общепринятой схеме в течение 14 дней.
Изучение кумулятивных свойств препарата проводили на 10 белых крысах массой тела 140-170 г. Суспензию препарата на 0,9 % растворе натрия хлорида ежедневно перорально вводили животным в определенном объеме в зависимости от массы тела и периода введения. Начиная с 1/10 от максимально вводимой дозы (2000 мг/кг массы тела) с увеличением в 1,5 раза в каждые последующие 4 дня. По прошествии 28 дней введения препарата за подопытными крысами вели наблюдение в течение 14 дней. После чего проводили эвтаназию животных декапитацией и патологоанатомическое исследование.
Раздражающее действие лечебнопрофилактического препарата изучали на 10 кроликах серой масти массой тела 2,63,2 кг, сформированных в 2 группы по 5 животных в каждой. Содержание кроликов проводили в условиях вивария, кормление осуществляли согласно зоотехническим нормам. Эксперимент заключался в оценке реакции слизистой оболочки глаза на воздействие препарата. Для этого на слизистую оболочку правого глаза закапывали суспензию препарата на 0,9 % растворе натрия хлорида в объёме 100 мкл (в концентрации 100 мг/мл), левый глаз служил контролем (100 мкл 0,9 % раствора натрия хлорида). Кроликам первой группы процедуру проводили однократно, животным второй группы – ежедневно на протяжении 7 дней. После закапывания препарата и ежедневно на протяжении 14 дней визуально оценивали состояние слизистой оболочки, склеры и роговицы.
Изучение характера кожнорезорбтивного действия препарата осуществляли наложением накожных аппликаций в опыте на кроликах светлой масти массой тела 2,2-2,5 кг, разделенных на 2 группы по 5 животных в каждой. Для этого на симметричных участках спины кроликов по обе стороны от позвоночника за день до опыта шерсть выстригали, участок аппликации составлял 25 см2. На правый бок животного при помощи шпателя наносили суспензию препарата на растительном масле, левая сторона служила контролем (было нанесено масло). Кроликам первой группы аппликации проводили однократно с продолжительностью наложения 4 часа, второй группе – ежедневно в течение 7 дней. После проведения процедуры осуществляли оценку кожной реакции. Мониторинг клинического состояния подопытных животных вели на протяжении последующих 14 суток.
Результат исследований. В эксперименте по установлению острой токсичности композиции лечебнопрофилактического действия было отме- чено, что пероральное введение водной суспензии препарата во всех испытуемых дозах не вызывало изменений в клиническом состоянии животных, отклонений со стороны поведенческих реакций, не приводило к гибели. На этом основании и в соответствии с руководством по проведению лабораторных испытаний определить смертельную дозу препарата не представляется возможным.
По причине того, что не представляется возможным ввести в желудок крысы большой объем жидкости и отсутствие видимых клинических признаков интоксикации, исследуемый препарат возможно классифицировать как малотоксичный и отнести к IV классу опасности «незначительно опасные вещества» (по ГОСТ 12.1.007-76 «Вредные вещества»).
Таблица 1 – Результаты определения острой токсичности композиции
|
Группа |
Наименование |
Падеж |
|
Опыт 1 |
Препарат в дозе 500 мг/кг массы тела |
отсутствует |
|
Опыт 2 |
Препарат в дозе 1000 мг/кг массы тела |
отсутствует |
|
Опыт 3 |
Препарат в дозе 1500 мг/кг массы тела |
отсутствует |
|
Опыт 4 |
Препарат в дозе 2000 мг/кг массы тела |
отсутствует |
|
Контроль |
0,9 % раствор натрия хлорида |
отсутствует |
Таблица 2 – Результаты определения степени кумуляции композиции
|
Период введения, дн. |
Суточная доза, мг/кг массы тела |
Суммарная доза за период введения, мг/кг массы тела |
Суммарная доза по периодам введения, мг/кг массы тела |
Падеж |
|
1-4 |
200 |
800 |
800 |
отсутствует |
|
5-8 |
300 |
1200 |
2000 |
отсутствует |
|
9-12 |
450 |
1800 |
3800 |
отсутствует |
|
13-16 |
680 |
2720 |
6520 |
отсутствует |
|
17-20 |
1010 |
4040 |
10560 |
отсутствует |
|
21-24 |
1520 |
6080 |
16640 |
отсутствует |
|
25-28 |
2280 |
9120 |
25760 |
отсутствует |
В ходе эксперимента по оценке кумулятивных свойств препарата не наблюдалось изменений в поведении подопытных крыс, они охотно поедали корм, выглядели клинически здоровыми, на внешние раздражители реакция была сохранена, падежа отмечено не было. Результаты при- ведены в таблице 2.
По результатам патологоанатомического исследования подопытных животных кровоизлияний, жидкости в полостях и изменений во внутренних органах выявлено не было. Коэффициент кумуляции композиции определяли по формуле:
К кум = общая суммарная доза / максимально вводимая доза
Коэффициент составил 12,88 (25760/2000), следовательно, кумулятив- ный эффект у исследуемого препарата отсутствует.
При однократном и многократных ежедневных закапываниях водной суспензии комплекса на слизистую оболочку гла- за патологических изменений слизистой оболочки, склеры и роговицы отмечено не было (Рисунок 1).
Следовательно, раздражающим действием препарат не обладает.
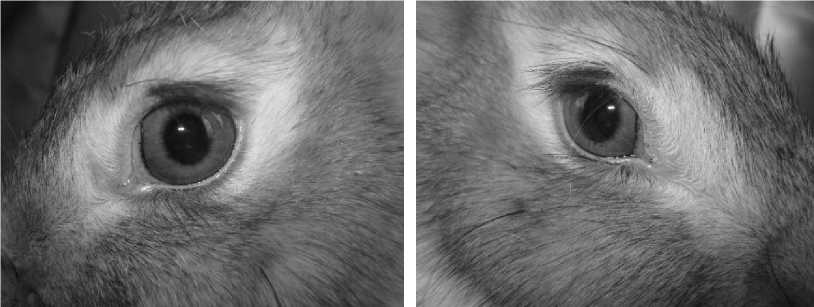
Рисунок 1 – Оценка раздражающего действия композиции на слизистую оболочку глаза (слева – контроль, справа — опыт)
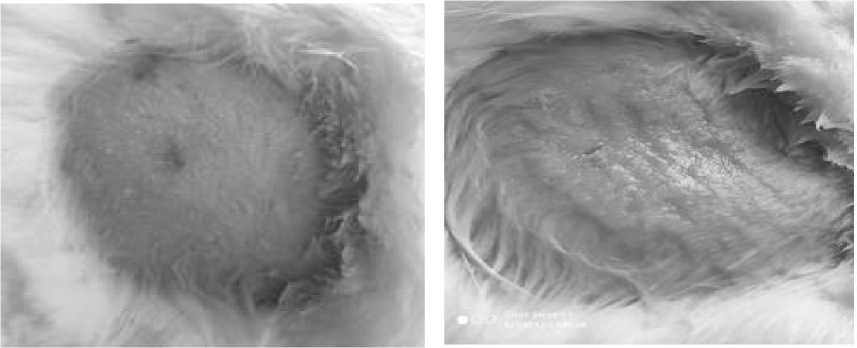
Рисунок 2 – Определение кожно-резорбтивного действия композиции в опыте на кроликах
(слева - контроль, справа – опыт)
Однократные и многократные накожные нанесения препарата функциональных изменений в виде болезненности, повышения местной температуры, отека, трещин, эритемы или изъязвлений не вызывали (Рисунок 2).
Изменений в поведении и общем клиническом состоянии подопытных животных в последующие 14 суток наблюдения отмечено не было.
Заключение. В результате проведенных исследований установлено, что композиция, включающая холин хлорид, янтарную кислоту, ксимедон, сорбитол, суспензию молочн- и пропионовокислых микроорганизмов, рекомендуемая для устранения последствий токсикозов жи- вотных, гепатопротекции и коррекции обмена веществ, при краткосрочном и длительном применении, не вызывает явных клинических признаков токсикоза, не оказывает местного раздражающего и кожнорезорбтивного действия, не обладает кумулятивными свойствами.
Резюме
В статье представлены материалы по изучению токсичности комплекса лечебнопрофилактических средств, включающего холин хлорид, янтарную кислоту, ксимедон, сорбитол, суспензию молочн- и пропионовокислых микроорганизмов, на организм лабораторных животных в опыте на белых крысах и кроликах. На основании результатов первичного скрининга средство рекомендуется для устранения последствий токсикозов животных, гепа-топротекции и коррекции обмена веществ. По результатам проведенных исследований было установлено, что данная композиция в соответствии с существующей классификацией является малотоксичной, местного раздражающего действия на слизистые оболочки глаз и кожу не оказывает, кумулятивными свойствами не обладает, следовательно, имеет перспективы для дальнейшего исследования.
Список литературы Изучение токсического действия на организм белых крыс и кроликов композиции лечебных средств
- Губеева, Е.Г. Изучение гистоструктуры печени цыплят-бройлеров при хронической интоксикации имидаклопридом на фоне применения сорбентов / Е.Г. Губеева, К.Ф. Халикова, Д.В. Алеев [и др.] // Ветеринарный врач. - 2019. - № 1. - С. 8-12.
- Гилдимырадов, Т. Определение острой и хронической токсичности углеводно-витаминно-минерального концентрата "Лизунец солевит" (лакто элита) на белых мышах / Т. Гилдимырадов // Сборник: Молодежные разработки и инновации в решении приоритетных задач АПК. Материалы Международной научной конференции студентов, аспирантов и учащейся молодежи. - 2019. - С. 26-28.
- Егоров, В.И. Патоморфологические исследования органов крыс при отравлении тиаклопридом и применении лечебных средств / В.И. Егоров, К.Ф. Халикова, Д.В. Алеев [и др.] // Ветеринарный врач. - 2017. - № 3. - С. 35-39.
- Егоров, В.И. Изучение эффективности лечебных средств при отравлении белых крыс неоникотиноидным пестицидом / В.И. Егоров, К.Ф. Халикова, Г.Р. Ямалова [и др.] / РЖ "Проблемы ветеринарной санитарии, гигиены и экологии". - Москва. - 2018. - № 1 (25). - С. 90-94.
- Идиятов, И.И. Оценка воздействия пробиотических штаммов на инфузорий" / И.И. Идиятов, С.Р. Хабирова, А.М. Тремасова [и др.] // Ветеринарный врач. - 2020. - № 3 - С. 12-16.
- Миронов, А.Н. Руководство по проведению доклинических исследований лекарственных средств. Часть первая. / А.Н. Миронов [и др.]. - М.: Изд. "Гриф и К", - 2012. - 944 с.
- Никитин, И.Г. Гепатопротекторы: мифы и реальные возможности / И.Г. Никитин // Фарматека. - 2007. - № 3. - С. 14-18.
- Портнов, О.В. Влияние биологически активных кормовых добавок на росто-весовые параметры и биохимические показатели сыворотки крови цыплят-бройлеров / О.В. Портнов, Э.К. Папуниди, И.И. Идиятов, Г.Ш. Закирова // Ветеринарный врач. - 2014. - № 6. - С. 56-59.
- Тремасова, А.М. Токсикологическая оценка консорциума микроорганизмов для использования с целью повышения качества кормов / А.М. Тремасова [и др.] // Вестник Марийского государственного университета. - 2020. - № 3. - С. 2127.
- Хабирова, С.Р. Оценка безопасности выделенных из природных биотопов молочнокислых бактерий путем биотестирования на простейших и культуре клеток / С.Р. Хабирова [и др.] // Российский журнал "Проблемы ветеринарной санитарии, гигиены и экологии". - 2020. - № 1 (33). - С. 67-72.


