Извлечение ионов тяжелых металлов клетками Rhodococcus ruber ИЭГМ 231
Автор: Костина Л.В., Куюкина М.С., Ившина И.Б.
Журнал: Вестник Пермского университета. Серия: Биология @vestnik-psu-bio
Рубрика: Микробиология
Статья в выпуске: 2, 2013 года.
Бесплатный доступ
Подобраны оптимальные условия аккумуляции ионов тяжелых металлов клетками Rhodococcus ruber ИЭГМ 231, с учетом физико-химических (исходная концентрации ионов металла, температура, диапазон активной кислотности, источник углерода и энергии) и био -логических (стадия роста и исходная концентрация клеток родококков) факторов, обеспечивающих до 95.0% извлечения ионов тяжелых металлов из среды культивирования родокок-ков.
Тяжелые металлы, родококки, аккумуляция
Короткий адрес: https://sciup.org/147204635
IDR: 147204635 | УДК: 579.22+579.695
Optimal conditions for heavy metal ion extraction by Rhodococcus ruber IEGM 231
Optimal conditions for heavy metal ion accumulation by Rhodococcus ruber IEGM 231 based on physico-chemical (initial metal ion concentration, temperature, active acidity range, source of carbon and energy) and biological (growth stage and initial Rhodococcus cell concentration) factors were determined. Those conditions enabled up to 95% extraction of heavy metal ions from the cultural medium.
Текст научной статьи Извлечение ионов тяжелых металлов клетками Rhodococcus ruber ИЭГМ 231
В последние годы большое внимание исследователей привлекает способность микроорганизмов накапливать ионы тяжелых металлов (ТМ), что обусловлено их важной ролью в биогеохимической циркуляции вещества и энергии [Fredrickson, Romine, 2005]. Металлы и радионуклиды эффективно сорбируются широким кругом микроорганизмов: микроводорослями [Cai et al., 1995, 1999], грибами [Magyarosy et al., 2002; Wang, Chen, 2009] и бактериями [Gadd, 1990; Peitzsch et al., 1998], принадлежащими к различным систематическим группам [Wang, Chen, 2009].
Проблема взаимодействия ТМ с клетками микроорганизмов исследуется в нескольких направлениях, связанных с изучением изменений биохимических, физиологических и генетических особенностей микроорганизмов при контакте с металлами. Достаточно подробно исследованы способы проникновения и места локализации ТМ в бактериальных клетках, влияние физиологических параметров культуры и внешних условий на накопление ионов ТМ [Dopson et al., 2003; Harms, 2007]. Выявлено, что на процесс извлечения ионов ТМ из среды культивирования влияют изменения параметров окружающей среды: температура, диапазон активной кислотности, источник углерода и другие факторы [Perkins, Gadd, 1995].
Все большую экологическую значимость приобретают представители класса Actinobacteria
[Stackebrandt, Rainey, Ward-Rainey, 1997], биологической особенностью которых является способность к окислению углеводородов. Они занимают доминирующее положение в экстремальных местообитаниях и обладают широкими метаболическими возможностями. Несмотря на то, что биология алканотрофных актинобактерий сейчас находится в центре внимания исследователей, работы, касающиеся изучения особенностей процесса потребления ТМ клетками актинобактерий рода Rhodococcus, единичны [Пешкур, Ившина, 2003; Dabbs, Sole, 1988; Mirimanoff, Wilkinson, 2000; Bell et al., 2004].
Цель настоящего исследования - оценка основных физико-химических и биологических факторов, определяющих условия поглощения ионов ТМ клетками родококков. Конкретные задачи исследования - подбор оптимальных условий эффективного извлечения ионов ТМ с учетом температуры, pH, концентрации ТМ, источника углерода, а также возраста и концентрации исходной культуры.
Материалы и методы
В качестве модельного объекта исследования использовали штамм R. ruber ИЭГМ 231 из Региональной профилированной коллекции алканотрофных микроорганизмов (акроним ИЭГМ, No. 768 во Всемирной федерации коллекций культур; Каталог штаммов..., 1994; , выделенный из грунтовых вод в районе Ольховского нефте-
промысла, Пермской области, Россия. Выбор данного бактериального штамма обусловлен его высокой устойчивостью к ионам ТМ [Костина, Куюкина, Ившина, 2010]. Предварительные исследования показали, что минимальные ингибирующие бактериальный рост концентрации ионов ТМ составляют 2.5 и 5.0 мМ для ионов МоО42" и Ni2+, соответственно, при выращивании культуры в мясопептонном бульоне, а также 10.0 и 20.0 мМ для ионов МоО42" и Ni2+, соответственно, при выращивании культуры в минеральной среде с н-гексадеканом.
Родококки выращивали в жидкой минеральной среде, содержащей (в г/л): КН2РО4 - 1.0; (МН4)2НРО4 - 1.5; MgSO,*H2O - 0.2; FeSO4*H2O -0.01; ZnSO4"$H2O - 0.002. Компоненты питательной среды растворяли в водном растворе солей ТМ: (МН4)6Мо7О24х4Н2О или NiSO4x7H2O, в концентрации 0.6-10.0 мМ, приготовленных на бидистилли-рованной воде. В качестве единственного источника углерода использовали ацетат аммония - 2.0 г/л, глюкозу -5.0 г/л, н-гексадекан или н-додекан, в концентрации 3.0 об.%. При изучении влияния диапазона активной кислотности на процесс аккумуляции ТМ применяли буферные растворы: 20 мМ янтарная кислота - NaOH (pH 4.5-5.5); 20 мМ Na-фосфатный (pH 6.0-8.5) и 20 мМ боратный (pH 9.010.0).
Посевным материалом служила бактериальная культура, предварительно выращенная в мясопептонном бульоне в течение 2 сут. Из полученной биомассы готовили инокулят, который вносили в количестве, обеспечивающем начальную оптическую плотность суспензии 0.1-3.0х109 клеток/мл. Родококки выращивали в условиях периодического культивирования в колбах Эрленмейера объемом 250 мл на орбитальном шейкере (120 об/мин), при температуре 18-28W в течение 2 сут. Пробы для измерений отбирали по 5 мл через 1, 3, 6, 9, 12, 22, 24 и 48 ч. Клеточную биомассу отделяли центрифугированием (20 мин, 3000 об/мин) в лабораторной стационарной центрифуге, после чего дважды отмывали деионизированной водой.
В экспериментах по изучению механизма поглощения ионов ТМ использовали живые и инактивированные путем автоклавирования (0.5 атм., 20 мин) бактериальные клетки. Контролем служил раствор металла без внесения исследуемой культуры, а также бактериальная культура, выращенная в питательной среде без добавления ионов металла.
О поглощающей способности родококков судили по степени исчезновения ионов ТМ из среды, определяемой по формуле: (СНач-СКон/СНач)'*00%, где Снач - исходная; Скон - конечная концентрация ТМ в среде культивирования. Одновременно регистрировали количество МоО42" и Ni2+, поглощенных клеточной биомассой. Для этого суспензию клеток осаждали центрифугированием (3000 об/мин; 20 мин), тщательно отмывали (до отсутствия ионов ТМ в промывных водах) бидистиллятом и разрушали ультразвуком (23 кГц; 0.7 А) с помощью низкочастотного гомогенизатора (Soniprep 150, Sanyo, Япония), в течение 15 мин в условиях охлаждения суспензии. Гомогенаты бактериальных клеток центрифугировали при 3000 об/мин в течение 20 мин. Полученные супернатанты анализировали на присутствие ионов МоО42" или Ni2+. Коэффициент биоаккумуляции определяли по формуле Свнугр/Скнеш, где С,, „я, - количество внутриклеточного металла, мкг/г; СВнеш - количество металла в культуральной среде, мкг/мл.
Физиологическое состояние бактериальной культуры контролировали по изменению оптической плотности клеточной суспензии и приросту биомассы. Оптическую плотность (ОП6оо) измеряли спектрофотометрически (/=600 нм) с помощью спектрофотометра (Lambda EZ201 (UV/Vis), Perkin-Elmer, США), кюветы с толщиной поглощающего слоя /=10 мм. Накопление биомассы фиксировали весовым и нефелометрическим методом. Контроль чистоты использованной в работе культуры родококков осуществляли методом прямого высева на МПА и визуально, просматривая препараты в световом фазово-контрастном микроскопе (Axiostar plus, CARL ZEISS, Германия).
Количественное определение молибдена проводили фотометрическим роданидным методом, никеля диметилглиоксимным - с помощью спектрофотометра при длине волны Х=470 нм [Лурье, 1984].
Все эксперименты проводили в трех- или пятикратной повторностях в зависимости от условий проведения эксперимента. Математическую обработку полученных результатов осуществляли традиционными методами с вычислением среднего арифметического, среднеквадратичного отклонения, стандартной ошибки и доверительного интервала с использованием пакета компьютерных программ Statistica, версия 6.0 для Windows (StatSoft Inc., 2001), и Excel 2003 (Microsoft Inc., 2003).
Результаты и их обсуждение
По нашим данным, коллекционный штамм R. ruber ИЭГМ 231 обладает способностью к извлечению ионов ТМ. Уровень потребления ионов ТМ зависит как от их исходной концентрации в среде культивирования, так и источника углерода (таблица). Как видно из таблицы, ТМ, присутствующие в среде культивирования в форме катионов извлекаются в среднем в 1.2 раза более эффективно по сравнению с таковыми анионной формы. Максимальное извлечение МоО42" и Ni2+ родокок-ками выявляется при исходной концентрации ТМ в среде культивирования от 0.6 до 2.5 мМ. Следует отметить, что аккумулирующая активность сохраняется и при повышенных (до 10.0 мМ) концентрациях ионов ТМ в среде культивирования. Из дан- ных, представленных в таблице, следует, что родо-кокки при росте на углеводородсодержащих питательных средах, а также в присутствии глюкозы более эффективно извлекают ионы ТМ по сравнению с ацетатом аммония в качестве единственного источника углерода и энергии. Несмотря на то. что степень извлечения ТМ из среды с углеводородами сопоставима с таковой в присутствии глюкозы.
временной промежуток. за который фиксируется максимум поглощения ТМ бактериальными клетками. в 12-24 раза короче при выращивании в среде с глюкозой. Эго позволяет проводить экспрессные исследования по поиску актинобактерий - активных биоаккумуляторов ионов ТМ с использованием глюкозосодержащей минеральной среды.
Влияние концентраций ТМ и источника углерода на степень (%) извлечения ионов МоО42- и Ni2+ клетками R. ruber ИЭГМ 231
|
Концентрация ТМ. мМ |
Источник углерода |
|||
|
Ацетат аммония |
и-Додекан |
н-Гексадекан |
Глюкоза |
|
|
МоО42 |
||||
|
0.6 |
55.3±2.14 |
80.3±1.20 |
98.3±1.26 |
91.7±0.32 |
|
1.3 |
44.6±1.21 |
73.2±1.14 |
90.3±1.18 |
82.6±0.27 |
|
2.5 |
20.3±1.12 |
58.4±1.26 |
74.6±1.28 |
68.3±1.00 |
|
5.0 |
12.5±0.34 |
32.6±0.86 |
38.7±2.22 |
34.Ш.12 |
|
10.0 |
10.4±0.18 |
28.4:0.44 |
30.2±0.84 |
27.2±0.68 |
|
№2+ |
||||
|
0.6 |
77.2±1.11 |
94.5±2.27 |
100.1±0.08 |
100.2±0.24 |
|
1.3 |
62.8±1.72 |
86.4±1.64 |
98.7±0.88 |
92.2±0.16 |
|
2.5 |
24.7±1.53 |
67.2±2.48 |
91.5±1.10 |
81.3±1.12 |
|
5.0 |
18.3±1.16 |
38.7±1.62 |
54.4±1.88 |
46.4±2.20 |
|
10.0 |
14.4±0.58 |
30.3±0.44 |
36.6±0.68 |
31.3±0.96 |
Примечание. Время культивирования, при котором зафиксирована максимальная степень извлечения ионов МоО42: 6 ч - ацетата аммония, глюкозы, 72 ч - и-додекана, н-гексадекана; Ni2+: 3 ч - ацетата аммония, глюкозы, 72 ч -н-додекана, н-гексадекана.
Изучение влияния температуры культивирования родококков на эффективность процесса аккумуляции ТМ показало, что максимальное извлечение ионов МоОу и Ni* наблюдается при температуре 28°С (рис. 1). Следует отметить, что данные результаты совпадают с температурным оптимумом для извлечения радиоактивных ионов Cs* показанным нами ранее в работе [Ившина. Пешкур. Коробов. 2002].
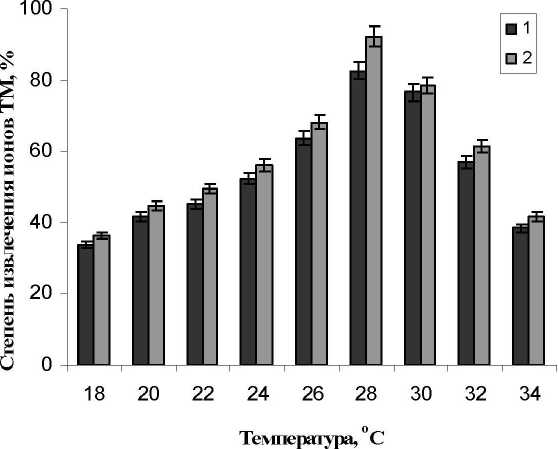
Рис. 1. Влияние температуры на степень извлечения ионов ТМ (1.3 мМ) клетками R. ruber ИЭГМ 231. Варианты опыта: 1 - поглощение ионов МоО42"; 2 - поглощение ионов Ni2*
На рис. 2 приведены результаты экспериментов по изучению влияния диапазона активной кислотности на интенсивность извлечения ионов ТМ. Установлено, что наиболее высокая степень поглощения ионов ТМ родококками получена при близких к нейтральным (6.0-7.5) значениях pH.
Как видно из рис. 3. фазы роста бактериальной культуры в среде, содержащей ионы ТМ. замедляются от 1.3 до 10.0 раз. Так. период лат-фазы, за который культура адаптируется к условиям среды и подготавливается к периоду быстрого размножения в среде без ТМ. составляет 3 ч. тогда как в присутствии ионов ТМ процесс адаптации к среде культивирования удлиняется в 2 раза и составляет 6 ч. Экспоненциальная фаза роста и размножения бактериальной культуры завершается к 10-12 ч при росте в среде без добавления ионов ТМ. тогда как в присутствии ТМ переход культуры в стационарную фазу начинается лишь после 18-22 ч культивирования.
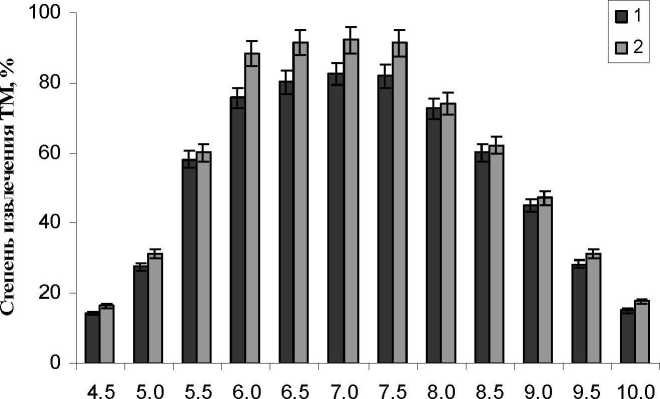
Диапазон акпшной кислотности, pH
Рис. 2. Влияние показателя активной кислотности на степень извлечения ТМ (1.3 мМ) клетками родококков.
Варианты опыта: 1 - поглощение ионов МоОД 2 - поглощение ионов NP*
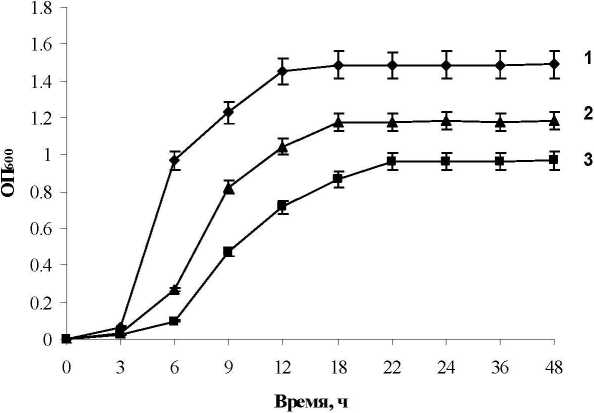
Рис. 3. Влияние ионов ТМ (1.3 мМ) на динамику роста клеток родококков.
Варианты опыта: 1 - контроль (минеральная среда с глюкозой); 2 - среда с ионами Ni2+; 3 - среда с ионами ' МоОг..... '
На рис. 4 представлены результаты опытов по ТМ (МоО42" и Ni2+) клетками R. ruber ИЭГМ 231. определению интенсивности поглощения ионов отобранных в разные стадии роста. По нашим дан- ним. родококки извлекают максимальное (до 92.2%) количество ионов никеля из среды культивирования в случае использования клеток, пребывающих в логарифмической фазе роста. Наибольшее извлечение молибдат ионов регистрируется при использовании клеток, пребывающих в экспоненциальной фазе роста.
На рис. 5 приведены результаты процесса извлечения ионов ТМ в зависимости от плотности бактериальной культуры. Так. при исходной концентрации клеток, равной 2.0 г сухого веса клеток/л среды культивирования, извлечение ионов ТМ достигает максимального (до 95%) уровня. Использование более высокой плотности бактериальных клеток не приводит к значительному увеличению (не более, чем на 0.5%) интенсивности извлечения ионов ТМ. Таким образом, в результате проведенных исследований показано, что максимальный уровень извлечения ионов ТМ наблюдается при посевной дозе 2.0 г сухого веса клеток/л среды.
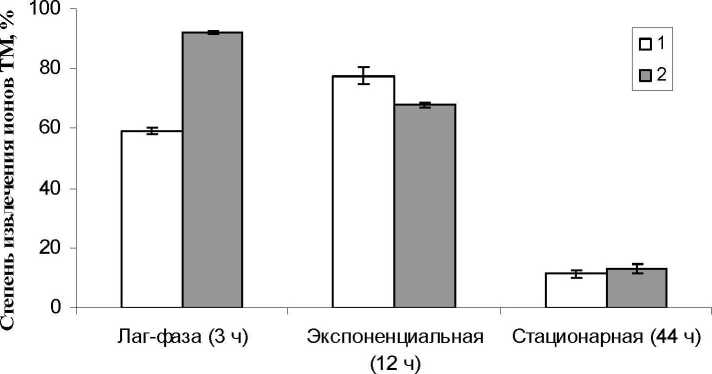
Стадии роста
Рис. 4. Влияние фазы роста клеток родококков на степень поглощения ионов ТМ (1.3 мМ).
В экспериментах использовали эквивалентное количество бактериальных клеток. Варианты опыта: 1 -поглощение ионов МоО4 * 2 - поглощение ионов Ni®
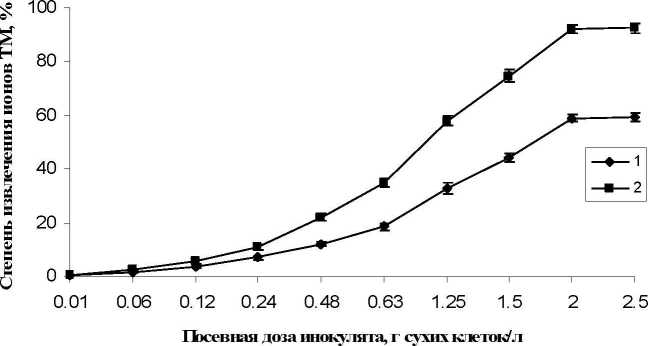
Рис. 5. Влияние исходной концентрации бактериальных клеток/?, ruber ИЭГМ 231 на степень поглощения ионов ТМ (1.3 мМ).
Варианты опыта: 1 - поглощение МоО42" через 6 ч культивирования; 2 - поглощение Ni2+ через 3 ч культивирования
В работе были изучены пути поступления ионов ТМ (МоО42" и Ni*). а также выявлены основные закономерности процесса их накопления живыми и мертвыми клетками родококков (рис. 6). Как видно из рис. 6. коллекционная культура
R. ruber ИЭГМ 231 обладает способностью поглощать как катионы, так и анионы ТМ. По данным сравнительных опытов с живыми и автоклавированными клетками R. ruber ИЭГМ 231. установлено. что уровень аккумуляции ионов ТМ в 9.4-10.0
раз ниже инактивированными, чем живыми клетками. В сравнительных опытах с использованием живых и автоклавированных клеток родококков установлено, что интенсивное поглощение ионов Ni2+ происходит в течение первых 3 ч, тогда как поглощение ионов МоО?" - в течение первых 6 ч эксперимента (рис. 6). В дальнейшем живые клетки начинают постепенно (до 60.0% от накопленного) выбрасывать аккумулированные ранее молиб ден и никель, в то время как инактивированные клетки стабильно удерживают от 6.0 до 13.0% связавшихся с ними ионов ТМ. На основании полученных данных можно заключить, что до 83.2% аккумулирующей активности приходится на способность концентрировать ионы молибдена энергозависимым образом, то есть биоаккумулированием.
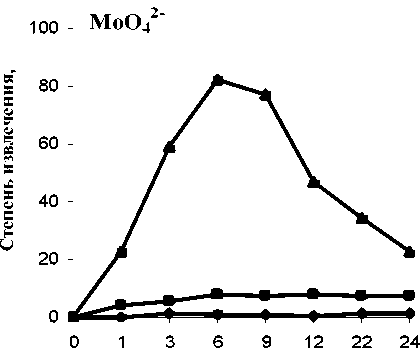
Рис. 6. Аккумуляция ионов ТМ живыми и инактивированными клетками R. ruber ИЭГМ 231
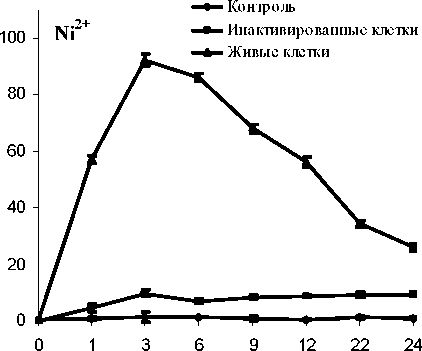
Увеличение времени взаимодействия с ионами ТМ до 48 ч не приводит к возрастанию их содержания в бактериальных клетках. В дальнейшем эта величина или не изменяется, или уменьшается, то есть ионы металла поступают из бактериальных клеток вновь в среду культивирования. При этом концентрация ионов ТМ в родококках снижается до уровня, который наблюдается в результате процесса биосорбции (6.0-13.0%).
Заключение
В результате проведенных исследований установлено, что коллекционный штамм R. ruber ИЭГМ 231 обладает способностью аккумулировать ионы ТМ. Процесс поглощения тяжелых металлов родо кокками является комплексным и осуществляется посредством пассивного связывания клеточными структурами и активного транспорта. Полученные данные позволяют утверждать, что значительная часть процесса поглощения ионов ТМ клетками родококков обеспечивается активным транспортом. Максимальное извлечение катионов ТМ наблюдается в логарифмической, анионов - в экспоненциальной фазе роста родококков. Определены оптимальные условия для эффективного извлечения ионов ТМ клетками родококков: температура, диапазон активной кислотности, источник углерода и энергии, стадия роста и исходная концентрация клеток родококков, обеспечивающие до 95.0-100.0% извлечения ионов тяжелых металлов из среды культивирования. Интенсивное (до 100.0%) извлечение ионов ТМ из среды культивирования происходит при следующих условиях: присутствие ТМ в среде в концентрациях до 10.0 мМ, при 26-30W; pH 6.0-7.5; в присутствии н-гексадекана или глюкозы и при исходной концентрации бактериальной культуры 2.0 г сухого веса клеток/л среды.
Работа выполнена при поддержке программ фундаментальных исследований Президиума РАН «Живая природа» (проект № 12-П-4-1044 ) и «Молекулярная и клеточная биология» (проект № 12-П-4-1052).
Список литературы Извлечение ионов тяжелых металлов клетками Rhodococcus ruber ИЭГМ 231
- Ившина И.Б., Пешкур Т.А., Коробов В.П. Эффективное извлечение цезия клетками бактерий рода Rhodococcus//Микробиология. 2002. Т. 71, № 3. С. 418-423
- Каталог штаммов Региональной профилированной коллекции алканотрофных микроорганизмов/под ред. И.Б. Ившиной. М.: Наука, 1994. 163 с
- Костина Л.В., Куюкина М.С., Ившина И.Б. Биосорбция, аккумуляция и способы извлечения тяжелых металлов. LAP Lambert Academic Publishing, 2010. 254 c
- Лурье А. Аналитическая химия промышленных вод. М.: Химия, 1984. 448 с
- Пешкур Т.А., Ившина И.Б. Особенности аккумуляции цезия бактериальными клетками Rhodococcus ruber при росте на н-гексадекане//Экология. 2003. № 1. С. 84-86
- Bell J.M.L. et al. Methods evaluating vanadium tolerance in bacteria isolated from crude oil contaminated land//J. Microbiol. Methods. 2004. Vol. 58. P. 87-100
- Cai X.H. et al. Application of eukaryotic algae for the removal of heavy metals from water//Molecular Marine Biol. Biotechnol. 1995. Vol. 4. P. 338344
- Cai X.H. et al. Growth and heavy metal binding properties of transgenic algae (Chlamydomonas reinhardtii) expressing a foreign metallothionein gene//Int. J. Phytoremediation. 1999. Vol. 1. P. 53-65
- Dabbs E.R., Sole G.J. Plasmid-borne resistance to arsenate, arsenite, cadmium, and chloramphenicol in a Rhodococcus species//Mol. Gen. Genom. 1988. Vol. 211, № 1. P. 148-154
- Dopson M. et al. Growth in sulfidic mineral environments: metal resistance mechanisms in acidophilic microorganisms//Microbiology. 2003. Vol. 149. P. 1959-1970
- Fredrickson J.K., Romine M.F. Genome-assisted analysis of dissimilatory metal-reducing bacteria//Curr. Opin. Biotechnol. 2005. Vol. 16. P. 269274
- Gadd G.M. Metal tolerance//Microbiol. Extreme Environ. Open University Press, Milton Keynes, 1990. P. 178-210.
- Magyarosy A. et al. Nickel accumulation and nickel oxalate precipitation by Aspergillus niger//Appl. Microbiol. Biotechnol. 2002. Vol. 59. P. 382-388
- Mirimanoff N., Wilkinson K.J. Regulation of Zn accumulation by a freshwater gram-positive bacterium (Rhodococcus opacus)//Environ. Sci. Technol. 2000. Vol. 34. P. 616-622
- Peitzsch N., Eberz G., Nies D.H. Alcaligenes eutrophus as a bacterial chromate sensor//Appl. Environ. Microbiol. 1998. Vol. 64, № 2. P. 453458
- Perkins J., Gadd G.M. The influence of pH and external K+ concentration on cesium toxicity and accumulation in Escherichia coli and Bacillus subtilis//J. Ind. Microbiol. 1995. Vol. 14, № 3-4. P. 218-225
- Stackebrandt E., Rainey F.A., Ward-Rainey N.L. Proposal for a new hierarchic classification system, Actinobacteria classis nov.//Int. J. Syst. Bacteriol. 1997. Vol. 47, № 2. P. 479-491
- Wang J., Chen C. Biosorbents for heavy metals removal and their future//Biotechnol. Advances. 2009. Vol. 27. P. 195-226
- Harms H. Biosensing of heavy metals//Microbiol. Monogr. 2007. Vol. 6. P. 143-157


