Эффективность филграстима в лечении цитостатических миелосупрессий у больных раком молочной железы
Автор: Хричкова Т.Ю., Гольдберг В.Е., Жданов В.В., Матяш М.Г., Высоцкая В.В., Симолина Е.И., Шаталова В.А., Попова Н.О., Мирошниченко Л.А.
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Клинические исследования
Статья в выпуске: 1 (25), 2008 года.
Бесплатный доступ
Изучали гематологические эффекты препарата гранулоцитарного колониестимулирующего фактора - филграстима (нейпогена) при его включении в химиотерапию больных раком молочной железы III-IV стадии по схеме адриабластин + таксотер. Проведенные исследования продемонстрировали стимуляцию подавленного цитостатиками костномозгового гранулоцитопоэза под действием нейпогена на уровне коммитированных предшественников, морфологически дифференцируемых элементов костного мозга и периферической крови.
Рак молочной железы, химиотерапия, миелосупрессия, филграстим (нейпоген)
Короткий адрес: https://sciup.org/14056739
IDR: 14056739 | УДК: 618.19-006.6+615.28+616.155.344
Filgastrim efficacy in treatment of cytostatic myelossuppressions for breast cancer patients
Hematologic effects of Filgastrim (granulocyte colony-stimulating factor) were studied for stage III-IV breast cancer patients who simultaneously received chemotherapy with adriablastin + taxofer. Filgastrim administration resulted in stimulation of bone marrow granulocytopoesis suppressed by cytostatic drugs on the level of committed progenitor cells, morphologically differentiated elements of bone marrow and peripheral blood.
Текст научной статьи Эффективность филграстима в лечении цитостатических миелосупрессий у больных раком молочной железы
Многочисленные клинические исследования продемонстрировали высокую эффективность доцетаксела в комбинации с антрациклинами в лечении диссеминированного рака молочной железы (РМЖ), что, по мнению ряда авторов, позволяет считать вышеназванную комбинацию новым стандартом химиотерапии распространенных форм РМЖ [4, 10]. Частым осложнением при использовании как доцетаксела, так и доксорубицина является угнетение костномозгового кроветворения, в большей степени гранулоцитарного ростка, что проявляется, соответственно, развитием лейкопении с преимущественным снижением в периферической крови количества нейтрофильных гранулоцитов. Анализ данных, полученных многочисленными исследователями, подтверждает факт развития нейтропении III–IV степени у 85–100 % больных, а фебрильной нейтропении – у 30–40 % пациентов, подвергнутых цитостатической терапии в указанном режиме [8]. Учитывая несомненную клиническую значимость последствий миелосупрессии, назначение филграстима как гемостимулирующего средства довольно часто оказывается необходимым и оправданным [9, 11].
В связи с изложенным целью настоящей работы явилось изучение эффективности фил- грастима в качестве корректора нарушений, возникающих в системе крови у больных раком молочной железы (РМЖ) III–IV стадии при проведении противоопухолевой химиотерапии по схеме доксорубицин + доцетаксел, и вскрытие механизмов, лежащих в основе гемостимулирующего эффекта препарата.
Материал и методы
В исследование включены результаты изучения системы крови 77 больных раком молочной железы III–IV стадии в возрасте от 35 до 55 лет. Все пациентки получали противоопухолевую полихимиотерапию, включающую внутривенное введение 50 мг/м2 доксорубицина (адриа-бластина) в 1-й день и 75 мг/м2 доцетаксела (таксотера) – во 2-й день. Длительность цикла составляла два дня, интервал между курсами – 3 нед. Показатели системы крови оценивали на протяжении 3 курсов химиотерапии. Наряду с указанным лечением, 30 больных в перерывах между курсами специального лечения получали филграстим (нейпоген) подкожно в дозе 300 мкг двукратно на 8-й и 12-й день от последнего введения таксотера [11]. Больные, не получавшие нейпогена в процессе химиотерапии, составили контрольную группу.
Материал для исследования (капиллярную и венозную кровь) забирали до и после каждого цикла цитостатического лечения. Проведение преднизолоновых проб и стернальных пункций было запланировано до начала специального лечения, а также перед II и III курсами химиотерапии. Определение показателей периферической крови (гемоглобин, эритроциты, лейкоциты, лейкоцитарная формула, тромбоциты) и дифференциальный подсчет миело-грамм в стернальных пунктатах производили стандартными гематологическими методами [3]. Колониеобразующую способность костного мозга и периферической крови определяли путем клонирования клеток – предшественников грануломоноцитопоэза (КОЕ-ГМ) и эритропоэза (КОЕ-Э) в полувязкой питательной среде на основе метилцеллюлозы [2].
Для оценки костномозгового резерва нейтрофильных гранулоцитов использовали преднизолоновую пробу [6]. Преднизолон (фирма «Гедеон Рихтер», Венгрия) вводили внутривен- но в дозе 60 мг. Общее количество лейкоцитов (ОКЛ) и содержание сегментоядерных форм нейтрофилов определяли до, а также через 2, 3, 4, 5 и 6 ч после введения препарата. Результат пробы оценивали по величине выброса нейтрофильных гранулоцитов в процентах от исходного уровня, отмечали величину максимального выброса нейтрофилов в процентах и абсолютных числах.
Статистическую обработку полученных данных проводили методом вариационной статистики с использованием t-критерия Стьюдента.
Результаты и обсуждение
Проведенные исследования показали, что общее количество лейкоцитов у обследованных пациентов закономерно уменьшилось (на 49,1 % от исходного) уже после I курса химиотерапии (рис. 1А). Развившаяся лейкопения была обусловлена преимущественно снижением абсолютного числа сегментоядерных нейтрофилов (рис. 1Б). К началу второго курса лечения ОКЛ в группе пациентов, получавших нейпоген, оказалось достоверно выше как исходного уровня, так и значений данного показателя в контрольной группе (на 2,44 Г/л), благодаря увеличению содержания в периферической крови сегментоядерных форм нейтрофильных гранулоцитов (рис. 1А, Б).
После 2-го курса химиотерапии также был зафиксирован достоверно более высокий уровень лейкоцитов в периферической крови больных, леченных нейпогеном, за счет не только сегментоядерных нейтрофилов, но также лимфоцитов и моноцитов. В динамике дальнейшего лечения, после второго курса введения препарата-корректора, уровни ОКЛ и их сегментоядерных форм в периферической крови больных, получавших инъекции гемопоэтина, статистически значимо превышали аналогичные показатели в контрольной группе (рис. 1А, Б). В то же время препарат гранулоцитарного колониестимулирующего фактора практически не оказывал влияния на содержание в периферической крови больных РМЖ эритроцитов, гемоглобина и тромбоцитов в процессе химиотерапии.
Анализ стернальных пунктатов выявил увеличение содержания незрелых нейтрофильных
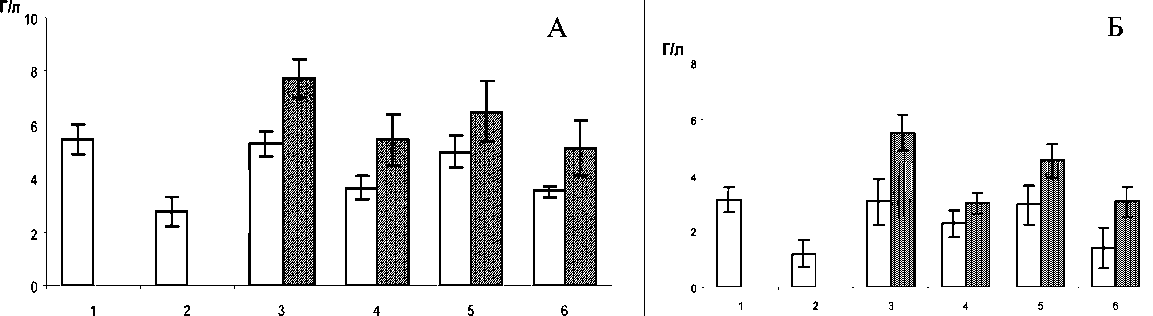

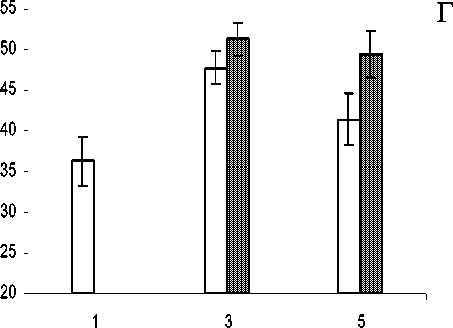
Рис. 1. Изменения общего количества лейкоцитов (А), сегментоядерных нейтрофилов (Б) в периферической крови, незрелых (В) и зрелых форм нейтрофильных гранулоцитов (Г) в костном мозге у больных РМЖ в динамике противоопухолевой химиотерапии по схеме адриабластин + таксотер ( z ) и адриабластин + таксотер + нейпоген ( ). По оси абсцисс – сроки исследования (1 – до лечения, 2 – после 1-го курса, 3 – перед 2-м курсом, 4 – после 2-го курса, 5 – перед 3-м курсом, 6 – после 3-го курса), по оси ординат – значения показателя; доверительные интервалы при р<0,05
гранулоцитов (миелобласты, промиелоциты, миелоциты, метамиелоциты) в кроветворной ткани больных РМЖ после введения нейпогена к началу второго курса химиотерапии на 14,3 % (p<0,05) по сравнению с таковым в контрольной группе (рис. 1В). При этом наблюдалось достоверное увеличение количества зрелых нейтрофильных гранулоцитов как перед вторым (на 7,4 %), так и перед третьим (на 19,4 %) курсами специального лечения (рис. 1Г). Это обстоятельство, возможно, обусловлено отсутствием значительных повреждений комбинацией адриабластина с таксотером способных к митозу предшественников гранулоцитопоэза, что создает основу для активации в костном мозге регенераторных процессов под влиянием гемостимулятора на ранних этапах цитостатической болезни [1]. В то же время со стороны эритроидного ростка костномозгового кроветворения отмечалась депрессия числа незрелых и зрелых эритрокариоцитов (в среднем в 1,45 раза), по сравнению с группой контроля, что, вероятно, связано со смещением баланса процессов кроветворения в сторону гранулоцито-поэза под влиянием нейпогена.
Определение колониеобразующей способности костного мозга подтвердило высказанные предположения, продемонстрировав достоверное увеличение содержания к началу второго и третьего курсов полихимиотерапии в комбинации с нейпогеном числа КОЕ-ГМ на 14 % и 56,6 % соответственно в сравнении с контрольной группой, что свидетельствует об активации процессов пролиферации гемопоэтических прекурсоров под влиянием препарата цитокина. В то же время в группе больных, не
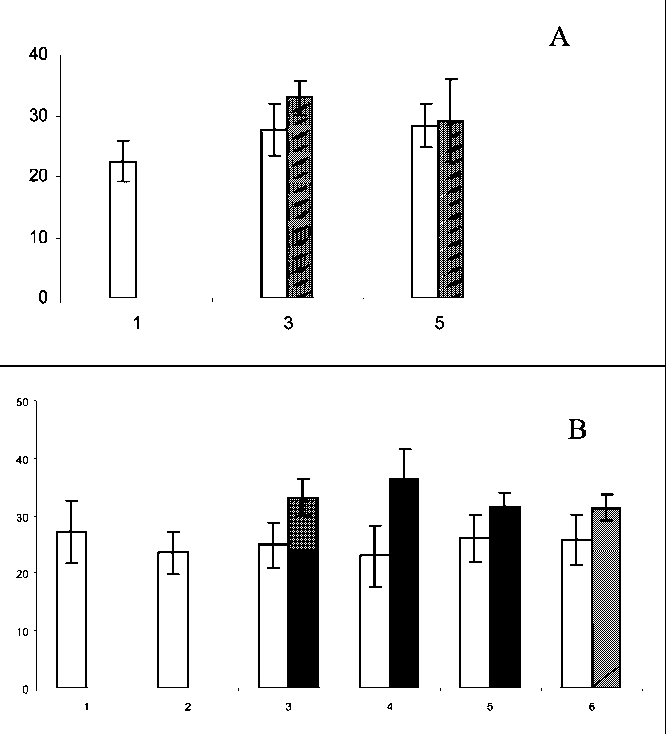
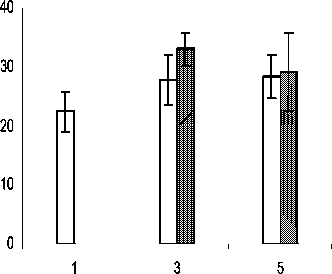
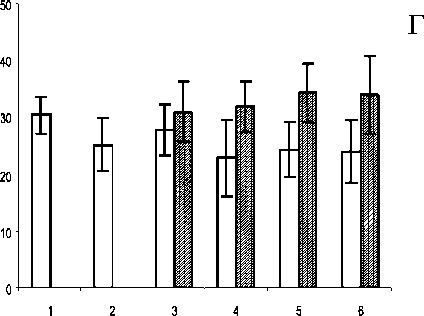
Рис. 2. Количество КОЕ-ГМ (А) и КОЕ-Э (Б) в костном мозге, а также КОЕ-ГМ (В) и КОЕ-Э (Г) в периферической крови больных раком молочной железы в динамике противоопухолевой химиотерапии с использованием режимов адриабластин + таксотер ( z ), либо адриабластин + таксотер + нейпоген ( ■ ). По оси абсцисс – сроки исследования (1 – до лечения, 2 – после 1-го курса, 3 – перед 2-м курсом, 4 – после 2-го курса, 5 – перед 3-м курсом, 6 – после 3-го курса), по оси ординат – значения показателя; доверительные интервалы при р<0,05
получавших препарата-корректора, значения вышеназванных показателей достоверно превышали исходный уровень лишь перед вторым курсом специального лечения (рис. 2А). Что касается клеток-предшественников эритропоэза, то, несмотря на некоторую тенденцию к росту числа КОЕ-Э в исследуемой группе по сравнению с контрольной, изменения оказались недостоверными (рис. 2Б).
Динамике возрастания числа гранулоцитомакрофагальных клеток-предшественников в костном мозге под влиянием нейпогена соответствовали изменения их количества в периферической крови, что проявлялось достоверным ростом (с максимумом после второго курса в 1,6 раза) числа циркулирующих КОЕ-ГМ во все сроки исследования в сравнении с контрольной группой (рис. 2В). Подобная тенденция имела место и в отделе циркулирующих клеток-пред- шественников эритропоэза – число КОЕ-Э в периферической крови больных, леченных нейпогеном, в среднем в 1,4 раза превышало аналогичный показатель в контрольной группе практически во все сроки наблюдения. Приведенные факты могут быть обусловлены, наряду с усилением пролиферативной активности коммитированных предшественников в костном мозге, перераспределительными реакциями в системе крови под действием нейпогена, поскольку обнаруженные изменения соответствуют картине мобилизации кроветворных прекурсоров из костного мозга в периферическую кровь. Как известно, мобилизирующий эффект препарата гранулоцитарного колониестимулирующего фактора достаточно широко используется в клинической практике с целью сбора CD34+ клеток для последующей аутологичной трансплантации [7].
Таблица
Прирост содержания нейтрофилов (Г/л) и их максимальный выброс в периферическуюкровь в ответ на введение преднизолона в процессе химиотерапии РМЖ (X¯±m)
|
Показатели |
Cроки исследования |
||||
|
До лечения |
Перед 2-м курсом |
Перед 3-м курсом |
|||
|
Динамика реакции (ч) |
До введения |
2,21 ±0,38 |
А |
3,10 ± 0,33 |
3,19 ± 0,38 |
|
Б |
3,40 ± 0,63 |
3,79 ± 0,58* |
|||
|
2-й |
3,88 ± 0,63 |
А |
5,93 ± 0,72* |
6,38 ± 0,71* |
|
|
Б |
9,76 ± 1,09*# |
8,55 ± 0,51*# |
|||
|
3-й |
4,27 ± 0,75 |
А |
6,23 ± 0,67 |
7,06 ± 0,78* |
|
|
Б |
9,23 ± 0,74*# |
9,65 ± 0,41*# |
|||
|
4-й |
4,51 ± 0,72 |
А |
6,57 ± 0,90 |
7,15 ± 0,92* |
|
|
Б |
8,70 ± 0,44*# |
9,41 ± 0,55*# |
|||
|
5-й |
4,22 ± 0,65 |
А |
7,88 ± 1,29* |
6,88 ± 0,82* |
|
|
Б |
8,16 ± 0,54* |
9,54 ± 0,96*# |
|||
|
6-й |
3,80 ± 0,70 |
А |
7,05 ± 1,03* |
6,42 ± 0,58* |
|
|
Б |
7,53 ± 0,48* |
8,73 ± 0,89*# |
|||
|
Максимальный выброс |
Г/л |
2,53 ± 0,43 |
А |
4,66 ± 0,84* |
5,42 ± 0,60* |
|
Б |
6,79 ± 0,53*# |
6,89 ± 0,35*# |
|||
|
% |
116,80 ± 17,06 |
А |
136,60 ± 23,15 |
181,50 ± 21,55* |
|
|
Б |
225,01 ± 29,04*# |
196,58 ± 24,22* |
|||
Примечание: А – режим адриабластин + таксотер; Б – режим адриабластин + таксотер + нейпоген; * – отличия от значения показателя до лечения достоверны (р<0,05); # – отличия между группами достоверны (р<0,05).
Одной из наиболее важных функциональных особенностей нейтрофилов костномозгового пула является их способность выходить в большом количестве в циркуляцию в ответ на введение глюкокортикоидов [6]. При введении преднизолона больным РМЖ нами было выявлено преходящее повышение числа нейтрофилов в периферической крови, что свидетельствует о наличии типичной реакции на гормональный препарат. При сравнительном анализе реакции на преднизолон костномозгового пула нейтрофильных гранулоцитов было установлено, что выраженность ее значительно возрастает (как перед 2-м, так и перед 3-м курсами химиотерапии) при использовании схемы адриабластин + таксотер в комбинации с нейпогеном по сравнению не только с исходными показателями (в 2–2,5 раза), но и с «чистой» схемой (в 1,4–1,5 раза). При этом достоверно выше в 1,5 раза перед вторым и в 1,3 раза – перед третьим курсами химиотерапии в комбинации с нейпогеном оказалась и величина максимального выброса нейтрофилов в ответ на введение преднизолона по сравнению с аналогичными показателями у больных, леченных по схеме адриабластин + таксотер без включения препарата-корректора (таблица).
Обсуждая возможные механизмы данного феномена, следует иметь в виду, что Г-КСФ стимулирует выработку ряда протеаз фермен- тативными системами нейтрофилов, ослабляющих связь клеток с внеклеточным матриксом, с одной стороны, а с другой – способствует наработке ростовых факторов, увеличивающих проницаемость эндотелия кровеносных сосудов костного мозга [5]. Кроме того, фактом, играющим немаловажную роль в усилении реакции на преднизолон на фоне включения нейпогена в программу цитостатического лечения, является накопление в костном мозге под влиянием гемопоэтина зрелых элементов гранулоцитарного ряда.
Таким образом, применение нейпогена на фоне химиотерапии по схеме адриабластин + таксотер приводит к возрастанию ОКЛ, подавленного цитостатическими препаратами, причем в большей степени за счет увеличения числа их сегментоядерных форм. В основе указанных изменений лежит стимуляция гранулоцитопоэза в костном мозге, обусловленная повышением активности морфологически дифференцируемых клеток и коммитированных предшественников. Кроме того, введение нейпогена приводит к усилению выхода в периферическую кровь гемопоэтических прекурсоров различных классов, возрастанию реакции костномозговых нейтрофилов на гормональный препарат и увеличению их пула.


