Эффективность гормональной терапии при синдроме инфантильных эпилептических спазмов у ребенка с перивентрикулярной лейкомаляцией и церебральным параличом: клинический случай
Автор: Эсентурова С.Э., Кадырова Б.Б., Кадырова А.Ш., Манапбаева Л.С., Кадыров Р.М.
Журнал: Бюллетень науки и практики @bulletennauki
Рубрика: Медицинские науки
Статья в выпуске: 4 т.12, 2026 года.
Бесплатный доступ
Синдром инфантильных эпилептических спазмов (СИЭС) относится к тяжелым формам эпилептических энцефалопатий раннего возраста и часто ассоциирован с неблагоприятным нейроразвитием. В статье представлен клинический случай ребенка с церебральным параличом, у которого на фоне фармакорезистентных эпилептических спазмов применение гормональной терапии привело к эффективному клинико-электроэнцефалографическому ответу. Данный случай подчеркивает значимость своевременной диагностики СИЭС и раннего назначения патогенетически обоснованного лечения.
Инфантильные эпилептические спазмы, гипсаритмия, гормональная терапия, детский церебральный паралич, перивентрикулярная лейкомаляция
Короткий адрес: https://sciup.org/14135157
IDR: 14135157 | УДК: 616.853-009.24:616.831-009.11-053.2:615.357 | DOI: 10.33619/2414-2948/125/26
Efficacy of Hormonal Therapy for Infantile Epileptic Spasm Syndrome in a Child with Periventricular Leukomalacia and Cerebral Palsy: A Clinical Case
Infantile epileptic spasms syndrome (IES) is a severe form of epileptic encephalopathy in infancy and is often associated with adverse neurodevelopmental outcomes. This article presents a clinical case of a child with cerebral palsy who, despite drug-resistant epileptic spasms, experienced an effective clinical and electroencephalographic response after hormonal therapy. This case highlights the importance of timely diagnosis of IES and early initiation of pathogenetically based treatment.
Текст научной статьи Эффективность гормональной терапии при синдроме инфантильных эпилептических спазмов у ребенка с перивентрикулярной лейкомаляцией и церебральным параличом: клинический случай
Бюллетень науки и практики / Bulletin of Science and Practice
Синдром инфантильных эпилептических спазмов (СИЭС) относится к наиболее тяжёлым формам возраст-зависимых эпилептических энцефалопатий раннего детского возраста [1, 2].
В ранее действовавших классификациях данное состояние было известно как синдром Веста, однако в соответствии с современной классификацией Международной противоэпилептической лиги (ILAE) используется термин «синдром инфантильных эпилептических спазмов», более точно отражающий клинико-электроэнцефалографическую сущность заболевания. Заболевание, как правило, дебютирует в первые два года жизни и характеризуется классической триадой признаков: эпилептическими спазмами, характерными электроэнцефалографическими изменениями по типу гипсаритмии и задержкой либо регрессом психомоторного развития [3].
Несмотря на достижения современной эпилептологии, СИЭС остаётся одной из ведущих причин развития фармакорезистентной эпилепсии, включая формирование синдрома Леннокса–Гасто, а также тяжёлых когнитивных и моторных нарушений в детском возрасте [4].
Этиология СИЭС является гетерогенной, однако в большинстве случаев носит структурный характер [5].
К наиболее частым причинам относятся гипоксически-ишемическое поражение головного мозга перинатального периода, перивентрикулярная лейкомаляция, врожденные пороки развития центральной нервной системы и генетически детерминированные энцефалопатии [6-8].
У детей с церебральным параличом риск развития инфантильных эпилептических спазмов существенно выше, при этом течение заболевания, как правило, отличается более выраженной фармакорезистентностью и неблагоприятным нейроразвитием [9, 10].
Электроэнцефалографически СИЭС ассоциирован с гипсаритмией — дезорганизованной высокоамплитудной асинхронной активностью с множественными мультифокальными эпилептиформными разрядами [4]. Длительное сохранение гипсаритмии рассматривается как независимый неблагоприятный прогностический фактор, поскольку она оказывает выраженное негативное влияние на созревание нейронных сетей и формирование высших корковых функций [11].
В связи с этим ключевое значение имеет не только купирование клинических приступов, но и достижение электроэнцефалографической ремиссии [3, 7].
Несмотря на широкое применение стандартных противоэпилептических препаратов, таких как вальпроевая кислота и леветирацетам, моно- или комбинированная противосудорожная терапия во многих случаях оказывается недостаточно эффективной при синдроме инфантильных эпилептических спазмов, особенно при структурной этиологии заболевания [6].
Это обусловлено тем, что традиционные противоэпилептические препараты преимущественно воздействуют на ионные каналы и синаптическую передачу, не влияя на ключевые патогенетические механизмы эпилептогенеза в незрелом головном мозге. В настоящее время гормональная терапия (адренокортикотропный гормон или системные глюкокортикостероиды) рассматривается как один из наиболее эффективных методов лечения инфантильных эпилептических спазмов, обеспечивающий быстрый клинический и электроэнцефалографический ответ [3].
Эффективность данного подхода связывают с модуляцией активности гипоталамо-гипофизарно-надпочечниковой оси и снижением экспрессии кортикотропин-рилизинг-гормона, обладающего проэпилептогенным действием в развивающемся мозге. Подавление патологической нейрональной гипервозбудимости и синхронизации нейронных сетей способствует быстрому регрессу гипсаритмии и купированию эпилептических спазмов. Рандомизированные клинические исследования демонстрируют преимущество гормональной терапии в достижении ранней ремиссии спазмов и редукции гипсаритмии по сравнению с традиционной противоэпилептической терапией [5].
Кроме того, раннее подавление эпилептической активности рассматривается как фактор, создающий условия для более благоприятного нейроразвития за счёт предотвращения длительного повреждающего влияния эпилептической активности на формирующиеся нейронные сети. Тем не менее в реальной клинической практике назначение гормональной терапии нередко откладывается, особенно у детей с тяжёлым фоновым поражением центральной нервной системы, вследствие опасений, связанных с возможными побочными эффектами и сомнениями в эффективности лечения при выраженной структурной патологии мозга [6, 7].
В этом контексте особую научную и практическую ценность представляют клинические случаи, демонстрирующие эффективность гормональной терапии у пациентов с перивентрикулярной лейкомаляцией и детским церебральным параличом. Представленный клинический случай иллюстрирует успешное применение системных глюкокортикостероидов у ребёнка с тяжёлым гипоксически-ишемическим поражением головного мозга, сопровождавшееся быстрым купированием эпилептических спазмов и положительной динамикой электроэнцефалографических показателей.
Описание клинического случая
Мальчик М. А., дата рождения — 21.11.2023 г.
Акушерский анамнез отягощён. Ребёнок рождён доношенным, в сроке гестации 40 недель 4 дня, с массой тела 3830 г и ростом 53 см. Крик при рождении был отсроченным. В родах отмечалась асфиксия; оценка по шкале Апгар составила 7–8 баллов. В раннем неонатальном периоде ребёнок находился в отделении палаты интенсивной терапии на фоне оксигенотерапии в течение 7 суток, после чего был переведён в отделение патологии новорождённых. В неонатальном периоде отмечалась затяжная конъюгационная желтуха продолжительностью до 3 месяцев; максимальный уровень общего билирубина в сыворотке крови достигал 260 мкмоль/л.
Из анамнеза заболевания известно, что с 8-месячного возраста у ребёнка появились приступы. По описанию матери, эпизоды сопровождались нарушением сознания и генерализованным тоническим напряжением мышц. В условиях амбулаторного наблюдения по месту жительства была назначена противоэпилептическая терапия вальпроевой кислотой в дозе 300 мг/сут (100 мг 3 раза в день). В связи с сохраняющейся приступной активностью впоследствии к терапии был добавлен леветирацетам в дозе 200 мг/сут (100 мг 2 раза в день). Несмотря на проводимую комбинированную противоэпилептическую терапию, эпилептические спазмы сохранялись.
В возрасте 1 года 9 месяцев ребёнок был направлен на специализированную консультацию. Со слов родителей и по данным видеозаписей, приступы преимущественно возникали после пробуждения и проявлялись сериями эпилептических спазмов, характеризующихся сгибательно-разгибательными движениями проксимальных мышц верхних конечностей. Спазмы возникали сериями по 5–6 эпизодов в течение одной минуты.
Неврологический статус и развитие
При осмотре состояние ребёнка стабильное. Сознание ясное (по шкале AGBO-A). Голова микроцефалической формы, окружность головы составляет 44 см (-3 SD). Лицо симметричное, глазные щели равны (D = S). Фотореакции сохранены, симметричные. Движения глазных яблок в полном объёме. Отмечается горизонтальный мелкоразмашистый нистагм.
Мышечный тонус снижен диффузно, по типу генерализованной мышечной гипотонии. Сухожильные рефлексы оживлены, симметричные (D=S) во всех конечностях. Патологический подошвенный рефлекс по типу Бабинского положительный с обеих сторон.
В двигательном развитии: ребёнок самостоятельно удерживает голову, однако не переворачивается, не сидит, не ползает и не стоит у опоры. Нейропсихическое развитие грубо задержано во всех сферах.
С учётом клинико-неврологических данных диагностирован церебральный паралич, смешанная форма, уровень функциональных ограничений - GMFCS IV.
Ребёнку проведено комплексное обследование, включавшее длительное видео-ЭЭГ-мониторирование и магнитно-резонансную томографию головного мозга.
Инструментальные исследования
Электроэнцефалография до лечения. Длительный видео-ЭЭГ мониторинг выявил грубые диффузные изменения биоэлектрической активности мозга с наличием мультифокальной эпилептиформной активности. Регистрировались многочисленные спайки, острые волны, комплексы «спайк–волна» и «полиспайк–волна» с межполушарной синхронизацией, что соответствовало картине гипсаритмии (Рисунок 1).
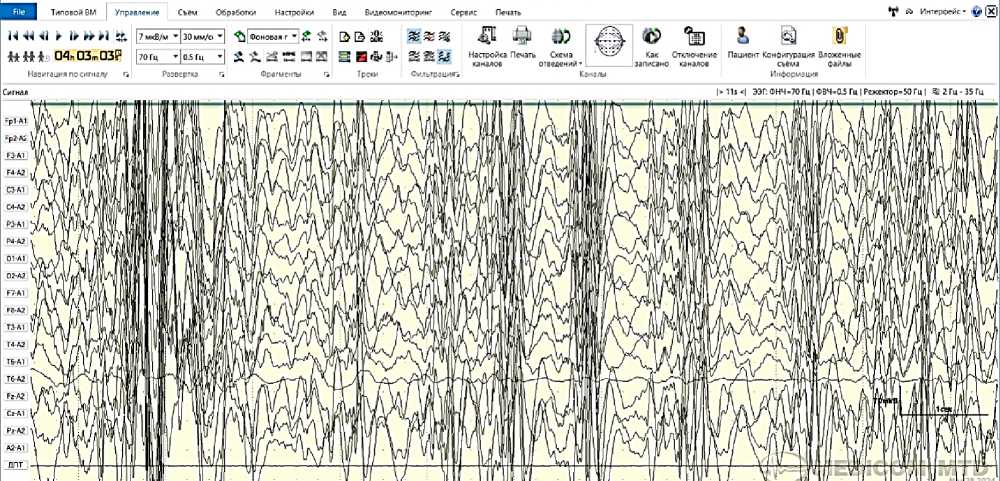
Рисунок 1. Электроэнцефалограмма до начала лечения
Магнитно-резонансная томография. МРТ головного мозга (T1-взвешенные изображения в сагиттальной и аксиальной проекциях) выявила выраженную диффузную атрофию обоих полушарий со вторичной микроцефалией, расширение ликворных пространств и вентрикуломегалию экс-вакуо. В перивентрикулярных отделах белого вещества определялись изменения, характерные для перивентрикулярной лейкомаляции, что соответствовало тяжелому гипоксически-ишемическому поражению головного мозга перинатального периода (Рисунок 2).
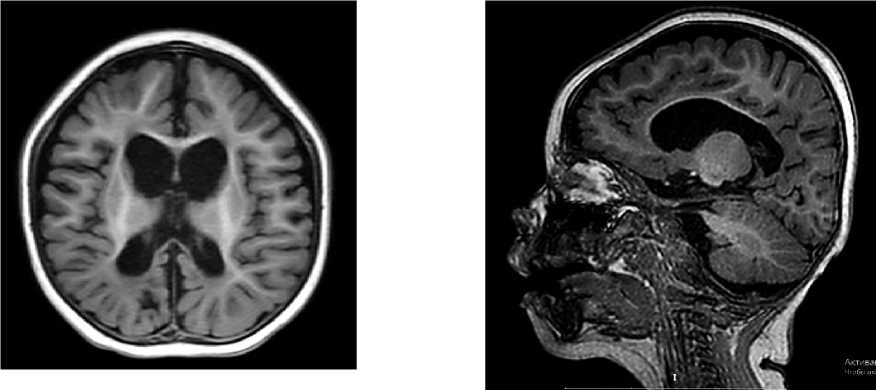
Рисунок 2. МРТ головного мозга
Лечение и динамика
С учётом клинической картины, данных электроэнцефалографии и выявленной структурной патологии головного мозга был установлен диагноз структурной эпилепсии с синдромом инфантильных эпилептических спазмов. До начала гормональной терапии с целью оценки эффективности ранее проводимой противоэпилептической терапии и исключения субтерапевтической концентрации препарата было выполнено определение уровня вальпроевой кислоты в сыворотке крови. Концентрация препарата составила 64 мг/л, что соответствовало терапевтическому диапазону. В связи с сохраняющимися эпилептическими спазмами и выраженными электроэнцефалографическими изменениями принято решение о назначении гормональной терапии преднизолоном в дозе 40 мг/сут.
Параллельно с началом гормональной терапии доза вальпроевой кислоты была увеличена до максимально рекомендованной для массы тела — 35 мг/кг/сут. При массе тела ребёнка 12 кг препарат назначен в дозе 140 мг 3 раза в сутки. Лечение проводилось под лабораторным контролем; показатели общего анализа крови и биохимического анализа крови (печёночные пробы) на данном этапе находились в пределах нормы.
На 3–4-е сутки от начала гормональной терапии отмечено полное купирование эпилептических спазмов. Через 14 дней выполнен повторный видео-ЭЭГ-мониторинг (Рисунок 3), продемонстрировавший выраженную положительную динамику в виде редукции гипсаритмии с сохранением лишь единичных эпилептиформных разрядов без тенденции к генерализации. На фоне приёма вальпроевой кислоты в максимально рекомендованной дозе через две недели концентрация препарата в сыворотке крови составила 100 мг/л, что соответствовало терапевтическому диапазону. В биохимическом анализе крови отмечалось умеренное повышение уровней аспартатаминотрансферазы, γ-глутамилтрансферазы и мочевины, что потребовало динамического лабораторного наблюдения. Уровень глюкозы крови оставался в пределах нормы.
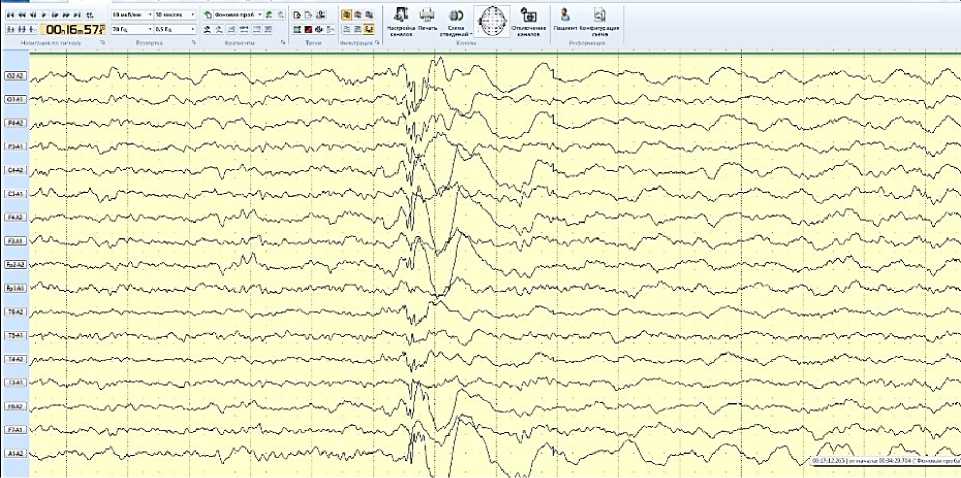
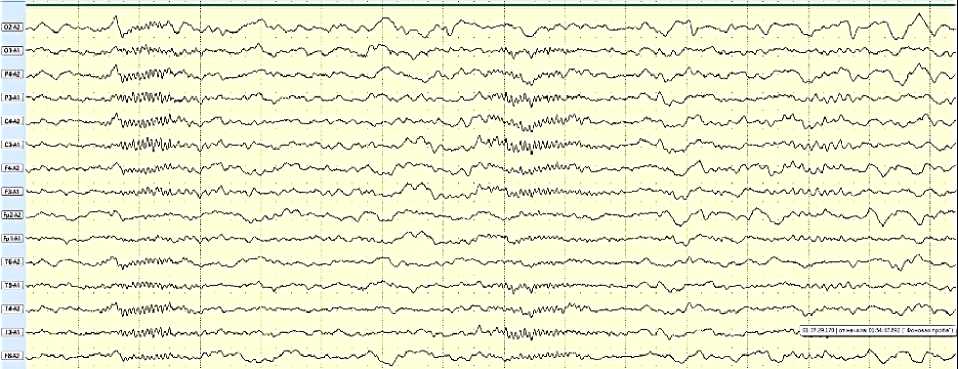

Рисунок 3. Электроэнцефалограмма после гормональной терапии
Гормональная терапия была отменена по ступенчатой схеме со снижением дозы преднизолона на 10 мг каждые 5 дней. Леветирацетам был полностью отменён. В дальнейшем рекомендовано продолжить лечение в режиме монотерапии вальпроевой кислотой. С учётом умеренных изменений показателей печёночных проб доза вальпроевой кислоты была снижена до 130 мг 3 раза в сутки, что соответствовало 32 мг/кг/сут, с рекомендацией регулярного приёма без дальнейшего снижения дозы.
При контрольном обследовании после отмены гормональной терапии показатели общего анализа крови оставались в пределах нормы. В биохимическом анализе крови сохранялось умеренное повышение уровня прямого билирубина и γ-глутамилтрансферазы при нормальных значениях АЛТ и АСТ, а также отмечалось снижение уровня щелочной фосфатазы. Электролитный состав крови (кальций, магний, натрий, фосфор, хлор) — без отклонений. Уровень 25(OH) витамина D составил 10 нг/мл, что соответствовало выраженному дефициту.
Назначена терапия препаратами витамина D в суточной дозе 3000 МЕ 1 раз в сутки сроком на 1 месяц. Рекомендован контроль показателей печёночных проб (АЛТ, АСТ, γ-глутамилтрансфераза, билирубин, щелочная фосфатаза) и уровня 25(OH) витамина D через 1 месяц. При последующих контрольных обследованиях клинического рецидива эпилептических спазмов не отмечалось; по данным ЭЭГ — без отрицательной динамики. Ребёнок начал занятия с физическим терапевтом.
Результаты и обсуждение
Представленный клинический случай иллюстрирует высокую эффективность гормональной терапии при синдроме инфантильных эпилептических спазмов даже у пациента с тяжелым структурным поражением центральной нервной системы и выраженной задержкой развития. Несмотря на фармакорезистентность к стандартной противоэпилептической терапии, применение системных глюкокортикостероидов позволило добиться быстрого клинического и электроэнцефалографического ответа. Согласно международным клиническим рекомендациям, препаратами первой линии при синдроме инфантильных эпилептических спазмов являются гормональная терапия (адренокортикотропный гормон или системные глюкокортикостероиды) в сочетании с вигабатрином. Вальпроевая кислота рассматривается как альтернативный противоэпилептический препарат в случаях, когда применение вигабатрина невозможно. В условиях Кыргызской Республики вигабатрин в настоящее время недоступен, в связи с чем была выбрана стратегия эскалации дозы вальпроевой кислоты до максимально рекомендованной терапевтической дозы в сочетании с гормональной терапией. Данная тактика позволила достичь терапевтической концентрации препарата в сыворотке крови и сопровождалась клинико-электроэнцефалографической ремиссией.
Проведение гормональной терапии сопровождалось регулярным лабораторным мониторингом, что обеспечило своевременное выявление транзиторных биохимических изменений и подтвердило безопасность выбранной схемы лечения. Таким образом, представленный клинический случай подтверждает ключевую роль ранней диагностики синдрома инфантильных эпилептических спазмов и своевременной эскалации терапии, поскольку длительное сохранение гипсаритмии ассоциировано с неблагоприятным нейроразвитием и ухудшением прогноза.
Заключение
Гормональная терапия является эффективным методом лечения синдрома инфантильных эпилептических спазмов структурного генеза. Даже при наличии тяжелого гипоксически-ишемического поражения головного мозга раннее назначение глюкокортикостероидов может привести к быстрому купированию эпилептических спазмов и значительному улучшению электроэнцефалографических показателей. Представленный клинический случай демонстрирует возможность эффективной альтернативной схемы лечения инфантильных эпилептических спазмов в условиях ограниченной доступности препаратов первой линии и подчеркивает решающую роль своевременной эскалации терапии.
Этические аспекты. Получено информированное согласие родителей на использование клинических данных и результатов обследований в научных целях. Идентифицирующая информация о пациенте не раскрывается.


