Эффективность этапных чресканальных видеоассистированных бурсооментоскопий и ретроперитонеоскопий в сочетании с ультразвуковой кавитацией в лечении небилиарного инфицированного панкреонекроза
Автор: Бухвалов Андрей Геннадьевич, Грекова Наталия Михайловна, Лебедева Юлиана Валерьевна, Бордуновский Виктор Николаевич, Шишменцев Николай Борисович, Васильев Вячеслав Сергеевич
Журнал: Человек. Спорт. Медицина @hsm-susu
Рубрика: Проблемы здравоохранения
Статья в выпуске: 1 т.15, 2015 года.
Бесплатный доступ
Цель - повышение эффективности хирургического лечения больных острым тяжелым панкреатитом, осложненного инфицированным панкреонекрозом и ретроперитонеонекрозом. Оперировано 83 пациента с острым тяжелым панкреатитом. Минимально инвазивные вмешательства выполнены 41 пациенту: видеоассистированные лапароскопии, бурсооментоскопии, ретроперитонеоскопии с ультразвуковой кавитацией гнойной полости и применением оригинального многоцелевого дренажа с имплантатом из никелида титана с памятью формы, а также оригинального многоканального ретроперитонеоскопа. 42 больным произведены открытые вмешательства. Общее количество манипуляций под наркозом в группе исследования составило 3,78 ± 0,37, в то время как в группе исследований было проведено 6,31 ± 0,67 наркоза на 1 пациента (р = 0,003). В группе исследования послеоперационные осложнения развились в 29,3 ± 7,1 % случаев, в группе сравнения - в 73,8 ± 6,8 % (р
Минимально инвазивное лечение инфицированного панкреонекроза, бурсооментоскопия, ретроперитонеоскопия, ультразвуковая кавитация гнойной полости
Короткий адрес: https://sciup.org/147153246
IDR: 147153246 | УДК: 616.37-002.3-089.819
Effectiveness of staging transcanal video-assisted bursoomentoscopy and retroperitoneoscopy with ultrasonic cavitation for treatment of nonbiliary infected pancreanecrosis
Enhanced effectiveness of surgical treatment of patients with acute severe pancreatitis complicated with infected pancreonecrosis and retroperitoneal necrosis. We operated on 83 patients with acute severe pancreatitis. Minimal invasive procedures were performed in 1 patients: video-assisted laparoscopy, bursoomentoscopy, retroperitoneoscopy with ultrasonic cavitation of pus pocket and applied original multi-purpose drainage with titanium nickelide smart implant as well as original multi-canal retroperitoneoscope. Open surgery was performed in 42 patients. Total number of anaesthetized procedures in experimental group was 3,78 ± 0,37, while in control group the same factor was 6.31 ± 0.67 general anesthetic supports per 1 patient (р = 0.003). In experimental group we observed post-surgery complications in 29.3 ± 7.1 % cases, in control group the same factor was 73.8 ± 6.8% (р
Текст научной статьи Эффективность этапных чресканальных видеоассистированных бурсооментоскопий и ретроперитонеоскопий в сочетании с ультразвуковой кавитацией в лечении небилиарного инфицированного панкреонекроза
Значительная частота острого тяжелого панкреатита (ОТП) и высокая летальность при этой патологии не могут не быть актуальными для абдоминального хирурга, оказывающего экстренную помощь. Вопрос этот в одинаковой мере интересен как отечественным хирургам, так и международному хирургическому сообществу [1, 9], о чем свидетельствует значительное число консенсусов, практических рекомендаций и итоговых документов конференций, как российских, так и зарубежных [5, 10]. Летальность при панкреонекрозе, асептическом и инфицированном, в его клинических проявлениях (панкреатогенные инфильтрат, абсцесс, забрюшинная флегмона, гнойный перитонит) остается стабильно высокой и изменяется весьма незначительно [2]. Количество пациентов, у которых развивается инфицированный панкреонекроз, поздняя по-лиорганная недостаточность (ПОН) и другие тяжелые гнойно-деструктивные осложнения острого панкреатита (ОП) такие как аррозив-ное кровотечение, дуоденальный свищ, тонко-и толстокишечные свищи, а также панкреатические свищи, увеличивается [3, 4, 6-8].
В последнее время проявились новые минимально инвазивные способы вмешательств, применение которых при ОТП позволяет более оптимистично оценивать эффективность хирургического лечения этой патологии. В то же время технологии производства таких вмешательств, вопросы показаний, времени и очередности их выполнения остаются предметом дискуссий [11].
Таким образом, изучение новых подходов к этапному комбинированному лечению гнойно-деструктивных осложнений острого тяжелого панкреатита на основе пересмотренной международной классификации ОП (Атланта 1992, 2012), а также совершенствование технологий минимально инвазивных вмешательств при помощи новых инструментов и материалов представляется весьма актуальным вопросом абдоминальной хирургии [1, 3, 11].
Цель исследования – улучшить результаты лечения острого тяжелого панкреатита, осложненного инфицированным панкреонек-розом и ретроперитонеонекрозом.
Материалы и методы
На базе НУЗ «Отделенческая больница на ст. Златоуст» ОАО «РЖД» в период с 2000 по 2013 год было выполнено проспективное рандомизированное контролируемое исследование, в котором приняли участие пациенты, госпитализированные в хирургический стационар в экстренном порядке с диагнозом «Острый панкреатит». Диагноз ставили при наличии абдоминального болевого синдрома, типичного для ОП, повышения уровня амилазы крови и мочи, и картины ОП при ультразвуковом и МРТ исследовании в соответствии с международной классификацией острого панкреатита (Атланта 1992, 2012) [5, 9, 10]. Всего за указанный период поступило 124 пациента.
Критерии исключения : Из исследования были исключены больные с легкой формой ОП (острый отечный панкреатит) – 23 пациента, с фульминантной формой ОТП, умершие в раннюю фазу заболевания – 4 пациента. Также исключены больные с острым билиарным (5 чел.) и послеоперационным панкреатитом (1 чел.), пациенты с асептическими осложнениями ОТП (неинфицированный панкреатогенный инфильтрат, неинфицированная псевдокиста), которые не были оперированы (6 чел.).
Больные, соответствовавшие критериям включения и исключения (83 чел.), были случайным образом (методом монеты) разделены на две группы – группу исследования (41 чел.) и группу сравнения (42 чел.). Пациенты обеих групп получали базовую терапию: устранение болевого синдрома (с использованием эпидуральной анальгезии Th5–Th9 сегментов), интенсивную гидратацию (250–500 мл/ч изотонического раствора кристаллоидов), подавление внешней секреции поджелудочной железы (ПЖ), миотроп- ные спазмолитики антиферментную и антибактериальную терапию.
У пациентов группы исследования были выполнены минимально инвазивные вмешательства с использованием предложенных нами многоцелевого дренажа и прибора для ретроперитонеоскопии (методика операции описана ниже). У пациентов группы сравнения выполнялись открытые лапаротомии с программированными санационными релапаротомиями и люмботомиями, дренированием брюшной полости, сальниковой сумки и забрюшинной клетчатки.
У всех пациентов при включении в исследование рассчитывался индекс тяжести панкреатита по шкале Ranson, оценка физиологических функций по шкале АРАСНЕ-II, визуализационные признаки ОП по классификации Baltazar. Интераоперационно оценивались характеристики и объем поражения ПЖ, перипанкреатической и забрюшинной клетчатки. Далее фиксировалась динамика лабораторных показателей, а также сроки восстановления перистальтики и начала энтерального питания. Для оценки болевого синдрома отмечалась потребность во введении наркотических анальгетиков, и для пациентов, находящихся в сознании, определялась выраженность болевого синдрома во время манипуляций по шкале VAS.
Протокол исследования был одобрен этическим комитетом ЮУГМУ. Все пациенты дали информированное согласие на участие в исследовании.
Статистическая обработка полученных данных осуществлялась с использованием критерия Манна – Уитни и критерия Фридмана. При анализе качественных признаков применяли критерий χ² и точный критерий Фишера.
Методика малоинвазивных вмешательств. Первый вариант (первичная видеолапароскопия (ВЛСК) + санационные этапные программные видеоассистированные бурсо-оментоскопии и/или видеоассистированные ретроперитонеоскопии).
Вмешательство начинается с ВЛСК. Выполняется ревизия брюшной полости, выявляются признаки ОП и/или признаки панкреатогенного абсцесса, забрюшинной флегмоны. К ним мы относили наличие мутного или гнойного геморрагического выпота в брюшной полости, стеатонекроз, гиперемию и инфильтрацию париетальной брюшины боковых каналов, чаще левого, выбухание желудочноободочной или желудочно-печеночной связок – как признак гнойного оментобурсита. Выявлялась инфильтрация корня mesocolon, и корня брыжейки тонкой кишки. 2. Эвакуация гнойного экссудата. Вскрытие сальниковой сумки через желудочно-ободочную или желудочно-печеночную связку и удаление гноя из сальниковой сумки. 3. Осмотр ПЖ, выявление сформированных отграниченных секвестров. При их наличии – некрсеквестрэктомия. При незавершенной секвестрации, фиксированные секвестры не удаляли. Мы дополняли ВЛСК ультразвуковой кавитацией брюшной полости при помощи аппарата УРСК-7Н-22 в режиме «вспенивания», с частотой колебания АПЧ 70 ± 20 кГц и экспозицией 7–10 мин. 4. Проведение многоцелевого дренажа в сальниковую сумку через отдельные проколы (троакары 20 мм) (рис. 1, а, б). Особенности конструкции дренажа заключаются в следующем. Диаметр – в 2 вариантах – 20 или 30 мм. Дренаж имеет наружную часть, располагающуюся вне брюшной стенки и внутреннюю, для гнойной полости. На наружной части дренаж имеет «отвод», через который проводится, холедохоскоп (лапароскоп) для видеоконтроля этапных санационных манипуляций.
кавитацией. Через окно возможно проведение инструментов для чрездренажной некрсекве-стрэктомии. Через это же окно проводится рабочая часть ультразвукового кавитатора. При санации сальниковой сумки к ПЖ подводится второй дренаж, устанавливаемый параллельно первому, но через контрапертуру в другом подреберье. Четыре перфорированных конца обоих дренажей укладываются во все отроги гнойной полости, по принципу «каждому отрогу – свой дренаж». Наружные концы дренажей с видео-каналами выводятся через контрапертуры в боковых отделах живота или в поясничной области. Через проколы в точках Калька устанавливаются 3 сконструированные нами металлические гильзы с заглушками для этапных видеоассистирован-ных бурсооментоскопий.
Второй вариант (первичная лапаротомия + санационные этапные программные видеоассистированные бурсооментоскопии и/или видеоассистированные ретроперито-неоскопии). Доступ – срединная лапаротомия. 1. Эвакуация гнойного экссудата из брюшной полости. 2. Вскрытие, удаление гноя из сальниковой сумки, ревизия ПЖ и перипанкреа-тического пространства. При сформированных секвестрах – некрсеквестрэктомия.
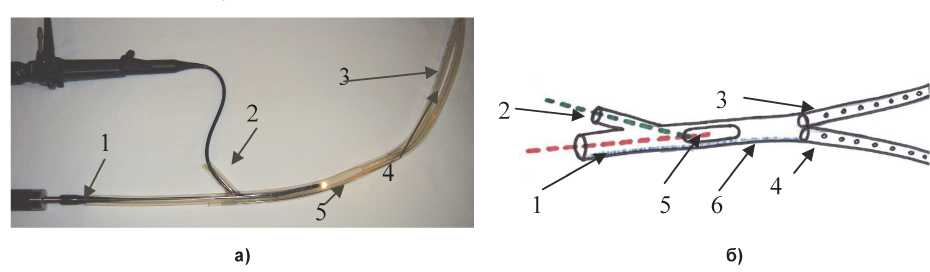
Рис. 1. Многоцелевой дренаж диаметром 30 мм, предложенный нами: а – фотография; б – схема:
1 – основной инструментальный канал дренажа (и для УЗ-кавитатора); 2 – видеоканал; 3, 4 – дренажные трубки для «отрогов» гнойной полости; 5 – инструментальное «окно»; 6 – имплантат никелид-титан
Внутри дренажа установлен имплантат из никелид титана с памятью формы для предупреждения перегибов и смещений дренажной трубки, деформации рабочего окна. Внутренняя часть дренажа – это 2 перфорированные трубки, соединенные с основным каналом в виде буквы «Y». В боковой стенке основного канала имеется широкое «рабочее окно» (12×30 мм), для дальнейших этапных санаций, например, видеоассистированной бурсоомен-тоскопии или ретроперитонеоскопии с УЗ-
-
3. «Открытая» УЗ-кавитация брюшной полости в течение 10 мин. 4. Установка в сальниковой сумке 2 многоцелевых дренажей по принципу «каждому отрогу гнойной полости – свой дренаж». 5. Установка в точках Калька предложенных нами гильз для плановых санационных ВЛСК (патент на полезную модель № 73185 от 20.05.2008 г.). Лапаротомная рана ушивается наглухо. Тампоны в сальниковую сумку не вводятся. Дренажи в боковые каналы и в малый таз не устанавливаются.
Техника ретроперитонеоскопии. Для ранней бактериоскопической верификации инфицированного панкреонекроза и ретроперито-неонекроза использовалась тонкоигольная аспирационная биопсия иглой типа Сhiba, Angiomed G под УЗ-контролем с микробиологическим исследованием пунктата. Доступ осуществлялся пункционными нефростомиче-скими дренажными наборами и телескопическим дилятационным набором бужей К. Storz от № 9 Fr до № 33 Fr и ренальных трубок Rush от № 30 Fr до № 36 Fr.
Вскрытие, санация и дренирование флегмоны парапанкреатической забрюшинной клетчатки производили ретроперитонеально через минилюмботомию при помощи изготовленного нами прибора. Ретроперитонео-скоп имеет 2 соединенных между собой металлических тубуса рабочей длиной 25 см, один из которых диаметром 20 мм используется как рабочий, инструментальный, второй – как видеоканал (рис. 2).
инструмента-концентратора в растворе диоксидина 0,1 % в течение 5–7 мин в режиме АПЧ 40 ± 20 кГц. После санации через просвет рабочего тубуса в забрюшинное пространство к ПЖ подводится описанный выше многоцелевой дренаж. В дальнейшем через него производятся программные санации забрюшинного пространства с УЗ-кавитацией. Поскольку при выполнении этапных чрездре-нажных санаций инструменты не касаются краев кожи и подкожной клетчатки наркоз пациентам не требуется.
Результаты исследования
Группа исследования и группа сравнения были сопоставимы по половозрастным признакам, по сопутствующей патологии, этиологии панкреатита, тяжести панкреатита по шкале Ranson, сроку операции, объему поражения ПЖ, перипанкреатической и забрюшинной клетчатки. При этом в возрастной группе от 18 до 60 лет находилось 72 пациента (86,8 ± 3,7 %), пациенты 61–80 лет соста-

Рис. 2. Ретроперитонеоскоп: а – фотография; б – схема: 1 – видеотубус;
2 – инструментальный тубус; 3 – система подачи жидкости в тубусы; 4 – лапароскоп;
5 – обтуратор-мандрен инструментального тубуса
Минилюмботомия длиной 3–4 см выполняется ниже XII ребра между задней и средней подмышечными линиями в вертикальном направлении. После рассечения поперечной фасции жировая клетчатка в заднем паранеф-ральном пространстве тупо расслаивается, почечная фасция и брюшинный мешок отодвигаются. Прибор вводится в забрюшинную клетчатку и продвигается к задней поверхности ПЖ под видеоконтролем и инсуфляцией СО2 до Р = 12 мм вод. ст. Для видеоконтроля используется лапароскоп, вводимый через уплотняющий клапан в видеотубус. После достижения дистальным концом ретропери-тонеоскопа забрюшинной гнойной полости удаляется обтуратор-мандрен и производится санация забрюшинного гнойного очага. Выполняется УЗ-кавитация при помощи 30-мм вили 13,2 ± 3,7 % (11 чел.), у большинства больных панкреатит имел алкогольную этиологию – 68 чел. (81,9 ± 4,3 %).
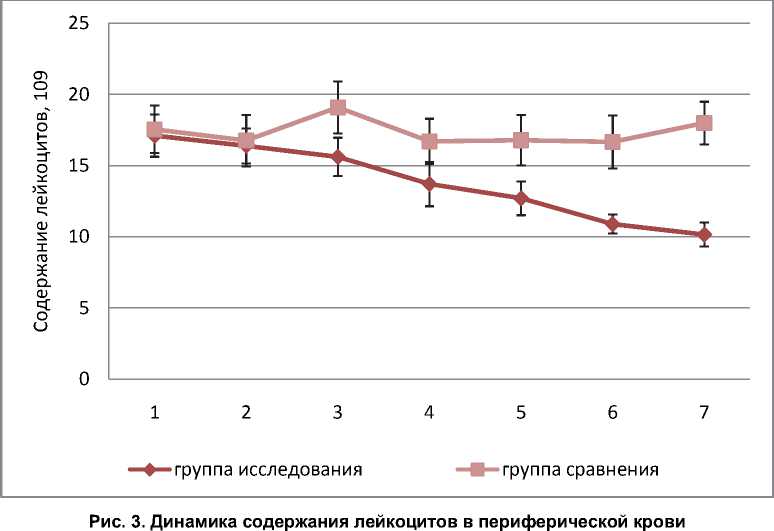
При поступлении у больных выявлены следующие виды гнойно-некротических осложнений ОТП (указано количество больных в группе исследования и сравнения соответственно). Инфицированный панкреонекроз (изолированный гнойный оментобурсит) – 3 и 7 пациентов, инфицированный ретроперито-неонекроз неотграниченный (панкреатогенная флегмона забрюшинной клетчатки) – 35 и 34 пациента, инфицированный ретроперитонео-некроз отграниченный (панкреатогенный абсцесс забрюшинной клетчатки) 3 и 1 пациент соответственно. Двусторонний характер поражения забрюшинной клетчатки имел место у 8 пациентов группы исследования и 11 па- циентов группы сравнения, преимущественно правосторонняя локализация наблюдалась у 3 и 5 пациентов, преимущественно левосторонняя локализация – у 27 и 19 пациентов группы исследования и сравнения соответственно. Лабораторные показатели до операции в группе исследования и сравнения не отличались. В послеоперационном периоде в группе исследования наблюдалось более быстрое купирование лейкоцитоза (рис. 3), температурной реакции, более быстрое восстановление перистальтики и начало раннего зондового питания (6,8 ± 0,52 сут в группе сравнения и 23,6 ± 2,1 в группе исследования, р < 0,001).
У одного пациентов из группы исследо- вания после первичной лапароскопической санации понадобилось применение открытой лапаротомии. У 5 пациентов группы исследования после первичной лапаротомии потребовалось повторное выполнение открытой лапа-ротомической санации. У 35 пациентов малоинвазивное лечение по приведенной схеме оказалось достаточным и переход к открытым вмешательствам не потребовался.
Меньший размер раневого дефекта и отсутствие соприкосновения инструментария с кожными краями и стенками раны при проведении трансканальной санации обусловило снижение болевого синдрома при выполнении манипуляций (рис. 4) и сокращение потребно-
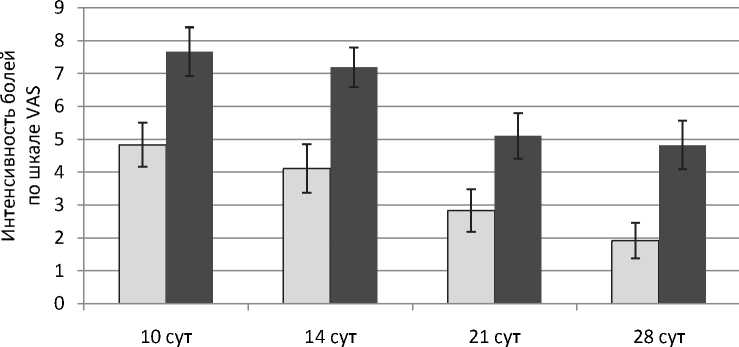
□ группа исследования
■ группа сравнения
Рис. 4. Интенсивность болевого синдрома при манипуляциях по шкале VAS
сти в медикаментозном купировании болей. Общее количество манипуляций под наркозом в группе исследования составило 3,78 ± ± 0,37, в то время как в группе исследований было проведено 6,31 ± 0,67 наркоза на 1 пациента (р = 0,003). Травматичная открытая санация требует введения наркотических анальгетиков в течение ближайших 6–30 ч после манипуляции. К 28 дню после проведения первичной операции 17 из 36 пациентов (47,2 ± 8,32 %), переживших месячный рубеж в группе сравнения, продолжали периодически получать наркотические анальгетики в течение ближайших часов после санаций. В группе исследования к 28 сут не требовалось обезболивания наркотическими анальгетиками после манипуляций ни у одного пациента (р < 0,001).
Применение малоинвазивных методик привело к значительному снижению частоты послеоперационных осложнений. В группе исследования были послеоперационные осложнения у 12 пациентов (29,3 ± 7,1 %), в группе сравнения – у 31 пациента 73,8 ± 6,8 % (р < 0,0001). В структуре осложнений преобладали свищи тонкой и толстой кишки (9,76 ± ± 4,36 и 23,8 ± 6,5 %), флегмона передней брюшной стенки (12,2 ± 5,1 и 38,1 ± 7,5 % в группе исследования и сравнения соответственно, р < 0,01).
Среди больных, прооперированных открытым способом, умерло 23 пациента (54,7 ± ± 7,8 %), летальность в группе исследования была ниже: всего умерло 7 человек (17,5 ± ± 7,0 %), различия статистически значимы (р < 0,001). Общий койко-день (исключая умерших пациентов) составил в группе исследования 37,3 ± 2,2 сут, а в группе сравнения 57,6 ± 6,4 сут (р = 0,003), койко-день в ОРИТ – 13,7 ± 1,55 и 20,1 ± 2,59 сут (р = 0,028) соответственно.
Обсуждение результатов
Предлагаемые многоцелевые дренажи, благодаря своему широкому просвету (20 или 30 мм), наличию двух обширных «окон» в проекции гнойной полости способствуют беспрепятственному оттоку гноя и эвакуации тканевых секвестров. Кроме того, исключают быстрое сужение раны и формируют широкий канал для последующего очищения раны и после удаления дренажей. Предложенный многоканальный ретроперитонеоскоп расширяет возможности чресканальных манипуляций под видеоконтролем: 1) осмотр гнойной полости с видеоархивом; 2) щадящие санации с удалением сформированных тканевых секвестров, которые могут быть эвакуированы только активными методами; 3) различные способы гемостаза; 4) ультразвуковые кавитации гнойных полостей. Кроме того, аппарат легко разбирается, промывается и стерилизуется.
Все вышеперечисленное дает возможность значительно уменьшить операционную травму у больного ОТП, не снижая при этом эффективность дренирования и некрэктомии, что и обуславливает выраженные преимущества малоинвазивных методик, снижающих летальность, число послеоперационных осложнений, болевой синдром и продолжительность госпитализации.
Выводы
-
1. Использование минимально инвазивных вмешательств при инфицированном панкрео-некрозе сокращает сроки пребывания больных в стационаре по сравнению с открытыми методами операций в 1,54 раза.
-
2. При использовании малоинвазивных методик болевой синдром менее выражен, что позволяет вдвое сократить необходимость в наркозе и избежать применения наркотических анальгетиков после вмешательств и перевязок.
-
3. Минимально инвазивные вмешательства позволяют снизить число послеоперационных осложнений при остром тяжелом панкреатите с 73,8 ± 6,8 до 29,3 ± 7,1 %, летальность с 54,7 ± 7,8 до 17,5 ± 7,0 %.
Список литературы Эффективность этапных чресканальных видеоассистированных бурсооментоскопий и ретроперитонеоскопий в сочетании с ультразвуковой кавитацией в лечении небилиарного инфицированного панкреонекроза
- Бухвалов, А.Г. Многофункциональный дренаж для динамических санационных лапаробурсоментоскопий в лечении инфицированного панкреонекроза/А.Г. Бухвалов, В.Н. Бор¬дуновский//Анналы хирург. гепатологии. -2008. -Т. 13, № 3. -С. 41.
- Галимзянов, Ф.В. Инфицированный панкреатогенный инфильтрат, панкреатогенный абсцесс и панкреатогенная флегмона, диагностика и лечение/Ф.В. Галимзянов, М.И. Прудков, О.П. Шаповалова//Вестник Урал. мед. акад. науки. -2011. -№ 4. -С. 34-37.
- Зайнутдинов, А.М. Методы интервенционной радиологии в комплексном лечении больных панкреонекрозом/А.М. Зайнутдинов, И.С. Малков, И.Ф. Шарафисламов и др.//Практ. медицина. -2014. -№ 5 (81). -С. 50-53.
- Крохин, А.А. Оценка риска формирования наружных панкреатических свищей после хирургического лечения деструктивных панкреатитов/А.А. Крохин, А.Г., Бухвалов, Д.М. Смирнов//Актуальные вопросы хирургии: сб. науч.-практ. работ/Региональная дирекция мед. обеспечения на ЮУЖД, ГБОУ ВПО ЮУГМУ Министерства здравоохранения РФ. -Челябинск, 2014. -С. 52.
- Неотложная хирургия. Клинические рекомендации по оказанию медицинской помощи населению УрФО/под ред. М.И. Прудкова. -Екатеринбург, 2013. -88 с.
- Острый панкреатит (протоколы, диагностика и лечение)/С.Ф. Багненко, Д.А. Благовестнов, Э.И. Гальперин и др. -М., 2014. -http://pancreonecrosis.ru/ostriy-pankreatit-protokoli-diag (дата обращения: 12.10.2014).
- Савельев, B.C. Хирургическая тактика при панкреатите/B.C. Савельев, М.И. Филимонов, С.З. Бурневич//Анналы хирургии. -2003. -№ 3. -С. 30-35.
- Успешное лечение больной с множественными кишечными свищами/Г.В. Динерман, В.Н. Бордуновский, М.А. Дрожжилов и др.//Хирургия. Журнал им. Н.И. Пирогова. -2003. -№ 11. -С. 44-45.
- Classification of acute pancreatitis -2012: revision of the Atlanta classification and definitions by international consensus/P.A. Banks, T.L. Bollen, C. Dervenis et al.//Gut. -2013. -№ 62. -Р. 102-111.
- Interventions for necrotizing pancreatitis: summary of a Multidisciplinary consensus conference/M.L. Freeman, J. Werner, H.C. Van Santvoort et al.//Pancreas. -2012. -Vol. 41. -Р. 1176-1194.
- Loveday, B.P. A comprehensive Classification of invasive procedures for treating the local complications of acute pancreatitis based on visualization, route, and purpose/B.P. Loveday, M.S. Petrov, S. Connor//Pancreatology. -2011. -Vol. 11. -Р. 406-413.


