Эффективность неопиодных анальгетиков у пациентов с травматическими ампутациями конечностей в раннем послеоперационном периоде
Автор: Крайнюков П.Е., Ким Е.А., Гудантов Р.Б., Борисова А.В., Агафонов Д.Е., Крайнюков Е.П.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 3 т.20, 2025 года.
Бесплатный доступ
Обоснование: данная работа является интеграцией более безопасных и эффективных препаратов в клиническую практику для оптимизации обезболивания и снижения рисков, связанных с использованием традиционных опиоидных анальгетиков. Цель исследования: оценить эффективность обезболивания в раннем послеоперационном периоде с использованием неопиоидных анальгетиков (ибупрофен, тафалгин, нефопам) у пациентов с минно-взрывными ранениями (МВР), сопровождающимися травматическими ампутациями конечностей. Методы: в исследование включены 45 пациентов, случайным образом распределенных на три группы в зависимости от используемого анальгетика: ибупрофен, тафалгин или нефопам. Результаты: во всех группах наблюдалось существенное снижение потребности в дополнительной послеоперационной анальгезии, включая опиоидные препараты. Нефопам обеспечивал наиболее выраженный анальгетический эффект, снижая интенсивность боли по шкале ВАШ сильнее, чем ибупрофен и тафалгин. Однако его применение сопровождалось более высокой частотой побочных эффектов (головокружение, тахикардия, гипертензия). Ибупрофен продемонстрировал оптимальное сочетание анальгетической эффективности и безопасности, с минимальной частотой побочных эффектов. Заключение: нефопам обладает выраженным анальгетическим эффектом в раннем послеоперационном периоде у пациентов с МВР, однако связан с повышенной частотой побочных эффектов. Ибупрофен показал высокий уровень безопасности и достаточную эффективность, что делает его предпочтительным компонентом мультимодальной аналгезии для данной категории пациентов.
Нефопам, ибупрофен, тафалгин, боль в раннем послеоперационном периоде, управление болью
Короткий адрес: https://sciup.org/140310615
IDR: 140310615 | DOI: 10.25881/20728255_2025_20_3_49
Efficiency of non-opioid analgesics in patients with traumatic limb amputations in the early postoperative period
Justification: This work is the integration of safer and more effective drugs into clinical practice to optimize pain relief and reduce the risks associated with the use of traditional opioid analgesics. Objective: to evaluate the effectiveness of pain relief in the early postoperative period using non-opioid analgesics (ibuprofen, tafalgin, nefopam) in patients with mine-blast wounds (MBW) accompanied by traumatic amputations of the limbs. Methods: The study included 45 patients randomly assigned to three groups depending on the analgesic used: ibuprofen, tafalgin or nefopam. Results: In all groups, there was a significant decrease in the need for additional postoperative analgesia, including opioid drugs. Nefopam provided the most pronounced analgesic effect, reducing pain intensity on the VAS scale more than ibuprofen and tafalgin. However, its use was accompanied by a higher frequency of side effects (dizziness, tachycardia, hypertension). Ibuprofen demonstrated an optimal combination of analgesic efficacy and safety, with a minimal frequency of side effects. Conclusion: Nefopam has a pronounced analgesic effect in the early postoperative period in patients with MVR, but is associated with an increased frequency of side effects. Ibuprofen showed a high level of safety and sufficient efficacy, which makes it a preferred component of multimodal analgesia for this category of patients.
Текст научной статьи Эффективность неопиодных анальгетиков у пациентов с травматическими ампутациями конечностей в раннем послеоперационном периоде
Болевой синдром остается одной из ключевых проблем современной медицины, затрагивая около 20% пациентов, которые испытывают сильную боль в первые 24 часа после оперативного вмешательства. Несмотря на внедрение новых анальгетиков, выраженность болевого синдрома у пациентов после хирургических вмешательств за последние 30 лет практически не изменилась [1].
С ростом объемов хирургических вмешательств возрастает необходимость совершенствования методов обезболивания, направленных на снижение зависимости от опиоидных анальгетиков. Использование мультимо- дальной анальгезии позволяет ускорить восстановление пациентов после хирургических вмешательств [2].
В настоящее время существуют различные схемы консервативного медикаментозного обезболивания пациентов с болевым синдромом после оперативных вмешательств, но зачастую они включают в себя прием опиоидных препаратов, что влечет за собой значимые побочные эффекты [3], такие как атония ЖКТ, тошнота, сонливость, снижение когнитивных функций, эндо-кринопатии, развития апноэ, угнетения дыхательной функции, вплоть до остановки дыхания, а также иммуносупрессии [4].

Более того, интенсивная боль в раннем послеоперационном периоде считается значимым предиктором развития хронического болевого синдрома [5]. Наиболее оптимальным методом обезболивания при МВР конечностей являются регионарные методики, но, к сожалению, они не всегда доступны по самым разным причинам, таким как: необходимость длительного обезболивания, отсутствие технической возможности, инфицирование места пункции, системный воспалительный процесс, непереносимость местных анестетиков, прием антикоагулянтов и пр.
Ведущим принципом управления болью в раннем послеоперационном периоде является мультимодальная анальгезия, которая уменьшает потребность в опиоидах и снижает частоту связанных с ними побочных эффектов. Мультимодальная анальгезия предусматривает одновременное назначение двух и более препаратов, воздействующих на разные уровни формирования острого болевого синдрома. [6]. Отмечается более широкое применение современных наиболее эффективных неопиоидных анальгетиков, таких как нестероидные противовоспалительные препараты (НПВП), центральные неопиоидные анальгетики и пр.
Ибупрофен является неселективным ингибитором ЦОГ-1 и ЦОГ-2 [7]. Он обладает выраженными аналь-гезирующими и жаропонижающими свойствами. Его эффекты обусловлены ингибирующим действием на циклооксигеназу, которая участвует в синтезе простагландинов [8]. Данный препарат был оценен как самый безопасный традиционный НПВС системой отчетности о спонтанных побочных реакциях на лекарства [9]. Однако, даже при низкой частоте побочных реакций со стороны ЖКТ, данные осложнения остаются основным ограничением его применения [10].
Нефопам ингибирует центральный обратный захват серотонина, норадреналина и дофамина и взаимодействует с α 2-адренорецепторами, а также модулирует кальциевые и натриевые каналы глутаматергического пути и тем самым снижает активацию постсинаптических глутаматергических рецепторов, таких как N-ме-тил-D-аспартат (NMDA), который играет особую роль в появлении гипералгезии [11]. Он не вызывает угнетения дыхания или осложнений со стороны ЖКТ, характерных для НПВС и опиоидных анальгетиков. Однако его применение может сопровождаться побочными эффектами, такими как тошнота, головокружение и тахикардия, что связано с центральным механизмом действия [12].
Тафалгин селективный агонист µ1-опиоидных рецепторов из группы тетрапептидов тирозил-D-аргинил-фенилаланил-глицин амид [13]. Он имеет выраженное анальгезирующее действие и является эффективным препаратом для лечения боли в раннем послеоперационном периоде после вмешательств разного объема. Применение данного препарата связано с низкой частотой возникновения нежелательных реакций, отсутствием дыхательной депрессии, характерной для опиоидных агонистов.
В рамках нашего исследования была проведена оценка интенсивности болевого синдрома у пациентов в раннем послеоперационном периоде с использованием неопиоидных анальгетиков, включая нефопам, ибупрофен и тафалгин. Полученные результаты направлены на совершенствование мультимодальных подходов к лечению выраженной послеоперационной боли.
Материал и методы
В рандомизированном открытом контролируемом исследовании приняли участие 45 пациентов в возрасте от 25 до 51 года, перенесших оперативные вмешательства под общей комбинированной анестезией или тотальной внутривенной анестезией на спонтанном дыхании. Участники были случайным образом распределены на три группы по 15 человек в зависимости от препарата, использованного для послеоперационного обезболивания:
-
• Группа I: пациенты получали ибупрофен в дозе 800 мг.
-
• Группа II: пациенты получали тафалгин в дозе 4 мг.
-
• Группа III: пациенты получали нефопам в дозе 20 мг.
Пациенты были включены в исследование после подписания информированного согласия и оценки критериев включения и исключения. Процедура рандомизации проводилась с использованием стандартной рандомизационной схемы.
В исследование были включены пациенты с травматическими ампутациями конечностей (n = 45) после МВР в возрасте от 25 до 51 года, поступившие на этапе оказания квалифицированной и специализированной медицинской помощи. Критерием включения для стартового назначение препаратов являлось наличие у пациентов выраженного болевого синдрома в раннем послеоперационном периоде.
Структура пациентов в зависимости от вида оперативного вмешательства представлена в табл. 1.
Критериями исключения являлись пациенты, по отношению к которым применяли регионарные методики, а так же пациенты с нарушением сознания, почечной и печеночной недостаточностью, сердечной недостаточностью, острой кровопотерей, в состоянии шока, психомоторным возбуждением, с которыми отсутствовал продуктивный контакт, с сопутствующими заболеваниями в анамнезе, такими как эпилепсия, заболевания уретры и предстательной железы, глаукома, бронхиальная астма, язва ЖКТ в анамнезе, почечная недостаточность , обострение которых может возникнуть при назначении исследуемых препаратов.
Табл. 1. Структура пациентов в зависимости от вида оперативного вмешательства
|
Вид оперативного вмешательства |
n |
Доля, % |
|
ППХО раны |
12 |
31 |
|
Реампутация конечности |
10 |
27 |
|
Ревизия раны |
14 |
22 |
|
Остеосинтез |
9 |
20 |
|
Всего |
45 |
100 |

Крайнюков П.Е., Ким Е.А., Гудантов Р.Б. и др. ЭФФЕКТИВНОСТЬ НЕОПИОДНЫХ АНАЛЬГЕТИКОВ У ПАЦИЕНТОВ С ТРАВМАТИЧЕСКИМИ АМПУТАЦИЯМИ КОНЕЧНОСТЕЙ В РАННЕМ ПОСЛЕОПЕРАЦИОННОМ ПЕРИОДЕ
Средний возраст пациентов в группах составил: 38,5 лет (группа I), 37,8 лет (группа II) и 38,9 лет (группа III). Группы были сопоставимы по возрасту, полу и типу проведенных операций, что обеспечивает надежность и достоверность полученных данных. Операции проводились по следующим показаниям и нозологиям: ППХО раны, ревизия раны, реампутация, остеосинтез.
Безопасность пациентов оценивалась в раннем послеоперационном периоде по частоте и тяжести побочных эффектов, таких как: тошнота, рвота, тахикардия, нарушения функции кишечника, когнитивные нарушения, седативный эффект.
В послеоперационном периоде у пациентов оценивался уровень болевого синдрома по шкале ВАШ через 2, 8, 12, 24 часа.
Эти меры позволили всесторонне оценить безопасность и эффективность применения ибупрофена, тафал-гина и нефопама в рамках мультимодальной аналгезии, обеспечивая достоверные клинически значимые данные.
Результаты
В процессе операции фиксировалось потребление фентанила у пациентов в каждой из групп. В среднем: в группе I - 0,4 мг, группе II – 0,3 мг, группе III – 0,4 мг. Продолжительность оперативных вмешательств в среднем составила:
– Группа I: 1 час 40 минут.
– Группа II: 1 час 30 минут.
– Группа III: 1 час 20 минут.
При анализе интенсивности болевого синдрома в раннем послеоперационном периоде, оцененной с использованием шкалы ВАШ, выявлены различия в динамике анальгетического эффекта между группами. Через 2 часа после завершения операции наиболее выраженный анальгезирующий эффект отмечен в группе пациентов, получавших нефопам (группа III), где средний уровень боли составил 1,5 балла. В группе, получавшей тафалгин (группа II), этот показатель составил 4,2 балла, а в группе ибупрофена (группа I) – 3,4 балла.
Через 8 часов после операции уровень болевого синдрома увеличился в группах I и II, составив 4,5 и 4,7 балла соответственно, тогда как в группе III оставался ниже, на уровне 3,5 балла. Однако к 12 и 24 часам после оперативного вмешательства интенсивность болевого синдрома во всех группах выровнялась. Через 12 часов средние значения ВАШ составили 2,4 балла в группе I, 3 балла в группе 2 и 2,5 балла в группе III. Через 24 часа уровень боли снизился до 1,5 балла в группах I и II, и до 1,8 балла в группе III (Рис. 1).
Полученные данные свидетельствуют о более быстром и выраженном начале анальгетического эффекта нефопама в раннем послеоперационном периоде, однако эффективность ибупрофена и тафалгина к 12–24 часам демонстрировала сопоставимые результаты, что подчеркивает значимость выбора препарата в зависимости от клинической ситуации.
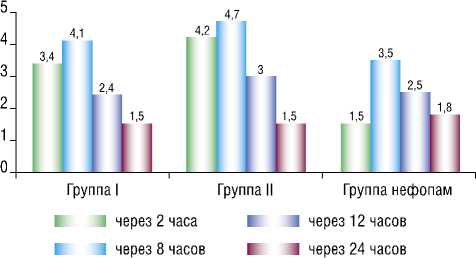
Рис. 1. Послеоперационная боль по шкале ВАШ в группах.
Табл. 2. Частота побочных эффектов в группах пациентов, %
|
Побочные эффекты |
Группа I |
Группа II |
Группа III |
|
Головокружение |
13,3 (n = 2) |
20 (n = 3) |
20 (n = 3) |
|
Тошнота |
20 (n = 3) |
13,3 (n = 2) |
20 (n = 3) |
|
Астения |
13,3 (n = 2) |
20 (n = 3) |
20 (n = 3) |
|
Тахикардия, гипертензия |
0 (n = 0) |
13,3 (n = 2) |
26,6 (n = 4) |
В раннем послеоперационном периоде пациенты группы I, получавшие ибупрофен, демонстрировали меньшую частоту и выраженность побочных эффектов по сравнению с пациентами групп II и III, которые получали тафалгин и нефопам соответственно.
Частота головокружения составила 10% в группе I, 15% в группе II и 20% в группе III. Тошнота наблюдалась у 15% пациентов группы I, у 5% группы II и у 20% группы III. Астения также была менее выражена в группе ибупрофена: 10% по сравнению с 15% в группах II и III. Тахикардия и гипертензия отмечались только в группах II и III, при этом их частота составила 10% в группе II и 25% в группе III, тогда как в группе I эти эффекты не наблюдались (Табл. 2).
Полученные результаты подтверждают преимущества ибупрофена в снижении частоты побочных эффектов по сравнению с тафалгином и нефопамом. Это подчеркивает его клиническую ценность в составе мультимодальной аналгезии для минимизации побочных эффектов и повышения качества жизни пациентов в послеоперационном периоде. Данные дополнительно свидетельствуют о важности выбора анальгетика с учетом как его эффективности, так и безопасности в раннем послеоперационном восстановлении.
Обсуждение
Результаты проведенного исследования показали, что применение нефопама в 90% случаев обеспечивало более выраженное снижение интенсивности болевого синдрома в раннем послеоперационном периоде у пациентов с травматическими ампутациями конечностей по сравнению с тафалгином и ибупрофеном. Однако у пациентов, получавших нефопам, значительно чаще наблюдались побочные эффекты, включая головокружение, тошноту, астению, тахикардию и гипертензию, что ограничивает его рутинное использование в этой категории пациентов.
Ибупрофен, напротив, продемонстрировал оптимальный баланс между эффективностью и безопасностью. У пациентов, получавших ибупрофен, в 70% случаев наблюдался достаточный уровень анальгезии в раннем послеоперационном периоде, исключающий необходимость в дополнительной анальгезии с использованием опиоидных препаратов. Более того, ибупрофен ассоциировался с меньшей частотой и выраженностью побочных эффектов, таких как тошнота, головокружение и астения, по сравнению с нефопамом и тафалгином.
Полученные данные подтверждают значимость ибупрофена как важного компонента мультимодальной аналгезии. Его использование способствует эффективному контролю боли, снижает потребность в опиоидах и минимизирует риск развития побочных эффектов, что существенно улучшает качество жизни пациентов в раннем послеоперационном периоде.
Результаты исследования также продемонстрировали, что использование тафалгина в 60% случаев не обеспечивало достаточного уровня анальгезии. При этом частота побочных эффектов в группе пациентов, получавших та-фалгин, была ниже, чем в группе, получавшей нефопам, но выше по сравнению с группой, получавшей ибупрофен.
Проведенное исследование продемонстрировало выраженную анальгетическую эффективность изучаемых препаратов. Среди них ибупрофен обладает наиболее благоприятным профилем безопасности, что делает его предпочтительным выбором для применения в клинической практике. Это особенно важно в контексте раннего послеоперационного периода у пациентов с травматическими ампутациями конечностей. Использование ибупрофена позволяет не только эффективно контролировать болевой синдром, но и снижает потребление опиоидных анальгетиков, что, в свою очередь, способствует минимизации связанных с ними побочных эффектов.
Полученные результаты подчеркивают перспективность дальнейших исследований, направленных на оптимизацию схем обезболивания и разработку клинических рекомендаций для повышения безопасности и эффективности аналгезии у данной категории пациентов. В то же время необходимы дополнительные исследования для оценки эффективности ибупрофена, тафалгина и нефопама при хирургических вмешательствах на других органах и системах.
Результаты данного исследования свидетельствуют о том, что нефопам обеспечивает наиболее выраженный анальгетический эффект у пациентов после операций, связанных с травматическими ампутациями конечностей. Однако высокая частота побочных эффектов ограничивает возможность его рутинного использования в раннем послеоперационном периоде. Вторую позицию по выраженности анальгетического эффекта занимает ибупрофен, который продемонстрировал минимальное количество побочных эффектов, что подчеркивает его высокий профиль безопасности. Тафалгин, напротив, проявил меньшую анальгетическую активность, чем не- фопам и ибупрофен, а также сопровождался побочными эффектами, частота которых превышала таковую у ибупрофена, но была ниже, чем у нефопама.
Выводы
Полученные данные подтверждают целесообразность включения данных препаратов в стандартные протоколы мультимодальной аналгезии для оптимизации управления болью в раннем послеоперационном периоде у пациентов с травматическими ампутациями конечностей. Их применение может способствовать снижению потребления опиоидов, уменьшая риск таких осложнений, как тошнота, рвота и когнитивные нарушения.
Тем не менее, дальнейшие исследования необходимы для оценки долгосрочных исходов применения ибупрофена, тафалгина и нефопама в рамках мультимодальной аналгезии, а также для изучения их эффективности при других типах хирургических вмешательств, не связанных с травматическими ампутациями конечностей.


