Эффективность применения дженериков иматиниба у больных хроническим миелолейкозом
Автор: Лямкина Анна Сергеевна, Аутеншлюс Александр Исаевич, Мирошников Павел Николаевич, Дубровин Андрей Владимирович
Журнал: Сибирский журнал клинической и экспериментальной медицины @cardiotomsk
Рубрика: Клинические исследования
Статья в выпуске: 2 т.32, 2017 года.
Бесплатный доступ
У 55 пациентов, принимающих дженерик иматиниба Филахромин, была изучена остаточная концентрация иматиниба в сыворотке крови через 24±3 часа после последнего приема препарата (Сtrough). При остаточной концентрации иматиниба в сыворотке крови 900 и более нг/мл число больных, достигших ПЦГО и БМО, было достоверно выше (p
Хронический миелолейкоз, ингибиторы тирозинкиназы, концентрация иматиниба
Короткий адрес: https://sciup.org/14920195
IDR: 14920195 | УДК: 616.155
Efficacy of application of generic imatinib in patients with chronic myeloid leukemia
We have measured the residual concentration of imatinib in blood serum of patients, who have been treated with generic imatinib (Philachromin) in 24±3 hours after last administration. Patients, who have residual serum blood level of imatinib higher 900 ng/ml, have attained complete hematologic response (CHO) and major molecular response (MMR) more often, than patients, who have lower level (p
Текст научной статьи Эффективность применения дженериков иматиниба у больных хроническим миелолейкозом
Хронический миелолейкоз (ХМЛ) – тяжелое клональное миелопролиферативное заболевание, развивающееся в результате злокачественной трансформации в ранних предшественниках кроветворения [14, 15]. Наиболее изучен цитогенетический маркер ХМЛ, который получил название филадельфийской хромосомы (Ph+) – приобретенная хромосомная транслокация t (9; 22) (q34; q11) между 9 и 22 хромосомами, в результате чего на 22 хромосоме образуется химерный ген BCR-ABL. Продукт химерного гена BCR-ABL (белок с высокой тирозинкиназной активностью) – тирозинкиназа p210BCR-ABL способен к аутофосфорилированию, приводящему к автономной активности клетки и практически полной ее независимости от внешних регуляторных механизмов. После присоединения аденозинтрифосфорной кислоты (АТФ) BCR-ABL-тирозинкиназа начинает фосфорилирование различных белков, участвующих практически во всех процессах жизнедеятельности клетки. Активируется множество сигнальных путей как усиливающих пролиферацию клетки, так и подавляющих апоптоз [21–24, 29, 31]. Усиленная пролиферативная активность и снижение чувствительности к апоптотическим сигналам приводит к быстрому накоплению лейкемических клеток. Характерный признак ХМЛ – способность к выходу незрелых клеток в периферическую кровь. В исследованиях Durig J. и др. и Peled A. и др. показано, что в гемопоэтических клетках, экспрессирующих ген BCR-ABL, снижена способность к связыванию с фибронектином. Нарушение адгезии клеток со стромой является следствием взаимодействия F-актина с актинсвязывающим участком белка p210BCR-ABL, что, вероятно, приводит к ослаблению взаимодействия клетки с белками цитоскелета, снижению контакта со стромой в костном мозге и к выходу незрелых клеток в периферическую кровь [13, 28]. Таким образом, усиление пролиферативной активности опухолевых клеток, снижение чувствительности к апоптозу, нарушение процессов дифференцировки и повышенная способность незрелых гемопоэтических клеток-предшественников к выходу из костного мозга в периферическую кровь, постепенная полная потеря зависимости от BCR-ABL-тирозинки- назы являются основными характеристиками лейкемических клеток при хроническом миелолейкозе [23, 32].
Современная терапия ХМЛ стремится к нескольким целям: достижение полной клинико-гематологической ремиссии (КГР), полного цитогенетического ответа (ПЦО) и большого молекулярного ответа (БМО) (максимально возможное сокращение количества клеток опухолевого клона в костном мозге, более чем в 1000 раз, и предотвращение появления опухолевых клонов, независимых от белка p210BCR-ABL). Убедительно доказано, что получение цитогенетического ответа приводит к значительному увеличению выживаемости больных хроническим миелолейкозом [11, 12]. Получение БМО и стабильное снижение уровня транскрипта гена BCR-ABL является достоверным предиктором длительного сохранения КГР и ПЦО, тогда как нарастание уровня транскрипта указывает на увеличение клеток опухолевого клона и возможную потерю ПЦО [10, 25].
Появление новых лекарственных препаратов, ингибиторов атипичной тирозинкиназы (ИТК), коренным образом изменило прогноз течения заболевания у больных ХМЛ. Данный вид терапии сопоставим с аллогенной трансплантацией гемопоэтических стволовых клеток (ал-лоТГСК) по эффективности, а по безопасности – радикально превосходит ее [20]. Согласно данным ретроспективного анализа, в 2001 г. ХМЛ был наиболее частым показанием для проведения аллоТГСК, тогда как в 2005 г., вскоре после появления иматиниба, он стал занимать лишь 8-ое место среди других заболеваний, при которых проводилась трансплантация костного мозга. Согласно литературным данным, полный цитогенетический ответ удается добиться у 75–90% пациентов, получающих има-тиниб в качестве терапии первой линии [7, 8, 9, 18, 20, 26]. Расчетная медиана выживаемости при лечении има-тинибом составляет более 15 лет [26]. Лечение ИТК наиболее эффективно в хронической фазе заболевания, тогда как в фазе акселерации полный гематологический и цитогенетический ответ удается достичь лишь в 71 и 24% случаев соответственно, а в фазе бластного криза прогноз остается неблагоприятным, медиана выживаемости составляет всего 6–8 месяцев [5, 27, 15]. Анализ результатов терапии ХМЛ свидетельствует о том, что у части больных не удается достичь полного цитогенетического ответа (ПЦГО), или впоследствии он утрачивается.
При достижении полного цитогенетического ответа в фазу акселерации (ФА) или бластного криза (БК) риск цитогенетического рецидива и прогрессии болезни практически приближается к нулю, однако на фоне терапии иматинибом его получают только около половины пациентов. Еще более редки случаи достижения полного молекулярного ответа (ПМО). Клинические исследования по применению новых ингибиторов тирозинкиназы (ИТК) – нилотиниба и дазатиниба – в ХФ ХМЛ доказали их преимущество перед иматинибом в получении ПЦГО и БМО, а также и по снижению риска трансформации в ФА/БК и увеличению общей выживаемости [4, 30]. В настоящее время, согласно критериям J.E. Sokal [17] и EUTOS [16], выделяют группу низкого, промежуточного и высокого риска. ИТК показали эффективность в лечении больных всех групп риска, однако наилучшие результаты по- лучены при лечении пациентов из группы низкого риска. Двухлетняя выживаемость больных, относящихся к группе низкого риска составляет 98%, к группе промежуточного риска – 86,4% и к группе высокого риска – 35,6%. Трехлетняя выживаемость составляет 78,8, 55,6 и 23,8% соответственно [1]. У части больных с хроническим миелолейкозом из группы высокого риска, получающих монотерапию иматинибом, наблюдается первичная или вторичная резистентность к проводимой терапии. Среди механизмов развития резистентности к терапии имати-нибом главная роль отводится мутациям киназного домена гена BCR-ABL [19].
В России в последние годы вместо оригинальных препаратов иматиниба используются дженерики, эффективность и безопасность которых требует дополнительного изучения. Джен е рик (англ. generic drug ) – лекарственное средство, продающееся под международным непатентованным названием, либо под патентованным названием, отличающимся от фирменного названия разработчика препарата. Отличающиеся от оригинального препарата остаточная концентрация препарата или количество побочных эффектов могут приводить к развитию первичной и вторичной резистентности, снижению приверженности пациентов к лечению и, в итоге, к снижению эффективности терапии.
Одним из способов оценки вероятности достижения полного цитогенетического и большого молекулярного ответа, а также токсичности препарата является изучение остаточной концентрации в сыворотке крови через 24±3 часа после последнего приема препарата (Сtrough), то есть перед очередным приемом иматиниба. Значимость этого метода показана в исследованиях, проведенных ранее у пациентов, принимающих оригинальный иматиниб – Гливек® [2, 3, 6].
Широкий диапазон имеющихся в настоящее время ИТК требует создания единой программы помощи больным хроническим миелолейкозом, достаточного финансирования из средств федерального и регионального бюджета, своевременного проведения современных цитогенетических и молекулярных методов исследования не только для диагностики, но и для мониторирования эффективности терапии всеми видами используемых ингибиторов тирозинкиназы.
Целью данного исследования явилось изучение эффективности и безопасности применения дженерика иматиниба у больных хроническим миелолейкозом.
Материал и методы
С января 2004 по июль 2016 гг. в ГБУЗ Городской клинической больнице № 2 на учете состояли 104 больных хроническим миелолейкозом: в хронической фазе – 86 пациентов, в фазе акселерации – 11 человек и в фазе бластного криза – 7 человек.
В группу вошли 40,4% мужчин (42 человека) и 59,6% женщин (62 человека). Средний возраст больных составил 44,7 ±18,2 года (от 16 до 78 лет), из всей группы обследуемых 81 пациент (77,8%) начал принимать ингибиторы тирозинкиназы (ИТК) сразу после установления диагноза хронический миелолейкоз (в первые 6 месяцев), а 23 человека (22,1%) получали различную предшеству-
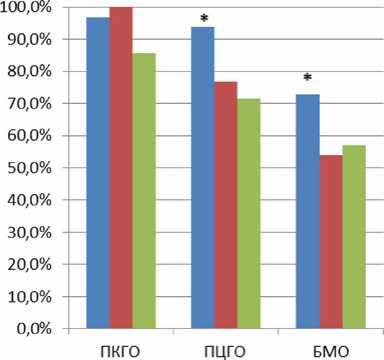
■ Группа 1: Ctrough 1000 и более нг/мл
■ Группа 2: Ctrough 700 -999 нг/мл
■ Группа 3: Ctrough 700 и менее нг/мл2
* - р<0,05
Рис. 1. Результаты лечения Филахромином (частота достижения полного клиникогематологического, полного цитогенетического и большого молекулярного ответа) в группе 1 по сравнению с группами 2 и 3
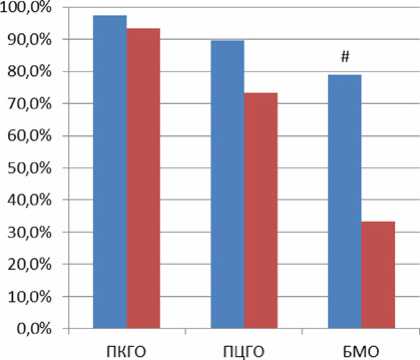
■ Группа А: исходно Гливек (12-36 мес.), потом Филахромин
■ Группа В: исходно Филахромин
#-р<0,05
Рис. 2. Результаты лечения иматинибом (частота достижения полного клиникогематологического, полного цитогенетического и большого молекулярного ответа) в группе А (исходно получающей Гливек, а потом переведенной на терапию Филахромином) по сравнению с группой В (исходно получающей Филахромин)
ле замены препарата Филахромин на препарат Имаглив степень выраженности побочных эффектов от терапии уменьшилась до уровня 0–1.
С целью мониторинга эффективности и безопасности препарата Филах-ромин у 55 пациентов была изучена остаточная концентрация иматиниба в сыворотке крови через 24±3 часа после последнего приема иматиниба (Фи-лахромина) (Сtrough) (то есть перед очередным приемом иматиниба) методом высокоэффективной жидкостной хроматографии с детекцией методом тандемной масс-спектрометрии.
Cтатистическая обработка полученных данных проводилась с использованием пакета прикладных программ Statistica 6.0 и электронных таблиц Exсel 2007. При оценке количественных признаков использовали вычисление средней арифметической (М) и ее ошибки (m). Значимость различий между между группами оценивалась с помощью критерия хи-квадрат, статистически значимыми считались различия при р<0,05.
Результаты и обсуждение
У 55 пациентов, продолжающих принимать иматиниба мезилат (Фи-лахромин), была изучена остаточная концентрация иматиниба в сыворотке крови через 24±3 часа после последнего приема (Сtrough), то есть перед очередным приемом иматиниба. Ранее уже было доказано влияние остаточной концентрации оригинального имати-ниба (Гливека) на эффективность терапии хронического миелолейкоза [2, 3, 6]. В данных клинических исследо-
ющую терапию (гидроксимочевиной, препаратами ИФ- α (Интрон, Реаферон), курсами малых доз цитоза-ра), так как диагноз ХМЛ им был установлен до 2005 г. Группа низкого риска по Sokal диагностирована у 39 человек (37,5%), промежуточного – у 34 (32,7%), высокого – у 31 (29,8%).
Иматиниб назначали в дозе 400–600 мг в сутки (в хронической фазе заболевания), 600–800 мг в сутки (в фазе акселерации), 800 мг в сутки в фазе бластного криза. С 2014 г. все пациенты с оригинального иматиниба (Гли-век) были переведены на препарат дженерик иматиниба: Филахромин, однако у 5 пациентов после перевода с Гли-века на Филахромин появились признаки непереносимости препарата: диспепсические явления, боли в мышцах, суставах (уровень токсичности 2–3), в связи с чем ухудшилась приверженность пациентов к лечению. Пос- ваниях показано, что имеются достоверные различия в вероятности достижения ПЦО и БМО при Сtroughменее 700 нг/мл, а также в диапазоне от 700 до 1000 нг/мл и более 1000 нг/мл. При более высоких концентрациях достоверных различий не было получено.
В исследуемой группе уровень остаточной концентрации иматиниба (Филахромина) варьировал от 390 до 4370 нг/мл, средний уровень составил 1496,9 нг/мл. С целью оценки эффективности терапии у больных, получающих Филахромин, все пациенты были разделены на 3 группы: с уровнем концентрации менее 700 нг/мл, 700– 999 нг/мл и 1000 и более нг/мл. У двух первично резистентных пациентов концентрация иматиниба составила 4340 и 4370 нг/мл, эти больные регулярно нарушали режим и дозу приема препарата, в связи с вероятным нарушением правил подготовки и забора крови для проведения исследования у этих больных их результаты было решено исключить из дальнейшего анализа. Полученные результаты сравнивались с результатами аналогичных исследований по изучению концентрации Гливека [2, 3, 6].
В группу 1 с остаточной концентрацией иматиниба в сыворотке крови через 24±3 часа после последнего приема (Сtrough) более 1000 нг/мл вошли 33 человека (62,3%), средняя концентрация иматиниба мезилата составила 1787,27 нг/мл. В данной группе полный клинико-гематологический ответ (ПКГО) получен у 32 человек (96,9%), полный цитогенетический ответ (ПЦГО) – у 31 (93,9%), большой молекулярный ответ (БМО) – у 24 (72,7%). Согласно данным литературы, в группе пациентов, принимающих Гливек, ПЦГО получен у 81,3% больных, а БМО – у 81,5% [2, 3, 6].
В группу 2 с остаточной концентрацией иматиниба в сыворотке крови через 24±3 часа после последнего приема (Сtrough) 700–999 нг/мл вошли 13 человек (24,5%), средняя концентрация иматиниба составила 906,92 нг/мл. В этой группе ПКГО получен у всех обследованных, ПЦГО – у 10 из 13 (76,9%), БМО – у 7 (53,8%). По данным литературы – у 100, 77,5 и 65,2% соответственно.
В группу 3 с остаточной концентрацией иматиниба в сыворотке крови через 24±3 часа после последнего приема (Сtrough) менее 700 нг/мл вошли 7 человек (13,2%), средняя концентрация иматиниба 521,42 нг/мл. ПКГО в этой группе получен у 6 человек из 7 (85,7%), ПЦГО – у 5 (71,4%), БМО – у 4 (57,1%). По данным литературы, ПЦГО у 48,1%, БМО – у 43,2% обследованных.
Таким образом, при концентрации иматиниба (Фи-лахромина) в сыворотке крови через 24±3 часа после последнего приема (Сtrough) 1000 и более нг/мл число больных, достигших ПЦГО и БМО, статистически значимо выше (с<0,05).
Гематологические (тромбоцитопения, нейтропения, анемия легкой и средней степени) и не гематологические побочные эффекты (периорбитальные отеки и отечность лица, задержка жидкости, диспепсия, боли в мышцах, суставах, дерматит, сыпь) встречались в группе 1 у 20 больных (54,1%), из них степень тяжести II – III у 3 человек (8,1%). В группе 2 побочные эффекты встречались у 11 пациентов (68,8%), а степень тяжести II – III наблюдалась у 4 больных (25%). Более высокая частота побочных эффектов от приема иматиниба и более высокая частота степени тяжести II – III в группе 2 могут привести к нарушению режима приема препарата пациентами, к снижению остаточной концентрации иматиниба в сыворотке крови и снижению эффективности терапии.
Все пациенты (53 человека) также были разделены на 2 группы (А и В) по длительности заболевания: больные из группы А болели 4 и более лет, они получали в первые 18 месяцев после диагностики заболевания препарат Гли-век, на котором были достигнуты ответы (ПКГО, ПЦГО, БМО), а потом были переведены на Филахромин. Пациенты из группы В болели 1–3 года, получали исходно терапию Филахромином.
В группе А (38 пациентов) полный клинико-гематологический ответ достигнут у 37 человек (97,4%), полный цитогенетический ответ – у 34 (89,5%), большой молекулярный ответ – у 30 больных (78,9%). В группе В (15 человек) полный клинико-гематологический ответ достигнут у 14 человек (93,3%), полный цитогенетический от- вет – у 11 (73,3%), большой молекулярный ответ – у 5 больных (33,3%).
Частота встречаемости гематологических (тромбоцитопения, нейтропения, анемия легкой и средней степени) и не гематологических (периорбитальные отеки и отечность лица, задержка жидкости, диспепсия, боли в мышцах, суставах, дерматит, сыпь) побочных эффектов составляла в группе А – 55,2% (21 человек), при этом до перевода на терапию Филохромином побочные эффекты наблюдались только у 17 больных (44,7%), получающих терапию Гливеком.
В группе В, получающей только терапию дженериком иматиниба Филахромином, побочные эффекты встречались у 66,6% больных (10 человек). Выраженная степень токсичности (2 или 3), требующая замены препарата на препарат второго поколения или другого производителя, в группе А встречалась у 4 больных (10,5%), в группе В – у 5 (33,3%).
Заключение
При исходном лечении оригинальным препаратом иматиниба Гливеком и дженериком Филахромином вероятность достижения полного клинико-гематологического ответа одинаковая, вероятность достижения полного цитогенетического ответа незначительно выше при лечении Гливеком (89,5% и 73,3% соответственно), однако статистически значимого различия не выявлено. Частота достижения большого молекулярного ответа достоверно выше при терапии Гливеком, чем при применении Филахромина (78,9% и 33,3% соответственно, с<0,01). Побочные эффекты при применении Филахромина встречаются чаще (у 66,6% больных), чем при применении оригинального препарата (44,7%).
Выводы
Появление ингибиторов тирозинкиназы принципиально изменило наше представление о возможностях консервативной терапии Ph+ хронического миелолейкоза. Контроль за соблюдением больным режима приема ИТК, а также за биодоступностью лекарственных препаратов можно осуществлять с помощью исследования остаточной концентрации уровня иматиниба в сыворотке крови через 24 часа после последнего приема препарата. При сравнении эффективности и безопасности применения оригинального иматиниба и дженериков оригинальный препарат демонстрирует большую эффективность на молекулярном уровне и меньшее количество побочных эффектов при использовании. Эффективность и безопасность применения дженериков иматиниба при хроническом миелолейкозе нуждается в дальнейшем изучении.
Список литературы Эффективность применения дженериков иматиниба у больных хроническим миелолейкозом
- Абдулкадыров К.М., Бессмельцев С.С., Рукавицын О.А. Хронический миелолейкоз. -СПб.: СпецЛит, 1998. -464 с.
- Куцев С.И. Генетический мониторинг таргетной терапии хронического миелоидного лейкоза: автореф. дисс.. докт. мед. наук. -М., 2009. -45 с.
- Куцев С.И., Оксенюк О.С., Кравченко Е.Г. и др. Лекарственный мониторинг терапии хронического миелолейкоза иматинибом//Клиническая онкогематология. Фундаментальные исследования и клиническая практика. -2010. -Т. 3, № 1. -С. 1-9.
- Ломаия Э.Г., Зарицкий А.Ю. Нилотиниб -новый этап успеха в терапии хронического миелолейкоза.//Современная онкология, экстравыпуск. -С. 7-12.
- Лорие С.С., Курова Е.С., Семочкин С.В., Туркина А.Г. и др. Эффективность и безопасность терапии иматиниб мезилатом (Гливеком) больных хроническим миелолейкозом в фазе акселерации//Вопросы гематологии/онкологии и иммунопатологии в педиатрии. -2002. -Т. 1, № 2. -С. 66-67.
- Оксенюк О.С. Влияние концентрации иматиниба в плазме крови на эффективность терапии хронического миелоидного лейкоза//Автореферат диссертации на соискание ученой степени кандидата медицинских наук. -М., 2011. -26 с.
- Туркина А.Г., Хорошко Н.Д. Практические рекомендации по лечению больных хроническим миелолейкозом. -М., 2005. -С. 4-5.
- Туркина А.Г., Хорошко Н.Д. Практические рекомендации по лечению больных хроническим миелолейкозом. -М., 2008. -С. 3-6.
- Туркина А.Г., Хорошко Н.Д., Дружкова Г.А. и др. Эффективность терапии иматиниба мезилатом (Гливеком) в хронической фазе миелолейкоза//Терапевтический архив. -2003. -Т. 75, № 8. -С. 62-67.
- Туркина А.Г., Челышева Е.Ю. Цитогенетический и молекулярный ответ -ранние маркеры эффективности терапии Гливеком больных Ph+ хроническим миелолейкозом//Фарматека. -2004. -№ 18. -С. 48-54.
- Хорошко Н.Д., Туркина А.Г., Кузнецов С.В. и др. Хронический миелолейкоз -успехи современного лечения и перспективы//Гематология и трансфузиология. -2001. -№ 4. -С. 7-12.
- Allan N.C., Richards S.M., Sheperd P.C.A. et al. UK Medical Research Council randomised multicentre trial of interferon-a in chronic myeloid leukemia: improved survival irrespective of cytogenetic response//The Lancet. -1995. -Vol. 345. -P. 1392-139.
- Durig J., Rosenthal S., Elmaagacli A. et al. Biological effects of stroma-derived factor-1 alpha on normal and CML CD34+ haemopoietic cells//Leukemia. -2000. -Vol. 14 (9). -P. 1652-1660.
- Fialkow P.J., Jacobson R.J., Papayannoulou T. Chronic myelocytic leukemia: clonal origin in a stem cell common to the granulocyte, erythrocyte, platelet and monocyte/macrophage//Am. J. Med. -1997. -Vol. 63. -P. 125-130.
- Gordon M.Y. Cellular and molecular mechanisms in chronic myeloid leukemia: biology and treatment//Brit. J. Haematol. -1996. -Vol. 95. -P. 10-20.
- Hasford J., Pfirrmann M., Hehlmann R. et al. A new prognostic score for survival of patients with chronic myeloid leukemia//Blood. -2011. -Vol. 118 (3). -P. 686-92.
- Sokal J.E., Cox E.B., Baccarani M. et al.//Blood. -1984. -Vol. 63. -P. 789-799.
- Kantarjian H.M., Cortes J.E., O,Brien S. et al. Imatinib mesylate therapy in newly diagnosed patients with Phyladelphya chromosome-positive chronic myelogenous leukemia: high incidence of early complete and major cytogenetic responses//Blood. -2003. -Vol. 101. -P. 97-100.
- Kantarjian H.M., Hochhaus A., Cortes J. et al. Высокая эффективность и безопасность Нилотиниба у пациентов в хронической фазе хронического миелоидного лейкоза с резистентностью к иматинибу или непереносимостью иматиниба//Blood. -2007. -Vol. 110. -226a (abs.735).
- Kantarjian H.M., Talpaz M., O,Brien S. et al. Imatinib mesylate for Phyladelphya chromosome-positive chronic-phase myeloid leukemia after failure of interferon-alpha: follow-up results//Clin. Cancer Res. -2002. -Vol. 8. -P. 2177-2187.
- Kloetzer W.S., Kurzrock R., Smith L. et al. The human cellular abl gene product in the chronic myelogenous leukemia cell line K-562 has associated tyrosine protein kinase activity//Virology. -1985. -Vol. 140. -P. 230-238.
- Kurzrock R., Kantarjian H.M., Druker B.J. et al. Philadelphia chromosome-positive leukemias: from basic mechanisms to molecular therapeutics//Ann. Intern. Med. -2003. -Vol. 138 (10). -P. 819-830.
- Lugo T.G., Pendergast A.M., Muller A.J. et al. Tyrosin kinase activity and transformation potency of bcr-abl oncogene products//Science. -1990. -Vol. 247. -P. 1079-1082.
- McWhirter J.R., Wang J.Y. Activation of tyrosinase kinase and microfilament-binding functions of c-abl by bcr sequences in bcr/abl fusion proteins//Mol. Cell. Biol. -1992. -Vol. 11. -P. 1553-1565.
- Moravkovа et al. Polymerase Chain Reaction Analyses Should Be Used as a Basis for Clinical Decision Making in Patients With Chronic Myelogenous Leukemia//Blood. -1999. -Vol. 94. -P. 3609-11.
- O,Brien S.G., Guilhot F., Larson R.A. et al. Imatinib compared with interferon and low-dose cytarabine for newly diagnosed chronic-phase chronic myeloid leukemia//N. Engl. J. Med. -2003. -Vol. 348. -P. 994-1004.
- O’Brien S., Guilhot F., Larson R. et al. Imatinib compared with interferon and low-dose cytarabine for newly diagnosed chronic-phase chronic myeloid leukemia//N. Engl. J. Med. -2003. -Vol. 348. -P. 994-1004.
- Peled A., Hardan I., Trakhtenbrot L. et al. Immature leukemic CD34+CXCR4+ cells from CML patients have lower integrin-dependent migration and adhesion in response to the chemokine SDF-1//Stem cells. -2002. -Vol. 20 (3). -P. 259-266.
- Rowley J.D. A new consistent chromosomal abnormality in chronic myelogenous leukemia giemsa starting//Nature. -1973. -Vol. 243. -P. 290-303.
- Soverini S., Colarossi S., Gnani A. et al. Contribution of ABL kinase domain mutations to imatinib resistance in different subsets of Philadelphiapositive patients: by the GIMEMA Working Party on Chronic Myeloid Leukemia//Clin. Cancer Res. -2006. -Vol. 12 (24). -P. 7374-7379.
- Steelman L.S., Pohnert S.C., Shelton J.G. et al. JAK/STAT, Raf/MEK/ERK, P13K/Akt and BCR-ABL in cell cycle progression and leukemogenesis//Leukemia. -2004. -Vol. 18 (2). -P. 189-218.
- Van Etten R.A. Cycling, stressed-out and nervous of c-abl//Trend Cell. Biol. -1999. -Vol. 9. -P. 179-186.


