Эффективность применения комбинированной химиоиммунотерапии в 1-й линии диссеминированного немелкоклеточного рака легкого
Автор: Исаева Г.К., Сарычева М.М., Важенин А.В., Дубинина А.В., Шевелева К.М., Макрута И.В.
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Случай из клинической практики
Статья в выпуске: 1 т.25, 2026 года.
Бесплатный доступ
Актуальность. Согласно национальным и международным данным, рак легкого входит в число наиболее распространенных злокачественных новообразований. Значительная часть первично диагностированных случаев заболевания сопровождается наличием отдаленных метастазов. Цель исследования – демонстрация успешного клинического случая с длительной общей и безрецидивной выживаемостью у пациента с метастатическим немелкоклеточным раком легкого (НМРЛ) при лечении комбинацией атезолизумаба с бевацизумабом и химиотерапией. Описание клинического случая. У пациента, 72 лет, с диагнозом: Периферический немелкоклеточный (аденокарцинома) рак верхней доли правого легкого T1bN0M1b (oth), IV ст. на фоне лечения комбинацией атезолизумаба с бевацизумабом и химиотерапией получена длительная стабилизация заболевания. Общая выживаемость и выживаемость без прогрессирования составили 38 мес при достаточно благоприятном профиле безопасности. Заключение. Даже при наличии широкого спектра современных терапевтических опций лечение метастатического НМРЛ сопряжено с определенными трудностями. Представленный клинический случай подтверждает целесообразность использования схемы, включающей атезолизумаб, бевацизумаб и химиотерапию при метастатическом НМРЛ с отрицательным статусом EGFR/ALK и отсутствием экспрессии лиганда запрограммированной клеточной гибели PD-L1.
Метастатический немелкоклеточный рак легкого, лиганды рецептора запрограммированной клеточной гибели PD-1, общая и безрецидивная выживаемость
Короткий адрес: https://sciup.org/140314359
IDR: 140314359 | УДК: 616.24-006.6-08:615.37 | DOI: 10.21294/1814-4861-2026-25-1-186-191
Effcacy of combination of immunotherapy and chemotherapy as frst-line treatment for disseminated non-small cell lung cancer: a case report
Background. Lung cancer is one of the most common cancers worldwide. Most newly diagnosed lung cancer patients present with distant metastases. Objective: to demonstrate a successful clinical case showing longterm overall and relapse-free survival rates in a patient with disseminated non-small cell lung cancer treated with a combination of immunotherapy and chemotherapy. Case presentation. A 72-year-old patient diagnosed with stage IV (T1bN0M1b) non-small cell lung asenocarcinoma of the right upper lobe achieved long-term disease stabilization using a combination of atezolizumab, bevacizumab and chemotherapy. The overall and progression-free survival was 38 months with a favorable safety profle. Conclusion. Despite current drug therapy options, the treatment of metastatic NSCLC remains challenging. This case report demonstrates the effcacy of atezolizumab in combination with bevacizumab and chemotherapy in patients with metastatic, untreated EGFR- and ALK -negative NSCLC negative for programmed cell death ligand 1 (PD-L1).
Текст научной статьи Эффективность применения комбинированной химиоиммунотерапии в 1-й линии диссеминированного немелкоклеточного рака легкого
Несмотря на успехи последних лет в диагностике и лечении немелкоклеточного рака легкого (НМРЛ), данная нозология по-прежнему занимает лидирующие позиции в структуре онкологической летальности. На момент постановки диагноза у подавляющего большинства больных определяется местнораспространенный или метастатический НМРЛ. По данным литературы, еще несколько лет назад больше половины пациентов с НМРЛ умирало в первый год после постановки диагноза. Однако в последнее время показатель одногодичной летальности от рака легкого в Челябинской области значительно улучшился, отмечается его стойкое снижение с 48,2 % в 2022 г. до 45,8 % в 2024 г. [1, 2].
Терапия ингибиторами иммунных контрольных точек (ИКК) является эффективным и относительно безопасным методом лечения НМРЛ IV стадии как в виде первой или последующих линий, так и в качестве поддерживающей терапии. Наибольшую эффективность эти препараты показывают в сочетании с химиотерапией. Ингибиторы PD-1, PD-L1 проявляют наибольшую эффективность при высоком уровне экспрессии PD-L1. При этом нежелательные явления (НЯ) III и более степени при иммунотерапии ИКК наблюдаются реже, чем при химиотерапии, что позволяет при должном эффекте длительное время применять данный метод лечения без влияния на качество жизни пациента. Согласно действующим клиническим рекомендациям, терапевтические режимы I линии при метастатическом НМРЛ включают следующие подходы: монотерапия ингибиторами ИКК; их комбинация с цитостатическими препаратами; сочетание с бевацизумабом или двойная иммунологическая блокада [3]. Интеграция ИКК в схемы I линии обеспечила существенное улучшение клинических результатов при распространенном НМРЛ [4, 5].
Представлен клинический опыт продолжительного применения ингибитора иммунных контрольных точек PD-L1 атезолизумаба в сочетании с бевацизумабом и химиотерапией при лечении метастатического НМРЛ с негативным уровнем экспрессии PD-L1.
Клинический случай
Пациент Г., 72 года, отмечает начало заболевания с марта 2022 г., когда было выявлено образование в мягких тканях правой лопатки. Согласно анамнезу, пациент не курил. При объективном осмотре статус по шкале ECOG – 2 балла (обусловлено болевым синдромом), 2 балла по ШВО (шкала вербальных оценок). Пальпаторно в области правой лопатки определяется объемное образование, размерами до 10 см, плотной консистенции, болезненное, неподвижное, кожа над ним не изменена).
По данным инструментального обследования при МРТ мягких тканей правой лопатки (16.06.22): образование в верхней трети правой лопатки, размерами 126×61×57 мм, с инвазией в окружающие мягкие ткани, в правой надключичной области имеются единичные лимфоузлы, размерами 12×7×6 мм. При МСКТ органов грудной клетки (4.07.22): периферическое новообразование S1–2 левого легкого, размерами 7×12×9 мм; деструктивные изменения ости и верхней трети тела лопатки, размерами 68×104×68 мм, с мягкотканым компонентом и распространением в окружающие мышцы. ПЭТ-КТ не проводилась. По данным МСКТ головного мозга (6.07.22) очаговой патологии не выявлено.
Трепан-биопсия образования мягких тканей правой лопатки выполнена 14.07.22. При гистологическом исследовании во фрагментах костной и поперечно-полосатой мышечной ткани выявлен рост злокачественной опухоли полиморфноклеточного состава. Диагноз уточнен при ИГХ-исследовании: иммунофенотип опухоли соответствует первичной аденокарциноме легкого, определялась мембранная и цитоплазматическая экспрессия Cytokeratin Pan (Clone AE1/AE3/РСК26) (Ventana), Cytokeratin 7 (Clone SP52) (Ventana), CK19 (b170) (Bond), AMACR (Clone 13H4) (Dako), ядерная экспрессия TTF-1 (SPT24) (Bond). Транслокаций в генах ALK, ROS1, мутаций EGFR, BRAF
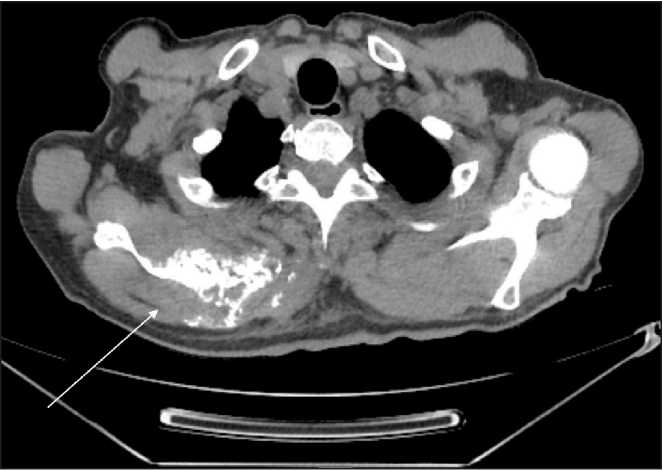
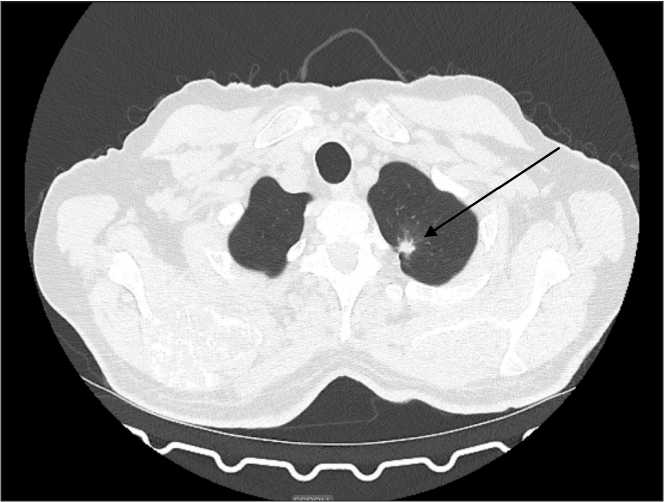
Рис. 1. МСКТ органов грудной полости (18.10.22): образование S1 левого легкого после 4 циклов терапии по схеме: атезолизумаб + бевацизумаб + карбоплатин + паклитаксел. В S1 легкого – образование с лучистыми тяжистыми контурами, размерами 10×11×8 мм (ранее 7×12×9 мм).
Примечание: рисунок выполнен авторами
Fig. 1. Chest CT scan (October 18, 2022). S1 mass in the right lung. After 4 cycles of combination therapy with atezolizumab + bevacizumab + carboplatin + paclitaxel. In S1 of the lung, a lesion with radiant cord-like contours measuring 10×11×8 mm (previously 7×12×9 mm) is visualized.
Note: created by the authors
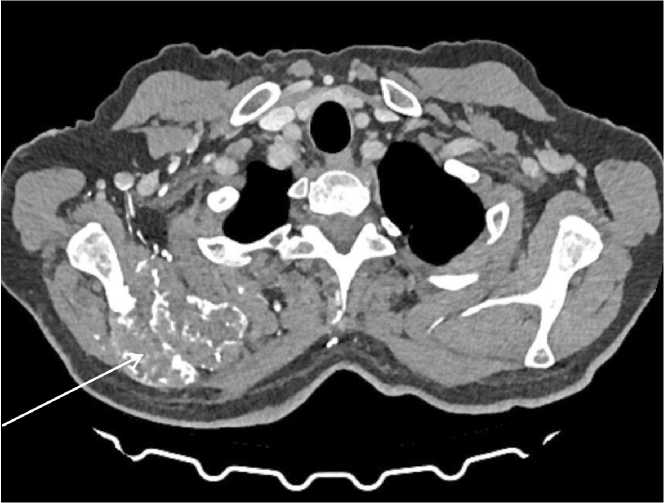
Рис. 2. МСКТ органов грудной полости (18.10.22): образование правой лопатки после 4 циклов комбинированной терапии по схеме: атезолизумаб + бевацизумаб + карбоплатин + + паклитаксел. В ости и верхней трети правой лопатки визуализируется объемное мягкотканое образование, размерами 80×57×73 мм (ранее 68×104×68 мм).
Примечание: рисунок выполнен авторами
Fig. 2. Chest CT scan (October 18, 2022). A mass on the right scapula. After 4 cycles of combination therapy: atezolizumab + bevacizumab + carboplatin + paclitaxel. In the spine and upper third of the right scapula, a volumetric soft tissue lesion measuring 80×57×73 mm (previously 68×104×68 mm) is visualized.
Note: created by the authors
Рис. 3. МСКТ органов грудной полости (22.09.25): образование правой лопатки после 54 циклов поддерживающей терапии по схеме атезолизумаб + бевацизумаб. В ости и верхней трети тела правой лопатки сохраняется неоднородной структуры объемное образование с признаками «вздутия», с деструкцией костной ткани, с мягкотканым компонентом, распространяющееся в мягкие ткани, неравномерно накапливающее контраст, размерами 69×53 мм, с наличием остео-бластического компонента.
Примечание: рисунок выполнен авторами Fig. 3. Chest CT (September 22, 2025). A mass on the right scapula. After 54 cycles of maintenance therapy with atezolizumab and bevacizumab. In the spine and upper third of the body of the right scapula, a volumetric lesion of heterogeneous structure with signs of “swelling” remains, with destruction of bone tissue, with a soft tissue component spreading into the surrounding soft tissues, unevenly moderately accumulating contrast, with axial dimensions of 69×53 mm, with the presence of an osteoblastic component.
Note: created by the authors
V600E не выявлено. Экспрессия PD-L1: TPS=0 (SP263) (Ventana).
Окончательный диагноз: Периферический немелкоклеточный (аденокарцинома) рак верхней доли правого легкого T1bN0M1b (oth), IV ст. Учитывая распространенность процесса, 11.08.22 начата иммунохимиотерапия по схеме: атезолизумаб 1200 мг в 1-й день + паклитаксел 200 мг/м2 – 380 мг в 1-й день + карбоплатин AUC 6 в 1-й день – 642 мг + бевацизумаб 15 мг/кг – 1110 мг в 1-й день; цикл 21 день. После завершения 4 циклов комбинированной терапии, которые пациент перенес без нежелательных явлений, проведена оценка эффективности терапии. При МСКТ-контроле органов грудной полости (18.10.22): в S1 легкого – образование с лучистыми тяжистыми контурами (рис. 1), размерами 10×11×8 мм (ранее 7×12×9 мм), в правой лопатке – мягкотканое образование, размерами 80×57×73 мм (ранее 68×104×68 мм) (рис. 2).
Далее больному регулярно, без нарушения интервального режима, проводилась поддерживающая терапия по схеме: атезолизумаб 1 200 мг и бевацизумаб 15 мг/кг внутривенно, в 1-й день, длительность цикла 21 день. На момент написания статьи проведено 55 циклов поддерживающей терапии (последний цикл 17.10.25). Длительность терапии составила 38 мес. Переносимость лечения удовлетворительная, нежелательные явления не наблюдались. Отмечено полное купирование болевого синдрома.
Оценка объективного ответа производилась согласно критериям iRECIST. По данным МСКТ органов грудной клетки от 22.09.25 зарегистрирована стабилизация процесса (-29,3 %) (рис. 3) по сравнению с исследованием от 4.07.22. Таргетные очаги: размеры очага в левом легком – ранее 12 мм, в настоящее время – 13 мм; размеры мягкотканого образования в области правой лопатки – ранее 104 мм, в настоящее время – 69 мм. Нетаргет-ные очаги: надключичные лимфоузлы справа – ранее 6 мм, в настоящее время не определяются.
Обсуждение
Представленный клинический случай демонстрирует эффективность комбинации паклитаксел + карбоплатин + бевацизумаб + атезолизумаб при лечении распространенного неплоскоклеточного немелкоклеточного рака легкого, характеризующегося негативной экспрессией PD-L1 (TPS <1 %) и значительной опухолевой массой. Выбор данной терапевтической стратегии требует обоснования в контексте современных клинических рекомендаций и альтернативных подходов, включая двойную иммунотерапию (ниволумаб + + ипилимумаб) с химиотерапией или без нее.
Ключевым аргументом в пользу выбора комбинации атезолизумаба с бевацизумабом и химиотерапией послужили результаты подгруппового анализа регистрационного исследования IMpower150, согласно которым добавление ате-золизумаба к бевацизумабу и химиотерапии (паклитаксел + карбоплатин) продемонстрировало улучшение исходов вне зависимости от уровня экспрессии PD-L1, включая пациентов с негативным статусом [5].
При использовании диагностического анализа SP263 (оценка экспрессии PD-L1 на опухолевых клетках) у пациентов с PD-L1 <1 % (n=237) медиана общей выживаемости (ОВ) составила 18,6 мес в группе атезолизумаб + бевацизумаб + химиотерапия против 14,0 мес в группе бевацизумаб + + химиотерапия (ОР 0,81, 95 % ДИ 0,61–1,07). При использовании анализа SP142 в подгруппе с полностью негативным статусом (TC0 и IC0) ОР составило 0,90 (95 % ДИ 0,71–1,14), а медиана ОВ в группе атезолизумаб + бевацизумаб + химиотерапия достигла 16,9 мес против 14,1 мес в группе бевацизумаб + химиотерапия. [5].
Важным фактором при выборе терапии у представленного пациента являлось наличие большой опухолевой массы. Распространенный опухолевый процесс традиционно ассоциируется с худшим прогнозом, более агрессивным течением и потенциально меньшей эффективностью моноиммунотерапии, особенно при негативной экспрессии PD-L1. В данной клинической ситуации требовалась стратегия, способная обеспечить быстрый и глубокий контроль над заболеванием.
При наличии большой опухолевой массы особенно важна способность режима индуцировать быструю регрессию очагов и преодолевать иммуносупрессивное микроокружение, характерное для распространенного процесса. Добавление беваци-зумаба играет в этом контексте ключевую роль: его антиангиогенная активность способствует нормализации сосудистой сети опухоли, снижению иммуносупрессии, опосредованной VEGF, и улучшению проникновения иммунных клеток в опухолевую ткань [6, 7]. Таким образом, комбинация атезолизумаб + бевацизумаб + химиотерапия позволяет реализовать синергизм трех механизмов: циторедуктивное действие химиотерапии для быстрого уменьшения опухолевой массы; анти-ангиогенный эффект бевацизумаба, модифицирующий микроокружение; иммуноопосредованное действие атезолизумаба, потенцируемое первыми двумя компонентами.
Учитывая неблагоприятное сочетание факторов (негативный PD-L1 и большая распространенность), выбор максимально активного режима, доказавшего свою эффективность в сложных клинических ситуациях, представляется патогенетически обоснованным. Представленное клиническое наблюдение демонстрирует, что применение режима атезолизумаб + бевацизумаб + химиотерапия позволило достичь контроля над заболеванием, несмотря на неблагоприятный прогностический статус.
В соответствии с клиническими рекомендациями пациенты с высоким уровнем PD-L1 получают наибольшую пользу от иммунотерапии. Однако у пациентов с негативным PD-L1 эффективность двойной иммунотерапии (ниволумаб + ипилиму-маб) без химиотерапии остается ограниченной. Согласно обновленным данным исследования CheckMate 227, у пациентов с PD-L1 <1 % применение двойной блокады иммунных контрольных точек позволяет достичь 5-летней выживаемости в 19 % случаев [8], поданализ подтверждает долгосрочные исходы в этой сложной подгруппе [9]. Тем не менее при наличии большой опухолевой массы и симптомного заболевания более быстрое и надежное достижение ответа требует включения цитостатиков в терапевтический режим.
Альтернативным подходом могло бы стать применение комбинации ниволумаба, ипилимумаба и двух циклов химиотерапии (режим CheckMate 9LA). Согласно 6-летним данным, эта стратегия демонстрирует впечатляющую эффективность: у пациентов с PD-L1 <1 % 6-летняя выживаемость достигает 20 %, медиана ОВ – 17,7 мес [10]. Однако прямое сравнение с режимом паклитаксел + + карбоплатин + бевацизумаб + атезолизумаб в подгруппе PD-L1-негативных пациентов отсутствует. Косвенные сравнения показывают, что при неплоскоклеточном раке легкого двойная иммуно- терапия с химиотерапией (CM9LA) может давать более высокую 5-летнюю выживаемость по сравнению с режимами на основе пембролизумаба [10]. Важно отметить, что добавление бевацизумаба к комбинации химиоиммунотерапии в исследовании IMpower150 обеспечивает дополнительное преимущество за счет антиангиогенного эффекта, который потенцирует противопухолевый иммунный ответ и модулирует микроокружение опухоли [6, 7].


