Эффективность применения препарата инфемин у пациентов с PIN низкой степени с сопутствующей доброкачественной гиперплазией предстательной железы
Автор: Киселев В.И., Друх В.М., Муйжнек Е.Л., Кузнецов И.Н., Андрианова Е.А., Барановский П.М.
Журнал: Экспериментальная и клиническая урология @ecuro
Рубрика: Андрология
Статья в выпуске: 3, 2015 года.
Бесплатный доступ
Проведено промежуточное исследование эффективности нового препарата Инфемин на основе дииндолилметана (DIM) с улучшенной биодоступностью. В исследовании приняли участие 11 пациентов с диагнозом простатическая интраэпителиальная неоплазия (PIN) низкой степени на фоне ДГПЖ. I группа (4 пациента) получала препарат Инфемин в дозе 900 мг DIM в сутки, II группа (7 пациентов) получала плацебо. Для оценки эффективности терапии проводился анализ динамики морфологического индекса (МИ) по результатам гистологического исследования биоптатов предстательной железы (ПЖ), а также рассчитывалась доля пациентов с сохраняющейся PIN/ДГПЖ через 12 месяцев после начала применения препарата Инфемин. Также исследователями оценивался размер ПЖ, показатели уродинамики (Qmax, Qave, Vres), индексы качества жизни по шкалам IPSS и QoL и эректильной дисфункции по шкале IIEF через 3, 6, 9 и 12 месяцев после начала применения препарата Инфемин. Через 12 месяцев терапии в группе приема препарата Инфемин МИ снизился с 0,50 до 0,04, в то время как в группе плацебо МИ увеличился с 0,42 до 0,58, значимость различий между группами составила p=0,008 (критерий Манна-Уитни). У 50% пациентов в группе терапии препаратом Инфемин также наблюдался полный регресс PIN, при этом в группе плацебо регресс PIN не наблюдался ни у одного пациента (p=0,209, хи-квадрат с поправкой Йетса). По результатам исследования в группе терапии препаратом Инфемин отмечена положительная динамика (уменьшение) в отношении объема предстательной железы, а показателя уродинамики Vres через 3 месяца после начала исследования (p=0,0497, критерий Манна-Уитни). Оценка качества жизни, симптомов, отражающих расстройство мочеиспускания, и симптомов эректильной дисфункции не выявила значимых отличий с группой плацебо.
Простатическая интраэпителиальная неоплазия, доброкачественная гиперплазия предстательной железы, 3'-дииндолилметан, препарат инфемин
Короткий адрес: https://sciup.org/142188047
IDR: 142188047
Efficacy of infemin in patients with low grade PIN and concurrent benign prostate hyperplasia
We have performed a preliminary study of the efficacy for new medication Infemin based on diindolylmethane (DIM) with improved bioavailability. Eleven patients were included with diagnosed prostatic intraepithelial neoplasia (PIN) and a background of benign prostatic hyperplasia (BPH). First group (4 patients) received Infemin 900 mg pro day, the second group (n=7) received placebo. Efficacy of therapy was controlled using morphological index (MI) in prostate bioptates, revealing the proportion of patients with persisting PIN/BPH at month 12 after treatment start. The prostate volume, urodynamic criteria (Qmax, Qave, Vres), IPSS and quality of life indices and IIEF-based estimation of erectile function were also considered in time points 3, 6, 9 and 12 months after the treatment initiation. MI after 12 months was lower in the Infemin group (dropped from 0,50 down to 0,04), in the control group it was increased from 0,42 up to 0,58 (p=0,008). Full regress of PIN was observed in 50% of cases in study group with no regress cases in the control group (p=0,209). In the Infemin group we have also observed the trend to the reduction of the prostate volume and Vres at 3 months after the treatment beginning (p=0,0497). Quality of life, micturition-related symptoms and erectile function did not show any significant changes from the baseline level.
Текст научной статьи Эффективность применения препарата инфемин у пациентов с PIN низкой степени с сопутствующей доброкачественной гиперплазией предстательной железы
Дополнительная информация:
We have performed a preliminary study of the efficacy for new medication Infemin based on diindolylmethane (DIM) with improved bioavailability. Eleven patients were included with diagnosed prostatic intraepithelial neoplasia (PIN) and a background of benign prostatic hyperplasia (BPH). First group (4 patients) received Infemin 900 mg pro day, the second group (n=7) received placebo. Efficacy of therapy was controlled using morphological index (MI) in prostate bioptates, revealing the proportion of patients with persisting PIN/BPH at month 12 after treatment start. The prostate volume, urodynamic criteria (Qmax, Qave, Vres), IPSS and quality of life indices and IIEF-based estimation of erectile function were also considered in time points 3, 6, 9 and 12 months after the treatment initiation. MI after 12 months was lower in the Infemin group (dropped from 0,50 down to 0,04), in the control group it was increased from 0,42 up to 0,58 (p=0,008). Full regress of PIN was observed in 50% of cases in study group with no regress cases in the control group (p=0,209). In the Infemin group we have also observed the trend to the reduction of the prostate volume and Vres at 3 months after the treatment beginning (p=0,0497). Quality of life, micturition-related symptoms and erectile function did not show any significant changes from the baseline level.
В.И. Киселев1, В.М. Друх1, Е.Л. Муйжнек2, И.Н. Кузнецов3, Е.А. Андрианова4, П.М. Барановский5
1Федеральное государственное автономное образовательное учреждение высшего образования «Российский университет дружбы народов», 2Закрытое акционерное общество «МираксБиоФарма», 3Государственное бюджетное образовательное учреждение высшего профессионального образования «Московский государственный медикостоматологический университет им. А.И. Евдокимова» Миниздрава России; 4Закрытое акционерное общество «ИльмиксГрупп»,
5Национальный исследовательский центр «Курчатовский институт»

ак предстательной железы (РПЖ) является одной из самых распространенных онкологических патологий в развитых странах [1]. В 2012 году в мире было зарегистрировано 1,1 млн.
новых случаев РПЖ и 307 тыс. смертей от данного заболевания [2]. В России в 2013 году было диагностировано около 31,5 тыс. новых случаев РПЖ, при этом показатели заболеваемости и смертности на 100 тыс. человек мужского населения составили, соответственно, 47,51 и 16,72 случаев [3].
Морфологическим эквивалентом предрака предстательной железы (ПЖ) считается простатическая интраэпителиальная неоплазия (PIN), которая формируется в результате пролиферативых изменений эпителия протоков и ацинусов ПЖ [4]. Многие исследователи выделяют две формы PIN: PIN низкой степени (low grade prostatic intraepithelial neoplasia) и PIN высокой степени (high grade prostatic intraepithelial neoplasia) в зависимости от выраженности цитологических и структурных изменений выстилающего железу эпителия [5]. В настоящее время диагноз PIN обычно устанавливается при выявлении изменений, характерных только для PIN высокой степени, поскольку изменения, характерные для PIN низкой степени, трудно отличить от нормальной ткани и/или атипической гиперплазии [6, 7]. Разными авторами PIN, как заболевание предшествующее РПЖ, выявлялось у 38-100% пациентов с подтвержденным диагнозом PIN высокой степени [8]. В некоторых исследованиях было показано, что изменения, характерные для PIN, часто встречаются у больных с доброкачественной гиперплазией предстательной железы (ДГПЖ) [9].
Общепризнано, что развитие гиперпластических процессов ПЖ в первую очередь обусловлено нарушением гормонального баланса [10]. С возрастом у мужчин в ПЖ происходит увеличение выработки фермента 5-α-редуктазы, отвечающего за синтез гормона 5α-дигидро-тестостерона (DHT) – более активного метаболита мужского полового гормона тестостерона [11]. DHT, обладая повышенной андрогенной активностью, приводит к усилению активности генов, отвечающих за □ пролиферацию клеток ПЖ и, как следствие, к развитию гиперплазии.
Известно, что мужские половые гормоны андрогены реализуют свою биологическую активность через анд-рогеновые рецепторы (ARs). Тем не менее, блокада гормональных стимулов (хирургическая и медикаментозная) не всегда останавливает развитие патологических процессов в ПЖ. К настоящему моменту обнаружено множество молекулярно-клеточных механизмов, стимуляция которых приводит к нарушению биологических функций ARs и, как следствие, к их аномальной активации низкими концентрациями андрогенов или другими негормональными индукторами и, в итоге, к развитию андроген-реф-рактерного РПЖ [12, 13]. Таким образом, становится все более понятно, что адекватная коррекция пролиферативных заболеваний ПЖ должна затрагивать не только андроген-зави-симые, но и другие, андроген-незави-симые, звенья их патогенеза.
Кроме того, с возрастом у мужчин повышается уровень женских половых гормонов эстрогенов. Эстрогены через эстрогеновые рецепторы стимулируют стромальные клетки ПЖ, а также воздействуют на эстроген-чувствительные клетки протоков желез, вызывая аномальную клеточную пролиферацию и воспаление [14] – механизмы, играющие важную роль в патогенезе РПЖ [15].
Наконец, злокачественная трансформация клеток ПЖ сопровождается нарушением эпигенетической регуляции, а именно усилением процессов промоторного ДНК-метилирования и деацетилирования гистонов хроматина, вызывающих эпигенетическое «умолкание» генов-супрессоров опухолевого роста [16, 17].
С целью профилактики РПЖ у пациентов, находящихся в группе риска по данному заболеванию, проводится поиск фармакологических субстанций, воздействующих на разные звенья патогенеза PIN и позволяющих добиться торможения трансформации клеток ПЖ в опухолевые.
Активная субстанция индол-3-карбинол (I3C) и его физиологический метаболит 3,3'-дииндолил-метан (DIM) – соединения с подтвержденной множественной противоопухолевой активностью [18]. Установлено, что в условиях in vitro и in vivo I3C и DIM ингибируют рост андроген-зависимых и андро-ген-независимых клеточных куль-тур/опухолей ПЖ [19, 20] благодаря нормализации уровня половых гормонов, а также сбалансированной регуляции активности андрогеновых и эстрогеновых рецепторов [21].
Доказана способность DIM восстанавливать функционирование опухоль-супрессорных генов, благодаря его ДНК-деметилирую-щей активности, а также способности ингибировать активность ферментов гистондеацитилаз [22, 23]. Помимо этого, DIM способствует активации системы интерферонов, в частности IFN-γ [24], а также обладает мощным противовоспалительным действием [25], подавляет активность фактора ангиогенеза VEGF и существенно снижает метастатический потенциал клеток, воздействуя на широкий спектр соответствующих молекулярных мишеней [26, 27]. Наконец, DIM проявляет избирательную активность в отношении пула так называемых опухолевых стволовых клеток, являющихся, согласно современным представлениям, основным источником опухолевых рецидивов и метастазирования [28].
С целью повышения биодоступности DIM был разработан препарат Инфемин, представляющий собой помещенный в твердые желатиновые капсулы раствор, содержащий DIM и вспомогательные компоненты [29].
Нами было проведено промежуточное двойное слепое плацебо-контролируемое клиническое исследование (II фаза) эффективности новой формуляции DIM у больных с PIN низкой степени с сопутствующей ДГПЖ.
МАТЕРИАЛЫ И МЕТОДЫ
Тестовые композиции. Препарат Инфемин, капсулы (ЗАО «Иль-миксГрупп», Россия), содержащие DIM (150 мг), рыбий жир (20 мг), α-токоферола ацетата (5 мг), в качестве вспомогательного вещества полисорбат 80 (575 мг). Препарат сравнения – плацебо, содержащий полисорбат 80 (750 мг).
Пациенты и лечение. В исследовании эффективности препарата Инфемин приняли участие 11 пациентов в возрасте 56-72 года с гистологически верифицированным диагнозом простатическая интраэпителиальная неоплазия (PIN) низкой степени и ДГПЖ. Исходно все пациенты имели объем остаточной мочи ≤150 мл, уровень ПСА ≤10 нг/мл, максимальную объемную скорость тока мочи ≥ 5 мл/с.
В исследование не включались пациенты с установленным диагнозом РПЖ и другими злокачественными новообразованиями, острой задержкой мочеиспускания, нейрогенными дисфункциями и дивертикулами мочевого пузыря, стриктурой уретры, склерозом шейки мочевого пузыря, инфекциями мочеполовой системы в фазе активного воспаления, а также пациенты, имеющие конкременты в мочевом пузыре. Критериями невключения в исследование также были: оперативные вмешательства на органах малого таза в анамнезе или их планирование в течение ближайших 12 месяцев, терапия хронического простатита за 1 месяц и терапия гиперплазии ПЖ или PIN за 3 месяца до приема первой дозы исследуемого препарата, злоупотребление алкоголем, наркотическая или лекарственная зависимость, наличие психического заболевания и/или неконтролируемого физического состояния. Не допускалось использование других экспериментальных лекарственных препаратов за 30 дней до приема первой дозы исследуемого препарата.
За 28 дней до начала периода активной терапии испытуемые проходили скрининговое обследование, в ходе которого осуществлялся сбор анамнеза, проводились физикальный осмотр и лабораторные исследования. Лабораторные исследования включали общие анализы крови и мочи, а также биохимический анализ крови (определение уровня общего белка, глюкозы, креатинина, общего билирубина, активности аспартатаминотрансферазы (АСТ), аланинаминотрансферазы (АЛТ)) и определение уровня ПСА в сыворотке крови. Также проводилась диагностка гепатитов В и С, ВИЧ-инфекции, анализ крови на RW.
В ходе начального скрининга для всех пациентов были получены данные ЭКГ (интервалы PQ, QRS, QT), проведены урологический осмотр с пальцевым ректальным исследованием, биопсия ПЖ, урофлоуметрия, трансректальное ультразвуковое исследование (ТРУЗИ) с определением остаточной мочи, заполнение опросников (IPSS+QoL, IIEF).
После подписания информированного согласия испытуемых распределили на две группы. Пациентам I группы (4 человека) препарат Инфемин назначался в дозе 900 мг DIM в сутки (3 капсулы, 2 раза в сутки), II группа пациентов (7 человек) получала плацебо (3 капсулы, 2 раза в сутки). Активная терапия проводилась в течение 12 месяцев с контрольными визитами в начале исследования, через 3, 6 и 9 месяцев после начала исследования.
Оценка эффективности терапии препаратом Инфемин проводилась на основании динамики морфологического индекса (МИ) к моменту окончания терапии (статистически значимое снижение МИ по сравнению с плацебо). МИ определялся по данным гистологического исследования биоптатов ПЖ на этапе скрининга и через 12 месяцев после начала исследования.
Расчет МИ проводился по формуле:
МИ={[число фокусов PIN низкой степени]+2*[число фокусов PIN высокой степени]+3*[число фокусов рака]} / [число столбиков биопсии]
В качестве дополнительных критериев эффективности использовались: доля пациентов с сохраняющейся PIN/ДГПЖ через 12 месяцев после начала применения препарата Инфемин и доля пациентов с РПЖ через 12 месяцев после начала применения препарата Ин-фемин. Исследователи также определяли: 1) объем ПЖ (см3) через 3, 6, 9 и 12 месяцев после начала применения препарата Инфемин; 2) показатели уродинамики: максимальную скорость потока мочи (Qmax), среднюю скорость потока мочи (Qave), объем остаточной мочи (Vres) через 3, 6, 9 и 12 месяцев после начала применения препарата Инфемин; 3) общие индексы IPSS (интенсивность симптоматики), QoL (качество жизни), IIEF (Международный Индекс Эректильной функции) и субиндексы IEEF (A, B, C, D, E) через 3, 6, 9 и 12 месяцев после начала применения препарата Ин-фемин. Анализ параметров эффективности проводился на основании результатов гистологического исследования биоптатов ПЖ, ТРУЗИ, уродинамического исследования, данных опросников IPSS, QoL и IIEF.
Статистическая обработка. Все рассчитанные показатели представлены в виде Ме (Q1; Q3), где Me – медиана, (Q1; Q3) - интерквартильный интервал: верхняя граница нижнего квартиля (Q1) и нижняя граница верхнего квартиля (Q3). Для определения статистической значимости различий между группами использовали U-критерий Манна-Уитни, а также критерий хи-квадрат с поправкой Йетса. Статистически достоверными считали различия при р<0,05. Статистическая обработка результатов исследования проводилась с использованием пакетов программ SPSS Statistics 19.0 и Microsoft Excel 2007.
РЕЗУЛЬТАТЫ
В исследование эффективности препарата Инфемин были включены мужчины в возрасте от 56 до 72 лет с верифицированным диагнозом PIN низкой степени. Необходимо отметить, что у всех включенных в исследование пациентов PIN развилась на фоне доброкачественной гиперплазии предстательной железы. Основная и контрольная группы до включения в исследование не отличались между собой по основным демографическим показателям (раса, возраст, курение), а также другим данным исходного состояния (заболевания в анамнезе и сопутствующие заболевания). В группах исследования не было выявлено значимых отличий по основным жизненным показателям, лабораторным показателям анализа крови и мочи, ЭКГ, уро-динамическим параметрам, уровню ПСА. Группы не различались по индексам IPSS, QoL и IIEF (общий и пять субиндексов A, B, С, D, E). Полученные данные свидетельствовали о возможности объединения пациентов в группы для анализа, считая выборку исследования гомогенной.
По результатам анализа промежуточных данных, полученных в ходе настоящего рандомизированного двойного слепого плацебо-контролируемого исследования эффективности препарата Инфемин при лечении PIN на фоне ДГПЖ, оценивалась динамика главного критерия эффективности – морфологического индекса.
Было показано, что если до начала лечения в группе терапии препаратом Инфемин МИ составлял 0,50, то после 12-месячного курса терапии МИ снизился до 0,04. В то же время в группе плацебо отмечалось увеличение МИ с 0,42 до 0,58 (рис. 1). Сравнение величин МИ в группах исследования через 12 месяцев лечения показало, что в группе терапии препаратом Инфе-мин МИ был значимо ниже в
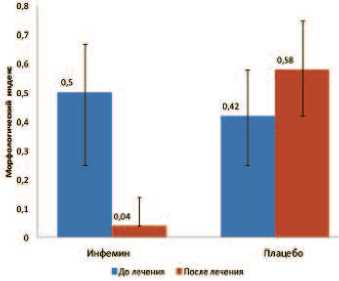
Рис. 1. Величина морфологического индекса у пациентов с диагнозом PIN до и после лечения в течение 12 месяцев в группах терапии препаратом Инфемин и плацебо. Данные представлены в виде Me (Q1; Q3)
(p=0,008, критерий Манна-Уитни), чем в группе плацебо и составлял, соответственно 0,04 против 0,58.
Известно, что наиболее важным дополнительным критерием эффективности лечения PIN является оценка частоты полного излечения данного заболевания. В настоящем исследовании оценивалась доля пациентов с сохраняющейся PIN/ДГПЖ по результатам терапии препаратом Инфемин. Было установлено, что проводимая в течение 12 месяцев терапия препаратом Инфемин привела к регрессу PIN у 50% пациентов. В то же время в группе плацебо регресс PIN не наблюдался ни у одного пациента (рис. 2). Однако при данном объеме выборки статистическая значимость различий между группами Инфемин и плацебо по данному показателю достигнута не была (p=0,209, хи-квадрат с поправкой Йетса).
Расчет доли пациентов с РПЖ не проводился, поскольку данный диагноз через 12 месяцев наблюдения был выявлен лишь у одного пациента в группе плацебо.
При анализе дополнительных критериев эффективности выявлено уменьшение показателя уродинамики Vres через 3 месяца после начала исследования (таб. 1). При этом значимость различий между группами Инфемин и плацебо составила 0,0497 (критерий Манна-Уитни), что позволяет предположить, что в дальнейшем при увеличении объема выборки значимость различий будет сохраняться на уровне менее 0,05. При этом через 6 месяцев терапии и через 9 месяцев терапии величина Vres в группе терапии препаратом Инфе-мин не различалась с соответствующими показателями в группе плацебо (p=0,176, p=0,807, соответственно; критерий Манна-Уитни).
Что касается других дополнительных параметров оценки эффективности терапии, в группе приема препарата Инфемин положительная динамика (уменьшение) была установлена для объема предстательной железы (табл. 1). Однако частота уменьшения объема предстательной железы в группе препарата по сравнению с плацебо не достигла уровня статистической значимости через 3, 6 и 9 месяцев после начала
Таблица 1. Динамика показателей эффективности лечения в группах терапии препаратом Инфемин и плацебо
применения препарата (p=0,170, p=0,311, p=0,365, соответственно; критерий Манна-Уитни), что, вероятно, связано с недостаточным объемом выборки. Возможно, по этой же причине при сравнении эффективности терапии в группах исследования по показателям Qmax и Qave через 3, 6 и 9 месяцев терапии значимых различий также установлено не было (табл. 1).
По результатам сравнения эффективности терапии в группах исследования в отношении качества жизни (QoL), симптомов, отражающих расстройство мочеиспускания (индекс IPSS), различных аспектов половой функции пациентов (индекс IIEF и субиндексы A, B, C, D, E) не было установлено значимых различий через 3, 6 и 9 месяцев терапии (критерий Манна-Уитни). Количественные значения исследуемых показателей представлены в таблицах 1 и 2.
Анализ дополнительных параметров эффективности по итогам 12 месяцев терапии не проводился в связи с недостаточным объемом выборки и, соответственно, количеством полученных данных.
ОБСУЖДЕНИЕ
Результаты проведенного промежуточного двойного слепого плацебо-контролируемого исследования под-
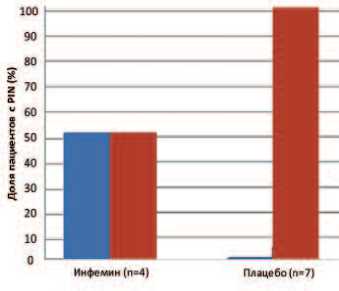
■ Нет «Да
Рис. 2. Доля пациентов с сохраняющейся PIN в группах терапии препаратом Инфемин и плацебо через 12 месяцев после начала лечения
|
Инфемин Me (Q1;Q3) |
Плацебо Me (Q1;Q3) |
|||||||
|
Показатель |
Скрининг |
3 мес. |
6 мес. |
9 мес. |
Скрининг |
3 мес. |
6 мес. |
9 мес. |
|
Объем остаточной мочи (Vres), мл |
25 (14;50) |
15* (0;32) |
19 (0;33) |
15 (0;30) |
30 (10;50) |
30 (15;65) |
39 (0;68) |
13 (0;48) |
|
Объем предстательной железы, см3 |
50 (37;64) |
48 (37;65) |
49 (37;61) |
46 (38;24) |
56 (41;72) |
53 (38;81) |
55 (40;93) |
58 (46;79) |
|
Максимальная скорость потока мочи (Qmax), мл/c |
15 (12;18) |
15 (12;20) |
14 (10;20) |
14 (12;19) |
14 (11;19) |
15 (12;18) |
15 (12;18) |
14 (9;18) |
|
Средняя скорость потока мочи (Qave), мл/c |
7 (5;9) |
8 (6;9) |
7 (5;10) |
6 (5;9) |
7 (5;10) |
8 (5;9) |
7 (6;9) |
7 (5;10) |
|
Интенсивность симптоматики (индекс IPSS) |
9 (5;17) |
10 (5;16) |
10 (7;16) |
10 (5;17) |
11 (5;16) |
12 (8;15) |
11 (7;15) |
8 (4;16) |
|
Качество жизни (индекс QoL) |
3 (2;5) |
3 (2;4) |
3 (2;4) |
3 (2;4) |
3 (2;4) |
3 (2;4) |
3 (2;4) |
3 (1;3) |
* p ≤0,05 – статистически значимые различия с группой плацебо
тверждают, что применение препарата Инфемин в течение 12 месяцев у больных с диагнозом PIN низкой степени на фоне ДГПЖ приводит к значительному улучшению морфологической структуры ПЖ (снижение МИ с 0,50 до 0,04), что свидетельствует о практически полном угнетении под действием данного препарата пролиферативной активности эпителия ПЖ. У 50% пациентов в группе терапии препаратом Инфемин также наблюдался полный регресс PIN, что является важ-
Таблица 2. Динамика различных аспектов половой функции пациентов (индекс IIEF и субиндексы A, B, C, D, E) в группах терапии препаратом Инфемин и плацебо
|
Инфемин Me (Q1;Q3) |
Плацебо Me (Q1;Q3) |
|||||||
|
Показатель |
Скрининг |
3 мес. |
6 мес. |
9 мес. |
Скрининг |
3 мес. |
6 мес. |
9 мес. |
|
Эректильная |
46 |
44 |
52 |
51 |
53 |
52 |
40 |
41 |
|
функция (индекс IIEF) |
13;58) |
(13;57) |
(27;60) |
(11;60) |
(12;62) |
(12;61) |
(11;55) |
(11;62) |
|
Субиндекс (A) собственно |
17 |
16 |
20 |
20 |
22 |
20 |
17 |
17 |
|
эректильной функции |
(4;25) |
(3;24) |
(8;24) |
(3;24) |
(3;27) |
(3;28) |
(4;24) |
(6;26) |
|
Субиндекс (B) |
8 |
8 |
8 |
9 |
8 |
8 |
6 |
6 |
|
оргазмической функции |
(0;10) |
(0;10) |
(2;10) |
(0;10) |
(0;10) |
(0;10) |
(0;10) |
(0;10) |
|
Субиндекс (C) |
6 |
6 |
6 |
5 |
6 |
6 |
6 |
5 |
|
интенсивности либидо |
(4;7) |
(4;7) |
(4;7) |
(3;7) |
(4;8) |
(4;7) |
(4;7) |
(4;7) |
|
Субиндекс (D) |
8 |
8 |
8 |
8 |
9 |
8 |
8 |
6 |
|
удовлетворенности половым актом |
(0;10) |
(0;10) |
(0;10) |
(0;10) |
(0;11) |
(0;10) |
(0;9) |
(0;11) |
|
Субиндекс (E) общей удовлетво- |
6 |
6 |
8 |
8 |
8 |
7 |
5 |
6 |
|
ренности половой функцией |
(3;8) |
(4;8) |
(4;8) |
(4;8) |
(4;8) |
(4;8) |
(4;8) |
(4;8) |
ным дополнительным критерием эффективности терапии, хотя значимость различий при данном количестве пациентов достигнута не была. На протяжении всего периода наблюдения за пациентами исследователями также была отмечена положительная динамика (уменьшение) объема предстательной железы и показателя уродинамики Vres через 3 месяца после начала исследования (p=0,0497, критерий Манна-Уитни). Оценка качества жизни, симптомов, отражающих расстрой- ство мочеиспускания и симптомов эректильной дисфункции не выявила значимых отличий с группой плацебо. Улучшение состояния по данным показателям будет проанализировано для большого количества пациентов.
Таким образом, можно заключить, что Инфемин является эффективным препаратом для лечения ДГПЖ и PIN низкой степени и, соответственно, для профилактики рака предстательной железы. Это позволяет рассматривать использование препарата Инфемин в клинической практике у пациентов с PIN низкой степени и симптомами ДГПЖ.
Научно-исследовательские и опытно-конструкторские работы были выполнены в ФГАОУ ВО «Российский университет дружбы народов» в рамках исполнения договора № 02.G25.31.0080 от «23» мая 2013 г. на реализацию комплексного проекта по созданию высокотехнологичного производства «Производство лекарственных средств на основе биотехнологий для лечения социально значимых заболеваний» финансируемого Министерством образования и науки Российской Федерации в соответствии с постановлением Правительства РФ №218 от 9 апреля 2010 года. □
Резюме:
Список литературы Эффективность применения препарата инфемин у пациентов с PIN низкой степени с сопутствующей доброкачественной гиперплазией предстательной железы
- Siegel R, Naishadham D, Jemal A. Cancer statistics, 2012.//CA Cancer J Clin. 2012. Vol. 62, N 1. P.10-29.
- Ferlay J, Soerjomataram I, Ervik M, Dikshit R, Eser S, Mathers C, Rebelo M, Parkin DM, Forman D, Bray, F. GLOBOCAN 2012 v 1.1, Cancer Incidence and Mortality Worldwide: IARC CancerBase No. 11 . Lyon, France: International Agency for Research on Cancer; 2014.//URL: http://globocan.iarc.fr, accessed on 16/01/2015.chp.fut.ru/?p=stages
- Злокачественные новообразования в России в 2012 году (заболеваемость и смертность). . М.: ФГБУ «МНИОИ им. П.А. Герцена» Минздрава России, 2014. 250 с.//URL: http://www.oncology.ru/service/statistics/malignant_tumors/2012.pdf.
- Bostwick DG, Brawer MK. Prostatic intra-epithelial neoplasia and early invasion in prostate Cancer.// Cancer. 1987. Vol. 59, N 4. P. 788-794.
- Helpap BG, Bostwick DG, Montironi R. The significance of atypical adenomatous hyperplasia and prostatic intraepithelial neoplasia for the development of prostate carcinoma. An update.// Virchows Arch. 1995. Vol. 426, N 5. P. 425-434.
- Bostwick DG, Amin MB, Damjanov I, Linder J. Prostate and seminal vesicles.//In: Anderson’s pathology. ,, 10th edn. St. Louis: Mosby, 1996, 2197-230.
- Epstein JI, Grignon DJ, Humphrey PA, McNeal JE, Sesterhenn IA, Tron-coso P, Wheeler TM. Interobserver reproducibility in the diagnosis of prostatic intraepithelial neoplasia.//Am J Surg Pathol. 1995 Vol. 19, N 8. P. 873-886.
- Bostwick DG, Liu L, Brawer MK, Qian J. High-Grade Prostatic Intraepithelial Neoplasia. // Rev Urol. 2004. Vol. 6, N 4. P. 171-179.
- Harvey H. A unifying hypothesis that links benign prostatic hyperplasia and prostatic intraepithelial neoplasia with prostate cancer. Invited comments.// Pathol Res Pract. 1995. Vol. 191, N 9. P. 924-934.
- Heilen CA, Chang C. Androgen receptor in prostate cancer.// Endocrine Reviews. 2004. Vol. 25, N 2. P. 276-308.
- Garda-Cruz E, Piqueras M, Ribal MJ, Huguet J, Serapiao R, Peri L, Izquierdo L, Alcaraz A. Low testosterone level predicts prostate cancer in re-biopsy in patients with high grade prostatic intraepithelial neoplasia.//BJU Int. 2012. 110, N 6, Pt B. P. 199-202.
- Roy AK, Lavrovsky Y, Song CS, Chen S, Jung MH, Velu NK, Bi BY, Chatterjee B. Regulation of androgen action. // Vitam Horm. 1999. Vol. 55. P. 309-352.
- Stein MN, Patel N, Bershadskiy A, Sokoloff A, Singer EA. Androgen synthesis inhibitors in the treatment of castration-resistant prostate cancer. // Asian J Androl. 2014.Vol. 16, N 3. P. 387-400.
- Farnsworth WE. Roles of estrogen and SHBG in Prostate physiology.// Prostate 1996. Vol. 28, N 1. P.17-23.
- De Marzo AM, Platz EA, Sutcliffe S, Xu J, Grönberg H, Drake CG, Nakai Y, Isaacs WB, Nelson WG. Inflammation in prostate carcinogenesis. // Nat Rev Cancer. 2007. Vol. 7, N 4. P. 256-269.
- Kang GH, Lee S, Lee HJ, Hwang KS. Aberrant CpG island hyperme-thylation of multiple genes in prostate cancer and prostatic intraepithelial neoplasia. // J Pathol. 2004. Vol. 202, N 2. P. 233-240.
- Abbas A, Gupta S. The role of histone deacetylases in prostate cancer. // Epigenetics. 2008. Vol. 3, N 6. P. 300-309.
- Banerjee S, Kong D, Wang Z, Bao B, Hillman GG, Sarkar FH. Attenuation of multi-targeted proliferation-linked signaling by 3, 3'-diindolylmethane (DIM): from bench to clinic. // Mutat Res. 2011. Vol. 728. P. 47-66.
- Le HT, Schaldach CM, Firestone GL, Bjeldanes LF. Plant-derived 3, 3'-Diindolylmethane is a strong androgen antagonist in human prostate cancer cells. // J Biol Chem. 2003. Vol. 278. P. 21136-21145.
- Souli E, Machluf M, Morgenstern A, Sabo E, Yannai S. Indole-3-carbinol (I3C) exhibits inhibitory and preventive effects on prostate tumors in mice. // Food Chem Toxicol. 2008. Vol. 46. N 3. P. 863-870.
- Fares F. The Anti-Carcinogenic Effect of Indole-3-Carbinol and 3, 3'-Diindolylmethane and their Mechanism of Action.//Med Chem. 2014. S1 DOI: 10.4172/2161-0444.S1-002
- Wu TY, Khor TO, Su ZY, Saw CL, Shu L, Cheung KL, Huang Y, Yu S, Kong AN. Epigenetic modifications of Nrf2 by 3, 3’-diindolylmethane in vitro in TRAMP C1 cell line and in vivo TRAMP prostate tumors. // AAPS J. 2013. Vol.15, N 3. P. 864-874.
- Beaver LM1, Yu TW, Sokolowski EI, Williams DE, Dashwood RH, Ho E. 3, 3'-Diindolylmethane, but not indole-3-carbinol, inhibits histone deacetylase activity in prostate cancer cells. // Toxicol Appl Pharmacol. 2012. Vol. 263. N 3. P. 345-51.
- Xue L, Firestone GL, Bjeldanes LF. DIM stimulates IFN-gamma gene expression in human breast cancer cells via the specific activation of JNK and p38 pathways.// Oncogene. 2005. Vol. 24. P. 2343-2353.
- Cho HJ, Seon MR, Lee YM, Kim J, Kim JK, Kim SG, Park JH. 3, 3'-Di-indolylmethane suppresses the inflammatory response to lipopolysaccha-ride in murine macrophages. // J Nutr. 2008. Vol. 138. N 1, P. 17-23.
- Kong D, Li Y, Wang Z, Banerjee S, Sarkar FH. Inhibition of angiogenesis and invasion by 3, 3'-diindolylmethane is mediated by the nuclear factor-kappaB downstream target genes MMP-9 and uPA that regulated bioavailability of vascular endothelial growth factor in prostate cancer. // Cancer Res. 2007. Vol. 67. N 7, P. 3310-3319.
- Wu T, Chen C, Li F, Chen Z, Xu Y, Xiao B, Tao Z. 3, 3'-Diindolylmethane inhibits the invasion and metastasis of nasopharyngeal carcinoma cells in vitro and in vivo by regulation of epithelial mesenchymal transition. // Exp Ther Med. 2014. Vol. 7, N 6. P. 1635-1638.
- Semov A, Iourtchenco L, Liu LF, Li S, Yan X, Xiaoxue S, Muyjnek E, Kiselev V, Alakhov V. Diindolylmethane (DIM) selectively inhibits cancer stem cells.//Biochem Biophys Res Commun. 2012. Vol. 424:45-51.
- Kiselev VI. Diindolylmethane-based drug for the treatment of hyperplastic and inflammatory diseases.//WO 2011/136691 A1. 2011.


