Эффективность протеаз панкреатина и трипсина при ферментативном гидролизе коллагена
Автор: Семенычева Людмила Леонидовна, Егорихина Марфа Николаевна, Часова Виктория Олеговна, Валетова Наталья Борисовна, Митин Александр Вячеславович, Кузнецова Юлия Леонидовна
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Органическая химия
Статья в выпуске: 1 т.12, 2020 года.
Бесплатный доступ
Проведен анализ молекулярно-массовых характеристик (ММХ) (молекулярной массы (ММ) и коэффициента полидисперсности (КП)) гидролизата высокомолекулярного рыбного коллагена (РК) в процессе ферментативного гидролиза двумя протеолитическими ферментами: панкреатином и трипсином при комнатной температуре. Показана высокая эффективность ферментов: основная часть РК гидролизуется в течение первой минуты как в случае панкреатина, так и трипсина, при этом образуется несколько фракций гидролизата РК. В случае трипсина наблюдается небольшая олигомерная фракция. Коэффициент полидисперсности Мw/Мn для фракций в процессе гидролиза имеет значения преимущественно не более 1,2, что свидетельствует об однородности фракций коллагена по ММ. Исходный нативный РК с ММ ~ 300 кДа во фракциях гидролизата отсутствует. Эти данные свидетельствуют о высокой скорости гидролиза в присутствии указанных ферментов. Для обоих ферментов наблюдается образование двух низкомолекулярных фракций гидролизата с близкими значениями ММ ~ 17 кДа и ~ 9 кДа, причем доля последней фракции в растворе больше 80 %. Последующий контроль ММХ показал, что происходит медленное уменьшение доли всех фракций до практически полного исчезновения за трое суток, кроме низкомолекулярной фракции с ММ ~ 9 кДа, содержание которой постепенно увеличивается. Вид кривых молекулярно-массового распределения (ММР) для разных ферментов практически одинаков, однако наблюдается небольшое различие в соотношениях фракций гидролизатов на разных стадиях гидролиза при использовании указанных ферментов, связанное с незначительной разницей в эффективности использованных ферментов, которое может отразиться на строении скаффолда в процессе его формирования. Различия в значениях ММ и соотношении фракций с разной ММ свидетельствуют о влиянии природы ферментов на процесс гидролиза высокомолекулярного коллагена. Представленные результаты хорошо согласуются с известными литературными данными о природе ферментов панкреатина. Протеолитические ферменты, входящие в состав панкреатина, - трипсин, пепсин и химотрипсин - катализируют гидролиз пептидных связей, образованных остатками аминокислот аргинина и лизина. Ярко выраженная ограниченная субстратная специфичность ферментов приводит к практически количественному образованию в процессе гидролиза узкодисперсного олигомера с ММ ~ 9 кДа. В совокупности с результатами исследований действия ферментов на другие компоненты конструкции скаффолдов, а также биомиметическими испытаниями они позволят моделировать состав, строение и важнейшие характеристики скаффолдов с оптимизированными свойствами. Это особенно важно, если в процессе формирования скаффолдов и биомедицинских клеточных продуктов используются реакции ферментативного гидролиза, так как получаемая в результате клеточная матрица формируется не из нативных молекул, а из их гидролизатов.
Биополимеры, скаффолды, высокомолекулярный рыбный коллаген, панкреатин, трипсин, эффективность гидролиза
Короткий адрес: https://sciup.org/147233159
IDR: 147233159 | УДК: 547.964:544.169 | DOI: 10.14529/chem200108
Efficacy of pancreatin and trypsin proteases in enzymatic hydrolysis of collagen
The analysis of molecular-mass characteristics (MMC) / molecular mass (MM) and polydispersity coefficient (PC) of high molecular weight fish collagen (FC) hydrolysate has been carried out in the process of enzymatic hydrolysis by two proteolytic enzymes: pancreatin and trypsin at room temperature. High efficiency of enzymes has been shown: the main part of FC is hydrolyzed within the first minute in the case of both pancreatin and trypsin. As a result, several fractions of FC hydrolysate are formed. A small oligomeric fraction is observed in the case of trypsin. The values of the polydispersity coefficient Mw / Mn for fractions in the hydrolysis process are typically no more than 1.2. This indicates the homogeneity of collagen fractions in MM. The original native FC with MM ~ 300 kDa is absent in the hydrolysate fractions. These data indicate a high hydrolysis rate in the presence of these enzymes. Formation of two low-molecular fractions of hydrolysate with close values of MM ~ 17 kDa and ~ 9 kDa has been observed for both enzymes, and the share of the latter fraction in the solution is more than 80 %. Further control of MMC has shown that there is a slow decrease in the proportion of all fractions, to almost complete disappearance in three days, except for the low-molecular fraction with MM ~ 9 kDa, the content of which gradually increases. The type of molecular weight distribution curves for different enzymes is almost the same. However, there is a small difference in the ratio of hydrolysate fractions at different stages of hydrolysis with the use of these enzymes, due to a minor difference in the efficiency of the enzymes used, which may affect the structure of the scaffold during its formation. Differences in the MM values and the ratio of fractions with different MM indicate the influence of the enzyme nature on hydrolysis of high-molecular collagen. The presented results are in good agreement with the known literature data on the nature of pancreatin enzymes (it contains the proteolytic enzymes: trypsin, pepsin and chymotrypsin). These three proteases catalyze the hydrolysis of peptide bonds formed by residues of the amino acids arginine and lysine. The strongly pronounced limited substrate specificity of enzymes leads to practically quantitative formation of a narrowly dispersed oligomer with MM ~ 9 kDa in the process of hydrolysis. In combination with the results of research on the effect of enzymes upon other components of the scaffold design, as well as biomimetic tests, these will model the composition, structure, and major characteristics of scaffolds with the optimized properties. This is especially important if the enzymatic hydrolysis reactions are used in formation of scaffolds and biomedical cell products, because the resulting cell matrix is formed not from the native molecules, but from their hydrolysates.
Текст научной статьи Эффективность протеаз панкреатина и трипсина при ферментативном гидролизе коллагена
Развитие реконструктивной медицины на базе тканевой инженерии связано прежде всего с созданием новых материалов высокой функциональности, способных имитировать биологические, структурные и физические функции естественных тканей организма. В настоящее время существует высокая потребность в продуктах тканевой инженерии, в том числе в продуктах скаффолд-технологий. Основная технология использования скаффолдов – заселение клетками непосредственно перед имплантацией или во время нее [1–7]. В то же время одной из ключевых проблем при использовании даже идеального источника клеточного материала является необходимость создания подходящего искусственного биомиметического матрикса. В связи с этим основной задачей тканевой инженерии является создание клеточных матриц (скаффолдов) с последующим образованием сложных клеточных композиций, подобных ткани или органу, для дальнейшей трансплантации их пациенту взамен поврежденных или утраченных. Для создания скаф-фолдов предлагают использовать природные и синтетические полимеры. Чаще других в случае биополимеров используют белки, такие как коллаген, фибрин, фиброин шелка и др. При получении скаффолдов применяют протеолитические ферменты [8–11], гидролизующие пептидную связь белков с целью образования новых связей уже в скаффолде, при этом отмечается влияние молекулярно-массовых характеристик (ММХ) используемого полимера на свойства получаемых матриц [12–14]. Изменения молекулярных и надмолекулярных параметров биополимеров клеточных матриц при формировании скаффолдов, влияние этих параметров на биомиметические свойства при построении тканеинженерных конструкций зависят не только от природы используемого белкового материала, но и от природы фермента [15, 16]. Варьирование фермента может позволить при построении тканеинженерных конструкций моделировать характеристики скаф-фолдов.
Разрабатываемые клеточные матрицы, имитирующие естественный внеклеточный матрикс, должны обеспечивать достаточную временную механическую поддержку для развития ткани и обладать физиологической активностью, достаточной для развития межклеточных контактов, но в то же время подвергаться естественной резорбции с трансформацией в натуральный внеклеточный матрикс [3, 17]. Использование коллагена I типа широко распространено при создании скаффолдов, так как он имеет несколько преимуществ, позволяющих использовать данный биополимер для получения продуктов тканевой инженерии: биосовместимость, волокнистая структура, хорошая сочетаемость с другими материалами, биодеградируемость [2, 3, 18, 19].
Однако нативный коллаген представляет собой быстро разлагаемый биополимер из-за своей фибриллярной волокнистой структуры. Но в сочетании с другими синтетическими и природными полимерами этот недостаток с легкостью устраняется, более того, наблюдается увеличение жесткости и упругости гибридного материала в условиях ферментативного разрушения нативных молекул белка [13, 20, 21]. Ранее было установлено, что при гидролизе нативного высокомолекулярного коллагена I типа, выделенного из кожных покровов разных животных, в стандартных условиях в присутствии панкреатина происходит гидролиз с достаточно высокой скоростью [22].
Целью данного исследования является сравнение ММХ рыбного коллагена (РК) в процессе гидролиза в присутствии многокомпонентного фермента панкреатина, в состав которого входят протеолитические ферменты трипсин, пепсин, и химотрипсин, а также только трипсина в условиях, близких к условиям формирования скаффолдов [23]. Главной задачей при этом стал контроль ММХ гидролизата коллагена в течение длительного времени.
Экспериментальная часть
В работе использовали коммерческие ферменты: панкреатин [Хубей Максфарм Индастриз Ко. Лтд (Китай)], трипсин [ООО НПП «ПанЭко»], AcOH (ХЧ). Высокомолекулярный рыбный коллаген (РК) выделяли по методу [24].
При проведении ферментативного гидролиза использовали 1%-ный раствор РК. К раствору высокомолекулярного РК добавляли 1М NaOH для достижения нейтральной среды и доводили дистиллированной водой до определенного объема. Гидролиз в присутствии ферментов проводили при фермент-субстратном соотношении коллаген : фермент = 10:1, добавляя к полученной смеси фермент. Из реакционной среды брали пробы (1 мл) через определенные промежутки времени после добавления фермента. Для прерывания гидролиза в пробы приливали 4%-ный раствор AcOH.
Молекулярно-массовые характеристики проб гидролизата РК определяли методом ГПХ с применением высокоэффективного жидкостного хроматографа фирмы Shimadzu CTO20A/20AC (Япония) с программным модулем LC-Solutions-GPC. Разделение проводили с применением колонки Tosoh Bioscience TSKgel G3000SWxl с диаметром пор 5 мкм. В качестве детектора применяли низкотемпературный светорассеивающий детектор ELSD-LT II. Элюентом служил 0,5 М раствор уксусной кислоты. Скорость потока 0,8 мл/мин. Для калибровки использовали узкодисперсные образцы декстрана с диапазоном молекулярных масс (ММ) 1 000– 410 000 Да (Fluca).
Обсуждение результатов
В соответствии с п ос та в л енной в исследовании целью проводили анал и з М МХ (ММ и КП) г идроли за т а Р К в п роц е с с е ферментативного гидролиза при комнатной тем п е ра ту ре . Ок а за лось, ч т о ос н овн ая час ть в ыс о комол екулярного РК гидролизуется в течение первой ми н уты к а к в с л учае панкреатина, так и три п с и н а (ри с . 1 ) . При использовании панкреатина образуется три фракции ги д ролиза та Р К с ММ мен е е 70 к Д а ( 13 –15 %), с ММ ~ 17,5 кДа (2,0–3,5 %) и ММ ~ 9 кДа (83–84 %), в с лу ча е ж е три п с и на н аблюдается еще небольшая олигомерная фрак ц и я (~ 1,0 %) с ММ ~ 300 Да , а фр а к ц ия и с ход н ого н а ти в н о го Р К с М М ~ 300 кДа отсутствует. То есть действ и е п а н к ре а ти н а и три п с ин а п риводит к полному разрушению исходного на ти в н ого Р К д о н и зкомол е к у лярн ых фра к ц и й у же в течение первой минуты, что свидетельствует о высокой эффективн ости ги дрол иза в п ри с у тс тв и и у к а за н н ых ферме н т ов .
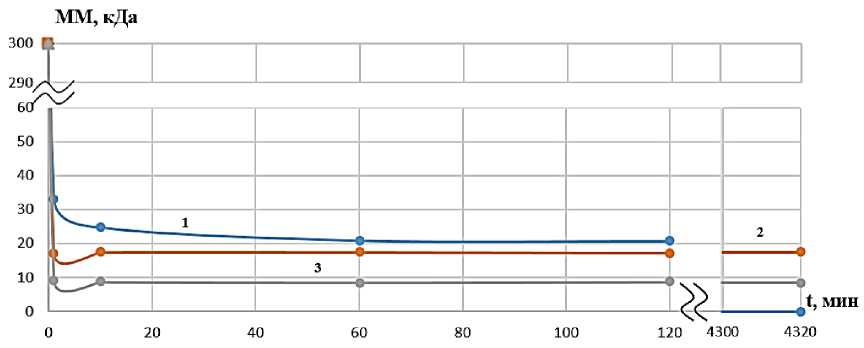
Рис. 1. Изменение молекулярной массы разных фракций при гидролизе РК панкреатином: 1 – фракция с ММ выше 17 кДа; 2 – фракция с ММ ~ 17 кДа; 3 – фракция с ММ ~9 кДа
Интересно о т ме ти ть, что наблюдается образование двух низкомолекулярн ых фрак ц и й ги д р олизата со значениями ММ ~ 17 кДа и ~ 9 кДа для обоих ферментов, при че м д оля п о с ле дн ей ф ра кци и в ра створе боль ш е 80 % (рис. 1, 2). Последующий контроль ММХ в течение трех часов показа л ( с м. ри с. 1, 2) , что п роисходит медленное уменьшение первой фрак ц и и с М М в ы ше 17 к Да д о полн ог о и с че з н ов е ния за трое суток (кривые 1 на рис. 3, 4), соде ржа н ие в торой фра кции с ММ ~ 1 7 кД а н е много у в еличивается вначале и для панкреатина, и дл я т ри п с и н а , х отя конц ентраци я фр а к ц и и н е много различается в образцах гидролизата разными ф е рме н та ми ( к ри в ы е 2 н а ри с . 3, 4) , а за те м и зме н яе т ся мало, содержание низкомолекулярной фр а к ц и и с ММ ~ 9 кДа п осте п е н н о ув е л и чи вае тся ( к ри в ые 3 н а ри с . 1, 2) . Оли гоме рн а я фрак ц и я в растворе с трипсином со в ре ме не м и с че з а е т, в ид и мо, за счет разрушения до неконтролируемых ме тод ом а ми н ок и слот (к ри в а я 4 н а ри с . 4) . В обра зц а х через трое суток в растворе с панкреатином ос та е т с я толь к о гидр оли з ат Р К с ММ ~ 9 к Да ( с м. ри с . 1) в с лу ча е гидролиза трипсином доля его составляет ~ 90 % (~ 10 % РК с ММ ~ 17 кДа ) . Т о ес ть н а блю да е тс я ра зру ш е н и е и с ход н о го высокомолекулярного коллагена с о б ра зов а н и ем д в ух низкомолекулярных фракций (рис. 5, 6). О б ращает на себя внимание небольшое различие в с оотношениях фракций гидролизатов на разн ых ста д и ях ги д ро ли за п ри и с п ол ьзовани и у к а зан н ых ферментов, которое может отразиться на строе н и и ск а ф фол д а в п роц е сс е его форми ров ани я (рис. 1, 2). В табл. 1, 2 приведены значения ММ и КП в процессе гидролиза, свидетель с тв у ю щ и е об о д н ород н о с ти фрак ц и й – коэффициенты полидисперсности (К П ) имею т значени я п реи му щ е с тв е н н о н е б ол е е 1,2.
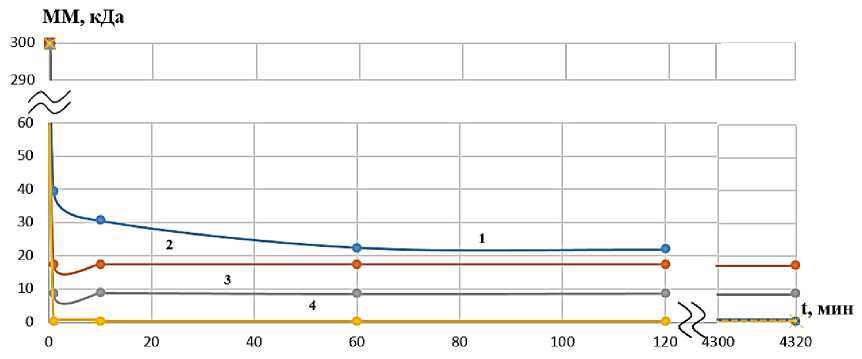
Рис. 2. Изменение молекулярной массы разных фракций при гидролизе РК трипсином: 1 – фракция с ММ выше 17 кДа; 2 – фракция с ММ ~ 17 кДа; 3 – фракция с ММ ~ 9кДа;
4 – олигомерная фракция с ММ ~ 0,3 кДа
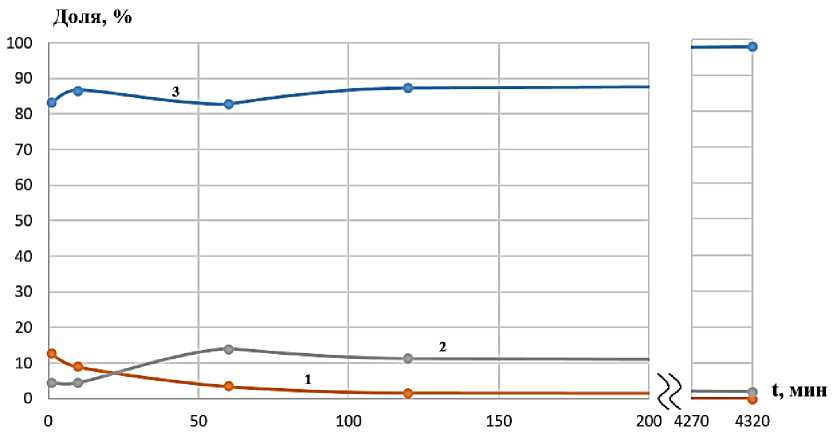
Рис. 3. Доля разных фракций при гидролизе РК панкреатином: 1 – фракция с ММ выше 17 кДа; 2 – фракция с ММ ~ 17 кДа;
3 – фракция с ММ ~ 9кДа
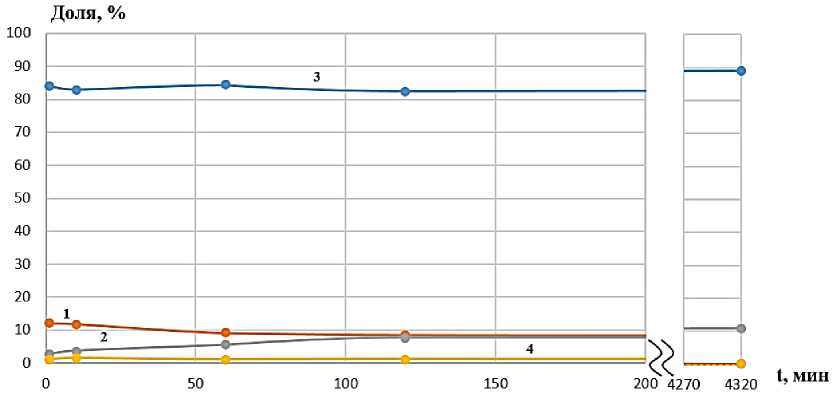
Рис. 4. Доля разных фракций при гидролизе РК трипсином: 1 – фракция с ММ выше 17 кДа; 2 – фракция с ММ ~ 17 кДа; 3 – фракция с ММ ~ 9кДа; 4 – олигомерная фракция с ММ ~ 0,3кДа
Таблица 1
Молекулярно-массовые параметры РК при ферментативном гидролизе панкреатином в течение 3 суток
|
№ п/п |
Значения ММХ во время гидролиза |
|||||||||
|
мин |
3 суток |
|||||||||
|
1 |
10 |
60 |
120 |
|||||||
|
М w ·10–3 |
М w /М n |
М w ·10–3 |
М w /М n |
М w ·10–3 |
М w /М n |
М w ·10–3 |
М w /М n |
М w ·10–3 |
М w /М n |
|
|
1 |
33,1 |
1,2 |
24,9 |
1,1 |
21 |
1,0 |
20,8 |
1,0 |
– |
– |
|
2 |
17,5 |
1,0 |
17,5 |
1,0 |
17,3 |
1,0 |
17,5 |
1,0 |
17,2 |
1,0 |
|
3 |
9,2 |
1,0 |
8,7 |
1,0 |
8,5 |
1,0 |
8,7 |
1,0 |
8,3 |
1,0 |
Таблица 2
|
№ п/п |
Значения ММХ во время гидролиза |
|||||||||
|
мин |
3 суток |
|||||||||
|
1 |
10 |
60 |
120 |
|||||||
|
М w ·10–3 |
М w /М n |
М w ·10–3 |
М w /М n |
М w ·10–3 |
М w /М n |
М w ·10–3 |
М w /М n |
М w ·10–3 |
М w /М n |
|
|
1 |
39,5 |
1,3 |
30,7 |
1,2 |
22,5 |
1,0 |
21,9 |
1,0 |
– |
– |
|
2 |
17,4 |
1,0 |
17,4 |
1,0 |
17,4 |
1,0 |
17,4 |
1,0 |
17,1 |
1,0 |
|
3 |
8,6 |
1,0 |
8,8 |
1,0 |
8,6 |
1,0 |
8,7 |
1,0 |
8,6 |
1,0 |
|
4 |
0,3 |
1,4 |
0,3 |
1,5 |
0,3 |
1,3 |
0,3 |
1,3 |
– |
– |
Различия в значениях ММ и соотношении фракций с разной ММ свидетельствуют о влиянии природы ферментов на процесс гидролиза высокомолекулярного коллагена. Представленные результаты хорошо согласуются с известными литературными данными о природе ферментов панкреатина (в его составе протеолитические ферменты трипсин, пепсин и химотрипсин), которые катализируют гидролиз пептидных связей, образованных остатками аминокислот аргинина и лизина [25]:
Н2О панкреатин, тромбин
R-Arg-Lys-R, ------* R~Arg—ОН + HlvsR,, где R и R1 – аминокислотные последовательности фрагментов коллагена.
Эта ярко выраженная ограниченная субстратная специфичность ферментов приводит к практически количественному образованию (более 80 % от исходного) в процессе гидролиза узкодисперсного (КП~ 1,1) низкомолекулярного полимера с ММ~9 кДа и небольшого количества его димера – олигомера с М w ~ 17–18 кДа (КП~ 1,1). Незначительные различия в значениях ММ первой, более высокомолекулярной в сравнении с олигомерными, фракции в присутствии двух разных ферментов связаны, видимо, с различиями в природе и эффективности, связанной с расположением аминокислот каталитических центров ферментов, что характерно для катализаторов любого происхождения [25].
Заключение
Таким образом, проведен ферментативный гидролиз коллагена, выделенного из покровных тканей трески, в условиях, близких к таковым при формировании скаффолдов, разными ферментами – панкреатином, трипсином. Анализ молекулярно-массовых характеристик гидролизатов коллагена методом гель-проникающей хроматографии в течение трех суток процесса показал, что разрушение белка происходит с образованием двух низкомолекулярных фракций сразу после 1-й минуты гидролиза, ММ которых независимо от природы фермента имеют значения Мw~9 кДа (M w /M n ~ 1,1) (более 80 % в смеси) и М w ~ 17–18 кДа (M w /M n ~ 1,1). Высокая эффективность панкреатина и трипсина приводит к тому, что в растворе сразу после первой минуты отсутствует высокомолекулярная фракция, ферменты разрушают коллаген до фрагментов не более 40 кДа. Однако заметно небольшое различие в характеристиках продуктов гидролиза и их соотношении, что обусловлено природой каталитических центров ферментов. Полученные данные представляют интерес для разработки матриц на основе коллагена в присутствии ферментов разной природы. В совокупности с результатами исследований действия ферментов на другие компоненты конструкции скаффолдов, а также биомиметическими испытаниями они позволят моделировать состав, строение и важнейшие характеристики скаффолдов с оптимизированными свойствами. Это особенно важно, если в процессе формирования скаффолдов и биомедицинских клеточных продуктов используются реакции ферментативного гидролиза и получаемая в результате клеточная матрица формируется не из нативных молекул, а из их гидролизатов.
Работа выполнена с использованием оборудования ЦКП «Новые материалы и ресурсосберегающие технологии» НИИХ ННГУ.
Список литературы Эффективность протеаз панкреатина и трипсина при ферментативном гидролизе коллагена
- Lu, T. Techniques for Fabrication and Construction of Three-dimensional Scaffolds for Tissue Engineering / T. Lu, Y. Li, T. Chen // Int. J. Nanomedicine. - 2013. - № 8. - P. 337-350. DOI: 10.2147/IJN.S38635
- Introduction to Tissue Engineering and Application for Cartilage Engineering / N. de Isla, C. Huseltein, N. Jessel et al. // Biomed. Mater. Eng. - 2010. - V. 20, № 3. - P. 127-133. DOI: 10.3233/BME-2010-0624
- Zhang, L. The Role of Tissue Engineering in Articular Cartilage Repair and Regeneration / L. Zhang, J. Hu, K.A. Athanasiou // Crit Rev. Biomed. Eng. - 2009. - V. 37, № 1. - P. 1-57.
- Rajangam, T. Fibrinogen and Fibrin Based Micro and Nano Scaffolds Incorporated with Drugs, Proteins, Cells and Genes for Therapeutic Biomedical Applications / T. Rajangam, S.S.A. An // Int. J. Nanomedicine. - 2013. - V. 8. - P. 3641-3662. DOI: 10.2147/IJN.S43945
- Fibrin Scaffold as a Carrier for Mesenchymal Stem Cells and Growth Factors in Shoulder Rotator Cuff Repair / A. Voss, McCarthy M. Beth, D. Allen et al. // Arthrosc. Tech. Arthroscopy Association of North America. - 2016. - V. 5, № 3. - P. e447-e451. DOI: 10.1016/j.eats.2016.01.029
- Osathanon, T. Immobilization of Alkaline Phosphatase on Microporous Nanofibrous Fibrin Scaffolds for Bone Tissue Engineering / T. Osathanon, C.M. Giachelli, M.J. Somerman // Biomaterials. - 2009. - V. 30, № 27. - P. 4513-4521.
- DOI: 10.1016/j.biomaterials.2009.05.022
- Riopel, M. Fibrin, a Scaffold Material for Islet Transplantation and Pancreatic Endocrine Tissue Engineering / M. Riopel, M. Trinder, W. Rennian // Tissue Eng. Part B Rev. - 2015. - V. 21, № 1. - P. 33-44.
- DOI: 10.1089/ten.teb.2014.0188
- Fibrin Gel as an Injectable Biodegradable Scaffold and Cell Carrier for Tissue Engineering / Y. Li, H. Meng, Y. Liu, B.P. Lee // Sci. World J. - 2015. - № 2015. - P. 1-10.
- DOI: 10.1155/2015/685690
- Терещенко, В.П. Матрицы-носители в тканевой инженерии костной ткани / В.П. Терещенко, И.А. Кирилова, П.М. Ларионов // Успехи современного естествознания. - 2015. - № 8. - С. 66-70.
- Yan, M. Purification and Structural Aspects of Type I Collagen from Walleye Pollock (Theragrachalcogramma) / M. Yan, S. Qin, B. Li // J. Aquat. Food Prod. Technol. - 2017. - V. 26, № 10. - P. 1166-1174.
- DOI: 10.1080/10498850.2015.1011797
- Effect of Enzymatic Hydrolysis on Surface Activity and Surface Rheology of Type I Collagen / A. Kezwoń, I. Chromińska, T. Fraczyk, K. Wojciechowski // Colloids Surf., B. - 2016. - № 137. - P. 60-69.
- DOI: 10.1016/j.colsurfb.2015.05.017
- Соколова, А.И. Зависимость биологических свойств скаффолдов из фиброина шелка и желатина от состава и технологии изготовления / А.И. Соколова, М.М. Боброва, Л.А. Сафронова // Современные технологии в медицине. - 2016. - Т. 8, № 3. - С. 6-15.
- DOI: 10.17691/stm2016.8.3.01
- Incorporation of Fibrin into a Collagen-glycosaminoglycan Matrix Results in a Scaffold with Improved Mechanical Properties and Enhanced Capacity to Resist Cell-mediated Contraction / C.M. Brougham, T.J. Levingstone, S. Jockenhoevel et al. // Acta Biomater. - 2015. - № 26. - P. 205-214.
- DOI: 10.1016/j.actbio.2015.08.022
- Bio-printing of Collagen and VEGF-releasing Fibrin Gel Scaffolds for Neural Stem Cell Culture / Y.B. Lee, S. Polio, W. Lee et al. // Exp. Neurol. - 2010. - V. 223, № 2. - P. 645-652.
- DOI: 10.1016/j.expneurol.2010.02.014
- Константиновская, М.А. Подбор условий получения ферментативного гидролизата из бульона, образующегося при производстве костной муки / М.А. Константиновская, А.А. Красноштанова // Техника и технология пищевых производств. - 2014. - № 4 (35). - С. 32-33.
- Закономерности гидролиза сывороточных белков экзо- и эндопротеазами / Т.Н. Головач, Н.В. Гавриленко, Н.К. Жабанос, В.П. Курченко // Труды БГУ. - 2008. - Т. 3 (1). - С. 85-98.
- Ma, P.X. Biomimetic Materials for Tissue Engineering / P.X. Ma // Adv. DrugDeliv. Rev. - 2008. - № 60. - P. 184-198.
- DOI: 10.1016/j.addr.2007.08.041
- Biocompatibility of Hydrogel-based Scaffolds for Tissue Engineering Applications / S. Naahidi, M. Jafari, M. Logan et al. // Biotechnol. Adv. Elsevier. - 2017. - V. 35, № 5. - P. 530-544.
- DOI: 10.1016/j.biotechadv.2017.05.006
- Zhu, J. Biomimetic Hydrogels as Scaffolds for Tissue Engineering / J. Zhu // J. Biochips Tissue Chips. - 2012. - V. 2, № 43. - P.1000e119.
- DOI: 10.4172/2153-0777.1000e119
- Viscoelastic, Physical, and Bio-degradable Properties of Dermal Scaffolds and Related Cell Behaviour / V. Sharma, N. Patel, N. Kohli et al. // Biomed. Mater. - 2016. - V. 11, № 5. - P. 1-12.
- DOI: 10.1088/1748-6041/11/5/055001
- Rowe, S.L. Microstructure and Mechanics of Collagen-fibrin Matrices Polymerized Using Ancrod Snake Venom Enzyme / S.L. Rowe, J.P. Stegemann // J. Biomech. Eng. - 2009. - V. 131, № 6. - P. 061012.
- DOI: 10.1115/1.3128673
- Молекулярно-массовые параметры коллагена из разного сырья и динамика их изменения при ферментативном гидролизе панкреатином / Л.Л. Семенычева, Н.Б. Валетова, В.О. Часова и др. // Все материалы. Энцикл. Справочник. - 2019. - № 4. - С. 27-33.
- DOI: 10.31044/1994-6260-2019-0-4-27-33
- Пат. 2653434 Российская Федерация. Способ создания биорезорбируемого клеточного скаффолда на основе фибрина плазмы крови / М.Н. Егорихина, Г.Я. Левин, И.Н. Чарыкова, Д.Я. Алейник, Л.Н. Соснина; заявитель и патентообладатель ФГБУ "Приволжский федеральный медицинский исследовательский центр" Министерства здравоохранения РФ. - № 2017112424; заявл. 11.04.2017; опубл. 08.05.2018, Бюл. № 13. - 13 с.
- Пат. 2567171 Российская Федерация. Способ получения уксусной дисперсии высокомолекулярного рыбного коллагена / Л.Л. Семенычева, М.В. Астанина, Ю.Л. Кузнецова, Н.Б. Валетова, Е.В. Гераськина, О.А. Таранкова; заявитель и патентообладатель ООО "Системы качества жизни". - № 2014140300/13; заявл. 06.10.2014; опубл. 10.11.2015, Бюл. № 31. - 11 с.
- Бендер, М. Биоорганическая химия ферментативного катализа / М. Бендер, Р. Бергерон, М. Комияма. - М.: Мир, 1987. - 352 с.


