Эффективность вакцинации против вируса ветряной оспы и опоясывающего герпеса: анализ и обзор научных данных
Автор: Кузнецова А.М., Негоднова Е.В.
Журнал: Огарёв-online @ogarev-online
Рубрика: Медицинские науки
Статья в выпуске: 1 т.14, 2026 года.
Бесплатный доступ
Введение. Опоясывающий герпес – вирусное заболевание кожи и нервной ткани, вызываемое реактивацией вируса герпеса 3 типа, характеризующееся поражением кожи и задних корешков спинного мозга, а также межпозвонковых ганглиев. Актуальность данной темы обусловлена относительно широкой распространенностью заболевания, риском развития серьезных осложнений у большого процента заболевших, тяжелым клиническим течением, частыми рецидивами у пациентов из групп риска. Цель исследования – анализ результатов клинических исследований эффективности вакцинации против Varicella zoster virus на примере адъювантной рекомбинантной вакцины Shingrix. Материалы и методы. Проведен систематический анализ показателей профилактической эффективности инактивированной рекомбинантной вакцины Shingrix на основании рандомизированных плацебо-контролируемых клинических исследований. Для включения в обзор отобраны релевантные публикации, индексированные в PubMed. Результаты исследования. Клинические исследования относительно Shingrix (ZOE-50 (ZOSTER-006), ZOE-70 (ZOSTER-022)) показали высокую профилактическую эффективность инактивированной рекомбинантной вакцины против опоясывающего герпеса среди лиц ≥ 50 лет – 97,2 %, ≥ 60 лет – 97,6, ≥ 70 лет – 91,3, ≥ 80 лет – 91,4 %. Кроме того, данная вакцина успешно предотвращала развитие постгерпетической невралгии, а также продемонстрировала стойкую защиту на протяжении длительного времени. Клиническая эффективность рекомбинантной вакцины сохраняется в течение как минимум 10 лет после вакцинации. Также Shingrix значительно снижает частоту возникновения опоясывающего лишая у людей после трансплантации аутологичных стволовых клеток, у пациентов с гематологическими злокачественными новообразованиями. Обсуждение и заключение. По причине роста уровня заболеваемости опоясывающим герпесом основной и эффективной мерой борьбы с данным заболеванием является вакцинопрофилактика. Разработка адъювантной рекомбинантной вакцины позволила значительно повысить качество жизни иммунокомпрометированных и пожилых пациентов, входящих в группы риска по развитию опоясывающего герпеса и его осложнений. Материалы статьи помогут повысить осведомленность медицинских работников и населения в целом о современных возможностях вакцинопрофилактики. Результаты исследования будут полезны для аллергологов-иммунологов, дерматологов и неврологов в процессе ведения пациентов с опоясывающим герпесом.
Опоясывающий герпес, постгерпетическая невралгия, ветряная оспа, вирус герпеса 3 типа, адъювантная рекомбинантная вакцина, иммуносупрессивное состояние
Короткий адрес: https://sciup.org/147253580
IDR: 147253580 | УДК: 616.914:616.523:615.371 | DOI: 10.15507/2311-2468.014.202601.108-117
Efficacy of Varicella-Zoster Vaccination: An Analysis and Overview of Scientific Data
Introduction. Herpes zoster is a viral disease of the skin and nervous tissue caused by reactivation of the herpes virus type 3, characterized by lesions of the skin and posterior roots of the spinal cord, as well as the intervertebral ganglia. The relevance of this topic is due to the relatively widespread prevalence of the disease, the risk of serious complications in a large percentage of patients, severe clinical course, and frequent relapses in patients at risk. The aim of the study is to analyze the results of clinical trials of the effectiveness of vaccination against Varicella zoster virus using the example of the adjuvant recombinant vaccine Shingrix. Materials and methods. A systematic analysis of the preventive efficacy of the inactivated recombinant Shingrix vaccine was performed based on randomized placebo-controlled clinical trials. Relevant publications indexed in PubMed have been selected for inclusion in the review. Results. Clinical studies on Shingrix (ZOE-50 (ZOSTER-006), ZOE-70 (ZOSTER-022)) have shown high preventive efficacy of the inactivated recombinant vaccine against herpes zoster among people ≥ 50 years – 97.2 %, ≥ 60 years – 97.6, ≥ 70 years – 91.3, ≥ 80 years – 91.4 %. In addition, this vaccine successfully prevented the development of postherpetic neuralgia, and also demonstrated long-term protection. The clinical efficacy of the recombinant vaccine persists for at least 10 years after vaccination. Shingrix also significantly reduces the incidence of shingles in humans after autologous stem cell transplantation in patients with hematological malignancies. Discussion and conclusion. Due to the increasing incidence of herpes zoster, vaccination is the main and effective measure to combat this disease. The development of an adjuvant recombinant vaccine has significantly improved the quality of life of immunocompromised and elderly patients at risk of developing herpes zoster and its complications. The materials of the article will help to raise awareness of medical professionals and the general population about the modern possibilities of vaccine prevention. The results of the study will be useful for allergologists, immunologists, dermatologists and neurologists in the management of patients with herpes zoster.
Текст научной статьи Эффективность вакцинации против вируса ветряной оспы и опоясывающего герпеса: анализ и обзор научных данных
EDN:
в
Вирус Варицелла–Зостер является причиной двух клинических форм заболевания – первичной инфекции (ветряной оспы) и ее рецидива (опоясывающего герпеса). После перенесенной ветряной оспы возникает латентное течение инфекции, так как данный вирус сохраняется в задних корешках спинного мозга и ганглиях черепно-мозговых нервов.
Реактивация вируса происходит при возрастном иммунодефиците и на фоне иммуносупрессивного состояния, возникшего по ряду причин (инфицирование ВИЧ, пересадка костного мозга, лейкоз, химиотерапия, лимфомы, лечение системными глюкокортикостероидами и цитостатиками). По статистике более 95 % людей старше 50 лет во всем мире перенесли первичную инфекцию, поэтому большой процент населения подвержен риску развития опоясывающего герпеса (ОГ).
Постгерпетическая невралгия (ПГН) является наиболее распространенным осложнением ОГ и представляет собой хроническую боль в области пораженного дерматома. Данное осложнение может длиться годами, часто приводя к потере трудоспособности и ухудшению качества жизни пациента.
ПГН занимает третье место по частоте среди всех типов невропатической боли. Риск развития ПГН составляет 20–48 %. Другими тяжелыми осложнениями ОГ являются офтальмологические осложнения (ретинит, быстро прогрессирующий герпетический некроз сетчатки, офтальмогерпес), возникающие в 10–25 % случаев заболевания, которые могут привести к продолжительному болевому синдрому и потере зрения. Около 3 % пациентов, страдающих опоясывающим лишаем, нуждаются в госпитализации1.
Лечение и профилактика обсуждаемого заболевания представляют собой сложные клинические проблемы с продолжающимися активными исследованиями данной сферы. Именно вакцинация является одним из перспективных и жизненно необходимых направлений профилактики развития ОГ и ПГН.
Цель исследования – проведение анализа результатов клинических исследований эффективности вакцинации против вируса Варицелла–Зостер на примере адъювантной рекомбинантной вакцины Shingrix.
ОБЗОР ЛИТЕРАТУРЫ
Заболеваемость ОГ растет в глобальном масштабе, а в будущем это заболевание может перейти в ранг одного из наиболее широко распространенных инфекционных заболеваний среди взрослого населения.
В странах Европы показатель заболеваемости ОГ составляет от 2,0 до 4,6 на 1000 человек. В США в течение жизни ОГ заболевает почти каждый третий человек, и ежегодно в стране регистрируется до 1 млн новых случаев этого заболевания [1].
В Российской Федерации в 2023 году было зарегистрировано 23477 случаев ОГ, что на 40% превышает зарегистрированный уровень 2022 года. Показатель заболеваемости составляет 28,6 на 100 тысяч населения. Наиболее высокие показатели заболеваемости отмечаются в Сахалинской и Курской областях, Алтайском крае. В возрастной структуре больных ОГ на долю взрослых приходится 92 %, но стоит отметить, что данное заболевание встречается и у детей2.
-
1 Зыблева С.В., Денисенко Е.Л. Вакцинопрофилактика при опоясывающем лишае (herpes zoster). Гомель: ГУ РНПЦ РМиЭЧ, 2020. C. 27. URL: https://www.rcrm.by/upload/science/posob_doctor/2020-16.pdf (дата обращения: 20.11.2025).
-
2 Ветряная оспа и опоясывающий лишай [Электронный ресурс]. ФМБА России : сайт. URL: https://mru153.fmba.gov.ru/press-tsentr/detail/?ELEMENT_ID=70337 (дата обращения: 19.11.2025).
Согласно последним исследованиям у лиц с иммунодефицитными состояниями риск возникновения ОГ значительно выше. К примеру, частота ОГ у ВИЧ-инфицированных в 8 раз превышает средний показатель заболеваемости, а среди пациентов отделений трансплантации органов и онкологических стационаров ОГ заболевают до 25–50 % больных с летальностью до 3–5 % [1].
Основным методом борьбы с опоясывающим герпесом является профилактика этого заболевания с помощью вакцинопрофилактики. В большинстве экономически развитых стран применяются вакцины двух основных видов – живая аттенуированная вакцина ( Zostavax ), разработанная « Merck & Co. Inc. » и адъювантная рекомбинантная субъединичная вакцина ( Shingrix ), производителем которой является « GlaxoSmithKline ». Производство вакцины Zostavax в США было прекращено в ноябре 2020 года из-за более высокой эффективности рекомбинантной вакцины [2; 3].
Препарат Shingrix представляет собой инактивированную рекомбинантную субъединичную вакцину, сочетающую антиген в виде оболочечного гликопротеина Е (gE) вируса ветряной оспы и адъювантную систему AS01B. Иммунное воздействие данного белка стимулирует выработку специфических антител, тем самым формируя адаптивный иммунитет против вируса герпеса 3 типа. Фирменный адъювант AS01B, заключенный в липосомальную рецептуру, комбинирует 3-O-десацил-4'- монофосфориллипида A (MPL) сальмонеллы ( Salmonella minnesota ) и молекулу сапонина (QS-21) из растительного экстракта квиллайи мыльной ( Quillaja saponaria Molina ) [4].
Монофосфориллипид работает как агонист толл-подобного рецептора 4, стимулирует антигенпрезентирующие клетки посредством активации врожденного иммунитета. QS-21 действует как стимулятор путей врожденного иммунитета в моноцитах. Липосомальная формуляция нивелирует гемолитическую активность QS-21 и усиливает презентацию антигена3.
В зарубежной и отечественной литературе представлено большое количество результатов клинических исследований, доказывающих высокую эффективность и безопасность адъювантной рекомбинантной вакцины Shingrix . Данная обзорная статья направлена на структуризацию основной информации, способствующей повышению осведомленности медицинских работников о возможностях вакцинации против ОГ.
МАТЕРИАЛЫ И МЕТОДЫ
Для систематического обзора использовались публикации, размещенные в базе данных PubMed. Также проводился ручной поиск по спискам литературы включенных статей, изучались реестры клинических исследований. Критерии отбора публикаций:
– для поиска необходимой информации использовались такие ключевые слова, как « Shingrix », « Herpes Zoster Vaccines », « Immunogenicity and safety of the adjuvanted recombinant zoster vaccine », « A Randomized Clinical Trial »;
– основа статей строится на клинических исследованиях: рандомизированных, двойных слепых, плацебо-контролируемых, многоцентровых, международных (ZOE-50 (ZOSTER-006), ZOE-70 (ZOSTER-022), ZOE-HSCT, ZOSTER-039) и рандомизирован ных, откр ытых (ZOSTER-049, ZOSTER-026);
3Dendouga N., Fochesato M., Lockman L., Mossman S., Giannini S. Cell-mediated Immune Responses to a VaricellaZoster Virus Glycoprotein E Vaccine Using Both a TLR Agonist and QS21 in Mice. Vaccine. 2012;30(20):3126-3135.
Medical sciences 111
– в клинических исследованиях производилась оценка эффективности, безопасности и иммуногенности адъювантной рекомбинантной вакцины.
В процесс поиска и отбора статей было вовлечено 2 человека. Данная работа включала 2 этапа: оценка статьи по заголовкам и аннотациям; оценка статьи по полномасштабному тексту.
Для данной работы избирались статьи, в которых была подробно представлена информация, основанная на клинических исследованиях.
Основные показатели, по которым оценивалось действие Shingrix :
-
а) эффективность вакцины против ОГ у пациентов в возрасте от 50 до 70 лет (ZOE-50) и от 70 до 90 лет (ZOE-70), которые получили 2 дозы адъювантной рекомбинантной вакцины против опоясывающего лишая или плацебо с интервалом в 2 месяца;
-
б) эффективность вакцины против ОГ у реципиентов аутологичных трансплантатов гемопоэтических стволовых клеток в возрасте 18 лет и старше, где вводилось 2 дозы вакцины с интервалом 1-2 месяца (ZOE-HSCT);
-
в) эффективность вакцины у пациентов старше 18 лет с гемобластозами (множественная миелома, B-клеточная неходжкинская лимфома, хронический лимфоцитарный лейкоз), где вводилось 2 дозы вакцины с интервалом 1–2 месяца (ZOSTER-039);
-
г) эффективность вакцины в отношении ПГН у пациентов в возрасте от 50 до 70 лет (ZOE-50) и от 70 до 90 лет (ZOE-70), у реципиентов аутологичных трансплантатов гемопоэтических стволовых клеток в возрасте 18 лет и старше;
-
д) Эффективность вакцины в отношении профилактики осложнений, связанных с опоясывающим герпесом, кроме постгерпетической невралгии у пациентов 50 лет и старше, 70 лет и старше и у реципиентов аутологичных трансплантатов гемопоэтических стволовых клеток;
-
е) иммуногенность Shingrix у пациентов, получивших 2 дозы вакцины с интервалом в 6 месяцев (Zoster-026);
-
ж) долгосрочная эффективность Shingrix (ZOSTER-049) в возрасте 50 лет и старше в течение 11 лет наблюдения.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ
В результате проведения клинических исследований ZOE-50 (ZOSTER-006) и ZOE-70 (ZOSTER-022) была установлена высокая профилактическая эффективность Shingrix против ОГ (табл. 1)4.
Таблица 1. Профилактическая эффективность вакцины Shingrix против опоясывающего лишая у людей старше 50 лет , %
Table 1. Preventive efficacy of Shingrix vaccine against herpes zoster in people over 50 years of age , %
|
Возраст, лет / Age, years |
Показатель профилактической эффективности опоясывающего герпеса / Indicator of the preventive effectiveness of herpes zoster |
|
≥ 50 |
97,2 |
|
≥ 60 |
97,6 |
|
≥ 70 |
91,3 |
|
≥ 80 |
91,4 |
Источник : здесь и далее таблицы составлены авторами на основе данных клинических исследований.
Source : here and further, the tables are compiled by the authors based on clinical research data.
4 «Шингрикс»: мощная вакцина против опоясывающего лишая [Электронный ресурс]. Мосмедпрепараты. ru : сайт. URL: (дата обращения: 20.11.2025).
Кроме того, адъювантная рекомбинантная вакцина успешно предотвращала развитие ПГН (табл. 2) [5].
Таблица 2. Профилактическая эффективность рекомбинантной вакцины по отношению к постгерпетической невралгии, %
Table 2. Preventive effectiveness of recombinant vaccine against postherpetic neuralgia, %
|
Возраст, лет / Age, years |
Показатель профилактической эффективности постгерпетической невралгии / Indicator of the preventive effectiveness of postherpetic neuralgia |
|
≥ 50 |
100,0 % |
|
≥ 60 |
100,0 % |
|
≥ 70 |
88,8 % |
|
≥ 80 |
71,2 % |
Данная вакцина обеспечивала стойкую защиту вне зависимости от возраста, предотвращая развитие ОГ на протяжении длительного времени после иммунизации. Профилактическая эффективность Shingrix в течение медианных 7 лет в среднем составила 91 %. Как уровень защиты изменялся с годами, показано на рисунке [6].
%
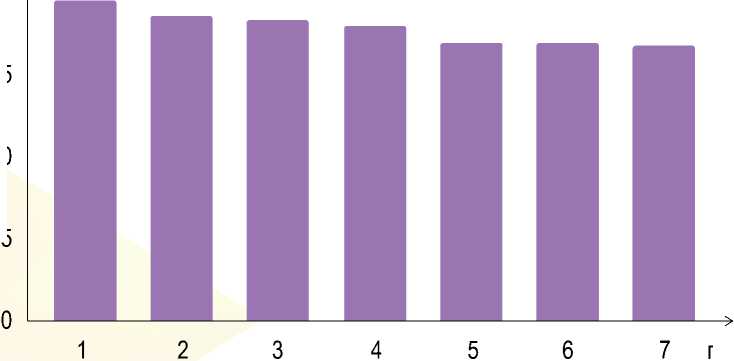
год / year
Р и су н о к . Эффективность вакцины Shingrix на протяжении семи лет, % F i g u re . The effectiveness of the Shingrix vaccine over seven years, %
Клиническая эффективность рекомбинантной вакцины против вируса Варицелла– Зостер сохраняется в течение как минимум 10 лет после вакцинации. В процессе клинического испытания ZOSTER-049 (рандомизированного, открытого многоцентрового, международного) было выявлено, что после вакцинации Shingrix иммунная защита сохранялась на прилично высоком уровне в период от 5 до 11 лет (табл. 3). Из исследования были исключены пациенты, у которых развился иммунодефицит в результате заболевания или иммуносупрессия во время соответствующей терапии [7].
Клиническое исследование ZOE-HSCT продемонстрировало эффективность вакцины в борьбе с опоясывающим лишаем после трансплантации аутологичных гемопоэтических стволовых клеток у пациентов: ≥ 18 лет – 68,2 %, ≥ 50 лет – 67,3 %. Эффективность вакцины после трансплантации стволовых клеток в предотвращении постгерпетической невралгии у пациентов ≥ 18 лет составила 89,3 %, ≥ 50 лет – 88,0 %. Кроме того, снижается частота развития других осложнений опоясывающего герпеса на 77,8 %. В период наблюдения, начинающегося через 6 месяцев после трансплантации гемопоэтических стволовых клеток и продолжающегося до 1 года, когда риск развития ОГ наиболее высок, эффективность вакцины составила 76,2 % [8].
Таблица 3. Профилактическая эффективность рекомбинантной вакцины во временной период от 5 до 11 лет , %
Table 3. Preventive efficacy of the recombinant vaccine over the time period of 5 to 11 years , %
|
Возраст, лет / Age, years |
Показатель профилактической эффективности / Indicator of preventive effectiveness |
|
|
опоясывающий герпес / herpes zoster |
постгерпетической невралгии / postherpetic neuralgia |
|
|
≥ 50 |
79,8 |
87,5 |
|
50–59 |
86,7 |
100,0 |
|
60–69 |
87,1 |
50,0 |
|
≥ 70 |
73,2 |
87,0 |
Рекомбинантная вакцина против опоясывающего лишая обладает высокой иммуногенностью и хорошо переносится пациентами старше 18 лет с гематологическими злокачественными новообразованиями, которые завершили противоопухолевую иммунотерапию или проходят ее. Согласно рандомизированному клиническому исследованию ZOSTER-039, у таких пациентов с множественной миеломой, хроническим лимфоцитарным лейкозом, неходжкинской лимфомой защитная эффективность данной вакцины составила 87,2 % [9].
В ходе клинических исследований ZOE-50 и ZOE-70 было выяснено, что введение Shingrix значительно снижало частоту развития других осложнений ОГ (васкулит, диссеминированный опоясывающий герпес, офтальмологический опоясывающий герпес, неврологические поражения, поражения внутренних органов) на 93,7 % у пациентов в возрасте ≥ 50 лет и 91,6 % в возрасте ≥ 70 лет [10].
Кроме того, в медицинской литературе появилась информация о том, что рекомбинантная инактивированная вакцина снижает риск развития деменции. Согласно анализу время без деменции у тех, кто получил рекомбинантную вакцину, увеличилось на 17 % по сравнению с теми, кто получил живую вакцину от опоясывающего герпеса. Этот эффект наблюдался как у мужчин, так и у женщин [11].
При исследовании безопасности рекомбинантной вакцины было выяснено, что нежелательные явления в основном характеризовались легкой или умеренной степенью тяжести и проходили в течение 3 дней. Согласно исследованиям « GlaxoSmithKline » после рекомбинантной адъювантной вакцины распространены такие местные и общие побочные реакции, как боль (80 % случаев), покраснение (38) и отечность (27) в месте инъекции, мышечная боль (47), головная боль (40), усталость (47), озноб (29), повышение температуры тела (22), желудочно-кишечные симптомы (18 %). Показатели, характеризующие серьезные побочные эффекты, случаи смерти и потенциальные иммуноопосредованные заболевания после введения первой дозы вакцины в течение года после вакцинации, сопоставимы с плацебо [7].
Клиническое исследование ZOSTER-026 (рандомизированное, открытое многоцентровое, международное) выявило, что вторую дозу вакцины Shingrix можно вводить как через два месяца после первой дозы, так и через шесть месяцев. Гуморальный иммунный ответ после схемы 0–6 месяцев не уступает ответу при схеме 0–2 месяца. Иммунологический коррелят защиты не определен, вследствие чего защитный уровень иммунного ответа против VZV неизвестен [10].
Живая аттенуированная вакцина Zostavax была одобрена для профилактики ОГ и ПГН у взрослых старше 50 лет с 2006 года. Профилактическая эффективность Zostavax в отношении развития опоясывающего лишая в среднем составляла 51 %, а относительно ПГН – 67 %. У пациентов в возрасте 60–69 лет профилактическая эффективность составляла 64 %, у пациентов старше 70 лет – 38 %. Защитный эффект Zostavax сохранялся на протяжении 7 лет после иммунизации. Так как Zostavax является живой ослабленной вакциной, то она противопоказана лицам, проходящим иммуносупрессивную терапию, а также лицам с первичным и приобретенным иммунодефицитом, беременным и кормящим женщинам и лицам с активной формой туберкулеза [12].
ОБСУЖДЕНИЕ И ЗАКЛЮЧЕНИЕ
Суммарные данные рандомизированных клинических исследований указывают на высокую профилактическую эффективность и благоприятный профиль безопасности адъювантной рекомбинантной вакцины Shingrix у лиц старше 50 лет, что сопровождается значительным снижением риска опоясывающего герпеса по сравнению с плацебо при сопоставимой переносимости.
В популяциях повышенного риска, включая реципиентов аутологичных гемопоэтических стволовых клеток и пациентов с гематологическими злокачественными новообразованиями на фоне противоопухолевой иммуносупрессивной терапии, двухдозовый режим рекомбинантной вакцины демонстрирует клинически значимое снижение заболеваемости опоясывающим герпесом.
Накопленные наблюдения свидетельствуют о сохранении клинической эффективности рекомбинантной вакцины на высоком уровне по крайней мере в течение 10 лет после завершения вакцинации.
Преимущественные местные реакции включают боль, эритему и отек в месте инъекции; к наиболее частым системным реакциям относятся миалгия, утомляемость и головная боль.
Живая аттенуированная вакцина Zostavax не достигла сопоставимых показателей эффективности и безопасности у иммунокомпрометированных пациентов по сравнению с адъювантной рекомбинантной вакциной. Ее ограничения включают более низкую эффективность, ускоренное снижение защитного эффекта во времени и невозможность использования при первичных/вторичных иммунодефицитах, системной иммуносупрессивной терапии.
С учетом бремени заболевания и доказательной базы вакцинация представляет собой ключевую стратегию первичной профилактики опоясывающего герпеса. Приоритетными задачами остаются расширение осведомленности медицинских работников и населения о возможностях вакцинопрофилактики и обеспечение доступности иммунизации для нуждающихся групп.
Практическая значимость полученных данных заключается в их применимости для врачей-аллергологов-иммунологов, дерматологов и неврологов при планировании вакцинации и последующего ведения пациентов из групп риска.


