Эффективность задней перикардиотомии в профилактике фибрилляции предсердий и перикардиального выпота после протезирования аортального клапана: рандомизированное клиническое исследование
Автор: Каледа Василий Иоаннович, Болдырев С.Ю., Белаш сА., Якуба И.И., Бабешко С.С., Белан И.А., Барбухатти К.О.
Журнал: Патология кровообращения и кардиохирургия @journal-meshalkin
Рубрика: Приобретенные пороки сердца
Статья в выпуске: 2 т.21, 2017 года.
Бесплатный доступ
Методы Исследование одобрено локальным этическим комитетом. Включены больные от 18 до 69 лет, которые подписали информированное согласие на участие и которым планировалось выполнить изолированное первичное протезирование аортального клапана. Критериями исключения были наличие в анамнезе эпизодов фибрилляции предсердий, тиреотоксикоза, прием амиодарона, тяжелая хроническая обструктивная болезнь легких, фракция выброса левого желудочка менее 30%, размер левого предсердия более 50 мм, активный инфекционный эндокардит, наличие спаек в перикарде/левой плевральной полости, а также выполнение операции через минидоступ. В период с октября 2013 г. по апрель 2015 г. 607 больных подверглись вмешательствам на аортальном клапане. В соответствии с критериями включения и исключения в исследование включены лишь 100 больных, которые были случайным образом распределены на две группы: 49 - выполнение задней перикардиотомии, 51 - контрольная группа. В обеих группах оценивалась частота послеоперационной фибрилляции предсердий, перикардиальный выпот более 5 мм, время от операции до выписки, а также отслеживались осложнения, связанные с выполнением задней перикардиотомии. Регистрационный номер исследования: ISRCTN11129539. Результаты Смертельных исходов, острого нарушения мозгового кровообращения, тампонады сердца в течение гос питального периода не было. Осложнений, связанных с выполнением задней перикардиотомии, также не было. Фибрилляция предсердий развилась у 8 (16%) больных в группе задней перикардиотомии против 7 (14%) больных в контрольной группе, p = 0,71. Перикардиальный выпот более 5 мм наблюдался у 5 (10%) больных в группе задней перикардитомии против 6 (12%) в группе контроля, p = 0,80. Средний срок лечения от операции до выписки из стационара составил 12,4±4,3 сут. в группе задней перикардиотомии против 11,9±4,1 в группе контроля, p = 0,27. Выводы Результаты исследования не подтверждают эффективность задней перикардиотомии с целью профилакти ки послеоперационной фибрилляции предсердий и перикардиального выпота в ближайшем послеоперационном периоде после протезирования аортального клапана у больных низкого риска. Однако для окончательных выводов требуются дальнейшие исследования.
Задняя перикардиотомия, перикардиальный выпот, послеоперационная фибрилляция предсердий, кардиохирургия, осложнения
Короткий адрес: https://sciup.org/142140797
IDR: 142140797 | DOI: 10.21688-1681-3472-2017-2-60-67
Efficacy of posterior pericardiotomy in prevention of atrial fibrillation and pericardial effusion after aortic valve replacement: a randomized controlled trial
Aim. Postoperative atrial fibrillation is one of the most frequent complications in cardiac surgery. The aim of this trial was to evaluate the effectiveness of posterior pericardiotomy in the prevention of postoperative atrial fibrillation and pericardial effusion in patients undergoing isolated primary aortic valve replacement. Methods. The trial was approved by the local ethics committee. It included adult patients under 70 y.o. who had signed the informed consent for participation in the study and who were planned to undergo isolated primary aortic valve replacement. Exclusion criteria were a history of atrial fibrillation, hyperthyroidism, amiodarone intake, severe chronic obstructive pulmonary disease, left ventricle ejection fraction less than 30%, the size of the left atrium exceeding 50 mm, active infective endocarditis, the presence of adhesions in the pericardium and/or left pleural cavity and mini-sternotomy. From October 2013 to April 2015 607 patients in our clinic underwent different aortic valve procedures. 507 patients were excluded from the study because of the inclusion and exclusion criteria. The remaining 100 patients were randomized into two groups: 49 patients underwent posterior pericardiotomy and 51 patients made up the control group. In both groups the frequency of postoperative atrial fibrillation, pericardial effusion greater than 5 mm, surgery-discharge time, as well as posterior-pericardiotomy-related complications were studied. This trial is registered with ISRCTN, number 11129539. Results. There were no deaths, stroke or cardiac tamponade during the postoperative stay. Neither were there any complications associated with the performance of posterior pericardiotomy. The incidence of atrial fibrillation, pericardial effusion and average duration of the postoperative stay were similar in both groups: 16% in posterior pericardiotomy group vs. 14% in the control group (p = 0.71), 10% in posterior pericardiotomy group vs. 12% in the control group (p = 0.80) and 12.4±4.3 days in posterior pericardiotomy group vs. 11.9±4.1 days in the control group (p = 0.27), respectively. Conclusion. The trial did not confirm the effectiveness of posterior pericardiotomy in preventing postoperative atrial fibrillation and pericardial effusion during the in-hospital period after isolated primary aortic valve replacement in low risk patients. However, further investigations are needed.
Текст научной статьи Эффективность задней перикардиотомии в профилактике фибрилляции предсердий и перикардиального выпота после протезирования аортального клапана: рандомизированное клиническое исследование
Как цитировать: Каледа В.И., Болдырев С.Ю., Белаш С.А., Якуба И.И., Бабешко С.С., Барбухатти К.О. Эффективность задней перикардиотомии в профилактике фибрилляции предсердий и перикардиального выпота после протезирования аортального клапана: рандомизированное клиническое исследование. Патология кровообращения и кардиохирургия. 2017;21(2):60-67.
Статья доступна по лицензии Creative Commons Attribution 4.0.
Послеоперационная фибрилляция предсердий (ПОФП) — одно из распространенных осложнений кардиохирургических операций [1, 2]. По данным крупных исследований, частота ПОФП при протезировании аортального клапана составляет 35–38% [3–5]. Послеоперационная фибрилляция предсердий может вызывать нестабильность гемодинамики, увеличение продолжительности и стоимости стационарного лечения, а также риск повторной госпитализации, ишемического инсульта и смерти как в раннем, так и позднем периодах после протезирования аортального клапана [2, 4]. Патогенез ПОФП до конца не изучен и связан с механизмами, которые подразделяют на предрасполагающие, интра- и послеоперационные факторы, а также триггеры [6]. К ним относится и перикардиальный выпот (ПВ) [7, 8]. Для устранения ПВ и профилактики ПОФП A. Mulay и коллеги в 1995 г. предложили использовать заднюю перикардиотомию (ЗП) [9]. Позже эффективность ЗП в профилактике послеоперационной фибрилляции предсердий была убедительно показана во многих исследованиях, в том числе и метаанализах [10–13], в результате чего ЗП появилась в рекомендациях по профилактике ПОФП в кардиохирургии Американской коллегии грудных врачей (англ. American College of Chest Physicians, ACCP, 2005) [14] и Европейской ассоциации кардиоторакальной хирургии (англ. European Association for Cardio-Thoracic Surgery, EACTS, 2006) [15]. В то же время современные представления об эффективности ЗП в профилактике ПОФП основаны только на исследованиях при коронарном шунтировании.
Цель исследования: оценка эффективности задней перикардиотомии в профилактике ПВ и ПОФП у больных, перенесших протезирование аортального клапана.
Методы
Данная публикация подготовлена в соответствии со стандартами предоставления результатов рандомизированных клинических исследований CONSORT 2010 [16].
Исследование одобрено этическим комитетом. Все участники исследования предварительно были проинформированы и дали согласие в письменной форме. Исследование зарегистрировано в международном регистре рандомизированных клинических испытаний ISRCTN и получило индивидуальный номер (ISRCTN11129539).
Дизайн — рандомизированное исследование с двумя параллельными группами. Для рандомизации использовалась таблица случайных чисел и последовательно пронумерованные запечатанные конверты. За процесс отбора и рандомизации участников был ответственен первый автор. «Ослепление» участников и исследователей не проводилось.
В исследование включены больные в возрасте от 18 до 69 лет, которым выполнялось первичное изолированное протезирование аортального клапана и которые подписали информированное согласие на участие. К критериям исключения отнесены: наличие в анамнезе эпизодов фибрилляции предсердий и нарушения функции щитовидной железы, прием амиодарона, перикардиальный выпот с максимальной сепарацией листков перикарда 5 мм и более, тяжелая хроническая обструктивная болезнь легких, фракция выброса левого желудочка менее 30%, размер левого предсердия более 50 мм, активный инфекционный эндокардит, спайки в полости перикарда и/или левой плевральной полости, а также выполнение операции через министернотомию.
В предоперационном периоде проводилось стандартное предоперационное обследование, после чего в соответствии с критериями включения и исключения отбирались больные для данного исследования.
Хирургическое вмешательство
Все операции выполнялись стандартно. Осуществлялась полная срединная стернотомия, канюлировались аорта и правое предсердие. Искусственное кровообращение проводилось в условиях спонтанного охлаждения. Во всех случаях использовалась ретроградная кардиоплегия раствором Custodiol® HTK Solution (Dr. F. Koehler Сhemie GmbH, Бенсхайм, Германия). В качестве протезов использовались механические Carbomedics Orbis Aortic (Sorin Biomedica Cardio S.p.I., Салуджа, Италия) и биологические Bovine Pericardium Organic Valvular Bioprosthesis (Braile Biomedica, Сан-Жозе-ду-Риу-Прету, Бразилия). После закрытия разреза аорты до окончания искусственного кровообращения вскрывался конверт и проводилась рандомизация. При попадании в группу задней перикардиотомии выполнялась процедура в соответствии с описанием A. Mulay и соавторов [9]. Дренажи в этой группе ставились в левую плевральную полость через перикард, а также ретрос-тернально. В контрольной группе ЗП не проводилась, дренажи ставились в косой синус перикарда и рет-ростернально. Критерием удаления дренажей являл- ся объем суточного отделяемого (100 мл и меньше). Всем больным подшивались электроды для временной электрокардиостимуляции (один электрод к миокарду правого желудочка, второй — к перикарду). Удаляли электроды на 5–7-е сут. после операции. Перикард частично ушивался во всех случаях. Вне зависимости от типа протеза все больные в ближайшем послеоперационном периоде получали варфарин с целевым значением МНО 2,5. При отсутствии клинически значимого кровотечения по дренажам подбор дозы варфарина начинался через сутки после операции с одновременным назначением низкомолекулярных гепаринов до достижения целевого значения МНО. Все больные получали также кетопрофен в дозе 100 мг внутримышечно как минимум в течение 5 сут. после операции.
Клинические исходы
В качестве первичной конечной точки выбран эпизод ПОФП; вторичные точки — смерть, ишемический инсульт, тампонада сердца. Кроме того, регистрировали ПВ, рестернотомии по поводу кровотечения, пункции левой плевральной полости, длительность инотропной поддержки, сроки пребывания в отделении реанимации и палате интенсивной терапии, а также период от операции до выписки из стационара.
В послеоперационном периоде проводился постоянный мониторинг электрокардиографии (ЭКГ) не ме-
Задняя перикардиотомия / Posterior pericardiotomy
Контрольная группа / Control group
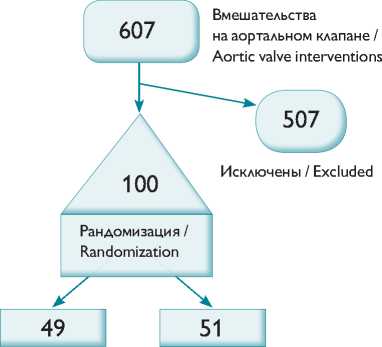
Схема отбора больных на исследование Patients’ selection design нее 48 ч во время нахождения больного в отделении реанимации и палате интенсивной терапии. В дальнейшем ЭКГ проводилась ежедневно, а также при возникновении симптомов аритмии. Эхокардиография в послеоперационном периоде выполнялась как минимум дважды: сразу после удаления дренажей и перед выпиской.
Послеоперационная фибрилляция предсердий считалась клинически значимой и регистрировалась в том случае, если она появлялась на фоне нормокалиемии ( ≥ 4,0 ммоль/л), приводила к нарушению гемодинамики и требовала инфузии амиодарона. Непродолжительные эпизоды ПОФП, проходящие спонтанно или на фоне инфузии раствора калия, считались клинически незначимыми и не регистрировались. При возникновении ПОФП тактика лечения заключалась в контроле ритма с помощью инфузии амиодарона (без применения электрической кардиоверсии). Перикардиальный выпот регистрировался по результатам эхокардиографии в том случае, если максимальная сепарация листков перикарда на уровне митрального клапана составляла 0,5 см и более.
Статистический анализ
Основные статистические характеристики представлены в виде средних значений со стандартными отклонениями или процентной доли от количества больных в каждой группе. Для сравнения использовались критерий согласия Пирсона для дискретных величин и критерии Краскелла – Уоллиса и Ван дер Вардена для непрерывных величин. Статистический анализ проводился с помощью программы SAS/STAT® версии 9.1 (SAS Institute Inc., Кэри, Северная Каролина, США). Значимым считалось p<0,05.
Оценка мощности групп проведена на основании данных литературы о частоте ПОФП при протезировании аортального клапана, которая составляет около 35% [3–5], а также предположении о том, что выполнение ЗП снизит частоту ПОФП при протезировании аортального клапана так же, как и коронарном шунтировании, то есть до 11% [8, 10]. При этом приняты уровень значимости 5% и мощность 80%. Расчетное количество наблюдений для включения в каждую группу составило 45.
Результаты
С октября 2013 г. по апрель 2015 г. в Краевой клинической больнице № 1 имени профессора С.В. Оча-
Таблица 1 Исходная характеристика пациентов
|
Показатель |
Покрытие |
Задняя перикар-диотомия, n = 49 |
Контроль, n = 51 |
р |
|
Возраст, лет |
56,6±9,9 |
55,4±10,5 |
0,5642 0,4563 |
|
|
Мужской пол, n (%) |
28 (57) |
33 (65) |
0,4381 |
|
|
двустворчатый аортальный клапан |
27 (55) |
29 (57) |
||
|
дегенеративный порок |
18 (37) |
17 (33) |
||
|
Диагноз, n (%) |
хроническая ревматическая болезнь сердца |
1 (2) |
1 (2) |
0,4251 |
|
неактивный инфекционный эндокардит |
1 (2) |
4 (8) |
||
|
сифилитический порок |
2 (4) |
0 (0) |
||
|
стеноз |
38 (76) |
36 (72) |
||
|
Порок, n (%) |
недостаточность |
8 (16) |
13 (26) |
0,4951 |
|
комбинированный |
3 (6) |
2 (2) |
||
|
Сахарный диабет, n (%) |
2 (4) |
3 (6) |
0,6801 |
|
|
Индекс массы тела, кг/м2 |
27±4 |
26±4 |
0,2512 0,3083 |
|
|
Курение, n (%) |
11 (22) |
14 (28) |
0,5631 |
|
|
Гипертензия, n (%) |
31 (62) |
39 (78) |
0,1501 |
|
|
Фракция выброса левого желудочка |
53±4,6 |
53±4,7 |
0,8342 0,7863 |
|
|
Размер левого предсердия, мм |
40±4 |
40±5 |
0,9392 0,8603 |
|
|
Терапия, n (%) |
β-блокаторы |
23 (46) |
22 (44) |
0,7021 |
|
статины |
9 (18) |
10 (20) |
0,8741 |
|
|
Холестерол, ммоль/л |
5,3±1,2 |
5,25±1,1 |
0,8682 0,7673 |
|
|
Креатинин, мкмоль/л |
90±13 |
95±17 |
0,1392 0,1163 |
|
|
Примечание. 1 — критерий χ2 классический; 2 — критерий Краскелла – |
Уоллиса; 3 — критерий Ван дер Вардена |
|||
повского вмешательства на аортальном клапане выполнены 607 больным. В соответствии с критериями включения и исключения 507 пациентов не попали в исследование. 100 больных были подвергнуты рандомизации, в результате чего 49 человек попали в группу задней перикардиотомии и 51 — в контрольную группу ( рисунок ).
Демографическая и другие предоперационные характеристики представлены в табл. 1.
Больные в обеих группах статистически значимо не различались по полу, возрасту, нозологиям и другим ха- рактеристикам дооперационного периода. Характеристика операций представлена в табл. 2.
В течение госпитального периода летальных исходов, инсультов и тампонады сердца не было ни в одной группе. Разница в частоте ПОФП и перикардиального выпота не была статистически значима. Среди послеоперационных характеристик только сроки стояния дренажей статистически значимо различались в двух группах (4,4±1,4 сут. в группе ЗП против 3,3±0,6 в группе контроля, p<0,0001). Подробная характеристика послеоперационного периода представлена в табл. 3.
Таблица 2 Характеристика операций
|
Показатель |
Задняя перикар-диотомия, n = 49 |
Контроль, n = 51 |
р |
|
Время искусственного кровообращения, мин |
64±16 |
64±20 |
0,6642 0,8733 |
|
Время ишемии миокарда, мин |
45±13 |
46±12 |
0,8442 0,7513 |
|
Механический протез, n (%) |
35 (70) |
40 (80) |
0,4191 |
|
Примечание. 1 — критерий χ2 классический; 2 — |
критерий Краскелла – Уоллиса; 3 — критерий Ван дер Вардена |
||
Таблица 3 Послеоперационная характеристика пациентов
|
Показатель |
Задняя перикар-диотомия, n = 49 |
Контроль, n = 51 |
р |
|
|
Рестернотомия, n (%) |
1 (2) |
4 (8) |
0,1831 |
|
|
Инотропная поддержка, ч |
7,1±14 |
7,7±9 |
0,4582 |
0,4223 |
|
Нахождение в отделении реанимации и палате интенсивной терапии, сут. |
2,6±1,6 |
2,3±1,0 |
0,3122 |
0,2243 |
|
Имплантация электрокардиостимулятора, n (%) |
0 (0) |
1 (2) |
0,3241 |
|
|
Выписка, п/о день |
12,4±4,3 |
11,9±4,1 |
0,2762 |
0,2633 |
|
Удаление дренажей, п/о день |
4,4±1,4 |
3,3±0,6 |
<0,00012 |
<0,00013 |
|
Фибрилляция предсердий, n (%) |
8 (16) |
7 (14) |
0,7161 |
|
|
Возникновение фибрилляции предсердий, п/о день |
3,6±2,5 |
3,0±2,6 |
0,5512 |
0,5683 |
|
Выписка с фибрилляцией предсердий, n (%) |
1 (2) |
1 (2) |
0,9771 |
|
|
Перикардиальный выпот ≥5 мм, n (%) |
5 (10) |
6 (12) |
0,8031 |
|
|
Плевральная пункция слева, n (%) |
0 (0) |
1 (2) |
0,3241 |
|
Примечание. п/о — после операции; 1 — критерий χ2 классический; 2 — критерий Краскелла – Уоллиса; 3 — критерий Ван дер Вардена
Обсуждение
Эффективность ЗП в профилактике ПОФП ранее показана в целом ряде когортных и рандомизированных исследований после коронарного шунтирования [9, 17–22]. В то же время в отдельных исследованиях эффективность ЗП показать не удалось [23–25], однако результаты метаанализов [10, 12, 13] и кохрейновского обзора [11] подтверждают снижение риска ПОФП при задней перикардиото-мии у больных после коронарного шунтирования.
В рандомизированном клиническом исследовании N. Erdil и коллеги доказали эффективность ЗП в отношении перикардиального выпота у больных с изолированными клапанными вмешательствами. Эффективность в отношении ПОФП в данном исследовании не оценивалась [26]. Также проведены исследования со смешанным составом больных, которым выполнялись как коронарные шунтирования, так и вмешательства на клапанах сердца, однако авторов не интересовало влияние ЗП на послеоперационную фибрилляцию предсердий, а только на ПВ [27, 28]. Некоторые исследователи применяли модифицированную технику ЗП с удалением фрагмента перикарда («перикардиальное окно»). Так, J. Zhao и соавторы в рандомизированном исследовании на смешанной группе больных показали эффективность данной техники в профилактике ПОФП и тампонады сердца [29]. K. Uzun и соавторы в нерандомизированном исследовании на больных, которым проводились клапанные вмешательства, показали эффективность «перикардиального окна» в профилактике послеоперационной тампонады сердца [30].
Таким образом, наше исследование является, по всей видимости, первым, предмет изучения которого — профилактика ПОФП с помощью ЗП у больных, перенесших изолированные клапанные вмешательства.
Однако в нашем исследовании значимых отличий в частоте ПОФП в двух группах не было. Очевидно, к таким результатам привел обширный список критериев исключения, в результате чего в исследование были включены лишь те больные, у которых риск послеоперационной фибрилляции предсердий изначально был крайне низким и, вероятно, ЗП не имела влияния.
Следует отметить, что в большей части случаев первый пароксизм ПОФП возникал до удаления дренажей, что противоречит гипотезе о причинно-следственной связи между ПОФП и ПВ у рассматриваемой категории больных. Относительно перикардиального выпота выявлено следующее: достоверной разницы между двумя группами не отмечено (табл. 3). Однако если в контрольной группе ПВ локализовался преимущественно за задней поверхностью сердца, то в группе задней перикардиотомии у отдельных больных ПВ сохранялся над правыми отделами сердца, что указывает на возможность образования ограниченных скоплений жидкости над правыми отделами, которые не могут дренироваться в левую плевральную полость через отверстие ЗП. Вероятно, классическая техника выполнения ЗП не всегда может предотвратить сдав- ление правых отделов сердца и тампонаду. Тем не менее тампонада сердца — настолько редкое осложнение, что в рамках нашего исследования невозможно сделать выводы об эффективности профилактики тампонады с помощью задней перикардиотомии.
Ограничения исследования
В исследовании не проанализированы некоторые важные факторы, которые могли потенциально влиять на возникновение ПОФП, включая прием ингибиторов ангиотензинпревращающего фермента, уровень тиреотропного гормона и послеоперационный лейкоцитоз. Отдельные критерии исключения основывались лишь на данных анамнеза, в том числе и эпизоды фибрилляции предсердий до операции. Послеоперационный непрерывный ЭКГ-мониторинг был непродолжительным, как и сроки послеоперационного наблюдения. Кроме того, в качестве ключевых временных точек выбраны сроки, зависящие от субъективного решения лечащих врачей (сроки перевода из отделения реанимации, выписки и др.). В целом из-за большого количества критериев исключения группы не соответствовали больным в реальной жизни (исключены 84%), поэтому переносить полученные данные в широкую практику некорректно.
Заключение
Результаты исследования не подтверждают эффективность задней перикардиотомии с целью профилактики ПОФП и перикардиального выпота в ближайшем послеоперационном периоде после протезирования аортального клапана у больных низкого риска. Однако для окончательных выводов требуются дальнейшие исследования.
Финансирование
Исследование проводилось в рамках диссертационного исследования в соответствии с планом научных работ Кубанского государственного медицинского университета и не имело финансирования помимо средств, выделяемых в рамках аспирантской стипендии.
Список литературы Эффективность задней перикардиотомии в профилактике фибрилляции предсердий и перикардиального выпота после протезирования аортального клапана: рандомизированное клиническое исследование
- Lomivorotov V.V., Efremov S.M., Pokushalov E.A., Karaskov A.M. New-onset atrial fibrillation after cardiac surgery: pathophysiology, prophylaxis, and treatment. J Cardiothorac Vasc Anesth. 2016;30(1):200-16. http://dx.doi.o DOI: rg/10.1053/j.jvca.2015.08.003
- Gillinov A.M., Bagiella E., Moskowitz A.J., Raiten J.M., Groh M.A., Bowdish M.E., Ailawadi G., Kirkwood K.A., Perrault L.P., Parides M.K., Smith li R.L., Kern J.A., Dussault G., Hackmann A.E., Jeffries N.O., Miller M.A., Taddei-Peters W.C., Rose E.A., Weisel R.D., Williams D.L., Mangusan R.F., Argenziano M., Moquete E.G., O'Sullivan K.L., Pellerin M., Shah K.J., Gammie J.S., Mayer M.L., Voisine P., Gelijns A.C., O'Gara P.T., Mack M.J.; CTSN. Rate control versus rhythm control for atrial fibrillation after cardiac surgery. N Engl J Med. 2016;374(20):1911-21. http://dx.doi. org/10.1056/NEJMoa1602002
- Dandale R., Rossi A., Onorati F., Krapivsky A., Kekes P., Milano A., Santini F., Faggian G. Does aortic valve disease etiology predict postoperative atrial fibrillation in patients undergoing aortic valve surgery? Future Cardiol. 2014;10(6):707-15. http://dx.doi. org/10.2217/fca.14.57
- Filardo G., Hamilton C., Hamman B., Hebeler R.F. Jr, Adams J., Grayburn P. New-onset postoperative atrial fibrillation and long-term survival after aortic valve replacement surgery. Ann Thorac Surg. 2010;90(2):474-9. http://dx.doi.o DOI: rg/10.1016/j.athoracsur.2010.02.081
- Saxena A., Shi W.Y., Bappayya S., Dinh D.T., Smith J.A., Reid C.M., Shardey G.C., Newcomb A.E. Postoperative atrial fibrillation after isolated aortic valve replacement: a cause for concern? Ann Thorac Surg. 2013;95(1):133-40. http://dx.doi.org/10.1016/j. athoracsur.2012.08.077
- Echahidi N., Pibarot P., O'Hara G., Mathieu P. Mechanisms, prevention, and treatment of atrial fibrillation after cardiac surgery. J Am Coll Cardiol. 2008;51(8):793-801. http://dx.doi.org/10.1016/j. jacc.2007.10.043
- Angelini G.D., Penny W.J., el-Ghamary F., West R.R., Butchart E.G., Armistead S.H., Breckenridge I.M., Henderson A.H. The incidence and significance of early pericardial effusion after open heart surgery. Eur J Cardiothorac Surg. 1987;1(3):165-8.
- Каледа В.И., Антипов Г.Н., Барбухатти К.О. Задняя перикардиотомия как метод профилактики фибрилляции предсердий и перикардиального выпота после операций на сердце (обзор литературы)//Кардиология и сердечно-сосудистая хирургия. 2012;5(6):48-53.
- Mulay A., Kirk A.J., Angelini G.D., Wisheart J.D., Hutter J.A. Posterior pericardiotomy reduces the incidence of supra ventricular arrhythmias following coronary artery bypass surgery. Eur J Cardiothorac Surg. 1995;9:150-2.
- Biancari F., Mahar M.A. Meta-analysis of randomised trials on the efficacy of posterior pericardiotomy in preventing atrial fibrillation after coronary artery bypass surgery. J Thorac Cardiovasc Surg. 2010;139:1158-61. http://dx.doi.o DOI: rg/10.1016/j.jtcvs.2009.07.012
- Arsenault K.A., Yusuf A.M., Crystal E., Healey J.S., Morillo C.A., Nair G.M., Whitlock R.P. Interventions for preventing postoperative atrial fibrillation in patients undergoing heart surgery. Cochrane Database Syst Rev. 2013;(1):CD003611. http://dx.doi. org/10.1002/14651858.CD003611.pub3
- Hu X.L., Chen Y., Zhou Z.D., Ying J., Hu Y.H., Xu G.H. Posterior pericardiotomy for the prevention of atrial fibrillation after coronary artery bypass grafting: A meta-analysis of randomized controlled trials. Int J Cardiol. 2016;215:252-6. http://dx.doi. org/10.1016/j.ijcard.2016.04.081
- Ali-Hassan-Sayegh S., Mirhosseini S.J., Liakopoulos O., Sabashnikov A., Dehghan H.R., Sedaghat-Hamedani F., Kayvanpour E., Ghaffari N., Vahabzadeh V., Aghabagheri M., Mozayan M.R., Popov A.F. Posterior pericardiotomy in cardiac surgery: systematic review and meta-analysis. Asian Cardiovasc Thorac Ann. 2015;23(3):354-62. http://dx.doi. org/10.1177/0218492314541132
- Creswell L.L., Alexander J.C. Jr, Ferguson T.B. Jr, Lisbon A., Fleisher L.A.; American College of Chest Physicians. Intraoperative interventions: American College of Chest Physicians guidelines for the prevention and management of postoperative atrial fibrillation after cardiac surgery. Chest. 2005;128(2 Suppl):28S-35S. http://dx.doi.o DOI: rg/10.1378/chest.128.2_suppl.28S
- Dunning J., Treasure T., Versteegh M., Nashef S.A.; EACTS Audit and Guidelines Committee. Guidelines on the prevention and management of de novo atrial fibrillation after cardiac and thoracic surgery. Eur J Cardiothorac Surg. 2006;30(6):852-72. http://dx.doi. org/10.1016/j.ejcts.2006.09.003
- Schulz K.F., Altman D.G., Moher D., for the CONSORT Group. CONSORT 2010 Statement: updated guidelines for reporting parallel group randomised trials. Ann Intern Med. 2010;152(11):726-32. http://dx.doi.org/10.7326/0003-4819-152-11-201006010-00232
- Kuralay E., Ozal E., Demirkili U., Tatar H. Effect of posterior pericardiotomy on postoperative supraventricular arrhythmias and late pericardial effusion (posterior pericardiotomy). J Thorac Cardiovasc Surg. 1999;118(3):492-495.
- Farsak B., Günaydin S., Tokmakoglu H., Kandemir O., Yorgancioglu C., Zorlutuna Y. Posterior pericardiotomy reduces the incidence of supra-ventricular arrhythmias and pericardial effusion after coronary artery bypass grafting. Eur J Cardiothorac Surg. 2002;22(2):278-81.
- Ekim H., Kutay V., Hazar A., Akbayrak H., Baçel H., Tuncer M. Effects of posterior pericardiotomy on the incidence of pericardial effusion and atrial fibrillation after coronary revascularization. Med Sci Monit. 2006;12(10):CR431-4.
- Kaygin M.A., Dag O., Güneç M., Senocak M., Limandal H.K., Aslan U., Erkut B. Posterior pericardiotomy reduces the incidence of atrial fibrillation, pericardial effusion, and length of stay in hospital after coronary artery bypasses surgery. Tohoku J Exp Med. 2011;225(2):103-8. http://dx.doi.o DOI: rg/10.1620/tjem.225.103
- Kaya M., Utkusavaç A., Erkanli K., Güler S., Kyaruzi M., Birant A., Karaçalilar M., Akkuç M., Bakir I. The preventive effects of posterior pericardiotomy with intrapericardial tube on the development of pericardial effusion, atrial fibrillation, and acute kidney injury after coronary artery surgery: a prospective, randomized, controlled trial. Thorac Cardiovasc Surg. 2016;64(3):217-24. http://dx.doi. org/10.1055/s-0035-1548737
- Fawzy H., Elatafy E., Elkassas M., Elsarawy E., Morsy A., Fawzy A. Can posterior pericardiotomy reduce the incidence of postoperative atrial fibrillation after coronary artery bypass grafting? Interact Cardiovasc Thorac Surg. 2015;21(4):488-91. http://dx.doi.o DOI: rg/10.1093/icvts/ivv190
- Asimakopoulos G., Della Santa R., Taggart D.P. Effects of posterior pericardiotomy on the incidence of atrial fibrillation and chest drainage after coronary revascularization: a prospective randomized trial. J Thorac Cardiovasc Surg. 1997;113(4):797-9.
- Arbatli H., Demirsoy E., Aytekin S., Rizaoglu E., Unal M., Yagan N., Sonmez B. The role of posterior pericardiotomy on the incidence of atrial fibrillation after coronary revascularization. J Cardiovasc Surg (Torino). 2003;44(6):713-7.
- Haddadzadeh M., Motavaselian M., Rahimianfar A.A., Forouzannia S.K., Emami M., Barzegar K. The effect of posterior pericardiotomy on pericardial effusion and atrial fibrillation after off-pump coronary artery bypass graft. Acta Med Iran. 2015;53(1):57-61.
- Erdil N., Nisanoglu V., Kosar F., Erdil F.A., Cihan H.B., Battaloglu B. Effect of posterior pericardiotomy on early and late pericardial effusion after valve replacement. J Card Surg. 2005;20(3):257-60.
- Bakhshandeh A.R., Salehi M., Radmehr H., Sattarzadeh R., Nasr A.R., Sadeghpour A.H. Postoperative pericardial effusion and posterior pericardiotomy: related? Asian Cardiovasc Thorac Ann. 2009;17(5):477-9. http://dx.doi.o DOI: rg/10.1177/0218492309341787
- Cakalagaoglu C., Koksal C., Baysal A., Alici G., Ozkan B., Boyacioglu K., Tasar M., Atasoy E.B., Erdem H., Esen A.M., Alp M. The use of posterior pericardiotomy technique to prevent postoperative pericardial effusion in cardiac surgery. Heart Surg Forum. 2012;15(2):E84-9. http://dx.doi.org/10.1532/HSF98.20111128
- Zhao J., Cheng Z., Quan X., Zhao Z. Does posterior pericardial window technique prevent pericardial tamponade after cardiac surgery? J Int Med Res. 2014;42(2):416-26. http://dx.doi. org/10.1177/0300060513515436
- Uzun K., Günaydin Z.Y., Tataroglu C., Bektaç O. The preventive role of the posterior pericardial window in the development of late cardiac tamponade following heart valve surgery. Interact Cardiovasc Thorac Surg. 2016;22(5):641-6. http://dx.doi.org/10.1093/icvts/ivv390


