Эффекты применения биосовместимого покрытия экстракорпорального контура «Bioline» у кардиохирургических пациентов
Автор: Пономаренко Игорь Валерьевич, Шипулин Владимир Митрофанович, Огуркова Оксана Николаевна, Суслова Татьяна Евгеньевна
Журнал: Патология кровообращения и кардиохирургия @journal-meshalkin
Рубрика: Анестезиология, реаниматология и перфузиология
Статья в выпуске: 2 т.17, 2013 года.
Бесплатный доступ
Целью исследования была оценка эффективности применения белково-гепаринового покрытия «Bioline» в кардиохирургии. Пациенты (n = 36), подвергнутые АКШ, были разделены на две количественно равные группы. В 1 -й группе искусственное кровообращение (ИК) проводили с использованием мембранного оксигенатора Quadrox, покрытого «Bioline». Во 2-й (контрольной) применяли тот же оксигенатор без покрытия. В артериальной крови оценивали уровень фибриногена, тромбоцитов, лейкоцитов, фактора некроза опухоли-α и интерлейкина-6 перед, во время и после ИК. Определяли дыхательные индексы, объем кровопотери, потребность в гемотрансфузиях и длительность ИВЛ. Были получены достоверные различия между группами в пользу «Bioline» по количеству тромбоцитов к окончанию ИК (179 (34) vs 151 (44) х 10 9/л; p = 0,01) и после введения протамина (146 (41) vs 128 (31) х 10 9/л; p = 0,04), по уровню лейкоцитов (11,1 (3,4) vs 13,8 (4,3) х 10 9/л; p = 0,02), интерлейкина-6 (24 (18) vs 34 (17) пг/мл; р = 0,02) и фибриногена (3,3 (0,7) vs 3,0 (1,0) г/л; p = 0,02) после окончания ИК, по индексам оксигенации (2,0 (0,4) vs 2,5 (0,9); р = 0,01) и вентиляции (4,9 (1,1) vs 6,6 (1,9); р = 0,03), объему кровопотери (90 (80) vs 115 (150) мл; р = 0,047) и длительности ИВЛ (9,5 (4,0) vs 13,8 (7,5) ч; р = 0,02). Включение в перфузионный контур мембранного оксигенатора, покрытого составом «Bioline», позволяет ослабить воспалительный ответ на ИК, снижает степень гипофибриногенемии, тромбоцитопении, что клинически проявляется в уменьшении объема послеоперационной кровопотери, динамике респираторных индексов и снижении длительности дыхательной поддержки.
Искусственное кровообращение, биосовместимые покрытия, воспалительный ответ, дыхательные индексы
Короткий адрес: https://sciup.org/142140540
IDR: 142140540 | УДК: 616.15;
Effects of biocompatible extracorporeal bypass circuit coating Bioline in cardiac surgery patients
Biocompatibility of heparin-based coating for extracorporeal circuits, the Bioline, was evaluated in cardiac surgery setting. Thirty six CABG pts, aged from 30 to 69 yrs, were randomly perfused with a circuit containing Bioline-coated Quadrox oxygenator (Bioline, n=18) or with a similar non-coated circuit (control, n=18). Leukocyte and platelet counts, levels of tumor necrosis factor, interleukin-6 and fibrinogen were assessed in arterial blood before, during and after cardiopulmonary bypass (CPB). Oxygenation and ventilation indices before and after surgery, post-operative chest tube drainage and transfusion volume as well as the duration of assisted ventilation were also measured. A platelet count and fibrinogen dropped less in the Bioline group significantly compared with that in control at the end of CPB (p
Текст научной статьи Эффекты применения биосовместимого покрытия экстракорпорального контура «Bioline» у кардиохирургических пациентов
ВАК 14.01.20
Поступила в редакцию 18 сентября 2012 г.
В.М. Шипулин,
О.Н. Огуркова, Т.Е. Суслова, 2013
Целью исследования была оценка эффективности применения белково-гепаринового покрытия «Bioline» в кардиохирургии. Пациенты (n = 36), подвергнутые АКШ, были разделены на две количественно равные группы. В 1-й группе искусственное кровообращение (ИК) проводили с использованием мембранного оксигенатора Quadrox, покрытого «Bioline». Во 2-й (контрольной) применяли тот же оксигенатор без покрытия. В артериальной крови оценивали уровень фибриногена, тромбоцитов, лейкоцитов, фактора некроза опухоли-α и интерлейкина-6 перед, во время и после ИК. Определяли дыхательные индексы, объем кровопотери, потребность в гемотрансфузиях и длительность ИВЛ. Были получены достоверные различия между группами в пользу «Bioline» по количеству тромбоцитов к окончанию ИК (179 (34) vs 151 (44) х 109/л; p = 0,01) и после введения протамина (146 (41) vs 128 (31) х 109/л; p = 0,04), по уровню лейкоцитов (11,1 (3,4) vs 13,8 (4,3) х 109/л; p = 0,02), интерлейкина-6 (24 (18) vs 34 (17) пг/мл; р = 0,02) и фибриногена (3,3 (0,7) vs 3,0 (1,0) г/л; p = 0,02) после окончания ИК, по индексам оксигенации (2,0 (0,4) vs 2,5 (0,9); р = 0,01) и вентиляции (4,9 (1,1) vs 6,6 (1,9); р = 0,03), объему кровопотери (90 (80) vs 115 (150) мл; р = 0,047) и длительности ИВЛ (9,5 (4,0) vs 13,8 (7,5) ч; р = 0,02). Включение в перфузионный контур мембранного оксигенатора, покрытого составом «Bioline», позволяет ослабить воспалительный ответ на ИК, снижает степень гипофибриногенемии, тромбоцитопении, что клинически проявляется в уменьшении объема послеоперационной кровопотери, динамике респираторных индексов и снижении длительности дыхательной поддержки. Ключевые слова: искусственное кровообращение; биосовместимые покрытия; воспалительный ответ; дыхательные индексы.
Хирургическая травма и искусственное кровообращение, в условиях которого в настоящее время выполняется большинство кардиохирургических вмешательств, вызывают патофизиологическую реакцию организма, известную как синдром системного воспалительного ответа (ССВО). Поступление в общую циркуляцию крови из операционного поля, а также контакт крови с чужеродными поверхностями экстракорпорального контура активируют плазменные белки, форменные элементы крови (нейтрофилы, моноциты, тромбоциты) и клетки эндотелия сосудов [6].
Во время операции с искусственным кровообращением активированные клетки продуцируют и высвобождают во внеклеточное окружение широкий спектр вазоактивных и цитотоксических субстанций, циркуляция которых опосредует многие проявления ССВО, характерные для клинической кардиохирургии. Синдром системного воспалительного ответа может стать причиной сердечной, легочной, почечной и неврологической дисфункций в раннем послеоперационном периоде [1, 7]. Так, дыхательная недостаточность вплоть до респираторного дистресс-синдрома, обусловленная синдромом системного воспалительного ответа, отмечается у 5–15% кардиохирургических пациентов [10].
Усилия, направленные на предупреждение синдрома системного воспалительного ответа и уменьшение степени его выраженности, могут положительно повлиять на результаты хирургического лечения сердечной патологии. Один из подходов, применяемых в данном аспекте, заключается в использовании биосовместимых покрытий экстракорпорального контура. Цель настоящего проспективного исследования – оценка эффективности применения белково-гепаринового покрытия «Bioline» у взрослых пациентов, подвергнутых в плановом порядке аортокоронарному шунтированию (АКШ) на фоне полной гепаринизации.
Материал и методы
В исследование включено 36 взрослых пациентов (все мужчины) с ИБС, которым в условиях ИК было выполнено АКШ. Случайным образом пациенты были разделены на две количественно равные группы. В основной группе для проведения ИК применялся мембранный оксигенатор «Quadrox» («Maquet», Германия), обработанный составом «Bioline». В контрольной группе ИК проводили с использованием такого же оксигенатора, но без покрытия. Во всех случаях применено одинаковое анестезиологическое обеспечение вмешательства: вводный наркоз фентанилом (4–5 мкг/кг) в сочетании с калипсолом, поддерживающая анальгезия проводилась также фентанилом (4–6 мкг/(кг · ч)). Миорелаксацию обеспечивали ардуаном (20–30 мкг/кг · ч). Искусственную вентиляцию легких (ИВЛ) проводили вентилятором «ServoS» («Maquet», Швеция).
Пациентов подключали к аппарату ИК после системной антикоагуляции гепарином (3 мг/кг) по схеме «правое предсердие – восходящая аорта». Искусственное кровообращение проводилось на консоли «S3» («Stökert», Германия) с использованием роликовых насосов с объемной скоростью перфузии 2,4 л/(мин · м)2 в режиме нормотер-мии. Защиту миокарда после наложения зажима на аорту осуществляли антеградным введением 1 000 мл охлажденного до 4 °С раствора «Custodiol» («Dr. Franz Köhler Chemie», Германия). После окончания ИК эффект гепарина нейтрализовали введением сульфата протамина.
Материалом для исследований была артериальная кровь пациентов. Забор образцов осуществляли после вводного наркоза (Т1), через 30 мин после начала ИК (Т2), перед его окончанием (Т3) и после введения протамина (Т4) из катетера, установленного в лучевую артерию для прямого измерения кровяного давления. В образцах крови на автоматическом гематологическом анализаторе «Micros 60» («Horiba ABX», Франция) ex tempore подсчитывали количество лейкоцитов и тромбоцитов.
Затем кровь центрифугировали и в полученной плазме определяли концентрацию медиаторов воспаления: фактора некроза опухоли (ФНО-α) и интерлейкина-6 (ИЛ-6) твердофазным иммуноферментным методом с использованием тест-систем «ПроКон» (Россия), а также уровень фибриногена по методу Клаусса с помощью набора реактивов «Helena Biosciences Europe» (Великобритания). С учетом антропометрической однородности групп и единообразия в заполнении экстракорпорального контура и проведении кардиоплегии коррекцию полученных данных на гемодилюцию было решено не проводить.
У всех пациентов перед началом искусственного кровообращения и через 30 мин после его окончания оценивали функцию внешнего дыхания. Критериями служили индексы оксигенации (ИО) и вентиляции (ИВ), которые вычисляли по следующим формулам: ИО = (FO 2 хMAP)/ paO2, где FiO2– содержание кислорода во вдыхаемой смеси, %, МАР – среднее давление в дыхательных путях, см вод.
ст., paO2– парциальное давление кислорода в артериальной крови, мм рт. ст.; ИВ = RRх (PIP - PEEP) х p a CO 2 /1 000, где RR – частота дыхательных движений, мин–1, PIP – пиковое давление на вдохе, мм рт. ст., PEEP – конечное положительное давление на выдохе, мм рт. ст., paCO2 – парциальное давление углекислого газа в артериальной крови, мм рт. ст.
Для вычисления дыхательных индексов использовали результаты анализа газового состава крови, который выполнялся на газоанализаторе «Stat Profile M» («Nova Biomedical», США). Клиническими критериями служили объем кровопотери в послеоперационном периоде (вплоть до удаления дренажей из средостения), потребность в гемотрансфузиях (проводились при снижении уровня гемоглобина <80 г/л), длительность ИВЛ (критерии отключения от ИВЛ: стабильная гемодинамика, приемлемый неврологический статус, РаО2 ≥60 мм рт. ст., SаО2 ≥90% при FiО2 ≤0,40) .
Статистическую обработку результатов проводили с помощью программного пакета «Statistica 6.0». Данные представлены в виде «медиана (межквартильный интервал)». Динамику внутригрупповых количественных показателей оценивали с помощью критерия Вилкок-сона. При анализе межгрупповых количественных показателей использовали критерий Манна – Уитни для двух независимых выборок. Качественные показатели анализировали по критерию Фишера. За статистически значимые принимали различия на уровне p<0,05.
Результаты
Как видно из табл. 1, группы статистически не различались по возрасту, массе и площади поверхности тела, исходному состоянию пациентов, объему и длительности оперативного вмешательства. Исходный уровень количества лейкоцитов в группах существенно не различался (рис. 1, а ). Искусственное кровообращение вызывало заметный рост показателя в обеих группах. Во всех контрольных точках после начала ИК межгрупповые различия достигали значимого уровня (p = 0,03, р = 0,03 и р = 0,02 в Т2, Т3 и Т4 соответственно).
Количество тромбоцитов, также исходно не отличавшееся между группами, с началом ИК достоверно снижалось в обеих группах по сравнению с исходным значением. Тенденция к снижению числа тромбоцитов сохранялась до конца перфузии, однако в группе «Bioline» среднее значение показателя перед ее окончанием было достоверно выше, чем в контрольной (p = 0,01). После введения протамина количество тромбоцитов в обеих группах в очередной раз существенно падало, но достоверные межгрупповые различия сохранялись (p = 0,04) (рис. 1, б ).
Исходный уровень ФНО-α составлял 54,5 (80,0) и 42,5 (37) пг/мл в основной и контрольной группах, при норме для здоровых индивидуумов ≤50 пг/мл. При этом статистически показатели не различались (р = 0,87). Для этого показателя характерными были высокая внутриг-
|
Таблица 1 |
Показатель |
«Bioline», n = 18 |
Контроль, n = 18 |
р |
|
Клиническая |
Возраст, лет |
56,0 (13,0) |
54,5 (8,0) |
0,69 |
|
характеристика |
Масса тела, кг |
78,5 (10,0) |
81 (17,0) |
0,77 |
|
пациентов |
Площадь поверхности тела, м2 |
2,0 (0,1) |
2,0 (0,2) |
0,16 |
|
ФВ ЛЖ, % |
63,0 (8,0) |
57,0 (13,0) |
0,58 |
|
|
EuroSCORE, % |
1,6 (0,9) |
1,7 (1,6) |
0,69 |
|
|
Кол-во дистальных анастомозов |
3,0 (2,0) |
3,0 (1,0) |
0,52 |
|
|
Продолжительность ИК, мин |
113,0 (45,0) |
105,0 (45,0) |
0,58 |
|
|
Время пережатия аорты, мин |
70,0 (30,0) |
68,0 (25,0) |
0,45 |
Рис. 1.
Динамика гематологических показателей: а – лейкоцитов;
б –тромбоцитов.
* достоверные межгрупповые различия
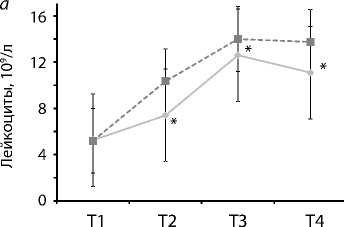
—•— Bioline — Контроль
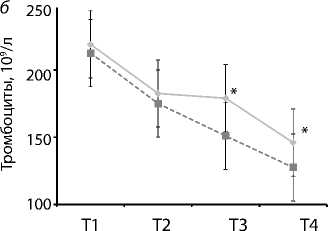
Рис. 2.
Динамика биохимических показателей:
а – фактора некроза опухоли-α;
б – интерлейкина-6;
в – фибриногена.
* достоверные межгрупповые различия
♦ Bioline —Контроль
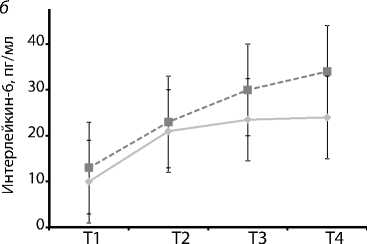
рупповая вариабельность показателя и его существенное повышение во время и после ИК (рис. 2, а). Концентрация ИЛ-6 в обеих группах была изначально высокой: 10 (21) пг/мл в группе «Bioline» и 13 (18) пг/мл в контрольной при норме <5 пг/мл. На фоне искусственного кровообращения показатель повышался в обеих группах более чем вдвое. По окончании искусственного кровообращения межгрупповые различия в содержании данного цитокина достигали статистической значимости (p = 0,03) (рис. 2, б). Уровень фибриногена прогрессивно снижался в обеих группах, особенно с началом искусственного кровообращения и после введения протамина.
Таблица 2
Дыхательные индексы p<0,05 различия достоверны: * между группами; # по сравнению с исходным значением
|
Группа |
Индекс оксигенации |
Индекс вентиляции |
||
|
до ИК |
после ИК |
до ИК |
после ИК |
|
|
«Bioline» |
1,3 (0,6) |
2,0 (0,4)*# |
4,2 (0,8) |
4,9 (1,1)*# |
|
Контроль |
1,5 (0,6) |
2,5 (0,9)# |
4,4 (1,0) |
6,6 (1,9)# |
|
р |
0,55 |
0,01 |
0,58 |
0,03 |
Таблица 3
Клинические показатели * достоверные межгрупповые различия
|
Показатель |
«Bioline» |
Контроль |
p |
|
Кровопотеря, мл |
90 (80)* |
115 (150) |
0,047 |
|
Гемотрансфузии |
|||
|
кол-во пациентов, n (%) |
6 (33) |
5 (28) |
0,50 |
|
объем, мл |
288 (183) |
506 (67) |
0,07 |
|
Длительность ИВЛ, ч |
9,5 (4,0) |
13,8 (7,5) |
0,02 |
Отмеченные нами различия в динамике этого показателя между группами состояли в том, что у пациентов контрольной группы к 30-й минуте искусственного кровообращения он снизился на 19%, а в группе «Bioline» – на 11% при равной степени гемодилюции (p = 0,04) (рис. 2, в ).
Исходно группы не отличались по дыхательным индексам. Индекс оксигенации значимо возрастал после искусственного кровообращения по сравнению с исходным значением в обеих группах. Межгрупповые различия также были статистически значимы. Было отмечено достоверное повышение индекса вентиляции в обеих группах, хотя и в меньшей степени. Межгрупповые различия также были существенны (табл. 2).
Как видно из табл. 3, доли пациентов, которым в послеоперационном периоде потребовалась донорская кровь, в обеих группах были сопоставимы, как и количество перелитой эритроцитарной массы. Однако средний объем послеоперационной кровопотери в контрольной группе был достоверно более высоким. Длительность искусственной вентиляции легких в группе «Bio-line» была существенно короче, чем в контрольной.
Обсуждение
Для профилактики и ослабления системного воспалительного ответа на ИК был разработан целый ряд биосовмести-мых материалов. Однако в отечественной литературе нам не удалось обнаружить результатов клинических исследований, посвященных этому вопросу. Наиболее популярны покрытия на основе гепарина. Их активная поверхность имеет отрицательный заряд, что позволяет предотвратить адгезию тромбоцитов, также отрицательно заряженных.
В данном исследовании в основной группе были использованы мембранные оксигенаторы, обработанные составом «Bioline». Это биосовместимое покрытие представляет собой комбинацию альбумина и гепарина. Молекулы гепарина ковалентно связаны с подлежащим слоем белка, что служит гарантией стабильности покрытия. Результаты про- веденного исследования показали, что применение «Bio-line» позволяет уменьшить выраженность общей воспалительной реакции на искусственное кровообращение.
В первую очередь данную гипотезу подтверждает динамика количества лейкоцитов в группах. Уровень ФНО-α и ИЛ-6 как основных провоспалительных медиаторов, участвующих в этой реакции [6], в группе «Bioline» был также в среднем ниже, чем в группе контроля. Полученные данные согласуются с результатами других исследований, продемонстрировавших противовоспалительный эффект гепариновых покрытий [3, 13].
Исходно повышенное содержание ФНО-α в плазме крови пациентов обеих групп можно объяснить усиленной экспрессией гена ФНО-α и его рецепторов у лиц, страдающих ИБС [5], особенно с учетом возраста и клинического статуса включенных в исследование пациентов. Значительная вариабельность данных в обеих группах на всех этапах, которую в отношении цитокинов отмечали и другие исследователи [11], может отражать влияние генетических факторов, что подтверждается многими источниками [2, 4, 12].
Таким образом, фактор наследственности, возможно, оказывает существенное влияние как на общую картину острого воспалительного ответа, так и на содержание отдельных маркеров воспаления в крови и способен как нивелировать, так и усиливать межгрупповые различия, оставаясь при этом неучтенным.
Положительный эффект использования гепаринового покрытия проявился и в отношении тромбоцитов. Степень тромбоцитопении в группе «Bioline» как во время искусственного кровообращения (особенно к его окончанию), так и после введения протамина была существенно ниже. И хотя, как и следовало ожидать, гепаринизация контактной поверхности не предотвращала заметного «потребления» тромбоцитов после введения протамина, их уровень оставался более высоким, чем в контрольной группе. Подобные же результаты были получены группой G. Pala-tianos [11]. Авторами этого исследования был показан протективный эффект покрытия «Bioline» в отношении тромбоцитов при использовании как полностью, так и частично (как в нашем случае) гепаринизированного контура.
Интерпретация изменений уровня фибриногена представляет определенную сложность, поскольку, с одной стороны, данный показатель, как известно, повышается при остром воспалении, с другой – при контакте крови с экстракорпоральным контуром его поверхности адсорбируют этот белок [14]. Считаем, что с учетом динамики прочих маркеров воспаления более высокий в целом уровень фибриногена в группе «Bioline» во время и после искусственного кровообращения – скорее следствие уменьшения его адсорбции мембраной оксигенатора, нежели признак воспалительной реакции.
Отмеченные изменения респираторных индексов соответствуют существующему мнению о негативном влиянии искусственного кровообращения на легочную функцию. Индекс оксигенации в обеих группах достоверно повышался. Не столь выраженные (в процентном отношении) изменения индекса вентиляции независимо от причины, вызвавшей нарушения (интерстициальный отек вследствие повышения сосудистой проницаемости, увеличение фракции шунта за счет ателектазирования или прямое повреждающее действие свободных радикалов и ферментов активированных нейтрофилов), могут объясняться более высокой проницаемостью альвеолярной мембраны для СО2в силу физико-химических свойств последнего.
Однако на основании полученных результатов можно говорить о благоприятном эффекте применения «Bioline» в отношении дыхательной функции. E. Apostolakis с коллегами также сообщали об уменьшении фракции легочного шунта, индекса резистентности легочных сосудов и меньшем снижении респираторного индекса paO2/FiO2 при использовании гепаринизированного контура [1].
Полученные биохимические и гематологические данные, по нашему мнению, могут объяснить и различия между группами по клиническим критериям. Про-тективный эффект «Bioline» в отношении тромбоцитов и фибриногена проявился в меньшем объеме кровопотери в послеоперационном периоде у пациентов основной группы. Меньшая длительность респираторной поддержки в группе «Bioline», как мы считаем, является результатом ослабления воспалительного ответа на искусственное кровообращение.
О более ранних экстубации и выведении из блока интенсивной терапии пациентов, у которых искусственное кровообращение проводилось с использованием гепаринизированного контура, сообщали также J. Marcoux с коллегами [9]. По данным A. Zimmermann, применение оксигенаторов, покрытых «Bioline», в симуляции искусственного кровообращения с использованием донорской крови показало меньшую адсорбцию фибриногена и адгезию лейкоцитов и тромбоцитов по сравнению с контурами без покрытия [14], что вполне соответствует полученным в данном исследовании результатам.
При прохождении крови через оксигенатор скорость потока естественным образом заметно снижается, так как площадь контактной поверхности (мембраны) оксигенатора «Quadrox» составляет 1,8 м2, что сопоставимо с площадью поверхности тела взрослого пациента. Это способствует адсорбции фибриногена и адгезии клеточных элементов к чужеродной поверхности с последующей их активацией. Предупреждение данных процессов на столь обширной площади может объяснять противовоспалительный и «тромбоцитосберегающий» эффекты «Bioline».
В обзоре более 140 исследований, посвященных влиянию биосовместимых покрытий на клинические результаты, О. Mangoush и др. на основе мета-анализа пришли к выводу, что применение гепаринсодержащих покрытий на 40% снижает частоту рестернотомий по поводу кровотечения, уменьшает в среднем на 78 мин продолжительность искусственной вентиляции легких, более чем на 9 ч – нахождение пациентов в блоке интенсивной терапии и на 12 ч – срок госпитализации в целом. Кроме того, на 20% уменьшается потребность в трансфузии эритроцитов [8]. Теми же авторами приведена оценка финансового эффекта вышеперечисленных бенефиций. Так, применение контура с ковалентно-связанным гепарином позволяет в среднем сэкономить 3 231 доллар на каждого пациента, с нековалентно-связанным – 1 068 долларов.
Недостатком дизайна данного исследования считаем сравнительно малый объем выборок вследствие ограниченных возможностей проведения биохимических анализов. Собственно биохимические критерии оценки воспалительного ответа в силу своей чрезвычайной вариабельности также могут представляться спорными и, очевидно, в дальнейших работах будут заменены более информативными.
Кроме того, представляется интересным проведение сравнительного анализа гематологических, биохимических и клинических эффектов различных покрытий как на основе альбумина (в том числе гепаринсодержащих), так и принципиально иного состава, например ПМЭА (поли-2-метоксиэтилакрилат).
Выводы
-
1. Включение в перфузионный контур мембранного оксигенатора, покрытого составом «Bioline», позволяет ослабить общий воспалительный ответ на искусственное кровообращение, уменьшить степень тромбоцитопении и снижение уровня фибриногена в крови.
-
2. Клинически эффекты этого покрытия проявляются в уменьшении объема кровопотери в послеоперационном периоде, динамике респираторных индексов и в снижении длительности дыхательной поддержки.


