Эхинококкоз человека - современное состояние проблемы и основные тенденции
Автор: Тищенко И.А.
Журнал: Московский хирургический журнал @mossj
Рубрика: Обзоры
Статья в выпуске: 3 (89), 2024 года.
Бесплатный доступ
Введение. Эхинококкоз человека является тяжёлым паразитарным заболеванием, требующим хирургического лечения и характеризующийся высокой долей осложнений и рецидивов. По публикуемым данным заболеваемость во всём мире составляет более 1000000 случаев в год и продолжает неуклонно расти.Основная часть. В статье рассмотрены основные методы диагностики, современные достижения в иммунологической верификации диагноза. Обсуждены проблемы, связанные с отсутствием стандартизации подходов к выбору метода лечения при различных локализациях, множественном и сочетанном поражении. В статье произведён анализ различных вариантов лечения эхинококкоза, изучение статистики результатов, сделан вывод о преимуществах и недостатках активной хирургической тактики лечения над другими методами. Описаны современные малоинвазивные методики, а также актуальность химиотерапии противопаразитарными препаратами. Сделан акцент на важности комбинации их друг с другом. Уделено внимание второй по частоте локализации эхинококковых кист - в лёгких, подчёркнута целесообразность органосохраняющих операций.Заключение. Несмотря на достигнутые успехи в борьбе с эхинококкозом человека, существует ряд вопросов, в отношении которых не достигнуто консенсуса, и решение которых поможет добиться лучших результатов лечения этого заболевания.
Гидатидный эхинококкоз, эхинококковая киста, малоинвазивная хирургия, эхинококкэктомия, карбаматы бензимидазола
Короткий адрес: https://sciup.org/142242556
IDR: 142242556 | УДК: 616-002.951.21 | DOI: 10.17238/2072-3180-2024-3-156-165
Human echinococcosis - the current state of the problem and the main trends
Introduction. Human echinococcosis is a serious parasitic disease that requires surgical treatment and is characterized by a high rate of complications and recurrences. According to published data, the global incidence of this disease is more than one million cases per year and continues to increase steadily.The main part. The article discusses the main diagnostic methods and modern achievements in the immunological verification of the diagnosis. It also discusses the problems related to the lack of standardized approaches to choosing a treatment method for different localizations and multiple and combined lesions. The article analyzes different treatment options for echinococcosis, examines the statistics of the results, and draws conclusions about the advantages and disadvantages of active surgical treatment compared to other methods. It describes modern minimally invasive techniques and the importance of using chemotherapy with antiparasitic drugs, emphasizing the need to combine them. Special attention is paid to the most common location of echinococcal cysts - in the lungs, where the expediency of organ-sparing operations is highlighted.Conclusion. Despite the successes achieved in the fight against human echinococcosis, there are still some issues that have not been fully addressed. The addressing of these issues could lead to better treatment outcomes for this disease.
Текст научной статьи Эхинококкоз человека - современное состояние проблемы и основные тенденции
Эхинококкоз человека в настоящее время это весьма распространенное во всём мире заболевание, характеризующееся высокой склонностью к рецидивированию и развитию осложнений. Наиболее частая локализация инвазии – печень (50–70 %), реже – лёгкие (20–30 %) [1, 2].
Статистические данные отражают неуклонный рост заболеваемости, а публикуемые результаты борьбы с этим зоонозом свидетельствуют о частых случаях инвалидизации, смерти больных, снижении качества жизни и больших трудопотерь, что подтверждает актуальность проблемы [3].
Основным методом лечения заболевания остаётся хирургический, в определённых случаях рекомендованы к применению малоинвазивные методики, а также консервативная терапия противопаразитарными препаратами [4].
По мере накопления опыта лечения больных эхинококкозом, анализа научных исследований, проводимых как в России, так и за рубежом, а также принимая во внимание тот факт, что действующие рекомендации Всемирной организации здравоохранения (ВОЗ) не пересматривались почти 25 лет, сформировался ряд проблем в отношении хирургии эхинококковых кист [5].
Диагностика
По причине того, что на ранних стадиях цистный эхинококкоз обычно протекает бессимптомно, часто обнаружение паразитарных кист – это результат случайной находки во время тех или иных исследований брюшной полости или лёгких, выполняемых по другим показаниям или в рамках диспансеризации.
Неинвазивная диагностика эхинококковых кист различных поражённых органов основана на использовании лучевых методов визуализации. Касаемо печени, ультразвуковое исследование (УЗИ) считается золотым стандартом для определения количества, локализации, размера и жизнеспособности кист, однако оно не всегда позволяет отличить гидатидные кисты от других кистоподобных образований – опухолей или абсцессов печени [6]. Кроме того, это исследование неприменимо при локализации паразита в лёгких. В этих случаях актуальны дополнительные диагностические методы: компьютерная томография (КТ) и магнитно-резонансная томография (МРТ). Предпочтение отдаётся МРТ, поскольку данный метод позволяет лучше визуализировать участки жидкости в матриксе [7].
Иммунодиагностика не является самостоятельным исчерпывающим методом подтверждения диагноза, но всё же – это важная составляющая диагностики в дополнение к лучевым. Также этот метод может быть полезным инструментом для последующего наблюдения после проведённого хирургического или фармакологического лечения, даже несмотря на то, что не у всех пациентов наблюдается выраженный иммунный ответ [8].
Практически все традиционные методы иммунодиагностики (внутрикожный тест Касони, тест фиксации комплемента, реакция непрямой гемагглютинации, непрямой иммунофлю-оресцентный тест на антитела, иммуноэлектрофорез и тест на латексную агглютинацию) в современных условиях заменены другими методиками: иммуноферментным анализом (ИФА) и/ или иммуноблоттингом [9]. Чтобы выявить реакцию антител на паразита, учёными было выделено несколько эхинококковых антигенов, которые впоследствии были использованы для серологической диагностики. Жидкостный антиген эхинококковой кисты В (AgB) и антиген 5 (Ag5) E. granulosus считаются наиболее специфичными нативными антигенами для иммунодиагностики цистного эхинококкоза [10]. При этом отсутствие абсолютной чувствительности и специфичности, перекрестная реактивность с антигенами других паразитов, необходимость стандартизации методов [11] являются основными проблемами, с которыми связана несовершенность иммунодиагностики цистного эхинококкоза.
В сомнительных случаях, когда имеется подозрение на паразитарную природу образования, при отсутствии антител к E. granulosus и необходимости произвести дифференциальную диагностику с новообразованиями или абсцессами, напоминающими эхинококковые кисты, применяется тонкоигольная пункция под ультразвуковой навигацией. Обнаружение протосколексов, эхинококковых оболочек или эхинококковых антигенов либо ДНК в аспирируемой жидкости из кисты подтверждает диагноз эхинококкоза [4]. При этом важно учитывать, что для того, чтобы свести к минимуму риск вторичного заражения, важно принимать антигельминтные препараты: Альбендазол следует рекомендовать принимать за 4 дня до процедуры и продолжать в течение как минимум 1 месяца в случае, если после пункции образование распознанного как эхинококковая киста [12].
Выбор метода лечения
В мировой клинической практике не существует четкого алгоритма в лечении эхинококкоза печени в зависимости от того или иного критерия: поражённый орган, число кист и их размер или других. Однако есть тенденция к попытке стандартизации применяемых методов. Так, в диагностической программе гидатидного эхинококкоза печени используется ультразвуковая классификация Всемирной организации здравоохранения [13]. Она всесторонне отражает стадии жизненного цикла E. granulosus и является определяющей для выбора метода лечения (рис. 1).
Ультразвуковая картина Аксиальный срез (КТ) Аксиальный срез (МРТ)
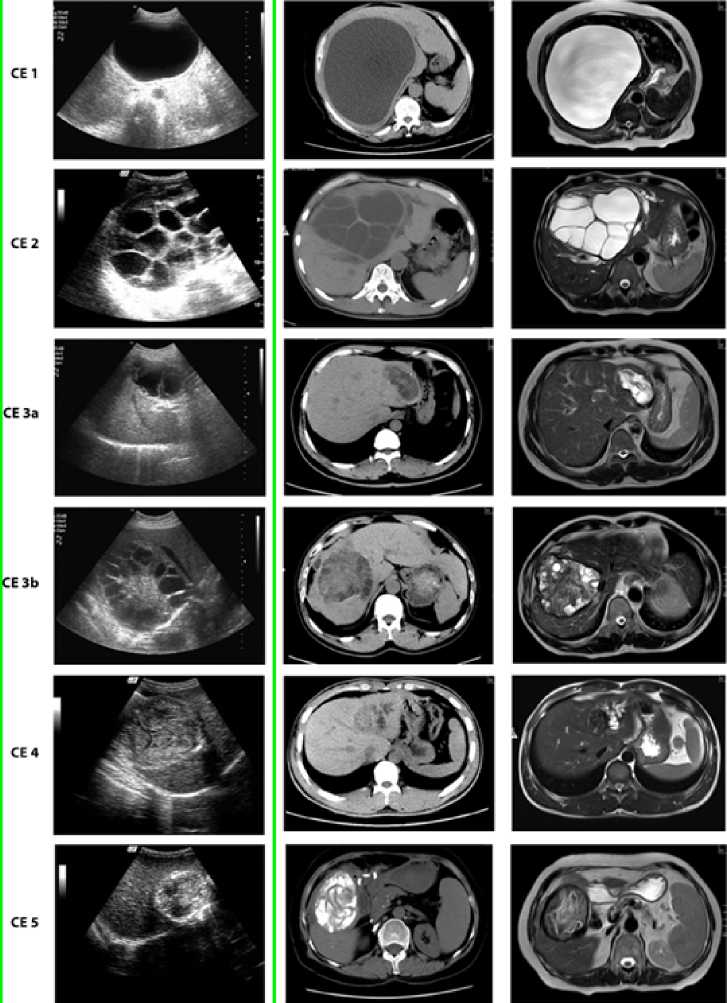
Рис. 1. Классификация эхинококковых кист (Совещание рабочей группы ВОЗ, 2019) и соответствующая визуализация при использовании лучевых методов исследований
Fig. 1. Classification of echinococcal cysts and appropriate imaging using radiation research methods (WHO-IWGE, 2019)
В зависимости от конкретной клинической ситуации, интерпретации результатов обследования на основе данной классификации Всемирной организацией здравоохранения предложены различные варианты лечения, включающие радикальные хирургические вмешательства, малоинвазивные, консервативную терапию противопаразитарными препаратами, динамическое наблюдение (рис. 2). Они могут применяться в качестве как отдельных исчерпывающих методов, так и их комбинации [14]. Активная хирургическая тактика на сегодняшний день остаётся наиболее часто применяемым методом лечения [1, 15].
СЕ
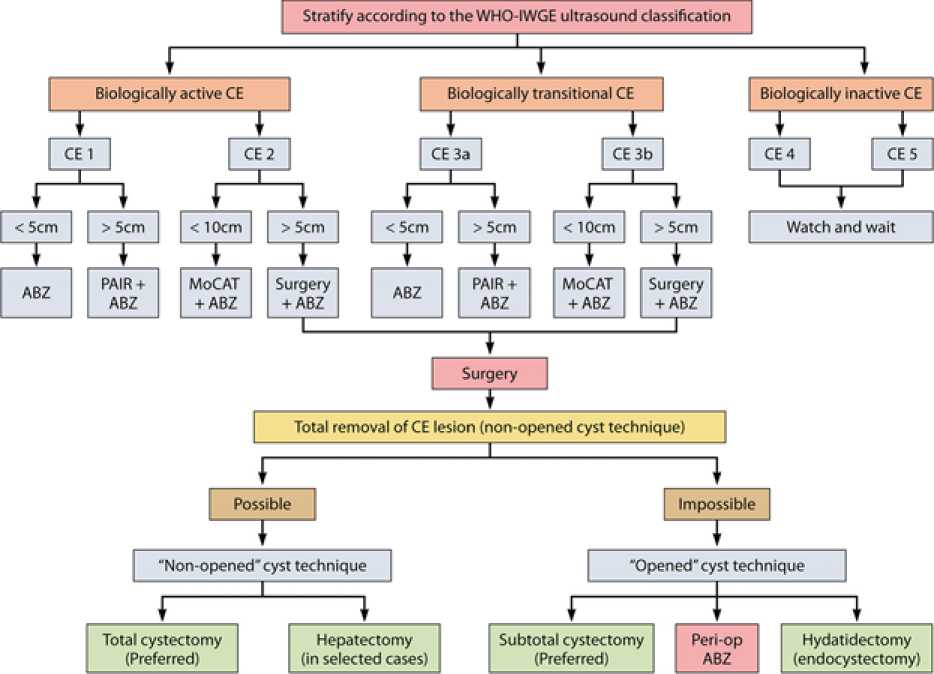
Рис. 2. Алгоритм лечения цистного эхинококкоза (Совещание рабочей группы ВОЗ, 2019)
Fig. 2. Algorithm of treatment of cystic echinococcosis (WHO-IWGE, 2019)
При этом необходимо учитывать, что эхинококкоз – это заболевание, склонное к рецидивированию, высокой частотой осложнений, требующее долгосрочного наблюдения за всеми пациентами, поэтому очень часто требуется мультидисци-плинарный подход для принятия тактических решений, что, в свою очередь, существенно затрудняет строгое следование каким-либо протоколам [16].
Касаемо других локализаций поражения гидатидным эхинококкозом, в частности лёгких, занимающих, как уже было сказано, второе место по частоте, то в настоящее время оперативное лечение остаётся единственным эффективным методом [2, 13, 17]. Также не вызывает расхождения мнений, что осложнённые, а также рецидивные эхино- кокковые кисты являются показанием для радикальной операции [18].
Далее будут рассмотрены применяемые в лечении методики, их особенности, преимущества и ограничения.
Лечение гидатидного эхинококкоза печени
Способы лечения эхинококкоза можно разделить на традиционные хирургические, малоинвазивные и консервативные.
Противопаразитарное медикаментозное лечение основано на применении двух препаратов из группы карбаматов бензимидазола – Мебендазола и Альбендазола. Их фармакологическое действие основано на необратимом нарушении всасывания глюкозы через мембраны клеток паразитов, с последующим истощением запасов гликогена, что в свою очередь приводит к снижению синтеза АТФ и, в конечном итоге, гибели особи. Данные препараты являются единственными с доказанной клинической эффективностью против личиночной стадии E. granulosus [19]. Альбендазол является препаратом выбора ввиду более высокой биодоступности и лучшей переносимости пациентами [20]. В целом, при приёме обоих препаратов достаточно часто возникают сходные побочные эффекты, препятствующие дальнейшему их приёму: диспепсические расстройства (преимущественно в виде тошноты), гепатоток-сические явления, нейтропения и алопеция [21]. Этот факт довольно критичен и является серьёзной проблемой в случаях, когда выполнение оперативного пособия невозможно и успех лечения полностью зависит от химиотерапии. К таким случаям относят множественные неоперабельные кисты в пределах одного органа или сочетанный характер поражения в двух и более органах. Если обобщить данные опыта лечения больных данным зоонозом, то можно сделать вывод, что химиотерапия карбаматами бензимидазола – это общепринятая практика [22]. Однако её необходимая продолжительность, в том числе как дополнение до операции и после, не стандартизирована и является предметом дискуссии.
При неосложнённых кистах стадии СЕ4 и СЕ5 медикаментозная терапия не показана [13].
Традиционные хирургические вмешательства широко применяются в лечении гидатидного эхинококкоза в различных вариациях и рекомендованы на стадиях СЕ2 – СЕ3b заболевания [23]. Основная цель любой из операций – добиться максимально полного удаления метацестоды E. granulosus со всеми элементами, способными привести к рецидиву заболевания. Наиболее часто применяемый доступ – лапаротомия, однако при технической осуществимости, наличии соответствующего оборудования и опыта применима видеолапароскопия [6]. Единого подхода к разделению видов оперативных вмешательств нет. Лучше всего их многообразие систематизирует классификация А.З. Вафина (рис. 3), основанная, в первую очередь, на сохранении или нарушении целостности полости кисты [24].
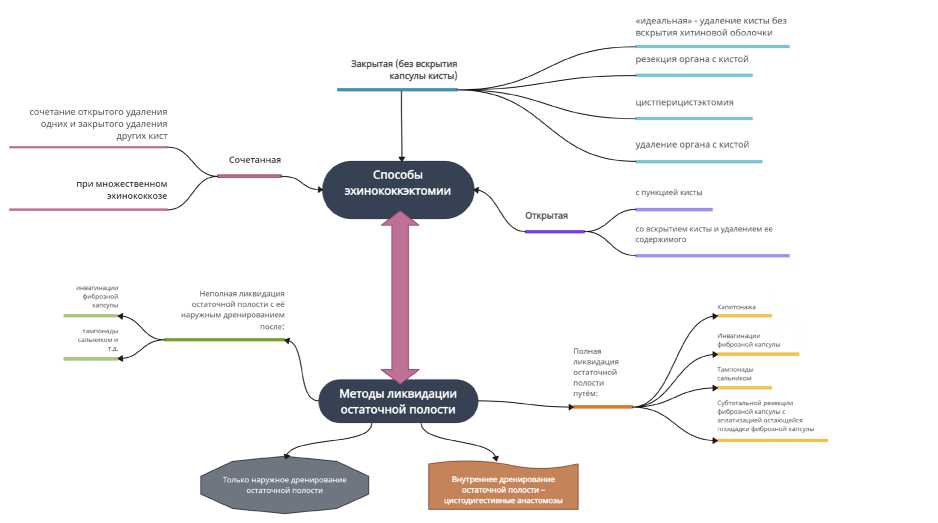
Рис. 3. Классификация эхинококкэктомии (Вафин А.З., 2000)
Fig. 3. Classification of echinococcectomy (A.Z. Vafin, 2000)
Также она характеризует методы ликвидации остаточной полости.
Золотым стандартом из предложенных операций является так называемая «идеальная» – закрытая эхинококкэктомия, при которой капсула кисты не вскрывается [1]. В то же время нет единого мнения в отношении необходимости удаления фиброзной капсулы. Существуют научные публикации, которые противоречат друг другу: одни показывают, что фиброзная капсула является надёжным барьером, который не пропускает зародышевые элементы паразитов [18], другие утверждают, что она сама по себе содержит их [25]. При этом важно осознавать, что выделение фиброзной капсулы, плотно спаянной с паренхимой, часто в условиях той или иной степени воспаления неизбежно приводит к большому объёму интраоперационной кровопотери и нарушению целостности билиарного дерева с последующим желчеистечением [26]. Несмотря на то, что, по мнению Всемирной организации здравоохранения, при наличии возможности более предпочтительна цистперицистэктомия, то есть удаление капсулы вместе с кистой [14], очевидно, что назрела необходимость более централизованных и обширных научных исследований для разрешения этого вопроса.
На практике осуществить закрытую эхинококкэктомию удаётся далеко не всегда. Необходимо понимать, какую бы операцию в конкретном случае не выбрал хирург, во время вмешательства следует руководствоваться принципами апара-зитарности и минимализировать риски обсеменения брюшной полости в случае прорыва или намеренного вскрытия просвета кисты [27]. Принцип антипаразитарности, в свою очередь, достигается обработкой полости кисты противосколецидным раствором. Однако данных о достоверной эффективности того или иного препарата перед другими нет.
Современные малоинвазивные методики основаны на использовании вмешательств, которые позволяют вызвать гибель живых элементов метацестоды, а также удалить или разрушить паразитарную ткань. Эти вмешательства осуществляются чрескожно, в широкой практике применяются три их вида: PAIR (аббревиатура от англ. Puncture, Aspiration, Injection, Re-aspiration), и методики катетеризации – CaT (от англ. Catheterization technique) и MoCaT (от англ. Modified catheterization technique) (рис. 4) [28].
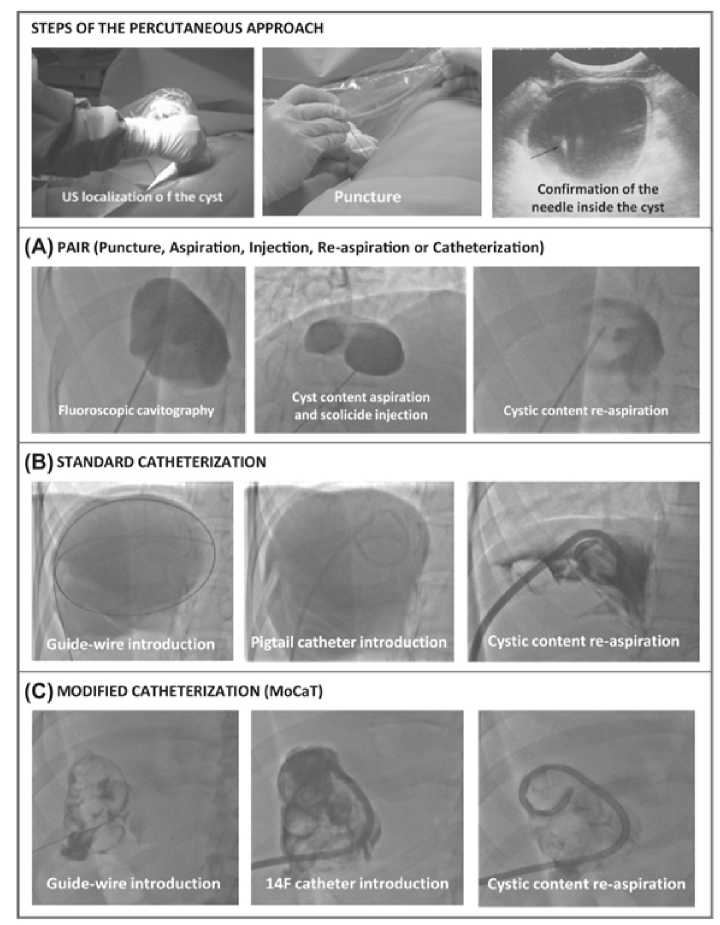
Рис. 4. Пункционно-дренирующие вмешательства
Fig. 4. Puncture-drainage procedures
Малоинвазивные методики применимы при стадиях кист CE1 и CE3a размерами в диаметре не менее 50 мм [13].
Суть данных вмешательств заключается в осуществлении доступа к полости кисты под местной инфильтративной анестезией транскутанным доступом под ультразвуковой навигацией, эвакуацией содержимого и обработкой тканей, выстилающих полость. Конечным итогом процедуры должно стать уничтожение жизнеспособных элементов E. granulosus, способных вызвать рецидив. CaT и MoCaT по сути своей являются модифицированным вариантом PAIR, принципиально отличающимся установкой дренажа в просвете опорожнённой кисты на определённое время [28].
В отличие от традиционных хирургических методов лечения, перечисленные являются менее инвазивными, травматичными и затратными. Также эти методики, по некоторым исследованиям, имеют меньшее число осложнений, способствуют сокращению времени пребывания пациентов в стационаре и более быстрому восстановлению [16].
Описанные методики не показаны к применению при труднодоступных или поверхностно локализованных кистах печени [28].
Лечение эхинококкоза лёгких
Локализация эхинококковых кист в лёгких не является казуистикой, однако, несмотря на это, большого числа иссле- дований и данных по лечению таких больных нет. Обобщив некоторый опыт и исходя из основных тенденций, практикующихся в лечении лёгочного эхинококкоза, можно выделить ряд принципиальных аспектов [29].
Хирургические вмешательства данной локализации должны быть по возможности органосохраняющими и как можно более щадящими по отношению к лёгочной ткани [2]. В то же время, при наличии соответствующих показаний – нагноение кисты, обширное поражение паренхимы и других осложнениях – объём должен быть максимально исчерпывающим и радикальным. Принципиально, все операции при лёгочном эхинококкозе удобно разделить на три вида по аналогии с применяемыми на печени:
-
– открытая эхинококкэктомия;
-
– закрытая эхинококкэктомия;
-
– резекция лёгкого с кистой.
Наряду с торакотомией, для доступа в плевральную полость широко внедряется как видеолапароскопия, так и их комбинация: VATS (видеоассистированная торакоскопическая хирургия, от англ. Video-assisted thoracoscopic surgery) [30]. Данная тенденция призвана снизить травматичность операций, сократить сроки пребывания больных в стационаре, период восстановления и, в конечном итоге, ускорить восстановление трудоспособности.
На рисунке 5 представлена интраоперационная визуализация этапов видеоторакоскопической открытой эхинококкэктомии лёгкого.
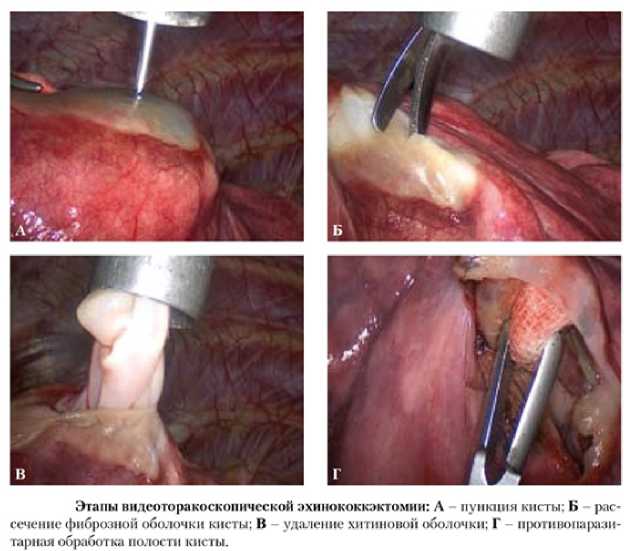
Рис. 5. Кадры, сделанные при торакоскопической эхинококкэктомии
Fig. 5. Footage taken during a thoracoscopic procedure for echinococcosis
Необходимо помнить, что следует дополнять хирургическое лечение эхинококкоза лёгких противопаразитарной фармакотерапией по рекомендованной ВОЗ схеме [20, 21].
Заключение
Эхинококкоз человека – это тяжёлое, зачастую диагностируемое на поздних стадиях заболевание, характеризующееся высокой склонностью к рецидивированию и осложнениям. Многие страны мира являются эндемичными к этому зоонозу и заявляют о существенном ущербе для здравоохранения и животноводства. В России эта проблема также затрагивает большое количество регионов, а заболеваемость ежегодно неуклонно растёт.
В последние годы достигнут значительный прогресс в изучении биологии эхинококкоза, его связи с иммунной системой, и, на основе этого, в создании более точных и чувствительных иммунологических тестов, а также внедрении ПЦР, которые вместе с современными лучевыми методами исследований существенно расширяют спектр инструментов диагностики.
Помимо этого, усовершенствование хирургических методов, внедрение малоинвазивных операций и комбинирование их с использованием эффективных лекарственных препаратов положительным образом влияют на успех лечения, продолжительность и качество жизни пациентов.
Несмотря на прогресс в диагностике и лечении, многие открытые проблемы требуют своего решения: например, существует необходимость ужесточения контроля за противо-паразитарными мероприятиями в отрасли животноводства, нужны программы и алгоритмы, направленные на раннее – доклиническое выявление заболевания. Кроме того, нужны научные исследования, в которых будут сравниваться варианты лечения гидатидного эхинококкоза с целью выработки наиболее оптимальной стандартизированной тактики.
Список литературы Эхинококкоз человека - современное состояние проблемы и основные тенденции
- Mjonnink G.L.E., Stijni, C., van Delden O.M., Spijker R., Grobusch M.P. Percutaneous versus surgical interventions for hepatic cystic echinococcosis: a systematic review and meta-analysis. Cardiovascular and Interventional Radiology, 2021, 44, pp. 1689-1696. https://doi.org/10.1007/s00270-021-02911-4
- Harlaftis N.N., Aletras H.A., Symbas P.N. Hydatid Disease of the Lung. General Thoracic Surgery, 2009, № 7, pp.1187-1195.
- Kern P., Menezes da Silva A., Akhan O., Mullhaupt B., Vizcaychipi K.A., Budke C., Vuitton D.A. The echinococcoses: diagnosis, clinical management and burden of disease. Advances in parasitology, 2017, № 96, pp. 259-369. https://doi.org/10.1016/bs.apar.2016.09.006
- Шевченко Ю.Л., Назиров Ф.Г., Зайниддинов Ф.А., Хасан О. Современные подходы к диагностике и лечению эхинококкоза. Вестник Национального медико-хирургического центра им. НИ Пирогова, 2020. № 15 (1). С. 13-22. https://doi.org/10.25881/BPNMSC.2020.37.47.002
- Siles-Lucas M., Uchiumi L., Tamarozzi F. No cyst, no echinococcosis’: a scoping review update on the diagnosis of cystic echinococcosis after the issue of the WHO-IWGE Expert Consensus and current perspectives. Current Opinion in Infectious Diseases, 2023, № 36(5), pp. 333-340.
- Govindasamy A., Bhattarai P. R., John J. Liver cystic echinococcosis: a parasitic review. Therapeutic Advances in Infectious Disease, 2023, № 10, pp. 1-12. https://doi.org/10.1177/20499361231171478
- Hosch W., Junghanss T., Stojkovic M., Brunetti E., Heye T., Kauffmann G.W., Metabolic viability assessment of cystic echinococcosis using high-field 1H MRS of cyst contents. NMR Biomed, 2008, № 21(7), pp. 734-754. https://doi.org/10.1002/nbm.1252
- Sarink, M.J., Genderen, P.V., Tielens, L., Hellemond, J.V. Ruptured Echinococcus granulosus cysts in migrants: Is excessive antigen release causing false negative serology? Travel Medicine and Infectious Disease, 2019, № 35, pp. 101412-101412. https://doi.org/10.1016/j.tmaid.2019.04.012
- Craig P.S., Rogan M.T., Campos-Ponce M. Echinococcosis: disease, detection and transmission. Parasitology, 2003, № 127(S1), pp. S5-S20. https://doi.org/10.1017/S0031182003004384
- Zhang W., McManus D.P. Recent advances in the immunology and diagnosis of echinococcosis. FEMS Immunology & Medical Microbiology, 2006, № 47(1), pp. 24-41. https://doi.org/10.1111/j.1574-695X.2006.00060.x
- Liu D., Rickard M.D., Lightowlers M.W. Assessment of monoclonal antibodies to Echinococcus granulosus antigen 5 and antigen B for detection of human hydatid circulating antigens. Parasitology, 1993, № 106(1), pp. 75-81. https://doi.org/10.1017/S0031182000074849
- Pedrosa I., Saiz A., Arrazola J., Ferreiros J., Pedrosa C. S. Hydatid Hydatid Disease: Radiologic and Pathologic Features and Complications. Radiographics, 2000, 20(3), pp. 795-817. https://doi.org/10.3748/wjg.v16.i24.3040
- Всемирная организация здравоохранения: эхинококкоз. ВОЗ, 2024. https://www.who.int/news-room/fact-sheets/detail/echinococcosis. (дата обращения 12.04.2024).
- Budke C.M., Casulli A., Kern P., Vuitton D.A. Cystic and alveolar echinococcosis: Successes and continuing challenges. PLoS neglected tropical diseases, 2017, № 11(4). https://doi.org/10.1371/journal.pntd.0005477
- О заболеваемости эхинококкозом и альвеококкозом в Российской Федерации: письмо Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека от 20.06.2016 № 01/7782-16-27. URL: https://docs.cntd.ru/document/420370904 (дата обращения: 09.05.2024).
- Hadzhiev B., Todorov A., Sakakushev B., Atanasov B. Surgical treatment of hepatic echinococcosis - 10-year experience. Khirurgiia, 2011, № 3, pp. 76-79.
- Потапов А.А., Горяйнов С.А., Охлопков В.А., Кравчук А.Д., Захарова Н.Е., Подопригора А.Е., Курносов А.Б., Хить М.А., Панина Т.Н., Елисеева Н.М. Множественный эхинококкоз головного мозга, сердца и почек. Вопросы нейрохирургии им. НН Бурденко, 2011. № 75(1). С. 57-65.
- Курбонов К.М., Давлатов Д.Ё., Махмадов Ф.И., Азизов А.З. Диагностика и тактика хирургического лечения рецидивного эхинококкоза печени. Здравоохранение Таджикистана, 2014. № 2. С. 36-42.
- Siles-Lucas M., Casulli A., Cirilli R., Carmena D. Progress in the pharmacological treatment of human cystic and alveolar echinococcosis: compounds and therapeutic targets. PLoS neglected tropical diseases, 2018, № 12(4). https://doi.org/10.1371/journal.pntd.0006422
- Senyuz O.F., Yesildag E., Celayir S. Albendazole therapy in the treatment of hydatid liver disease. Surg Today, 2001, № 31, pp. 487-491. https://doi.org/10.1007/s005950170106
- Alvela-Suarez L., Velasco-Tirado V., Belhassen-Garcia M., NovoVeleiro I., Pardo-Lledias J., Romero-Alegria A., Villar L.P., Valverde-Merino M.P., Cordero-Sanchez M. Safety of the combined use of praziquantel and albendazole in the treatment of human hydatid disease. The American journal of tropical medicine and hygiene, 2014, № 90(5), pp. 819. https://doi.org/10.4269/ajtmh.13-0059
- Одишелашвили Г.Д., Пахнов Д.В., Одишелашвили Л.Г. Сравнительная оценка способов облитерации остаточных полостей после дренирующих операций по поводу эхинококкоза печени. Вестник Ивановской медицинской академии, 2020. № 25(2). С. 34-37.
- Brunetti E., Kern P., Vuitton D. A. Expert consensus for the diagnosis and treatment of cystic and alveolar echinococcosis in humans. Acta tropica, 2010, 114(1), pp. 1-16. https://doi.org/10.1016/j.actatropica.2009.11.001
- Вафин А.З., Айдемиров А.Н., Попов А.В. Классификация методов хирургического лечения эхинококкоза. Анналы хирургической гепатологии, 2000. № 5(2). С. 19.
- Martel G., Ismail S., Begin A., Vandenbroucke-Menu F., Lapointe R. Surgical management of symptomatic hydatid liver disease: experience from a Western centre. Canadian Journal of Surgery, 2014, № 57(5), pp. 320-326. https://doi.org/10.1503/cjs.024613
- Айтназаров М.С., Касыев Н.Б., Мадаминов Э.М. Результаты ликвидации желчных свищей при эхинококкозе печени. Актуальные проблемы гуманитарных и естественных наук, 2017. № 5-2. С. 80-82.
- Sharafi S.M., Sefiddasht, R.R., Sanei B., Yousefi M., Darani, H.Y. Scolicidal agents for protoscolices of Echinococcus granulosus hydatid cyst: review of literature. Journal of Research in Medical Sciences: The Official Journal of Isfahan University of Medical Sciences, 2017, № 22 (1), p. 92. https://doi.org/10.4103/jrms.JRMS_1030_16
- Akhan O., Gumus B., Akinci D., Karcaaltincaba M., Ozmen M. Diagnosis and percutaneous treatment of soft-tissue hydatid cysts. Cardiovascular and interventional radiology, 2007, № 30, pp. 419-425. https://doi.org/10.1007/s00270-006-0153-1
- Tunc H., Gorur R., Erdik O., Isitmangil T., Sebit S., Kunter E., Toker A., Kunter B., Ozturk O. Y. Clinical experience of surgical therapy in 207 patients with thoracic hydatidosis over a 12-year period. Swiss medical weekly, 2002, № 132(3738), pp. 548-552.
- Cai B., Li C., Luo Z., Ciren D., Guo W., Huang J., Dawa, Q. Efficacy and safety of video-assisted thoracoscopic surgery and thoracotomy in the treatment of pulmonary hydatid disease in the Tibetan Plateau: a retrospective study. Journal of Thoracic Disease, 2022, № 14(6), pp. 2247. https://doi.org/10.21037/jtd-22-714


