Экспериментальная модель для изучения процессов репаративного остеогенеза
Автор: Гребнева О.Л., Ковинька М.А., Силантьева Т.А., Дюрягина О.В., Сбродова Л.И., Кузнецова Е.И., Розова Л.В., Стогов М.В., Ткачук Е.А.
Журнал: Сибирский журнал клинической и экспериментальной медицины @cardiotomsk
Рубрика: Лабораторные и экспериментальные исследования
Статья в выпуске: 1-1 т.26, 2011 года.
Бесплатный доступ
Приведены экспериментальные данные морфологических, гематологических, иммунологических и биохимических исследований, характеризующие компенсаторно&адаптационные реакции белых лабораторных мышей линии СВА после моделирования травмы реберной кости. Доказано, что перелом реберной кости у животных вызывает умеренное напряжение адаптационных систем и приводит к стабильно воспроизводимой морфологической картине регенерации костной ткани. Исследования показали пригодность модели перелома реберной кости для экспериментальных исследований процессов репаративного остеогенеза и метаболического ответа на костную травму.
Модель, репаративный остеогенез, лабораторные мыши
Короткий адрес: https://sciup.org/14919360
IDR: 14919360 | УДК: 57.084.1:599.323.4-092.9:611.018.4
Experimental model for research of reparative osteogenesis processes
Experimental findings of morphological, haemotological, immune and biochemical studies describing compensatory and adaptative response of lab СBA white mice following simulated rib injury have been reviewed. Rib fracture in animals has shown to cause moderate tensioning in adaptative response and results in stable reproducible morphological pattern of bone tissue regeneration. The findings have shown that the injured rib model can be applied to experimental study of reparative osteogenesis and metabolic response to osseous injury.
Текст научной статьи Экспериментальная модель для изучения процессов репаративного остеогенеза
Одним из актуальных вопросов травматологии и ортопедии является тестирование различных способов и средств в экспериментальных условиях, которое требует адекватной модели репаративного остеогенеза. Нами была предложена модель перелома реберной кости у лабораторных мышей. В доступной литературе нам не удалось найти описания такой операции, хотя работы на подобной модели цитируются [24]. Цель работы: характеристика протекания репаративного остеогенеза при моделировании перелома тела реберной кости у лабораторных мышей, а также динамики изменения биохимических, гематологических и иммунологических показателей.
Материал и методы
В опытах был исследован материал от 464 белых мышей-самцов линии СВА массой 25–30 г. Уход за животными, эксперименты и эвтаназию проводили в соответствии с этическими нормами работы с лабораторными животными, отраженными в Правилах проведения работ с использованием экспериментальных животных (приказ №755 Министерства здравоохранения СССР от 12
августа 1977 г.).
Выполнение операции по моделированию перелома реберной кости у мышей. Перелом реберной кости у мышей осуществляли под общим наркозом. Для этого подкожно в область шеи инъецировали по 0,04 мл каждого из препаратов Рометар и Золетил после их разведения стерильной дистиллированной водой в 3 и 15 раз соответственно. Готовили операционное поле в зоне интереса размером 1,5 см х 1,5 см, проводили разрез кожного покрова длиной около 0,8 см по линии позвоночного столба, после чего на расстоянии 3–4 мм от последнего перерезали 4-е ребро. Операционную рану ушивали узловыми швами шелком и обрабатывали клеем БФ-6.
Исследования биологического материала. Морфологические исследования выполняли на биологических образцах фрагментов реберных костей, извлеченных после эвтаназии животных через 10 и 30 суток после операции; количество животных (n) – от 8 до 10 в каждой группе. Образцы фиксировали в 10-процентном растворе формалина, обезжиривали в ацетоне, декальцинировали в Трилоне Б, обезвоживали и заливали в парафин. Гистологические срезы толщиной 5–7 мкм окрашивали гематоксилином и эозином. Светооптическое исследование гистологических препаратов проводили на микроскопе
“Микмед 5” (“ЛОМО”, Россия). Для выполнения гистомор-фометрического исследования на проекционном экране микроскопа Visopan (“Reichert-Jung”, Австрия) размещали тестовую систему в виде решетки с ячеями известной площади. В произвольно выбранных неперекрыва-ющихся полях зрения производили подсчет количества дифференцированных клеток хондробластического и ос-теобластического ряда в периосте, а также числа микрососудов в параоссальной области. Через 1, 3, 5 и 7 суток после операции (п=7 ^ 10) проводили гематологические исследования, включавшие подсчет количества лейкоцитов, эритроцитов в единице объема, лейкоцитарной формулы, ретикулоцитов в периферической крови. Иммунологические исследования (п=6 ^ 10) проводили спустя 1, 3 и 7 суток после операции. Они заключались в определении бактерицидной активности сыворотки крови (БАСК) по методике С.А. Паевского в модификации [16, 20], лизоцимной активности сыворотки крови (ЛАСК) [22], фагоцитарной активности нейтрофилов по поглощению микробных клеток Staphylococcus epidermidis (штамм №9198 НИИЭМ) с подсчетом фагоцитарного показателя и фагоцитарного числа [11]. Биохимические исследования сыворотки крови, проводимые спустя 3 и 10 суток после операции (п=6 ^ 21), включали спектрофотометрическое определение в сыворотке крови активности щелочной (ЩФ) и тартратрезистентной кислой фосфатаз (ТрКФ), содержания кальция, магния, фосфора и хлоридов, молочной кислоты (МК) с помощью наборов Vital Diagnostic (СПб), пировиноградной кислоты (ПВК) по методу Умбрайта [2]. Для всех перечисленных показателей были определены их величины у интактных животных, принятые в качестве контрольных.
Статистическую обработку результатов проводили с использованием непараметрического критерия Вилкок-сона для независимых выборок. Критический уровень гипертрофированы, в части клеток отмечались дегенеративные изменения (рис. 1Б на 3-й стр. обложки). Новообразованная костная ткань наблюдалась в виде тонкого слоя непосредственно на поверхности компактной пластинки кости (рис. 1В на 3-й стр. обложки), реже – в виде перихондрально образованных костных трабекул. К 30-м суткам после операции было сформировано периостальное костно-хрящевое и эндостальное костно-волокнисто-соединительнотканно-хрящевое сращение перелома. Компактная костная пластинка отломков реберной кости была спонгизирована (рис. 2А на 3-й стр. обложки). Объемные периостальные наслоения были представлены губчатой костной тканью с сетью пластинчатых трабекул и красным костным мозгом межтрабекулярных пространств (рис. 2Б на 3-й стр. обложки). В плоскости перелома сохранялись очажки гиалинового хряща (рис. 2В на 3-й стр. обложки) и поля рыхлой волокнистой соединительной ткани (рис. 2Г на 3-й стр. обложки), формировались периостальные костные перемычки. Численная плотность клеток опорных тканей для обоих сроков эксперимента представлена в таблице 1.
Общее количество лейкоцитов периферической крови в сроки эксперимента достоверно не изменялось. Статистически значимо на всех сроках опыта снижалось количество нейтрофильных лейкоцитов за счет палочкоядерных и сегментоядерных с восстановлением количества последних на 7-е сутки опыта (рис. 3). С 1-х суток после операции снижалось содержание моноцитов, также оставаясь низким спустя 7 суток после операции. Единственным видом лейкоцитов, количество которых не снижалось, остались лимфоциты; их относительное содержание на 1, 3 и 5-е сутки эксперимента было даже выше дооперационных значений.
Среди изученных показателей неспецифической резистентности единственным достоверно изменявшимся значимости при проверке статистических гипотез принимался равным 0,05.
Результаты и обсуждение
На гистологических препаратах исследовали фрагменты тел реберных костей, включающие зону сращения перелома и прилежащие участки костных отломков. Спустя 10 суток после операции в интермеди-арной части зоны сращения перелома располагалась рыхлая, реактивно измененная волокнистая соединительная ткань, бесструктурные массы детрита. В периостальной части зоны сращения формировалась объемная костно-хрящевая мозоль (рис. 1А на 3-й стр. обложки). Хрящевая ткань отличалась высокой клеточной плотностью. Поверхностно расположенные хондроциты имели меньший диаметр и входили в состав изогенных групп, тогда как глубоко расположенные хондроциты были
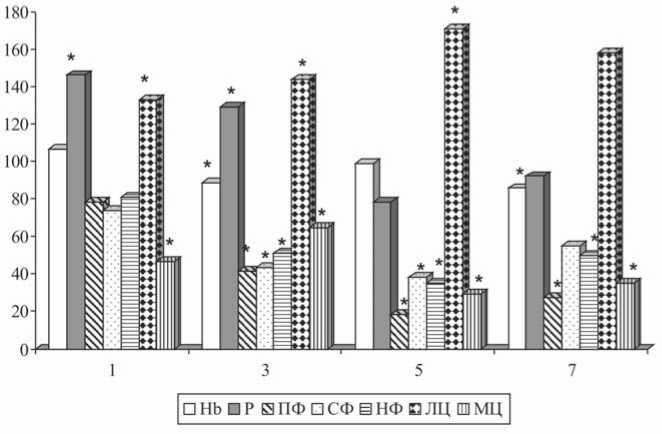
Рис. 3. Гематологические показатели периферической крови животных, % от контрольных значений. Приведены медианы показателей, имеющие в динамике наблюдений достоверные отличия от контрольных (* – р<0,05). По оси абсцисс – сутки после операции. Обозначения: Hb – гемоглобин (г/л), Р – ретикулоциты (х 109/л), ПФ – палочкоядерные нейтрофилы (х 109/л), СФ – сегментоядерные нейтрофилы (х 109/л), НФ – нейтрофилы (х 109/л), ЛЦ – лимфоциты (%), МЦ – моноциты (%)
Таблица 1
Количество клеток и микрососудов на единицу площади периоста/параоссальной ткани (0,0025 мм2)
|
Срок опыта* |
Костные клетки |
Хрящевые клетки |
Микрососуды |
|
|
Медиана |
0,600 |
6,40 |
0,163 |
|
|
1 квартиль |
10 суток |
0,529 |
5,90 |
0,140 |
|
3 квартиль |
0,921 |
7,39 |
0,173 |
|
|
Медиана |
4,04 |
1,70 |
0,088 |
|
|
1 квартиль |
30 суток |
3,90 |
1,49 |
0,075 |
|
3 квартиль |
4,33 |
2,47 |
0,119 |
|
|
p-значение |
0,005 |
0,005 |
0,035 |
Примечание: * – для обеих точек опыта, объемы выборки n=6.
была лизоцимная активность сыворотки крови (табл. 2), которая оставалась ниже значений интактных животных на всех сроках опыта.
Концентрации электролитов (кальция, хлорида, фосфора, магния) в сроки эксперимента не отличались от контрольных значений. Активность ЩФ в два раза возра- стала, а ТрКФ снижалась в полтора раза на 10-е сутки после операции (табл. 3). Концентрация МК к этому сроку опыта также снижалась. Содержание ПВК повышалось к 3-м, после чего снижалось к 10-м суткам после операции.
Обсуждение
В литературе имеются исследования, оценивающие репаративные способности реберной кости как промежуточные между таковыми у большеберцовой и бедренной кости [13]. Гистологические исследования подтвердили адекватность выбора именно этой кости для моделирования перелома. Анатомические особенности ее расположения оказались благоприятными как для получения воспроизводимой морфологической картины периостального регенерата, так и для количественной оценки интенсивности регенераторного процесса. К 10-м суткам после операции периостальный регенерат представлен исключительно грубоволокнистой костной и гиалиновой хрящевой тканями, не подвергается резорбции и сосудистой инвазии. Подсчет численной плотности дифференцированных клеточных элементов остео-бластического и хондробластического ряда и микрососудов пароссальных тканей позволяет выявить влияние различных факторов на процессы остео-, хондро- и ангиогенеза.
Хорошо изученные основные принципы регенерации тканей при переломе остаются справедливыми и для данной модели, однако мы обнаружили ряд особенностей в реакции некоторых систем. Деструкция клеток и тканей при переломе вызывает последовательно протекающие защитно-приспособительные процессы, начальными из которых являются реакции воспаления [4, 8, 17]. В первые 6–24 ч в очаг воспаления эмигрируют нейтрофилы, через 24–48 ч – моноциты и лимфоциты. Острые воспалительные процессы с травмой опорно-двигательного аппарата, к числу которых принадлежит и приведенная
Таблица 2
Показатели неспецифической резистентности экспериментальных животных
|
Показатели* |
Срок после операции, сут |
n** |
Медиана |
Квартиль 1 |
Квартиль 3 |
р*** |
|
БАСК, мм |
Интактные |
9 |
18,5 |
17,00 |
19,00 |
- |
|
ЛАСК, % |
животные |
9 |
81,90 |
80,8 |
83,4 |
- |
|
БАСК, мм |
1 |
7 |
18,00 |
18,00 |
18,00 |
0,611 |
|
ЛАСК, % |
1 |
7 |
74,90 |
70,40 |
77,00 |
0,001 |
|
БАСК, мм |
3 |
6 |
16,00 |
15,25 |
16,00 |
0,066 |
|
ЛАСК, % |
3 |
6 |
70,95 |
66,53 |
73,05 |
0,002 |
|
БАСК, мм |
5 |
6 |
18,00 |
17,25 |
19,50 |
0,952 |
|
ЛАСК, % |
5 |
6 |
77,95 |
75,50 |
79,88 |
0,021 |
|
БАСК, мм |
7 |
6 |
18,00 |
18,00 |
18,75 |
0,620 |
|
ЛАСК, % |
7 |
6 |
66,55 |
65,38 |
69,30 |
0,002 |
Список литературы Экспериментальная модель для изучения процессов репаративного остеогенеза
- Бабаева А.Г. Прошлое, настоящее и будущее проблемы лимфоидной регуляции нелимфоидных клеток//БЭБМ. -1995. -№ 9. -С. 230-234.
- Бабаскин, Б.С. Определение пировиноградной кислоты модифицированным методом Умбрайта//Лабораторное дело. -1976. -№ 3. -С. 76-79.
- Бердюгина О.В. Иммунологические тесты в оценке замедленной консолидации костной ткани при дистракционном остеогенезе нижней челюсти//Тезисы участников Юбилейной научно&практической конференции, посвященной 70-летию кафедры травматологии, ортопедии РГМУ [Электронный ресурс]. -URL: http://travmatology.narod.ru/tezis01.htm.
- Воспаление. Руководство для врачей/под ред. В.В. Серова, В.С. Паукова. -М.: Медицина, 1995. -640 с.
- Герасимов А.М., Фурцева Л.Н. Биохимическая диагностика в травматологии и ортопедии. -М.: Медицина, 1986. -240 с.
- Долгушин И.И., Эберт Л.Я., Лифшиц Р.И. Иммунология травмы. -Свердловск: Изд-во Урал. ун-та, 1989. -188 с. 139
- Иммунология в клинической практике. -1-й том издания медицинской электронной библиотеки [Электронный ре& сурс]/под ред. проф. К.А. Лебедева. -1996. -URL: http://www.rosmedic.ru/immunologiya/immunologiya-v-klinicheskoy-praktike-2.html.
- Корж Н.А., Дедух Н.В. Репаративная регенерация кости: современный взгляд на проблему. Стадии регенерации (сообщение 1)//Ортопедия, травматология и протезирование. -2006. -№ 1. -С. 77-84.
- Кравцов В.И., Рыков В.А., Даровский Б.П., Загородников И.В. Моделирование травматической болезни в эксперименте на животных [Электронный ресурс]//Медицина в Кузбассе: Восстановительное лечение пострадавших от производственных травм и профессиональных заболеваний на санаторном этапе. Материалы межрегиональной научно-практической конференции, г. Новокузнецк, 19 мая 2006 г. -Кемерово: Медицина и просвещение, 2006. -Спецвыпуск № 5. -С. 62-65. -URL: http://www.kuzdrav.ru/medlib/mk/mksp2006_5.pdf.
- Куприянова А.Д., Дыдыкина Н.И. Полиферментные препараты и острые расстройства пищеварения у собак [Электронный ресурс]//Проблемы и перспективы современной науки: сборник научных трудов (выпуск 1)/под редакцией проф., д.м.н. Ильинских Н.Н. -2009. -URL: http://teleconf.ru/aktualnyie-problemyi-tehnologii-i-primeneniya-bav/polifermentnyie-preparatyi-i-ostryie-rasstroystva-pischevareniya-u-sobak.html.
- Лабораторные методы исследования в клинике: справочник/под ред. В.В. Меньшикова. -М.: Медицина, 1987. -С. 310-311.
- Лунева С.Н., Стогов М.В., Столбиков С.А. Изменения биохимических показателей сыворотки крови у пациентов с закрытыми переломами костей голени в нижней трети при лечении по методу Илизарова//Травматология и ортопедия России. -2007. -№ 3 (45). -С.63-67.
- Маланчук В.А., Астахова В.С., Циленко О.Л. Остеогенные клетки-предшественники костного мозга человека в реконструктивно-восстановительной хирургии лицевого скелета//Журнал академии медицинских наук Украины. -2009. -Т. 15, № 2. -С. 276-289.
- Методические рекомендации по применению препарата "Золетил 50" в подразделениях государственной ветеринарной службы города Москвы [Электронный ресурс]. -М., 2004. -URL: http://www.msu.ru/bioetika/doc/pismoveterenar.doc.
- Огнев А.С. Иммунобиохимические показатели крови маралов в норме и при патологии: автореф. дис. … канд. ветеринар. наук: 16.00.03 [Электронный ресурс]/Алтайский гос. аграрный университет. -Барнаул, 2009. -17 с. -URL: http://www.asau.ru/doc/nauka/Autoreferat_Ognev.doc.
- Паевский С.А. Способ определения бактерицидной активности тканей при лечении ортопедических больных методом чрескостного остеосинтеза//Клиническая лабораторная диагностика. -1993. -№ 5. -С.25-29.
- Попсуйшапка А.К., Литвишко В.А., Подгайская О.А. Сращение отломков после перелома кости [Электронный ресурс]//Международный медицинский журнал. -2009. -№2. -С. 73-80. -URL: http://www.nbuv.gov.ua/portal/Chem_Biol/Mmzh/2009_2.pdf.
- Предварительные результаты влияние препарата "Мицеллат" на репаративную регенерацию костной ткани [Электронный ресурс]/Российский научный центр "Восстановительная травматология и ортопедия" им. акад. Г.А. Илиза& рова, г. Курган. -URL: http://www.micellat.ru/doc/02.doc.
- Разина А.В., Фролова А.И., Сергеев М.А. Влияние нейролептанальгезии на клинический статус кроликов//Ветеринарная клиника. -2008. -№ 1. -С. 27-28.
- Розова Л.В., Науменко З.С. Использование агара Мюллера-Хинтон при определении бактерицидной активности: рационализаторское предложение № 56/08 от 18.12.08.
- Сергеев М. А., Фролова А. И., Равилов Р. Х. Влияние общего обезболивания и операционной травмы на показатели специфического и неспецифического иммунитета у щенков//Ветеринарная клиника. -2008. -№ 5. -С.11-13.
- Стогний В.И., Голик В.П., Ткаченко В.В., Воропаева Л.В., Полякова С.В. Способ определения активности лизоцима в слюне и сыворотке крови//Лабораторное дело. -1989. -№ 8. -С. 54.
- Ястребов А.П., Осипенко А.В. Система крови и регенерация костной ткани. -Свердловск: Изд-во Урал. ун-та, 1990. -124 с.
- Asaumi K., Nakanishi T., Asahara H. et al. Expression of neurotrophins and their receptors (TRK) during fracture healing//Bone. -2000. -Vol. 26, No. 6. -P. 625-633.


