Экспериментальный цифровой атлас зон кровоснабжения ветвей внутренней сонной артерии
Автор: Губский Илья Леонидович, Наместникова Дарья Дмитриевна, Черкашова Эльвира Андреевна, Гумин Иван Сергеевич, Губский Леонид Васильевич, Баклаушев Владимир Павлович, Чехонин Владимир Павлович, Ярыгин Константин Никитич
Журнал: Клиническая практика @clinpractice
Рубрика: Оригинальные исследования
Статья в выпуске: 1 т.16, 2025 года.
Бесплатный доступ
Обоснование. Создание нейроанатомического атласа на большой выборке данных является, по сути, фундаментальным трудом, но создание цифрового атласа в эпоху широкого применения методов лучевой диагностики в клинической и экспериментальной практике, а также систем искусственного интеллекта придаёт исследованию значимое прикладное значение. Крысы являются основным видом лабораторных животных, на которых происходят исследования по моделированию ишемического инсульта, тестированию церебропротекторных препаратов и разработке новых стратегий регенеративной терапии последствий инсульта. На данный момент не существует полноценного цифрового атласа артериального кровоснабжения мозга крыс, а единичные работы опираются на небольшие группы животных и их гистологическое описание. В связи с этим представляется крайне интересным и важным сделать первый шаг для освещения данной проблемы. Цель исследования - создать атлас зон кровоснабжения интракраниальных ветвей внутренней сонной артерии в условиях экспериментальной окклюзии средней мозговой артерии.
Ишемический инсульт, крысы, кровоснабжение, магнитно-резонансная томография, искусственный интеллект
Короткий адрес: https://sciup.org/143184134
IDR: 143184134 | DOI: 10.17816/clinpract642757
Experimental Digital Atlas of Blood Supply Zones of the Internal Carotid Artery
Background: The compilation of a neuroanatomic atlas based on a large sample is essentially a fundamental research work, but compiling a digital atlas during the epoch of wide usage of radiodiagnostics methods in the clinical and experimental practice along with using the artificial intelligence systems brings a significant applied relevance to the research. Rats are the main species of laboratory animals, in which the studies of modeling the ischemic stroke, of testing the cerebroprotective drugs and of developing new strategies of regenerative therapy of stroke consequences are carried out. At the present moment, there is no available and comprehensive digital atlas of the arterial blood supply of the rat brain, while single research works are based on small groups of animals and their histological description. Within this context, it is deemed very interesting and important to take the first step in addressing this issue.
Текст научной статьи Экспериментальный цифровой атлас зон кровоснабжения ветвей внутренней сонной артерии
Gubskiy IL, Namestnikova DD, Cherkashova EA, Gumin IS, Gubsky LV, Baklaushev VP, Chekhonin VP, Yarygin KN. Experimental digital atlas of blood supply zones of the internal carotid artery. Journal of Clinical Practice. 2025;16(1):30–37. doi:
Submitted 10.12.2024 Accepted 12.03.2025 Published online 12.03.2025
ОБОСНОВАНИЕ
Для решения современных научных задач исследователям приходится всё глубже осваивать и применять новые методы обработки и анализа данных [1]. Технический прогресс ускоряется, что способствует развитию прикладных исследований, однако отмечается снижение внимания к фундаментальной науке [2]. Данная статья посвящена


изучению распределения зон артериального кровоснабжения в мозге крыс, которые уже более 150 лет остаются, пожалуй, самыми популярными лабораторными животными для моделирования заболеваний в экспериментальных биомедицин- ских исследованиях [3]. Экспериментальная мо- дель ишемического инсульта, основанная на тран-зиторной окклюзии средней мозговой артерии с использованием монофиламента, максимально точно воспроизводит патогенетические процессы, происходящие при развитии двух самых частых вариантов ишемического инсульта — атеротром-ботического и кардиоэмболического инсульта с феноменом реперфузии [4, 5]. Несмотря на высокую популярность данной модели, до настоящего времени отсутствует цифровой атлас зон артериального кровоснабжения в высоком разрешении, который мог бы быть интегрирован в современные методы автоматической обработки данных лучевой визуализации. Существующие описания небольших серий магнитно-резонансных [6] и гистологических исследований, посвящённых этому вопросу [7, 8], не привели к созданию данного инструмента.
Внедрение систем искусственного интеллекта в трансляционные исследования ишемического инсульта [9–11] делает эту задачу ещё более актуальной. Обусловлено это прежде всего тем, что подобные системы, включая системы морфометрического анализа, сегментации очагов поражения вещества головного мозга с учётом анатомической привязки и другие, на определённом этапе функционирования требуют использования цифрового атласа, который служит основой для проведения анализа. Одним из преимуществ методов прижизненной визуализации мозга у экспериментальных животных является возможность сократить размер выборки и получить объективные данные об анатомии без необходимости их эвтаназии. Магнитно-резонансная томография (МРТ) как один из таких методов [12] позволяет накопить объём цифровых данных, необходимых для создания подобного атласа.
Цель исследования — создать цифровой атлас зон кровоснабжения интракраниальных ветвей внутренней сонной артерии в условиях экспериментальной окклюзии средней мозговой артерии.
МЕТОДЫ
Дизайн исследования
Данное исследование является одноцентровым экспериментальным ретроспективным (все данные, используемые в работе, были получены в рамках выполнения других экспериментальных работ).
Критерии соответствия
Критерии включения. В работу включены рет- роспективные данные магнитно-резонансных исследований головного мозга крыс с моделью острой фокальной ишемии и наличием в протоколе изотропных Т2-взвешенных изображений.
Критерии исключения. Критериями исключения при оценке архивных данных было отсутствие очага инфаркта мозга по данным МРТ и отсутствие необходимой импульсной последовательности в протоколе сканирования.
Условия проведения
Архивные данные МРТ экспериментальных животных были получены на крысах линии Вистар в Центре коллективного пользования «Медицинские нанобиотехнологии» ФГАОУ ВО «Российский национальный исследовательский медицинский университет имени Н.И. Пирогова» Минздрава России (РНИМУ им. Н.И. Пирогова). В рамках получения этих данных в предыдущих экспериментах животных содержали в стандартных условиях (12-часовой световой режим, 22±2°С, влажность 45–65%) по 4–5 особей в клетке до и по одной после моделирования ишемического инсульта при свободном доступе к воде и стандартному корму. Все оперативные вмешательства и МРТ проводили под общим ингаляционным наркозом, который обеспечивался системой анестезии животных (E-Z-7000 Classic System; E-Z-Anesthesia Systems). Для индукции наркоза применялся 3,5–4% изофлуран (Aerrane, Baxter HealthCare Corporation), для поддержания анестезии — 2–2,5% изофлу-ран. При моделировании экспериментального инфаркта мозга применялась смесь анестетика с атмосферным воздухом, а при проведении МРТ — с чистым кислородом. Во время всех оперативных вмешательств и при проведении МРТ поддерживалась температура тела животных 37°C. В конце срока наблюдения животных подвергали эвтаназии с использованием индукционной камеры (E-Z-7000 Classic System; E-Z Anesthesia Systems) и ингаляционного наркоза непосредственно перед транскардиальной перфузией животным вводили летальную дозу золетила. Все результаты экспериментов на животных изложены в соответствии рекомендациям ARRIVE.
Продолжительность исследования
Ретроспективный анализ архивных данных включал период работы научного коллектива с 2017 по 2024 год.
Описание исследования
Для создания атласа бассейна кровоснабжения интракраниальных ветвей внутренней сонной артерии использовали архивные данные МРТ экспериментальных животных с моделью временной окклюзии средней мозговой артерии монофиламентом.
Инфаркт мозга в рамках других научных исследований коллектива авторов моделировался путём транзиторной (90 минут) окклюзии правой средней мозговой артерии монофиламентом, заведённым через наружную сонную артерию во внутреннюю сонную артерию [13]. Монофиламент имеет силиконовый наконечник длиной 4 мм и диаметром 0,37 мм (монофиламент 4-0, Doccol Corporation), вследствие чего в зависимости от глубины его расположения возможна остановка кровообращения по артериям, расположенным рядом с отхождением средней мозговой артерии.
В качестве объективного контроля очага инфаркта мозга у всех животных выполняли МР-ис-следование на томографе для малых лабораторных животных ClinScan (Bruker BioSpin) с индукцией магнитного поля 7 Тл.
Статистический анализ
Для наиболее объективной сегментации очага инфаркта мозга применялся заранее обученный программный алгоритм с помощью системы искусственного интеллекта. Данная система создана на основе трансформера Swin-UNETR [14] как одной из самых современных архитектур нейронных сетей, демонстрирующей высокое качество при сегментации медицинских данных лучевых методов диагностики. Вся обработка данных производилась с использованием языка программирования Python [15]. Полученные данные сегментации инфаркта мозга приводились в одно координатное пространство путём использования пакета SimpleITK [16] и заранее подготовленного шаблона мозга крысы (регистрировались к шаблону). Затем все данные сегментации объединялись и анализировались с использованием программного пакета 3D Slicer [17].
РЕЗУЛЬТАТЫ
Объекты (участники) исследования
В работу включено 243 архивных исследования, в которых получены изотропные Т2-взвешенные изображения (с использованием импульсной последовательности трёхмерного быстрого спинового эха с изменяющимся углом возбуждения SPACE, размером вокселя 0,2 х 0,2 х 0,2 мм, временем повторения и временем эхо-сигнала 4000 и 251 мс соответственно).
Основные результаты исследования
Для создания атласа бассейнов кровоснабжения интракраниальных ветвей внутренней сонной артерии по данным МРТ использовалась система искусственного интеллекта, позволяющая достоверно сегментировать зону инфаркта мозга после окклюзии средней мозговой артерии (рис. 1). Полученные результаты сегментации экспериментального инфаркта мозга регистрировали в одно координатное пространство с использованием шаблона мозга крысы (рис. 2, a ). На основании полученных файлов сегментации, суммированных в одной координатной системе, были созданы тепловые карты частоты формирования очага инфаркта мозга (см. рис. 2, b ).
Поиск зон кровоснабжения основных интракраниальных ветвей внутренней сонной артерии (субкортикальной и кортикальной области средней
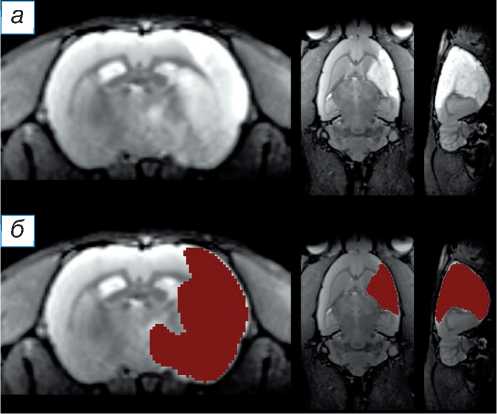
Рис. 1. Пример сегментации инфаркта мозга с использованием искусственного интеллекта: а — Т2-взвешенные изображения в аксиальной, фронтальной и сагиттальной плоскостях (слева направо), на которых в правом полушарии визуализируется гиперинтенсивный очаг инфаркта мозга; б — автоматическая сегментация очага инфаркта мозга (обозначена красным цветом).


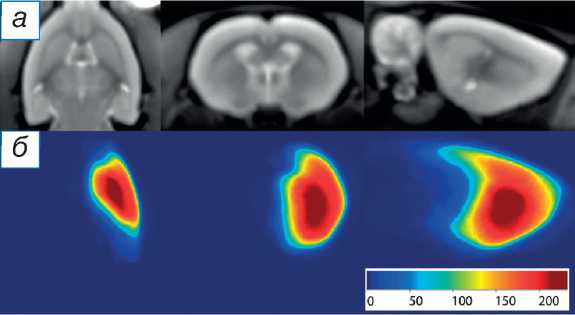
Рис. 2. Частота расположения очага инфаркта мозга у экспериментальных животных с моделью временной окклюзии правой средней мозговой артерии (получена путём суммирования всех очагов инфаркта мозга в одном координатном пространстве): а — шаблон интактного мозга, к которому производилась регистрация данных (приведён для ориентира); б — частота расположения очага инфаркта мозга: чем теплее цвет, тем чаще поражалась данная часть мозга (приведена цветовая шкала с указанием соответствия цвета и количества усреднённых значений).
мозговой артерии, передней ворсинчатой артерии и гипоталамических артерий) производился в несколько этапов. В соответствии с последовательностью отхождения артерий от внутренней сонной артерии филамент, установленный в её просвете, может вызывать окклюзию её различных ветвей (рис. 3, a). Зная последовательность отхождения артерий, можно выделить животных, у которых при глубоком положении филамента не наблюдается очага инфаркта в бассейне проксимальных ветвей внутренней сонной артерии, а также животных с недостаточно глубоким положением филамента, у которых в очаг инфаркта не вовлекаются дистальные ветви внутренней сонной артерии (см. рис. 3, a).
Первый этап создания атласа заключался в генерации тепловых карт частоты формирования очага в зависимости от объёма инфаркта мозга: 0–25 мм3, 0–50 мм3, 0–75 мм3, 0–100 мм3, 0–200 мм3, 0–300 мм3, 25–75 мм3, 50–150 мм3, 100–200 мм3, 200–300 мм3, 300–500 мм3, 200–500 мм3, 150 мм3 и более. Полученные тепловые карты визуально анализировали и с использованием метода Оцу; производилась первичная сегментация интересующих нас областей. На втором этапе производилась автоматическая фильтрация по включению и/или исключению в суммирующую тепловую карту исследований, где присутствовали и/или отсутствовали отобранные на первом этапе ре-
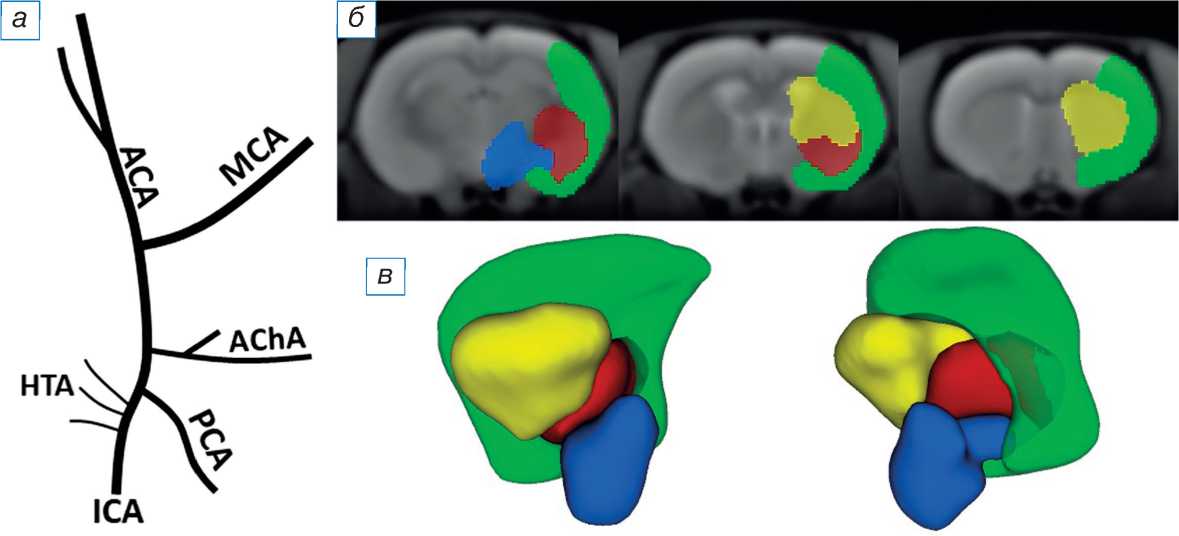
Рис. 3. Схема отхождения интракраниальных ветвей внутренней сонной артерии и созданный атлас зон их кровоснабжения: а — схема отхождения интракраниальных ветвей внутренней сонной артерии (схема создана на основании данных Z. He и соавт. [7]); б — последовательные срезы в аксиальной плоскости с расположением на них зон кровоснабжения (зелёным цветом обозначен бассейн корковых ветвей средней мозговой артерии, жёлтым — бассейн средней мозговой артерии, питающий субкортикальную область, красным — бассейн передней ворсинчатой артерии, синим — бассейн гипоталамических артерий); в — трёхмерная реконструкция атласа зон кровоснабжения интракраниальных ветвей внутренней сонной артерии (обозначения цветом аналогичны пункту « б »). ICA — внутренняя сонная артерия; PCA — задняя мозговая артерия; MCA — средняя мозговая артерия; AChA — передняя ворсинчатая артерия; HTA — гипоталамические артерии.
ференсные точки в области очага инфаркта мозга: всего было отобрано пять таких комбинаций. Полученные тепловые карты анализировались в дополнение к полученным на первом этапе, и производилась их разметка с перекрытием областей кровоснабжения выбранных ветвей внутренней сонной артерии. На заключительном этапе выполнялось сглаживание контуров с поиском оптимальных границ между бассейнами кровоснабжения для нивелирования областей перекрытия.
Полученный атлас зон кровоснабжения основных интракраниальных ветвей внутренней сонной артерии представлен на рис. 3 ( б ), его трёхмерная реконструкция — на рис. 3 ( в ).
ОБСУЖДЕНИЕ
Созданный нами цифровой атлас зон кровоснабжения основных интракраниальных ветвей внутренней сонной артерии может быть использован для объективной и количественной оценки частоты формирования различных типов инфаркта мозга (полушарный, подкорковый, с поражением гипоталамуса) на модели транзиторной окклюзии средней мозговой артерии. На основании этих данных возможно осуществить подборку параметров филамента (длину силиконового наконечника, его диаметр), а также прогнозировать возможные осложнения, например гипертермию при поражении гипоталамуса [18]. Достоинством данной работы является то, что впервые создан атлас кровоснабжения на большом (более 200 исследований) объёме данных, полученных неинвазивным способом с высоким пространственным разрешением у крыс (использовался изотропный воксель 0,2 х 0,2 х 0,2 мм). В большинстве существующих работ для оценки зон кровоснабжения применялась либо ex vivo гистологическая окраска мозга на ишемию [7, 8], либо МРТ с анизотропными срезами на малой выборке данных, без создания атласа кровоснабжения [6]. Существуют также подробные атласы по зонам кровоснабжения у мышей [19, 20], созданные на единичных экспериментальных животных, вследствие чего слабо отражающие вариативность их расположения.
Следует отметить, что предложенный подход к созданию атласа зон артериального кровоснабжения, основанный на анализе экспериментальных данных, представленных в данной работе, обладает потенциалом для адаптации и применения в клинической практике. За период реализации сосудистой программы в Российской Федерации накоплен значительный объём данных нейровизуализации пациентов с ишемическим инсультом. Их ретроспективный анализ с учётом демографических и клинических характеристик на основании разработанной нами методологии может способствовать получению новых фундаментальных знаний в области сосудистой неврологии.
Ограничения исследования
Основным недостатком данной работы является создание атласа только для зон кровоснабжения интракраниальных ветвей внутренней сонной артерии справа. Однако модель транзиторной окклюзии средней мозговой артерии монофиламентом является золотым стандартом и самой распространённой моделью в трансляционных доклинических исследованиях ишемического инсульта как наиболее близкой по патофизиологии [21–23]. Ограничение по стороне оценки может быть также нивелировано на этапе регистрации данных путём их отражения. Возможным недостатком является и применение специализированного протокола (изотропные Т2-взвешенные изображения с помощью импульсной последовательности трёхмерного быстрого спинового эха с изменяющимся углом возбуждения) на этапе создания атласа, однако сам атлас может быть использован вне контекста работы с искусственным интеллектом, и его регистрация возможна на любые Т2-взвешенные изображения, в том числе анизотропные.
ЗАКЛЮЧЕНИЕ
Впервые на основании выборки более чем 200 прижизненных МР-исследований с высоким разрешением создан цифровой атлас зон кровоснабжения основных интракраниальных ветвей внутренней сонной артерии. Данный атлас применим в рамках трансляционных исследований на наиболее релевантной экспериментальной модели ишемического инсульта — транзиторной окклюзии средней мозговой артерии монофиламентом. Разработанная нами методология применима для высокопроизводительного ретроспективного анализа данных нейровизуализации пациентов с ишемическим инсультом, полученных в рамках реализации сосудистой программы в Российской Федерации.

kV ГА
ДОПОЛНИТЕЛЬНАЯ ИНФОРМАЦИЯ
Вклад авторов. И.Л. Губский , Д.Д. Наместни-кова , Э.А. Черкашова , И.С. Гумин — подготовка и анализ данных, написание программного кода, написание текста статьи; И.Л. Губский , Л.В. Губ-ский , В.П. Баклаушев , В.П. Чехонин , К.Н. Ярыгин — разработка концепции, предоставление ресурсов, редактирование рукописи. Авторы подтверждают соответствие своего авторства международным критериям ICMJE (все авторы внесли существенный вклад в разработку концепции, проведение исследования и подготовку статьи, прочли и одобрили финальную версию перед публикацией).
Этическая экспертиза. Данная работа выполнена на архивном наборе данных, получение которых в рамках выполнения научной работы коллектива авторов одобрено этическим комитетом РНИМУ им. Н.И. Пирогова (протокол № 22/2023 от 15.12.2023), и в соответствии с Директивой 2010/63/EU Европейского парламента и Совета ЕС по защите животных, используемых в научных целях.
Источник финансирования. Работа выполнена при поддержке Российского научного фонда (грант РНФ № 23-25-00300). Часть работы по анализу данных тепловых карт выполнена на оборудовании и при финансовой поддержке ФМБА России.


