Экспрессия CD68+, BCL-2+, KI-67+ в сторожевых, нативных и постнатально индуцированных лимфатических узлах
Автор: Рустамханов Расул Айдарович, Зайратьянц Олег Вадимович, Ганцев Шамиль Ханяфиевич
Журнал: Морфологические ведомости @morpholetter
Рубрика: Оригинальные исследования
Статья в выпуске: 2 т.25, 2017 года.
Бесплатный доступ
В работе исследованы иммуногистохимические особенности постнатально индуцированных лимфатических узлов в сравнении со сторожевыми и нативными лимфатическими узлами в эксперименте. Для постнатального формирования лимфатических узлов проведен эксперимент на 25 белых крысах-самцах линии Wistar. Первой группе животных (15 крыс) произведена перевивка саркомы М1, вторая группа состояла из интактных животных (10 крыс). В эксперименте на модели перевиваемой саркомы М1 показана возможность воспроизведения постнатальной индукции неолимфогенеза при опухолевом росте. Исследование продемонстрировало высокий уровень антигенной стимуляции Т- и В-лимфоцитов в постнатально индуцированных лимфоузлах и показало возможную роль клеток макрофагального ряда в стимуляции неолимфогенеза и образованных лимфоузлов.
Постнатально индуцированный лимфоузел, саркома м-1, неолимфогенез, всl-2
Короткий адрес: https://sciup.org/143177173
IDR: 143177173 | DOI: 10.20340/mv-mn.17(25).02.06
Expression of CD68+, BCL-2+, KI-67+ in sentinel, native and postnatal induced lymph nodes
Immunohistochemically features of postnatal induced lymph nodes in comparison with sentinel and native lymph nodes in the experiment were studied. For the postnatal formation of lymph nodes, an experiment was performed on 25 white male rats of the Wistar line. The first group of animals (15 rats) was treated with sarcoma M1, the second group consisted of intact animals (10 rats). In the experiment, the possibility of reproducing postnatal induction of neolymphogenesis in tumor growth was demonstrated in the model of sarcoma M1. The study demonstrated a high level of antigen stimulation of T and B lymphocytes in postnatal induced lymph nodes and showed the possible role of macrophage cells in stimulating neolymphogenesis and the formation of new lymph nodes.
Текст научной статьи Экспрессия CD68+, BCL-2+, KI-67+ в сторожевых, нативных и постнатально индуцированных лимфатических узлах
Рустамханов Р.А., Зайратьянц О.В., Ганцев Ш.Х. Экспрессия CD68+, BcL-2+, Ki-67+ в сторожевых, нативных и постнатально индуцированных лимфатических узлах// Морфологические ведомости.- 2017.- Том 25.- № 2.- С. 37-42. (25).02.06
Rustamkhanov RA, Zayrat’yants OV, Gantsev ShKh. Expression of CD68+, BСL-2+, KI-67+ in sentinel, native and postnatal induced lymph nodes. Morfologicheskie Vedomosti – Morphological Newsletter. 2017 Jun 30;25(2):37-42. (25).02.06
Введение. Исследования последних лет в области клинической онколимфологии позволили обнаружить ранее не описанный феномен постнатального неолимфогенеза при онкологических заболеваниях [1-2]. Этот феномен характеризуется появлением новых лимфатических узлов, имеющих некоторые анатомические особенности, которые позволяют отличить их от нативных по числу приносящих и отводящих лимфатических сосудов, структуре капсулы и «привязанности» к сторожевому лимфатическому узлу. Ранее проведенные исследования при раке молочной железы с метастазами в подмышечный лимфатический регион установили, что центром перераспределения потоков лимфы является сторожевой лимфатический узел. Функционирование этой анатомической структуры определяет движение лимфы и масштабы лимфогенного метастазирования [2-3]. Предполагается, что появление новых лимфатических узлов при злокачественных опухолях можно рассматривать с позиций сложных механизмов взаимодействия иммунной системы с опухолью. В постнатально индуцированных лимфатических узлах (далее - ПНИЛУ) у онкологических больных содержатся различные вещества, которые обладают высокой биологической активностью [1, 3]. Макрофаги играют важную роль в реакциях иммунной системы на процессы онкогенеза, представляют собой центральное звено врождённого иммунного ответа, и именно их реакция на патоген детерминирует развитие адаптивного иммунитета. Макрофаг является основным клеточным трансдуктором биологического сигнала как для патогенных микроорганизмов, так и для опухолевых клеток на иммунную систему организма [4-5]. Можно предположить важную роль макрофагов в процессах неолимфогенеза. Для объективной визуализации макрофагов и ряда других клеток системы мононуклеарных фагоцитов в тканях используется иммуногистохимическое выявление экспрессии их мембранного маркера - белка СD68 [6]. Выявляемый иммуногистохимически белок-ингибитор апоптоза Bcl-2 в лимфатических узлах обнаруживается в цитоплазме лимфоцитов лимфоидных узелков кортикальной зоны (в малых В-лимфоцитах мантии, лимфоцитах и лимфобластах зародышевых центров), а также в единичных Т-лимфоцитах паракортикальной Т-зависимой зоны. Этот белок осуществляет защиту клеток от эндогенных и экзогенных воздействий, индуцирующих апоптоз [7-8]. Для оценки пролиферативной активности различных клеток используется иммуногистохимический метод с выявлением экспрессии белка Ki-67. Экспрессия Кi-67 – негистонового ядерного белка, позволяет выделить пролиферирующие клетки, находящиеся в поздней G1, S, M и G2 фазах клеточного цикла, кроме G0 и ранней G1 фаз, поскольку в течение 60–90 минут после митоза этот белок разрушается [9].
Цель работы - изучить иммуногистохимические особенности ПНИЛУ в сравнении со сторожевыми и нативными лимфатическими узлами в эксперименте.
Материалы и методы исследования . Исследование проводили на белых крысах-самцах альбиносах линии Wistar, вес животных варьировал в пределах 120-180 грамм. Животные были разделены на две группы. Первая группа (экспериментальная) включала 15 крыс, которым перевивался опухолевый штамм саркомы М1 в мягкие ткани правой боковой области живота; вторая группа (контрольная) состояла из 10 интактных крыс. Все манипуляции на лабораторных животных проводили согласно международным и отечественным этическим и научным стандартам планирования и выполнения исследований на животных (приказ МЗ и СР РФ от 23.08.2010 г. № 708н «Правила лабораторной практики», приложения к приказу Минздрава СССР от 12.08.1977 г. № 755 и приказу Минсельхоза РФ от 05.11.2008 г. № 490 «Об утверждении правил проведения лабораторных исследований в области ветеринарии»; Европейская конвенция по защите позвоночных животных, используемых для экспериментальных и других научных целей, ЕЭС, Страсбург, 1985; требования Хельсинкской декларации и Всемирной медицинской ассоциации, 2000; рекомендации, содержащиеся в Директивах Европейского сообщества, 86/609 ЕС). Объектом исследования явились новообразованные лимфатические узлы аксиллярной области, индуцированные опухолевым ростом перевивной саркомы М1 с лимфогенными метастазами в регионарные лимфатические узлы. Для сравнительного анализа изучали сторожевые с метастазами опухоли (далее - СЛУ) животных основной группы и нативные лимфоузлы (далее - НЛУ) аксиллярной области у интактных крыс контрольной группы. Лимфатические узлы фиксировали в 10% растворе нейтрального формалина, обрабатывали по стандартной гистологической методике и заливали в парафин. Гистологические срезы окрашивали гематоксилином и эозином. Для иммуногистохимического исследования парафиновые гистологические срезы изготовленные на микротоме LEICA RM 2145 (Германия) толщиной 4 мкм, окрашивали с помощью иммуногистостейнера Leica Microsystems Bond™ (Германия) согласно протоколам фирм-изготовителей антител. В качестве первичных моноклональных антител применяли следующую панель: Вcl2 в разведении 1:200 (клон N-19, Santa Cruz Biotechnology, США); CD68 в разведении 1:300 (клон ED 1, Santa Cruz Biotechnology, США); Ki-67 в разведении 1:75 (клон Mib 5, Daco, Дания). Для окрашивания использовали непрямую стрептавидин-биотиновую систему детекции Leica BOND (Novocastra™, Германия). Оценку специфичности реакции проводили при окрашивании срезов без первичных антител. Полученные препараты исследовали с использованием микроскопа Leica DM 2500 (Германия) со специализированным программным обеспечением управления настройками и захвата изображения. Для оценки результатов иммуногистохимической реакции проводили подсчет индексов экспрессии CD68, Bcl-2 и Ki-67 в процентах на 1000 клеток (или их ядер для Ki-67) в 10 случайным образом отобранных полях зрения (увеличение микроскопа х400). Учитывали умеренное и выраженное иммуногистохимическое окрашивание.
Полученные данные подвергали статистическому анализу. В зависимости от характера распределения выборок (групп) использовали как параметрические, так и непараметрические методы статистической обработки. Для выборок, которые не отличались по распределению от нормального, и имели положительные тесты на равенство дисперсий применяли параметрические методы. В отдельных случаях после параметрических расчетов анализ проверялся ранговыми методами для исключения возможных ошибок. Применяли однофакторный дисперсионный анализ с расчетом критерия Фишера (F) и уровня его статистической значимости. Множественное сравнение средних проводили при помощи одного из самых жестких тестов – теста Тьюки для равных и неравных выборок. В случае отсутствия условий для использования параметрических тестов применяли непараметрические (ранговые) тесты. При наличии большего числа групп оценку проводили с помощью рангового дисперсионного анализа Краскела-Уоллиса. При множественном сравнении средних рангов учитывали поправку Бонферрони (0,05/n, n - число групп). Критический уровень статистической значимости при сравнении 2-х групп принимали за 0,05.
Результаты исследования и обсуждение. Лимфоидная ткань СЛУ была в разной степени вытеснена метастазами опухоли. Исследовали сохранные участки лимфоидной ткани с неизмененной структурой их строения. СD68+клетки (макрофаги и гистиоциты) определялись преимущественно в краевом и промежуточных синусах, а также в кортикальной межузелковой и паракортикальной зонах (рис. 1-а). Исследование экспрессии ингибитора апоптоза Всl-2 показало, что она была выражена в клетках (В-лимфоцитах) герминативных центров лимфоидных узелков и отдельных клетках (Т-лимфоцитах, макрофагах) паракортикальной зоны и локализованных в краевом и промежуточном синусах. Такая картина характерна для узелковой гиперплазии лимфатического узла (рис. 1-б). Экспрессия маркера пролиферации Кi-67 была выражена в ядрах клеток (В-лимфоцитов) герминативных центров лимфоидных узелков (до 90% клеток). Она была высокой в лимфоцитах и макрофагах синусов (до 20-30%) и отмечалась также в единичных клетках (лимфоцитах, макрофагах) других структур лимфатического узла. Однако в паракортикальной зоне встречались очаги высокой пролиферативной активности Т-лимфоцитов, в которых интенсивность составляла 50-60% (рис. 1-в).
Исследование НЛУ контрольной группы показало, что CD68+клетки (макрофаги и гистиоциты) локализовались преимущественно в краевом и промежуточных синусах (рис. 2-а). Исследование экспрессии ингибитора апоптоза Всl-2 показало, что она была более выражена в клетках (В-лимфоцитах) герминативных центров лимфоидных узелков и отдельных клетках (Т-лимфоцитах, макрофагах) паракортикальной зоны, а также краевого и промежуточного синусов (рис. 2-б). Экспрессия маркера пролиферации Кi-67 преобладала в ядрах клеток (В-лимфоцитов) герминативных центров лимфоидных узелков (до 90% клеток), лимфоцитах и макрофагах синусов (до 20-30%) и определялась лишь в единичных клетках (лимфоцитах, макрофагах) других структур лимфатического узла. Распределение клеток, экспрессирующих этот маркер, указывает на нормальную функциональную активность лимфатического узла (рис. 2-в) [4].
Исследование экспрессии маркера CD68 в ПНИЛУ позволило выявить большое количество макрофагов и гистиоцитов в просвете синусов. Местами они определялись в лимфоидных узелках и в паракортикальной зоне (рис 3-а). Экспрессия ингибитора апоптоза белка Всl-2 выявлялась в цитоплазме лимфоцитов герминативных центров лимфоидных узелков, единичных макрофагах и лимфоцитах, расположенных в синусах и вокруг лимфатических узелков (рис. 3-б).
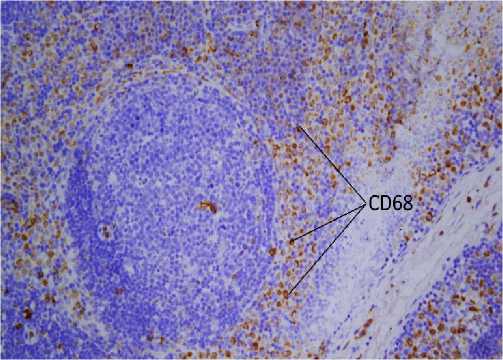
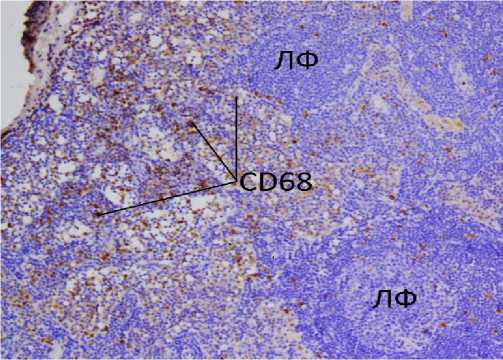
Рис. 1-а. Сторожевой лимфатический узел. CD68+ макрофаги и гистиоциты в краевом и промежуточных синусах, кортикальной межузелковой и паракортикальной зонах. Непрямой иммунопероксидазный метод. Ув.: х200.
Рис. 2-а. Нативный лимфатический узел. CD68+ макрофаги и гистиоциты в краевом и промежуточных синусах; ЛФ – лимфоидные узелки. Непрямой иммунопероксидазный метод Ув.200.
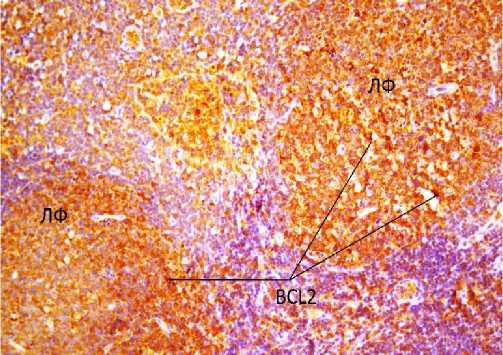
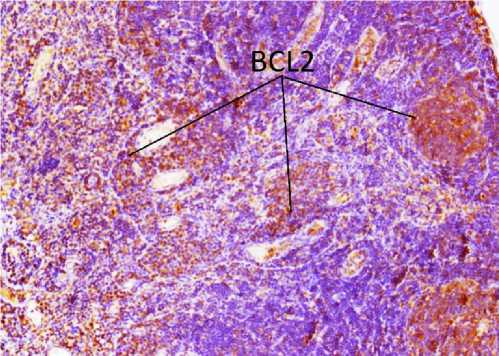
Рис. 1-б. Сторожевой лимфатический узел. Экспрессия Вс1- 2 в В-лимфоцитах герминативных центров лимфоидных узелков, Т-лимфоцитах и макрофагах паракортикальной зоны, краевого и промежуточного синусов. Непрямой иммунопероксидазный метод. Ув.: х200.
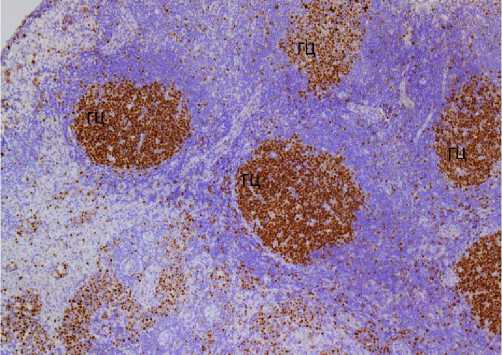
Рис. 2-б . Нативный лимфатический узел. Экспрессия Вс1-2 в В-лимфоцитах герминативных центров лимфоидных узелков и отдельных Т-лимфоцитах и макрофагах паракортикальной зоны, краевого и промежуточного синусов. Непрямой иммунопероксидазный метод. Ув.: х200.
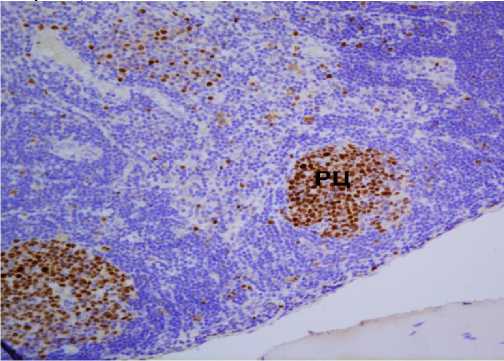
Рис. 1-в. Сторожевой лимфатический узел. Экспрессия Кi-67 в ядрах В-лимфоцитов герминативных центров лимфоидных узелков и в лимфоцитах, макрофагах и других структурах. Непрямой иммунопероксидазный метод. Ув.: х200.
Рис. 2-в . Экспрессия Кi-67 в ядрах (В-лимфоцитов герминативных центров лимфоидных узелков (РЦ), лимфоцитах, макрофагах и других структурах. Непрямой иммунопероксидазный метод. Ув.: х250.
Таблица 1
Показатели индекса экспрессии CD68 в сторожевых, нативных и постнатально индуцированных лимфоузлах
|
№№ |
Структурно- функциональные зоны лимфоузлов |
n |
СЛУ |
НЛУ |
ПНИЛУ |
|
1 |
Краевые синусы |
10 |
17,7±4,0* 0,000128 ᴾ 0,000127 ᶰ |
6,1±2,6* 0,387462 ᴾ 0,000127 ˢ |
8,1±3,3* 0,387462 ᶰ 0,000128 ˢ |
|
2 |
Промежуточные синусы |
10 |
23,0(20,0-28,0)** 1,000000 ᴾ 0,001076 ᶰ |
10,0(8,010,0)** 0,000180 ᴾ 0,001076 ˢ |
25,0(20,0-30,0)** 0,000180 ᶰ 1,000000 ˢ |
|
3 |
Лимфатические узелки |
10 |
28,5(12,0-35,0)** 0,000021 ᶰ 0,006084 ᴾ |
0,0 (0,0-0,0)** 0,475884 ᴾ 0,000021 ˢ |
1,0 (1,0-2,0)** 0,475884 ᶰ 0,006084 ˢ |
|
4 |
Паракортикальная зона |
10 |
19,2±7,0* 0,175656 ᴾ 0,000130 ᶰ |
3,8±1,3* 0,000855 ᴾ 0,000130 ˢ |
14,5±6,9* 0,000855 ᶰ 0,175656 ˢ |
Список литературы Экспрессия CD68+, BCL-2+, KI-67+ в сторожевых, нативных и постнатально индуцированных лимфатических узлах
- Ганцев Ш.Х. Новые технологии диагностики и лечения рака молочной железы// Креативная хирургия и онкология. -2009.-№ 1.- С. 6-9.
- Ганцев Ш.Х. Аксиллярный лимфатический аппарат при раке молочной железы: Атлас.- М.: МИА, 2011.- 194 с.
- Gantsev ShKh, Umezawa K, Islamgulov DV et al. The role of inflammatory chemokines in lymphoid neoorganogenesis in breast cancer. Biomed. Pharmacother. 2013;67(5):363-366.
- Бородин Ю.И. Лимфатическая система и старение// Фундаментальные исследования.- 2011.- № 5.- С. 11-15.
- Martin TR, Frevert CW. Innate Immunity in the Lungs. Proc. Am. Thor. Soc. 2005;2:403-411.
- Holness CL, Simmons DL. Molecular cloning of CD68, a human macrophage marker related to lysosomal glycoproteins. Blood. 1993;81(6):1607-1613.
- Белкин А.Д. Содержание белков регуляторов апоптоза bcl-2 и bad в регионарных лимфатических узлах печени при воздействии магнитного поля 50 гц//Гигиена и санитария.- 2015.- № 1.- С. 112-114.
- Белушкина Н.Н., Северин С.Е. Молекулярные основы патологии апоптоза// Архив патологии.- 2001.- Том 63.- № 1.- С. 51-60.
- Scholzen T, Gerdes J. The Ki-67 protein: from the known and the unknown. J. Cell. Physiol. 2000;182:311-322.


