Экстирпация пищевода при кардиоспазме IV стадии и его рецидиве после открытой и эндоскопической кардиомиотомии
Автор: Ручкин Д.В., Ян Цинь, Раевская М.Б., Бурякина С.А., Сизов В.А., Субботин В.В.
Журнал: Московский хирургический журнал @mossj
Рубрика: Клинические исследования
Статья в выпуске: 3 (37), 2014 года.
Бесплатный доступ
Широкое применение в клинической практике лапароскопической кардиомиотомии с различными модификациями полной или неполной фундопликации, часто выполняемой в качестве первичного и единственного способа лечения без учета стадии болезни, неизбежно приводит к появлению пациентов с рецидивом дисфагии, развитием пептического рефлюкс-эзофагита и прогрессированием заболевании. Трансхиатальная экстирпация пищевода с одномоментной заднемедиастинальной эзофагопластикой изоперистальтической желудочной трубкой и пищеводным анастомозом на шее является операцией выбора у больных с IV стадией кардиоспазма (ахалазии кардии). Целесообразность выполнения повторной операции на кардии после неудачного первичного вмешательства весьма сомнительна.
Кардиоспазм, кардиомиотомия, рецидив дисфагии, экстирпация пищевода
Короткий адрес: https://sciup.org/142211162
IDR: 142211162 | УДК: 616.3;
Текст научной статьи Экстирпация пищевода при кардиоспазме IV стадии и его рецидиве после открытой и эндоскопической кардиомиотомии
Несмотря на известное многообразие способов диагностики нервно-мышечных заболеваний пищевода, у ряда больных (28–40%) кардиоспазм выявляют только в IV стадии [1]. Кроме того, широкое применение в клинической практике лапароскопической кардиомиотомии с различными модификациями полной или неполной фундопликации, часто выполняемой в качестве первичного и единственного способа лечения без учета стадии болезни, неизбежно приводит к появлению пациентов с рецидивом дисфагии, развитием пептического рефлюкс-эзофагита и прогрессированием заболевании.
Материал и методы
В период с апреля 2011 по март 2013 гг. оперированы 9 больных: 8 мужчин и 1 женщина. Возраст пациентов находился в интервале от 23 до 63 лет, составив в среднем 37,8 лет. Средняя длительность анамнеза составила 13,7 лет (от 3 до 36 лет). У 4 пациентов кардиоспазм IV стадии был выявлен впервые, у 1 пациента ахалазия кардии III стадии диагности- рована уже в сочетании с множественными эпифренальны-ми дивертикулами пищевода. В клинической практике мы используем 4-х стадийную классификацию Б.В. Петровского 1963 года (Петровский Б.В., 1962, 1957). Мы считаем, что термин кардиоспазм и ахалазия кардии одинаково применимы к IV стадии заболевания и не требуют дополнительного объяснения в рамках данной статьи.
С рецидивом дисфагии после предшествующей кардиомиотомии госпитализированы 4 больных, которым в других стационарах ранее была выполнена лапароскопическая кардиомиотомия с антирефлюксной манжеткой по Ниссену, Тупе или Дору. Рецидив дисфагии наступил в сроки от 2 недель до 1 года, после чего у 2 больных попыток баллонной дилатации кардии больше не предпринималось. Двое других пациентов еще до поступления в ин-т Вишневского были оперированы повторно: одному выполнили робот-ассистированную, а другому – открытую рекардиомиотомию с неполной рефундопликацией. В обоих наблюдениях наступил быстрый рецидив дисфагии – через 1 и 6 мес. со- ответственно. Запоздалая попытка баллонной дилатации кардии у этих больных эффекта уже не имела.
По данным традиционных рентгенологического и эндоскопического исследований у 8 больных, в т.ч. и у 4 ранее оперированных, диагностирована IV стадия заболевания и выставлены показания к экстирпации пищевода. У 1 больного с пятью псевдодивертикулами пищевода и III стадией ахалазии кардии показаниями к удалению пищевода послужили не только множественные дефекты мышечной оболочки, но и высокий риск перфорации дивертикулов при проведении баллонного дилататора.
С целью более качественной оценки зоны пищеводножелудочного перехода и исключения патологических изменений органов брюшной полости, способных повлиять на план оперативного вмешательства, 6 больным выполнили МСКТ исследование шеи, грудной и брюшной полостей с болюсным контрастным усилением. МСКТ проведена на мультидетекторных компьютерных томографах Philips Brilliance CT-64, iCT-256 (Philips Medical Systems (Cleveland)). Постпроцессинговую обработку осуществляли с использованием программного обеспечения Brilliance Portal (Philips Medical Systems (Cleveland)). Изображения оценивали во все фазы исследования. Последующая обработка данных включала обязательное построение мультипланарных реконструкций, что улучшало визуализацию пищевода до операции и наглядно представляло зону патологических изменений.
Важно отметить необходимость тщательного промывания пищевода перед любым из инструментальных исследований для улучшения визуализации. Процедура может быть выполнена как самостоятельно пациентом, так и лечащим врачом и состоит в зондовом промывании пищевода до чистой воды.
После предоперационной подготовки всем 9 пациентам выполнили плановую трансхиатальную экстирпацию грудного отдела пищевода с одномоментной субтотальной заднемедиастинальной эзофагопластикой изоперистальти-ческой желудочной трубкой. Во всех наблюдениях концевое пищеводное соустье сформировали на шее.
Трансхиатальный доступ имеет ряд преимуществ: он малотравматичен, позволяет избежать торакотомии и однолегочной вентиляции, снизить частоту легочных осложнений, уменьшить послеоперационный болевой синдром, раньше активизировать больного. Кроме того, использование трансхиатального доступа предполагает формирование внеполостного анастомоза на шее, несостоятельность которого не фатальна и протекает как местный воспалительный процесс (рис. 1). Этот доступ требует опыта, чтобы избежать повреждения дуги непарной вены, мембранозной части трахеи и главных бронхов. Мануальная мобилизация пищевода в заднем средостении сопровождается аритмией, снижением сердечного выброса и гипотонией. Тщательный
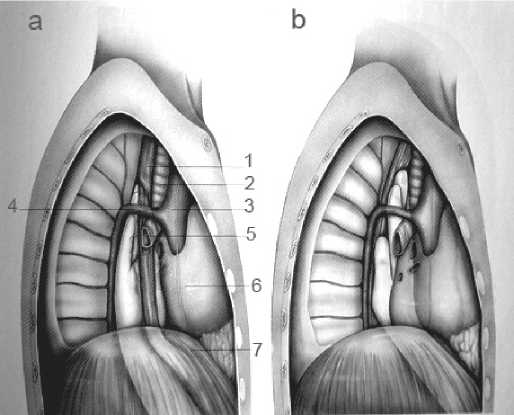
Рис. 1. Трансхиатальная мобилизация грудного отдела пищевода гемостаз средостения обеспечивается тампонированием большими салфетками.
После мобилизации пищевода формируют изопери-стальтический желудочный трансплантат. Желудок сначала мобилизуют по большой кривизне с пересечением всех сальниковых ветвей a. gastroepiploica dextra с сохранением пери-гастральной аркады. Для сохранения непрерывной перига-стральной аркады требуется пересечение a. gastroepiploica sinistra ниже ее развилки (т.е. с сохранением ассоциативной ветви двух бассейнов желудочно-сальниковых артерий). Затем мобилизуют малую кривизну с иссечением ствола правой желудочной артерии на протяжении 5–6 желудочных ветвей. Желудок отсекают от пищевода при помощи сшивающего аппарата. Питающую ножку трансплантата образуют правые желудочно-сальниковые сосуды ( а. et v. gastroduodenalis ). При помощи линейных стейплеров формируют изоперистальтическую желудочную трубку шириной до 4,0 см. Механический шов укрывают непрерывным серозно-мышечным швом (рис. 2).
Левый косой шейный доступ, разрез кожи по внутреннему краю m. sternocleidomastoideus , последовательно вскрывают платизму, поверхностный и глубокий листки собственной фасции. Затем пересекают m. оmohyoideus , лигируют a. thyroidea inferior . Доходят до предпозвоночной фасции, где мобилизуют заднюю стенку пищевода. Переднюю стенку пищевода обнажают, отделяя ее острым путем от мембранозной части трахеи, избегая повреждения возвратных нервов.
Через шейный разрез извлекают полностью мобилизованный пищевод, а следом за ним через заднее средостение проводят желудочный трансплантат. Непрерывность пищеварительного тракта восстанавливают двухрядным эзофа-гогастроанастомозом «конец в конец» (рис. 3).
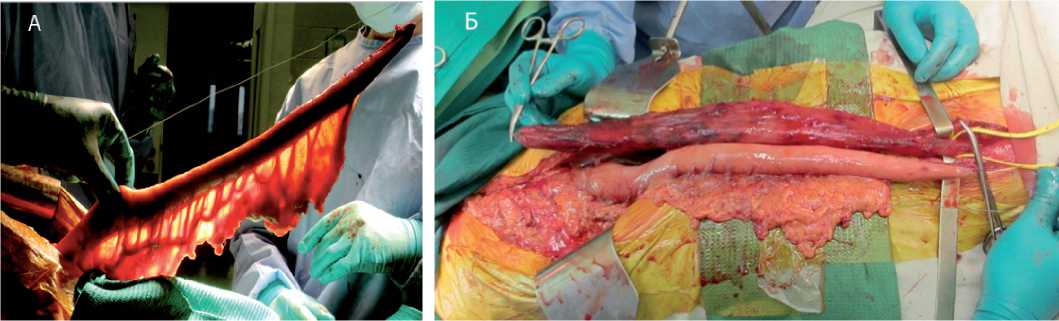
Рис. 2. а) законченный вид трансплантата. При транслюминации видна длинная непрерывная сосудистая аркада (стрелкой указан переток между правой и левой желудочно-сальниковыми артериями); б) перед пластикой
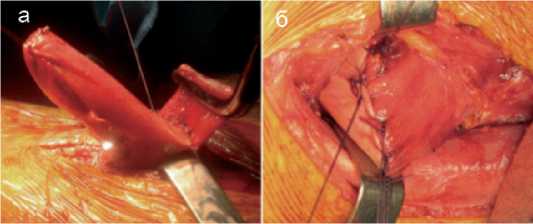
Рис. 3. Пищеводно-желудочный соустье: а) трансплантат проводят через заднее средостение на шею, формирование двухрядного шейного соустья отдельными узловыми швами; б) законченный вид анастомоза
Приводим клиническое наблюдение больного с впервые выявленным кардиоспазмом 4 стадии.
Больной Ж., 29 лет. Госпитализирован в ин-т Вишневского с жалобами на затрудненное глотание, дискомфорт в эпигастральной области, срыгивание съеденной пищи, ночной кашель. Анамнез заболевания: болен в течение 7 лет, когда появилась и прогрессировала дисфагия. Обследован амбулаторно по месту жительства – установлен диагноз ахалазия кардии. Специального лечения не получал. В марте 2013 г. при контрастной рентгенографии диагностирована 4 ст. заболевания.
При рентгенографии в ин-те Вишневского: пищевод расширен до 8 см, S-образно изогнут. В его просвете большое количество остатков пищи и слизи. Эвакуация контраста в желудок отсутствует. При КТ: кардия сомкнута, расширенный пищевод смещает и сдавливает чревный ствол – стеноз до 70% (рис. 4, 5). Другие возможные причины дисфагии (опухоль кардиоэзофагеального перехода, пептическая стриктура и др.) исключены.
15.05.13. Плановая операция: трансхиатальная экстирпация пищевода с одномоментной пластикой изопе-
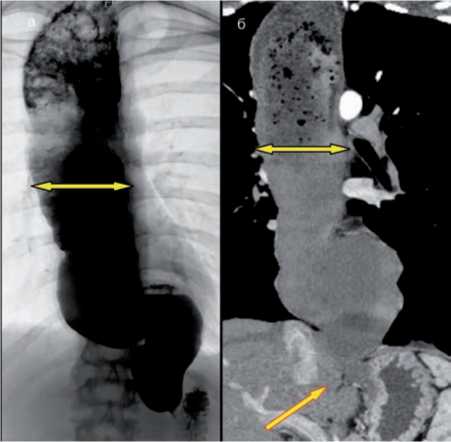
Рис. 4. а) рентгенологическое исследование пищевода с барием; б) МСКТ-мультипланарная реконструкция пищевода, кардия плотно сомкнута
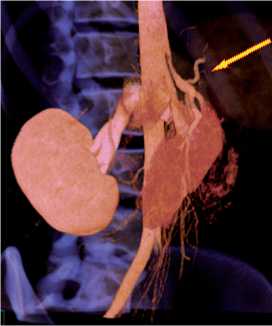
Рис. 5. МСКТ ангиография с 3D-реконструкция, расширенный пищевод смещает и ком-премирует чревный ствол со стенозом до 70%
ристальтической желудочной трубкой. После трансхиатальной мобилизации и выпрямления пищевода видна его избыточная длина (рис. 6). Удаленный пищевода представляет собой атоничный мешок с наличием язвы в нижней его трети вследствие застойного эзофагита (рис. 7).
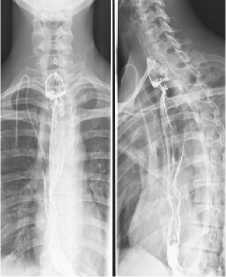
На 5 сутки после операции при контрольной рентгенографии пищевода подтверждена состоятельность и свободная проходимость эзофагогастроанастомоза (рис. 8). Пациенту разрешено пить. На 7 сутки назначен стол №1, и пациент выписан из стационара.
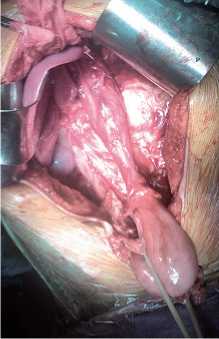
Рис. 6. После мобилизации пищевода видна избыточная его длина
Поздняя диагностика ахалазии кардии IV стадии может привести к развитию тяжелых аспирационных осложнений. Приводим еще одно клиническое наблюдение.
Больной: Р., 23 лет. Госпитализирован в ин-т Вишневского с жалобами на затрудненное глотание твердой и жидкой пищи, ежедневное срыгивание пищи, ночной кашель, необходимость запивать пищу большим количеством воды. Затрудненное глотание отмечал на протяжении последних 5 лет, постепенно росло количество выпиваемой
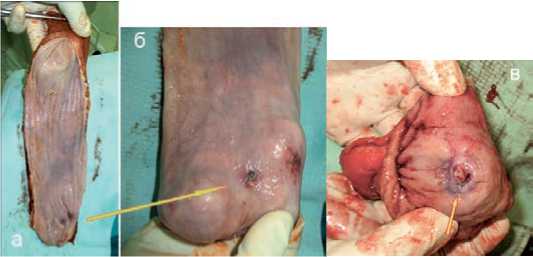
Рис. 8. На 5-е сутки эзофагогастроа-настомоз состоятелен, свободно проходим
Рис. 7. Макропрепарат: а) атоничный и дилатированный пищевод; б) язвы в нижней его трети вследствие застойного эзофагита; в) плотно сомкнутая кардия
во время еды жидкости. Специального лечения не получал. В августе 2011 г. развилась правосторонняя пневмония. Диагноз кардиоспазма IV стадии поставлен в декабре 2011 г. при амбулаторной R-графии пищевода в ин-те Вишневского. Тогда больной от госпитализации отказался, а поступил в стационар только через 3 мес. со значительным ухудшением состояния – нарастанием дисфагии, усилением кашля, удушья.
При рентгенографии определяется значительное расширение пищевода до 8 см с большим количеством содержимого в просвете. Дагностирована хроническая аспирационная правосторонняя пневмония с обтурацией бронха и ателектазом S3 правого легкого. По данным КТ диагноз подтвержден: в пищеводе определяется значительное количество жидкого содержимого с остатками пищи, высокий риск повторной аспирации.
Сначала произведена эндоскопическая санация трахеобронхиального дерева с удалением инородного тела сегментарного бронха (рис. 9). Спустя 2 дня, 23.03.12 больной был оперирован. Выполнена трансхиатальная экстирпация пищевода с эзофагопластикой желудочной трубкой. Послеоперационный период протекал гладко. При контрольной рентгенографии на 5 сутки эзофагогастроанастомоз состоятелен, свободно проходим. Разрешено пероральное питание. Пациент выписан на 12 сут. в удовлетворительном состоянии после окончания курса антибактериальной терапии и разрешения аспирационной пневмонии (рис. 10).
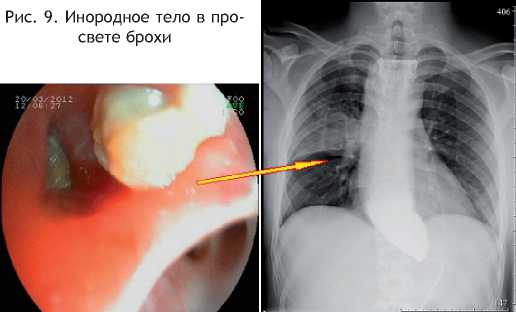
Рис. 9. Инородное тело в просвете брохи
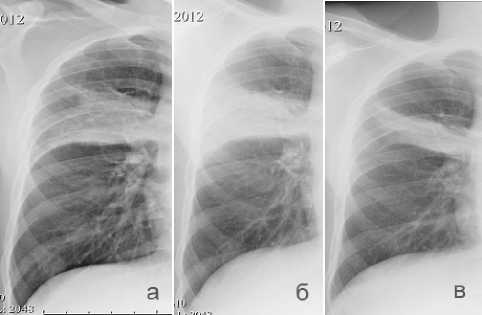
Рис. 10. При динамическом рентгенологическом исследовании определяется расправление ателектаза: а) при поступлении; б) после санации; в) при выписке
При формировании желудочной трубки мы принципиально не выполняем пилоропластику, поскольку ни разу не наблюдали спазма привратника и нарушения эвакуации из трансплантата (рис. 11). При контрольной рентгенографии через полгода виден свободно проходимый шейный эзофа-гогастроанастомоз, дилатированный дистальный отдел желудочного трансплантата в виде резервуара (рис. 12).
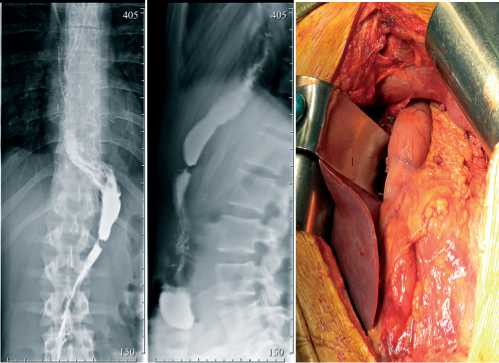
Рис. 11. Выходной отдел трансплантата, привратник
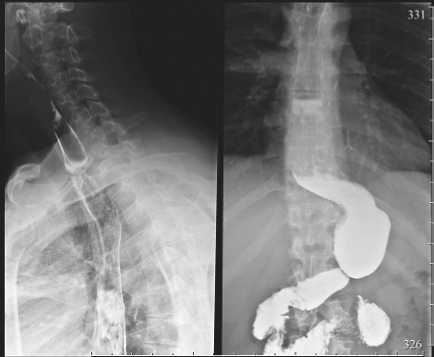
Рис. 12. Контрольная рентгенография через полгода: анастомоз проходим, стеноза нет. Антральный отдел желудка растягивается как резервуар
При вторичном диффузном эзофагоспазме (синдроме Барсони–Тешендорфа) на фоне ахалазии кардии могут образоваться множественные псевдодивертикулы. Появление дивертикулов таит в себе угрозу развития таких осложнений, как кровотечение и перфорация. Приводим клиническое наблюдение.
Пациент У., 52 года. Длительность анамнеза составила 3 года. При рентгенографии и МСКТ хорошо видны множественные дивертикулы пищевода, кардия плотно сомкнута, просвет пищевода расширен до 6,0 см. При эзофагоско- пии видны устья дивертикулов (рис. 13). В плановом порядке выполнена трансхиатальная экстирпация пищевода с эзофагопластикой желудочной трубкой (рис. 14). При контрольной рентгенографии на 5 сутки – шейный анастомоз состоятелен. На 7 сутки выписан из стационара.
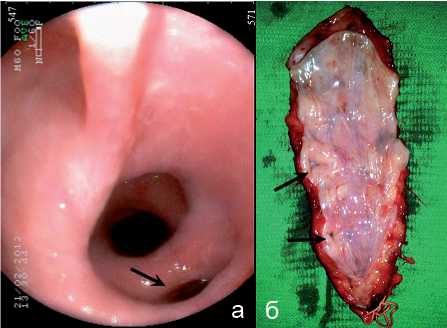
Рис. 13. Просвет пищевода: а) при эндоскопическим исследованием видны устья дивертикулов; б) макропрепарат (стрелки показано соустье дивертикулы)
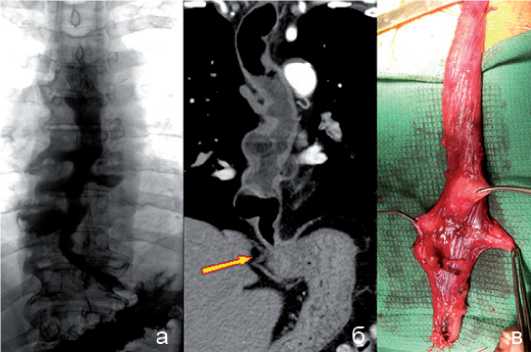
Рис. 14. Пищевод, видны 5 дивертикулов: а) рентгенограмма; б) МСКТ-Мультипланарная реконструкция пищевода, кардия плотно сомкнута (показано стрелкой), просвет пищевода расширен; в) макропрепарат снаружи
Экстирпация пищевода при рецидиве дисфагии после кардиомиотомии
По исходным данным рентгенографии 4 больных до радикальной операции у двух больных выявлена полная дисфагия. У больных после кардиомитомии пищевод расширен с наличием рубцового блок в зоне эзофагокардиального перехода, кардия деформирована, выраженый эрозивноязвенный эзофагит (рис. 15, 16). Также обращаем внимание, что у больных после операции на кардии отмечен дефицит тканей дна желудка, что отчасти ограничивало длину желудочного трансплантата.
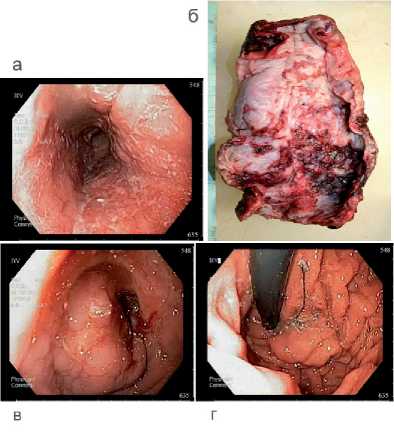
Рис. 15. Состояние после кардиомиотомии: а) просвет пищевода, выраженный эрозивно-язвенный эзофагит; б) макропрепарат – выраженный эрозивно-язвенный эзофагит; в) зона кардии с стороны пищевода, кардия деформирована; г) при ретроградном осмотре свода желудка видна грубая деформация в зоне кардии с лигатурой в просвете (показано стрелкой)
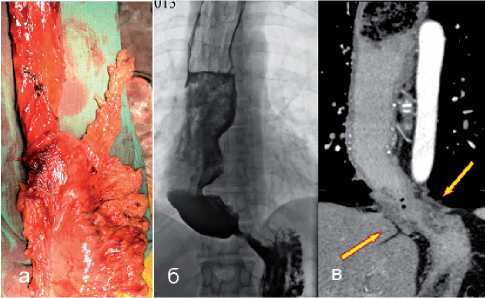
Рис. 16. Расширенный пищевод и рубцовый блок в зоне эзофаго-кардиального перехода: а) макропрепарат; б) исходная рентгенография данного больного; в) МСКТ-Мультипланарная реконструкция пищевода и желудка: фундаппликационная манжетка (рубцовый блок) после ранее выполненной операции (показано стрелкой)
Больные с III и IV степенью дисфагии не могут принимать большой объем очищающего средства для подготовки к операции, мы рекомендуем за 3 дня до операции ограничиться пероральном приемом только жидкой высококалорийной пищи. А при полной дисфагии производится установка зонда для питания и проводится внутривенная нутритивная поддержка, а также коррекция водноэлектролитного баланса у всех больных.
При коррекции водно-электролитных нарушений следует обратить внимание на то, что все больные с дисфагией поступают с высокой степенью гемоконцентрации, гемато- крит достигает 40–50%. При этом не рекомендуется быстрая коррекция его до нормальных показателей. Рекомендуемый уровень коррекции гематокрита – около 35%.
С целью предупреждения возможных интраоперационных осложнений необходимо в рамках предоперационной подготовки тщательное промывание пищевода за 8– 10 часов и за 2–3 часа до начала анестезии, данная процедура позволяет в случае произошедшей аспирации снизить риск развития фатальных осложнений.
Особенности интенсивной терапии
Особенности интенсивной терапии данной группы больных определяются длительным анамнезом заболевания, ранее проведенными вмешательствами, а также системным характером изменений, обусловленных поражением пищевода, и следующими за этим органными и метаболическими сдвигами.
У всех больных данной группы существует гиповолемия различной степени выраженности, гипопротеинемия и дефицит массы тела. Для улучшения результатов хирургического лечения перед операцией всем пациентам должна проводиться предоперационная подготовка, обязательно включающая в себя парентеральное питание и коррекцию гипопротеинемии, а пациентам с дефицитом массы тела желательно проводить ее до момента, когда дефицит составит не более 5%. Также на госпитальном предоперационном этапе подготовки необходимо учитывать, что больные с ахалазией кардии часто страдают от неспецифических хронических заболеваний легких, вызванных микроаспирацией застойного содержимого, что может приводить к изменению функции внешнего дыхания и скрытым изменениям газообмена, следовательно, исследование функции внешнего дыхания и оценка показателей газообмена необходимы для последующей успешной терапии и ранней экстубации в послеоперационном периоде.
Не вызывает сомнения, что течение послеоперационного периода зависит от адекватности анестезии. Однако предоперационная подготовка и адекватное интраоперационное сопровождение зачастую способны лишь смягчить тяжелые изменения гомеостаза, развившиеся за длительное время течения заболевания. После завершения операции действие факторов операционного стресса не заканчивается, развивается относительная гипергидратация вследствие нарушений водно-онкотического баланса, поэтому должно осуществляться систематическое наблюдение за состоянием больного, оценка витальных функций. Существуют несколько основных направлений послеоперационной интенсивной терапии.
Инфузионная терапия – направленная на коррекцию водно-электролитных нарушений, с учетом факторов операционного стресса и относительной гиповолемии в условиях гипергидратации легочной ткани и тканей периопе- рационной области. Также при необходимости коррекция трансфузионных нарушений.
Респираторная терапия – направленная на коррекцию дыхательных нарушений и предупреждение, а в некоторых случаях и на лечение дыхательной недостаточности раннего послеоперационного периода.
Адекватное обезболивание – в нашем случае всем больным проводится многокомпонентная анальгезия, включающая как внутривенное введение анальгетиков разных групп, так и продолжение эпидурального обезболивания, начатого интраоперационно.
Антибиотикопрофилактика и противовоспалительная терапия.
В течение послеоперационного периода выделяют четыре фазы: катаболическую, обратного развития, анаболическую и фазу увеличения массы тела.
Для первой фазы характерны усиленное выделение азотистых шлаков с мочой, диспротеинемия, гипергликемия, лейкоцитоз, умеренная гиповолемия, потеря массы тела. Она охватывает ранний и частично поздний послеоперационный период. И именно на этом самом раннем и наиболее важном этапе, часто определяющем дальнейший результат лечения, очень важен результат предоперационной подготовки, о которой было сказано выше. В раннем послеоперационном периоде продолжается парентеральное питание, коррекция диспротенемиии и водно-электролитного баланса. Также одним из основных моментов является продолжение интраоперационного (при наличии эпидурального катетера) и/или обеспечение адекватного послеоперационного обезболивания. Значение болей как пускового механизма, вызывающего ряд нарушений компенсации и нормальной функции различных органов, не вызывает сомнений. Боль препятствует адекватному самостоятельному дыханию и эвакуации мокроты при помощи кашля, следовательно, возникает необходимость в санации трахеобронхиального дерева, смещаются сроки экстубации и активизации больного. Большое количество мокроты приводит к развитию трахеобронхита с возможным последующим переходом в пневмонию. Послеоперационное обезболивание достигается введением наркотических и ненаркотических анальгетиков, с помощью различных вариантов проводниковой анестезии. Больной не должен ощущать боль, но программа лечения должна быть составлена так, чтобы обезболивание не угнетало сознание и дыхание.
Респираторная поддержка, проводимая в раннем послеоперационном периоде, в большинстве случаев направлена на поддержание функции адекватного газообмена в условия послеоперационной дыхательной недостаточности, вызванной депрессией самостоятельного дыхания на фоне приме-ния лекарственных средств анестезии. Режимы вентиляции должны быть, по возможности, щадящими, максимально обеспечивающими потребности пациента и облегчающи- ми переход на самостоятельное дыхание. Мы используем такие, как SIMV+PS c последующими переходом на PSV, с последующей ранней экстубацией больных. Среднее время послеоперационной респираторной поддержки в среднем составляет 6–10 часов. Учитывая невозможность у данной категории больных проведения неивазивных методов дыхательной терапии, вопрос о переводе на самостоятельное дыхание через естественные дыхательные пути должен решаться тщательно и основываться на результатах объективных исследований показателей газообмена каждого конкретного больного, так как реинтубация может быть связана с техническими трудностями и привести к развитию нежелательных осложнений.
Интенсивная терапия должна начинаться с момента госпитализации, быть продуманной, многокомпонентной и включать каждодневные изменения с учетом изменений состояния больного и данных биохимических исследований. Индивидуально разработанный уход и лечение обеспечивают положительный эффект, позволяющий сохранить жизнь больного [13, 14, 15].
Особенности анестезии
Анестезиологическое обеспечение трансхиатальной экстирпации пищевода по поводу ахалазии соответствует всем принципам ведения пациентов, которым выполняют эзофагэктомию с одномоментной пластикой тем или иным доступом.
К важным аспектам хирургического обеспечения трансхиатальной экстирпации пищевода относят:
— Предотвращение аспирации на всех этапах анестезиологического обеспечения.
— Стратегию безопасной вентиляции; дыхательный объем не более 6–8 мл/кг в режиме нормовентиляции на фоне применения ПДКВ 6–8 см Н2О, давления плато не более 30 см Н2О и регулярными маневрами раскрытия альвеол.
-
— Раннюю или немедленную экстубацию. Ранней считают экстубацию в течение 4 часов после эзофагэктомии.
-
— Инфузионную терапию, направленную на предотвращение гипо- и гиперволемии. Идеально – цель-ориентированная инфузионная терапия при помощи SVV, PPV, транспищеводный допплер.
-
— Интраоперационную и послеоперационную эпидуральную аналгезию.
-
— Обеспечение перфузии кондуита за счет адекватной инфузионной терапии, применения вазопрессоров и потенциальной пользы от эпидуральной аналгезии [2, 3, 4, 5].
Принципиальный момент анестезиологического обеспечения при экстирпации пищевода по поводу ахалазии – предотвращение аспирации. Доказано, что многие дыхательные нарушения после эзофагэктомии связаны с аспирацией пищеводно-желудочного содержимого [6, 7].
Эффективным методом профилактики аспирации при ахалазии считается быстрая последовательная индукция.
Этот метод позволяет безопасно и быстро разобщить пищеварительный тракт и дыхательные пути и предотвратить аспирацию.
Ключевые моменты быстрой последовательной индукции:
-
— преоксигенация (денитрогенизация);
-
— отсутствие масочной вентиляции;
-
— прием Селлика сразу после потери сознания.
Для правильной преоксигинации (денитрогенизации) необходимо при открытом клапане вдоха на высоком потоке дыхательной смеси (больше 10 л/мин), при высокой фракции О2 (80–100%) герметично приложить маску и под контролем газоанализатора дождаться примерного выравнивания О2 на вдохе и выдохе (около 3–5 мин.).
В дальнейшем провести быструю индукцию по очередности – современные гипнотик (не титруя), быстрый миорелаксант (листенон или рокуроний в индукционной дозе) и наркотический анальгетик.
После потери сознания выполнить прием Селлика (давление на перстневидный хрящ с усилием 3 Ньютона, 3 кг) и, исключая вентиляцию маской, после действия миорелаксанта интубировать трахею. Прекратить давление на перстневидный хрящ после подтверждения положения интубационной трубки в трахее (с помощью капнограммы).
Необходимость применения метода Селлика дискута-бельна [8], однако исполнение двух других принципов быстрой последовательной индукции обеспечивает безопасную индукцию.
В дополнение к быстрой последовательной индукции можно использовать гель-смазку на манжету одно- или двухпросветной интубационной трубки, это снижает риски «тихой» аспирации [9, 10]. Также необходима регулярная санация рото- и носоглотки в течении операции, перед экстубацией [11]. Постоянная аспирация под низким давлением из ротоглотки также снижает риски аспирации у больных, которым выполняют эзофагэктомию [12].
Результаты
В раннем послеоперационном периоде осложнений и летальных исходов не было. Время первичной и вторичной операций составляло 322±6,3 мин. Трудностью вторичных операции было иссечение послеоперационных спаек рубцовых тканей кардии. У всех больных были вскрыты плевральные полости при выделении сращений. Кровопотеря средняя – 722±51,4 мл, без особенной разницы.
Питание через рот начинали с 5-х суток после контрастного рентгенологического исследования, подтверждающего состоятельность шейного эзофагогастроанастомоза. 8 пациентов выписали на 7–9 сутки после операции, полноценно питающихся через рот. 1 больной – на 12 сут. в связи с необходимостью антибактериальной терапии исходной аспирационной пневмонии. Качество жизни больных в течение 1 года после операции признано удовлетворительным. Рубцового стеноза шейного анастомоза в отдаленном периоде не наблюдали.
Обсуждение
Несмотря на то, что все симптомы кардиоспазма возникают преимущественно из-за нарушения функции кардии, а патогенез – нейромышечный, захватывает пищевод на всем протяжении, все консервативные методы лечения и оперативные вмешательства на кардии мы считаем не радикальными.
Таблица 1
Признаки кардиоспазма (ахалазия кардии) 4 стадии
|
◆ |
Резко расширенный пищевод (6–8 см и более) занимает большую часть грудной полости. Он удлинен и искривлен в дистальных отделах, часто имеет S-образную форму |
|
◆ |
Пищевод представлен в виде атоничиного мешка, перистальтика его стенок отсутствует |
|
◆ |
Контрастный препарат поступает в желудок тонкой струйкой (симптом «редиски» или «мышиного хвоста») |
|
◆ |
Контрастная масса задерживается в пищеводе более 24 часов |
Ошибочной операцией является резекция кардии с наложением прямого пищеводно-желудочного анастомоза. При кардиоспазме IV стадии стенки пищевода атоничны, перистальтики стенки нет, т.к. анастомоз выше диафрагмы, отсутствует механический антирефлюксный клапан, часто развивается тяжелой рефлюкс-эзофагит. При еде лежа, при дыхании возможна регургитация желудочного содержимого, высокий риск аспирации, развития пневмонии. И после такой операции пластика желудка уже не получится [16, 43].
Хирургический подход к лечению ахалазии был описан Heller в 1913 году [17, 18]. Миотомия Хеллера с фундопликацией является оптимальным способом хирургического лечения ахалазии с эффективностью у 90 до 97% пациентов [19, 20].
Обе методики фундопликации: передняя по Dor и задняя по Toupet, одинаково часто используются, и до сих пор нет единого мнения, какая из них лучше:
-
• Фундопликации по Dor позволяет избежать мобилизации большой части дна желудка и технически проще выполнима. Кроме того, она дает возможность покрывать перфорации слизистой оболочки, произошедшие при кардиомиотомии.
-
• Фундопликация Toupet сшивает края миотомии, что может уменьшить развитие фиброза в месте разреза и рецидив дисфагии.
Окружная полная фундопликация по Nissen, как правило, не используется, что позволяет избежать чрезмерного сужения в месте желудочно-пищеводного перехода. Мы от- даем предпочтение частичной фундопликации по Toupet, что, как мы считаем, снижает риск рецидива дисфагии путем сшивания открытых краев миотомии, таким образом предотвращает образование рубцов, но прежде всего потому, что это лучший антирефлюксного барьер. Мы выполняем фундопликацию по Дор только при необхоимости укрыть перфорации слизистой оболочки [16, 26].
После лапароскопической кардиомиотомии по Хеллер показатель заболеваемости колеблется от 1 до 10%, а смертность составляет <0,1% в первые 30 дней после операции [20, 27–30]. Открытая кардиомиотомия может сопровождаться большим процентом осложнений в первые 30 дней, уровень смертности составляет от 0 до 5,4% [31]. Также данный способ лечения является более болезненным для пациента, все это увеличивает сроки госпитализации [32].
Наиболее распространенные осложнения после лапароскопической и открытой миотомии с фундопликацией включают: перфорацию, рецидивирующую дисфагию и гастроэзофагеальной рефлюк.
Но операция кардиомиотомии имеет высокий риск перфорации пищевода и/или желудка, с диапазоном от 10–16% [19, 21]. Послеоперационные перфорации обычно являются результатом либо прямого повреждения слизистой оболочки в интераоперационном периоде, либо случайной термической травмы. Перфорация обычно приводит к разлитому перитониту и/или медиастиниту и может быть опасной для жизни [22]. Риск повреждения селезенки колеблется от <1 до 5 процентов [27, 33, 34]. На заре использования лапаро-скомических методов данный вид осложнения встречался гораздо чаще.
Рецидив дисфагии – это самое позднее возникающее осложнение после проведения миотомии по Хеллеру. Частота рецидива дисфагии с появлением симптомов через 6 месяцев или позже после операции примерно составляет от 3 до 10% пациентов [20, 27, 29, 35, 42, 43]. Наиболее распространенной причиной является недостаточный разрез при миотомии, когда его длина менее 3 см, и ниже желудочно-пищеводного перехода. Это чаще встречается у пациентов, которым выполнено вмешательство торакоскопическим доступом [34]. В некоторых случаях разрез не был оптимальным даже при лапароскопии. В результате повторную процедуру может быть оправдано проводить через живот [33, 27].
Доля гастроэзофагеальной рефлюксной болезни (ГЭРБ), развившейся у пациентов, перенесших кардиомиотомию с частичной фундопликацией (Dor или Toupet), составляет от 2 до 26% в различных исследованиях [27, 36–40]. Доля ГЭРБ для пациентов, которым выполнена только миотомия без фундопликации, еще выше. Это было продемонстрировано в рандомизированном исследовании 43 пациентов с ахалазией, в котором у пациентов, перенесших кардиомиотомию по Хеллер с Dor-фундопликацией, была выявлена значи- тельно более низкая частота развития патологической ГЭРБ через 6 месяцев после операции по сравнению с пациентами, перенесшими Хеллер-миотомию без фундопликации (9 против 48 процентов) [36]. В отечественной литературе опыт проведенных 2425 операций показает развитие ГЭРБ до 40%, у 7,7% развивается пептический эзофагит, а пептическая стриктура – у 3%, на этом фоне возникает рецидив дисфагии до 5,1% [43] (табл. 2).
Другие осложнения – пневмоторакс, кровотечение, случайное повреждение блуждающего нерва и инфекции встречаются редко, по крайней мере, каждое примерно в 3% случаев [41] .
Кардиомиотомию с различной полной и неполной фундопликацией можно тоже считать как «местное хирургическое лечение», вследствие чего высок процент рецидивов или рефлюкс-эзофагитов с последовательном развитием пептических стриктур.
Ретроспективный анализ 394 пациентов с ахалазией после лапароскопической кардиомиотомии по Хеллер доказали, что в IV стадии кардиоспазма ее проведение неэффективно [20]. В группе было 13 пациентов с IV стадией заболевания, из которых у 5 были получены хорошие результаты, и у 8 пациентов данный вид лечения был неэффективен.
Лечение кардиоспазма должно быть систематическим. Непосредственно перед выбором метода лечения необходима тщательная оценка патогенеза и стадии заболевания. Опыт РНЦХ РАМН и ФГБУ ИХВ показал, что пневматическая кардиодилатация является адекватным выбором для лечения I, II, III стадии заболевания. После 5–6 процедур ее эффективность составляет 80–90% [1, 16].
Экстирпация пищевода является операцией выбора при кардиоспазме IV стадии при условии неэффективности курса пневмобаллонной дилатации.
При выполнении баллонодилатации на оперированной ранее кардии проведение дилататора часто затруднено в
Таблица 2
Осложнения после кардиомиотомии
При мануальной дилатации, конечно, требуются определенный опыт и сопровождение хирурга, обладающего достаточными навыками для выполнения реконструкции пищевода, в случае необходимости. Разрыв пищевода при проведении процедуры дилатации является показанием к экстренному оперативному вмешательству, с целью предупреждения развития медиастинита и перитонита. В таких случаях мы рекомендуем сразу выполнять экстирпацию пищевода с пластикой желудочной трубкой.
При возникновении перфорации выполнение кардиомиотомии с фундопликацией противопоказано, а ушивания перфорации не эффективно:
-
1. разрыв острый и инфицированный, после ушивания в течение длительного времени сохраняется воспалительный процесс и инфильтрация, усиливается проявление дисфагии и высокий риск повторной перфорации;
-
2. в отдаленном послеоперационном периоде дилатация может вызывать повторный разрыв пищевода;
-
3. безусловно, повторная операции всегда труднее, чем первичная.
При рецидиве дисфагии экстирпация пищевода показана только при невозможности или неэффективности баллонной дилатации, что является относительным показанием к удалению пищевода. Часто, учитывая молодой возраст пациентов, риск развития осложнений (прогрессирование заболевания и аспирация, малигнизация) и длительную ожидаемую продолжительность жизни, мы считаем целесообразным выполнить радикальное вмешательство (табл. 3).
Таблица 3
Абсолютными показаниями к экстирпации пищевода мы считаем
|
1 |
Кардиоспазм 4 ст. |
|
2 |
Кардиоспазм (2–4 ст.) с диффузным эзофагоспазмом и псевдодивертикулезом |
|
3 |
Разрыв пищевода при баллонной дилатации (ахалазия 2–4 ст.) |
|
4 |
Рецидив дисфагии после кардиомиотомии, вторичный рефлюкс-эзофагит, пептическая стриктура |
|
5 |
Группа больных, не имеющих возможности регулярно выполнять баллонную дилатацию при рецидиве кардиоспазма 3 ст. |
Заключение
Трансхиатальная экстирпация пищевода с одномоментной заднемедиастинальной эзофагопластикой изопери- стальтической желудочной трубкой и пищеводным анастомозом на шее является операцией выбора у больных с IV стадией кардиоспазма (ахалазии кардии), диффузным эзофагоспазмом (синдром Барсони–Тешендорфа) в сочетании с псевдодивертикулезом и рецидивом дисфагии после неудачной кардиомиотомии. Целесообразность выполнения повторной операции на кардии после неудачного первичного вмешательства весьма сомнительна.
Список литературы Экстирпация пищевода при кардиоспазме IV стадии и его рецидиве после открытой и эндоскопической кардиомиотомии
- Годжелло Э.А. Оперативная эндоскопия доброкачественных стенозирующих заболеваний пищевода: Дис.. д-ра мед. наук. М., 2002. 166 с.
- Ng J.M. Perioperative anesthetic management for esophagectomy//Anesthesiology Clinics. 2008. Vol. 26, № 2. P. 293-304.
- Ng J.M. Update on anesthetic management for esophagectomy//Current Opinion in Anesthesiology. 2011. Vol. 24, № 1. P. 37-43.
- Jaeger J.M., Collins S.R., Blank R.S. Anesthetic Management for Esophageal Resection//Anesthesiology clinics. 2012.
- Futier E. et al. A trial of intraoperative low-tidal-volume ventilation in abdominal surgery//New England Journal of Medicine. 2013. Vol. 369, № 5. P. 428-437.
- Atkins B.Z. et al. Reducing hospital morbidity and mortality following esophagectomy//The Annals of thoracic surgery. 2004. Vol. 78, № 4. P. 1170-1176.
- Kauer W.K. H., Stein H.J., Bartels H. Intratracheal long-term pH monitoring: A new method to evaluate episodes of silent acid aspiration in patients after esophagectomy and gastric pull up//Journal of gastrointestinal surgery. 2003. Vol. 7, № 5. P. 599-602.
- Cui Y. Pulmonary complication after esophagectomy results from multiple factors//The Annals of thoracic surgery. 2002. Vol. 74, № 5. P. 1747.
- Ovassapian A., Salem M.R. Sellick's maneuver: to do or not do//Anesthesia & Analgesia. 2009. Vol. 109, № 5. P. 1360-1362.
- Blunt M.C. et al. Gel lubrication of the tracheal tube cuff reduces pulmonary aspiration//Anesthesiology. 2001. Vol. 95, № 2. P. 377-381.
- Sanjay P.S. et al. The effect of gel lubrication on cuff leakage of double lumen tubes during thoracic surgery//Anaesthesia. 2006. Vol. 61, № 2. P. 133-137.
- Illing L., Duncan P.G., Yip R. Gastroesophageal reflux during anaesthesia//Canadian journal of anaesthesia. 1992. Vol. 39, № 5. P. 466-470.
- Shackcloth M.J. et al. Randomized clinical trial to determine the effect of nasogastric drainage on tracheal acid aspiration following oesophagectomy//British J. of Surgery. 2006. Vol. 93, № 5. P. 547-552.
- Cao S. et al. Fast-track rehabilitation program and conventional care after esophagectomy: a retrospective controlled cohort study//Supportive Care in Cancer. 2013. Vol. 21, № 3. P. 707-714.
- Nagai Y. et al. Preventive effect of sivelestat on postoperative respiratory disorders after thoracic esophagectomy//Surgery today. 2013. P. 1-6.
- Рак пищевода (3-е изд., испр. и доп.)/Под ред. М.И. Давыдова, И.С. Стилиди.
- Черноусое А.Ф., Богопольский П.М., Курбанов Ф.С. Хирургия пищевода: Руководство для врачей. М.: Медицина, 2000. С. 73-74.
- HellerE. Extra mucous cardioplasty in chronic cardiospasm with dilatation of the esophagus (Extramukose Cardiaplastik mit dilatation des oesophagus)//Mitt Grenzgels Med. Chir. 1913. № 27. S. 141.
- Payne W.S. Heller's contribution to the surgical treatment of achalasia of the esophagus//The Annals of thoracic surgery. 1989. Vol. 48, № 6. P. 876-881.
- Litle V.R. Laparoscopic Heller myotomy for achalasia: a review of the controversies//The Annals of thoracic surgery. 2008. Vol. 85, № 2. P. S743-S746.
- Zaninotto G., Costantini M., Rizzetto C. et al. Four hundred laparoscopic myotomies for esophageal achalasia: a single centre experience//Ann. Surg. 2008. Vol. 248. P. 986.
- Omura N., Kashiwagi H., Ishibashi Y. et al. Laparoscopic Heller myotomy and Dor fundoplication for the treatment of achalasia. Assessment in relation to morphologic type//Surg. Endosc. 2006. Vol. 20. P. 210.
- Vaziri K., Soper N.J. Laparoscopic Heller myotomy: technical aspects and operative pitfalls//Journal of Gastrointestinal Surgery. 2008. Vol. 12, № 9. P. 1586-1591.
- Cacchione R.N., Tran D.N., Rhoden D.H. Laparoscopic Heller myotomy for achalasia//The American Journal of Surgery. 2005. Vol. 190, № 2. P. 191-195.
- Peracchia A. et al. Laparoscopic treatment of functional diseases of the esophagus//International Surgery. 1995. Vol. 80, № 4. P. 336.
- Bonavina L. et al. Primary treatment of esophageal achalasia: long-term results of myotomy and Dor fundoplication//Archives of Surgery. 1992. Vol. 127, № 2. P. 222.
- Tatum R.P., Pellegrini C.A. How I do it: laparoscopic Heller myotomy with Toupet fundoplication for achalasia//Journal of Gastrointestinal Surgery. 2009. Vol. 13, № 6. P. 1120-1124.
- Wright A.S. et al. Long-term outcomes confirm the superior efficacy of extended Heller myotomy with Toupet fundoplication for achalasia//Surgical Endoscopy. 2007. Vol. 21, № 5. P. 713-718.
- Rosemurgy A.S. et al. A single institution's experience with more than
- laparoscopic Heller myotomies for achalasia//Journal of the American College of Surgeons. 2010. Vol. 210, № 5. P. 637-645.
- Schuchert M.J. et al. Minimally-invasive esophagomyotomy in 200 consecutive patients: factors influencing postoperative outcomes//The Annals of Thoracic Surgery. 2008. Vol. 85, № 5. P. 1729-1734.
- Torquati A. et al. Laparoscopic myotomy for achalasia: predictors of successful outcome after 200 cases//Annals of Surgery. 2006. Vol. 243, № 5. P. 587.
- Roberts J.R., Vela M.F., Richter J.E. Part 1: Gastrointestinal disoders. Charpter 4: Esophageal motility disorders: Achalasia and spastic motor disorders./In: Evidenced-based gastroenterology and hepatology, McDonald J.W.D., Burroughs A.K., Fegan B.G., Finnerty M.B. (Eds), Wiley-Blackwell, -Hoboken, 2010. P. 78.
- Velanovich V. Comparison of symptomatic and quality of life outcomes of laparoscopic versus open antireflux Surgery//Surgery. 1999. Vol. 126, № 4. P. 782-789.
- Oelschlager B.K., Chang L., Pellegrini C.A. Improved outcome after extended gastric myotomy for achalasia//Archives of Surgery. 2003. Vol. 138, № 5. P. 490.
- Patti M.G. et al. Laparoscopic Heller myotomy and Dor fundoplication for achalasia: analysis of successes and failures//Archives of Surgery. 2001. Vol. 136, № 8. P. 870.
- Zaninotto G. et al. Etiology, diagnosis, and treatment of failures after laparoscopic Heller myotomy for achalasia//Annals of Surgery. 2002. Vol. 235, № 2. P. 186.
- Richards W.O. et al. Heller myotomy versus Heller myotomy with Dor fundoplication for achalasia: a prospective randomized double-blind clinical trial//Annals of Surgery. 2004. Vol. 240, № 3. P. 405.
- Petersen R.P., Pellegrini C.A. Revisional surgery after Heller myotomy for esophageal achalasia//Surgical Laparoscopy Endoscopy & Percutaneous Techniques. 2010. Vol. 20, № 5. P. 321-325.
- Donahue P.E. et al. Floppy Dor fundoplication after esophagocardiomyotomy for achalasia//Surgery. 2002. Vol. 132, № 4. P. 716-723.
- Luketich J.D. et al. Outcomes after minimally invasive esophagomyotomy//The Annals of Thoracic Surgery. 2001. Vol. 72, № 6. P. 1909-1913.
- Zaninotto G. et al. Long-term outcome and risk of oesophageal cancer after surgery for achalasia//British Journal of Surgery. 2008. Vol. 95, № 12. P. 1488-1494.
- Ludemann R. et al. Pneumothorax during laparoscopy//Surgical Endoscopy and other Interventional Techniques. 2003. Vol. 17, № 12. P. 1985-1989.
- Домрачев С.А. Экстирпация пищевода с одномоментной пластикой при доброкачественных стриктурах пищевода: Дис. д-ра мед. наук. М., 1995. С. 119, 125-126.


