Экстракционно-хроматографическое определение глюкозы и фруктозы в присутствии ароматических аминокислот
Автор: Бычкова Анна Александровна, Пахомова Оксана Анатольевна, Коренман Яков Израильевич
Журнал: Вестник Воронежского государственного университета инженерных технологий @vestnik-vsuet
Рубрика: Фундаментальная и прикладная химия, химическая технология
Статья в выпуске: 1 (51), 2012 года.
Бесплатный доступ
Изучена экстракция глюкозы и фруктозы из водно-солевых растворов, содержащих ароматические аминокислоты (фенилаланин, триптофан, тирозин), гидрофильными растворителями (алифатические спирты, алкилацетаты, кетоны). Рассчитаны количественные характеристики процесса (коэффициенты распределения, степень извлечения, фактор разделения). Установлена зависимость коэффициентов распределения моносахаридов от содержания аминокислот в растворе. Разработана подвижная фаза для анализа концентрата методом восходящей тонкослойной хроматографии.
Глюкоза, фруктоза, фенилаланин, триптофан, тирозин, экстракция, хроматография
Короткий адрес: https://sciup.org/14039767
IDR: 14039767 | УДК: 543.635.22
Extraction-chromatographic determination of glucose and fructose in the presence of aromatic amino acids
The extraction of glucose and fructose from aqueous salt solutions containing aromatic amino acids (phenylalanine, tryptophan, tyrosine), hydrophilic solvents (aliphatic alcohols, alkyl acetates, ketones) have been studied. The quantitative characteric of the process (the distribution coefficients, the degree of extraction, separation factors) are calculeted. The dependence of distribution ratios of monosaccharides from the amino acid content in the solution has been established. A mobile phase for analysis of the concentrate by ascending thin layer chromatography have been developed.
Текст научной статьи Экстракционно-хроматографическое определение глюкозы и фруктозы в присутствии ароматических аминокислот
актуальность приобретает разработка способов определения компонентов фармацевтических аминокислотных препаратов и установление их подлинности. Количественное определение моносахаридов в протеиновых комплексах затруднено вследствие высокого содержания аминокислот в составе анализируемых препаратов.
Известны многочисленные сведения о хроматографических и электрохимических методах разделения и определения органических веществ, однако жидкостная экстракция продолжает занимать лидирующее положение среди методов разделения и концентрирования.
Цель исследования состоит в разработке экстракционно-хроматографического способа определения фруктозы и глюкозы в присутствии аминокислот в водных растворах.
К 20 см3 водно-солевого раствора аминокислот ( L- триптофан, L- фенилаланин , L- тирозин ) и моносахаридов (фруктоза, глюкоза) добавляли 1 см3 гидрофильного растворителя (объемное соотношение водной и органической фаз 20 : 1), экстрагировали на вибросмесителе 7-10 мин, после расслаивания системы (2-3 мин) отделяли экстракт.
Для определения содержания аминокислоты органическую фазу количественно помещали в ячейку для потенциометрического титрования. В качестве титранта применяли 0,01 моль/дм3 раствор КОН в безводном этиловом спирте. При неводном титровании индикаторным электродом служил стеклянный электрод; электрод сравнения - хлоридсеребряный электрод, заполненный насы- щенным раствором хлорида калия в этиловом спирте [1]. Электродвижущую силу раствора измеряли на высокоомном потенциометре. На дифференциальной кривой потенциометриче ского титрования имеется максимум, соответствующий содержанию аминокислоты в экс- тракте.
Для определения моносахарида в кон- центрате после экстракции микрошприцем отбирали 0,001 см3 экстракта, наносили на линию старта пластины и подсушивали на воздухе. На дно хроматографической камеры помещали этилацетат, н.пропиловый спирт, концентрированную уксусную кислоту, формамид и дистиллированную воду. После достижения подвижной фазой линии финиша пластину «Sorbfil» извлекали из камеры и подсушивали. По градуировочному графику зависимости площади пятна от концентрации моносахарида находили концентрацию фруктозы или глюко зы в водном растворе.
Коэффициенты распределения моносахарида и аминокислоты ( D M и D A ), степень извлечения ( R M и R A ) и факторы разделения (в )
моносахарида и аминокислоты вычисляли по уравнениям [2]:
^ I ,A(o)
’
VVI ,A(a)
Rt а - ^ ''— 100,
I,A D1Л + f ’ в -
где N} ^(0) и N} ^(а) - концентрации моносаха- рида и аминокислоты в органической и водной фазах, мг/см3; f - соотношение объемов равновесных водной и органической фаз.
Глюкоза и фруктоза - гидрофильные соединения, содержащие альдегидную и спиртовые группы, поэтому для экстракции применяли частично или полностью смешивающиеся с водой растворители (алифатические спирты, алкилацетаты, кетоны) в присутствии высали-вателя, необходимого для образования двухфазной системы. Предварительно установлено, что оптимальные параметры процесса достигаются в системах, практически насыщенных сульфатом аммония.
Коэффициенты распределения и степ ень извлечения глюкозы и фруктозы при экстракции из водно-солевых растворов максимальны для систем на основе ацетона, этилацетата и н.пропилового спирта (табл. 1).
Таблица 1 Коэффициенты распределения ( D ) и степень извлечения ( R , %) фруктозы и глюкозы при экстракции из насыщенных растворов сульфата аммония ( n = 3, Р = 0,95)
|
Экстрагент |
Фруктоза |
Глюкоза |
||
|
D |
R , % |
D |
R , % |
|
|
H. пропиловый спирт |
16,7±0,8 |
45,5 |
24,7±1,2 |
55,3 |
|
H.бутиловый спирт |
11,3±0,6 |
36,2 |
20,5±1,0 |
51,5 |
|
H.пентиловый спирт |
9,0±0,5 |
31,1 |
15,7±0,8 |
44,0 |
|
Изопропиловый спирт |
9,2±0,5 |
31,5 |
13,8±0,7 |
39,3 |
|
Изобутиловый спирт |
7,0±0,4 |
25,9 |
12,0±0,6 |
35,9 |
|
Изопентиловый спирт |
6,2±0,3 |
23,7 |
9,9±0,5 |
30,7 |
|
1,4-Диоксан |
12,1±0,6 |
37,7 |
17,5±0,9 |
46,7 |
|
Этилацетат |
20,4±1,0 |
50,4 |
24,6±1,2 |
55,2 |
|
Бутилацетат |
14,1±0,7 |
41,3 |
16,3±0,8 |
44,9 |
|
Ацетон |
17,5±0,9 |
46,6 |
25,4±1,3 |
55,9 |
При этом для глюкозы наиболее эффективным экстрагентом является ацетон, для фруктозы - этилацетат.
Известно, что в отношении ароматических аминокислот наиболее эффективны в качестве экстрагентов этилацетат и пропиловый спирт, менее эффективен ацетон [3, 4, 5]. Наличие в структуре аминокислот ОН-, NH 2 -,
СООН‐групп обусловливает различный механизм экстракции.
Изучена экстракция смеси моносахарида и ароматической аминокислоты из водносолевого раствора пропиловым спиртом, этилацетатом и ацетоном. Рассчитаны экстракционные характеристики фруктозы, глюкозы и ароматических аминокислот (табл. 2).
Таблица2
Максимальные коэффициенты распределения, степень извлечения и фактор разделения моносахаридов и ароматических аминокислот
|
Состав смеси |
& 8 8 2 m |
D 1 |
D 2 |
R 1 |
R 2 |
β |
|
фруктоза – триптофан |
я 8 в |
33,3 |
0,14 |
62,3 |
0,07 |
210 |
|
фруктоза – фенилаланин |
22,0 |
0,15 |
52,4 |
0,73 |
150 |
|
|
фруктоза – тирозин |
1 О1 § В у О )S & 3 |
21,6 |
0,10 |
51,9 |
0,50 |
200 |
|
глюкоза – триптофан |
я 8 в |
45,0 |
0,22 |
69,3 |
1,09 |
200 |
|
глюкоза – фенилаланин |
м 8 в |
42,5 |
0,26 |
68,0 |
1,23 |
180 |
|
глюкоза – тирозин |
39,4 |
0,27 |
66,3 |
1,34 |
150 |
Установлено, что наиболее полно разделяется смесь фруктозы и триптофана при экстракции ацетоном, фактор разделения 210. При этом степень извлечения фруктозы достигает 63,3 %, триптофан в этих условиях извлекается не более, чем на 0,4 %.
Следует отметить, что высокие факторы разделения получены и для других систем, содержащих глюкозу, например, 200 и 180 для систем с триптофаном и фенилаланином при экстракции ацетоном.
Экстракция глюкозы и фруктозы из водно‐солевого раствора моносахарида и аминокислоты гидрофильным растворителем представляет собой вариант распределения в двухфазной четырехкомпонентной системе. Механизм распределения моносахаридов и аминокислот между водной и органической фазами во многом определяется природой экстрагента.
Эффективность экстракции глюкозы и фруктозы из водно‐солевого раствора, содержащего аминокислоту, возрастает по сравнению с экстракцией отдельных компонентов смеси в 1,5 – 2 раза. Происходит частичное вытеснение моносахарида из водно‐солевого раствора за счет накопления гидрофобного компонента (аминокислота).
Об этом свидетельствуют коэффициенты распределения фруктозы и глюкозы в пяти- и шестикомпонентных системах моносахарид – смесь аминокислот - сульфат аммония – вода (табл. 3).
Таблица 3
Коэффициенты распределения и степень извлечения моносахаридов при экстракции этилацетатом в присутствии смеси аминокислот ( n = 3, P = 0,95)
|
Смесь аминокислот |
Фруктоза |
Глюкоза |
||
|
D |
R , % |
D |
R , % |
|
|
Фенилаланин - триптофан |
64,0±1 |
76,2 |
67,7±1,2 |
77,2 |
|
Фенилаланин - тироз ин |
63,9±2,1 |
76,2 |
52,9±3,2 |
72,3 |
|
Триптофан - тироз ин |
61,9±1,2 |
75,6 |
75,9±4,2 |
80,0 |
|
Триптофан - тирозин -фенилаланин |
82,3±4,2 |
80,6 |
91,8±4,6 |
82,1 |
Например, степень извлечения фруктозы и глюкозы из раствора, содержащего три ароматические аминокислоты, достигает 80,6 и 82,1 %, что превышает степень извлечения этих моносахаридов из индивидуальных растворов и растворов с одной аминокислотой в 1,2-1,5 раза (рисунок).
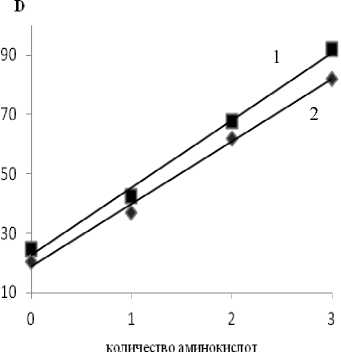
Рисунок. Зависимость коэффициентов распределения глюкозы (1) и фруктозы (2) от количества аминокислот в растворе
Для анализа концентратов нами применен метод хроматографии в тонком слое, который позволяет достаточно быстро обнаружить моносахариды при концентрациях на уровне 0,1 – 10,0 мкг/дм3.
Выбор хроматографической системы обусловлен природой определяемых веществ. Для элюирования моносахаридов рекомендуется система пиридин – смесь алифатических спиртов – вода. Ограничение известного способа связано с использованием резкопахнущих токсичных растворителей.
Нами применена подвижная фаза на основе этилацетата, н.пропилового спирта, концентрированной уксусной кислоты, формамида и дистиллированной воды в объемном соотношении 5 : 5 : 1 : 1 : 3. Установлено, что такая смесь обеспечивает полное разделение моносахаридов. С увеличением содержания уксусной кислоты в подвижной фазе эффективность разделения моносахаридов повышается, однако при этом происходит размытие пятна.
Минимально определяемые концентрации моносахаридов в анализируемых водных растворах составляют 0,1 – 1,0 мкг/дм3. Относительная погрешность определения микроколичеств моносахаридов по предложенной экстракционно-хроматографической методике с применением офисного сканера и ПК не превышает 10 %.


