Экстракт из листьев Astilbe rubra: фитохимический состав и влияние на активность пищеварительных ферментов in vitro
Автор: Кроль Т.А., Соколова Е.В., Осипов В.И., Балеев Д.Н.
Журнал: Сельскохозяйственная биология @agrobiology
Рубрика: Фитохимические соединения
Статья в выпуске: 3 т.60, 2025 года.
Бесплатный доступ
Резюме: Astilbe rubra Hook. f. & Thomson - это многолетнее травянистое растение семейства Saxifragaceae . Его ареал расположен на территории восточной Азии. В России естественные популяции произрастают на юге Дальнего Востока. A. rubra представляет интерес не только как декоративное растение, но и как лекарственное, пищевое и медоносное. В странах восточной Азии корневище используется как традиционное средство при различных заболеваниях, а листья и стебли в пищевых целях. Однако их фитохимический состав и биологическая активность изучены недостаточно. Ранее был показан ингибирующий потенциал водного и метанольного экстрактов A. rubra в отношении a-амилазы и липазы, который позволяет предположить комплексное воздействие на ключевые ферменты, дисфункционирующие при ряде метаболических нарушений у человека, ассоциированных с ожирением и диабетом. В настоящей работе впервые установлен подробный состав фенольных соединений, содержащихся в листьях A. rubra . Выявлено присутствие не только флавоноидов, но и фенольных кислот и проантоцианидинов типа А и B. Получены новые данные о содержании фенольных соединений и о воздействии экстракта на α-амилазу и липазу. Нашей целью было изучение состава и содержания фенольных соединений в экстракте из листьев Astilbe rubra , а также его действия на пищеварительные ферменты - липазу и α-амилазу, полученные из поджелудочной железы свиньи. Растения A. rubra были интродуцированы и произрастали на территории Ботанического сада лекарственных растений ФГБНУ ВИЛАР. Отбор образцов листьев проводили в период массового цветения растений (I декада июля) в 2023 году. Собранные листья замораживали и лиофильно высушивали. Проводили 3-кратную экстракцию 80 % ацетоном. Для изучения состава фенольных соединений использовали ультра-эффективную жидкостную хроматографическую систему (УЭЖХ, Acquity UPLC® 2.9.0, «Waters Corporation», США), которая включала фотодиодный детектор (190-500 нм) и тройной квадрупольный масс-спектрометр Xevo TQ («Waters Corporation», США) (УЭЖХ-ДД-МС). Полученные МС-данные анализировали с применением программы DataAnalysis 4.0 («Bruker Daltonik GmbH», Германия). Идентификацию фенольных соединений проводили с учетом анализа УФ- и МС-спектров, сравнивая полученные результаты с опубликованными данными. Общее содержание фенольных соединений определяли методом Фолина-Чокальтеу, содержание флавоноидов - методом, основанным на реакции комплексообразования флавоноидов с хлоридом алюминия. Влияние метаболитов экстракта из листьев A. rubra на активность a-амилазы, выделенной из поджелудочной железы свиньи («Nordmark Pharma GmbH», Германия), измеряли прямым колориметрическим методом. Активность липазы, выделенной из поджелудочной железы свиньи («Nordmark Pharma GmbH», Германия), оценивали прямым колориметрическим методом на основе модифицированного протокола, разработанного ранее. В результате проведенного анализа в экстракте из листьев A. rubra были идентифицированы 27 фенольных соединений: 10 олигомеров процианидина типа А и B со степенью полимеризации до 4, 12 флавоноидов (производные кверцетина, кемпферола и хризоэриола, катехин и эпикатехин) и 5 фенольных кислот (изомеры кофеоилтреоновой и кофеоилхинной кислот, кумароилхинная кислота). Общее содержание фенольных соединений составило 276,8±9,2 мг-экв. галловой кислоты/г сухой массы, флавоноидов - 46,7±6,08 мг-экв. кверцетина/г сухой массы. Исследованный экстракт не обладал ингибирующим эффектом в отношении амилазы, но умерено ингибировал активность панкреатической липазы. Полученные результаты расширяют знания в области биологически активных веществ из листьев A. rubra и их применения, показывая потенциальную возможность использования не только корневищ, но и листьев.
Процианидины, флавоноиды, фенольные кислоты, амилаза, липаза
Короткий адрес: https://sciup.org/142246214
IDR: 142246214 | УДК: 615.322 | DOI: 10.15389/agrobiology.2025.3.547rus
A Stilbe rubra leaf extract: phytochemical composition and effect on digestive enzyme activity in vitro
Astilbe rubra Hook. f. & Thomson, a perennial herbaceous plant of the Saxifragaceae family. The range of this species is in East Asia. In Russia, natural populations grow in the south of the Far East. A. rubra is of interest not only as an ornamental plant, but also as a medicinal, food, and honey plant. In East Asian countries, the rhizome is used as a traditional remedy for various diseases, and the leaves and stems are used for food purposes. Unlike the roots, phenolic compounds of leaves of A. rubra and their biological activity have not been sufficiently studied. Polyphenols are known to exert positive effects on human health through multiple mechanisms including mitigation of oxidative stress, protection of integrity of key macromolecules such as low-density lipoprotein cholesterol and supercoiled DNA. This bioactive group is also able to interact with proteins, which makes them have inhibitory effects on metabolic enzymes associated with type 2 diabetes (e.g., α-amylase, α-glucosidase) and obesity (e.g., pancreatic lipase). Inhibitory potential for aqueous and methanol extract of this species on &alpha-amylase and lipase has been previously shown, suggesting a complex effect on key enzymes dysfunctional in a number of human metabolic disorders associated with obesity and diabetes. This work provides the first detailed study of the composition of phenolic compounds of the leaves. In this regard, the aim of the study was to investigate the composition and content of phenolic compounds in A. rubra leaves extract, as well as their effect its effect on digestive enzymes. The studied A. rubra plants were introduced and grew on the territory of the Botanical Garden of All-Russian Scienti c Research Institute of Medicinal and Aromatic Plants (VILAR). An ultra-efficient liquid chromatographic system with a photodiode detector and a triple quadrupole mass spectrometer was used to determine the composition. The obtained MS data were analyzed using the DataAnalysis 4.0 program (Bruker Daltonik GmbH, Germany). For identification, we applied the analysis of UV and MS spectral data, comparing the obtained results with published data. The total content of phenolic compounds was determined by the Folin-Ciocalteu method, and the content of flavonoids by the method based on the complexation reaction of flavonoids with aluminum chloride. The effect of the extract on the activity of pancreatic amylase and lipase was measured by a colorimetric method. The significance of differences was analyzed using one-way analysis of variance followed by Tukey's multiple comparison test for group means. The performed analysis revealed 27 phenolic compounds were identified in the extract of leaves of A. rubra : 10 oligomers of procyanidin types A and B with a degree of polymerization of up to 4, 12 flavonoids (derivatives of quercetin, kaempferol, chrysoeriol, catechin and epicatechin) and 5 phenolic acids (isomers of caffeoylthreonic and caffeoylquinic acids, coumaroylquinic acid). The total content of phenolic compounds in the leaf extract was 276.8±9.2 mg of gallic acid equivalent/g of dry weight, and flavonoids were 46.7±6.08 mg of quercetin equivalent/g of dry weight. The studied extract did not have an inhibitory effect on pancreatic α-amylase in vitro but moderately inhibited the activity of pancreatic lipase. The obtained results expand knowledge in the field of biologically active substances of A. rubra leaves and their application, showing the potential possibility of using not only rhizomes but also leaves.
Текст научной статьи Экстракт из листьев Astilbe rubra: фитохимический состав и влияние на активность пищеварительных ферментов in vitro
Предполагается, что инактивация α -амилазы, α -глюкозидазы и липазы фенольными соединениями происходит в результате неспецифического связывания с этими ферментами (26, 27). Лекарства, применяемые в официальной медицине для лечения сахарного диабета 2-го типа и действующие по механизму прямого ингибирования пищеварительных ферментов, обладают рядом нежелательных побочных эффектов (диарея, метеоризм, вздутие живота и цистоидный пневматоз кишечника) (28, 29). Препараты из растений отличаются небольшим числом противопоказаний, минимальными побочными эффектами и сравнительно низкой токсичностью (30).
В настоящей работе впервые установлен подробный состав фенольных соединений, содержащихся в листьях A. rubra . Выявлено присутствие не только флавоноидов, но и фенольных кислот и проантоцианидинов типа А и B. Получены новые данные о содержании фенольных соединений и о воздействии экстракта на α -амилазу и липазу.
Нашей целью было определение состава и содержания фенольных соединений в экстракте из листьев Astilbe rubra , а также его действия на пищеварительные ферменты — липазу и α -амилазу, полученные из поджелудочной железы свиньи.
Ìåòîäèêà. Объект исследования — листья растений A. rubra , произрастающих на территории Ботанического сада лекарственных растений ФГБНУ Всероссийского НИИ лекарственных и ароматических растений (ВИ-ЛАР). A. rubra была ранее интродуцирована и в условиях г. Москвы проходит все фенологические фазы развития (31). Отбор образцов листьев проводили в период массового цветения растений (I декада июля) в 2023 году.
Собранные листья помещали в охлажденный термоконтейнер с хла-доэлементами и транспортировали в лабораторию, где замораживали и лиофильно высушивали (FreeZone 2.5 L, «Labconco», США). Измельченные листья (MM 400, «Retsch», Германия) массой 20 мг (CPA 225D, «Sartorius AG», Германия) экстрагировали 1 мл 80 % ацетона для хроматографии («Компонент-Реактив», Россия) в течение 60 мин при комнатной температуре и постоянном перемешивании (VORTEX Genie 2, «Scientific Industries», США). Экстракт отделяли центрифугированием в течение 20 мин при 14000 об/мин (5430R, «Eppendorf», Германия). Экстракцию образца повторяли еще два раза, объединенный экстракт концентрировали под вакуумом при 45 ° С (CentriVap, «Labconco», США) (32, 33). Полученный сухой экстракт растворяли в 1 мл деионизированной воды в течение 60 мин, центрифугировали в течение 20 мин при 14000 об/мин, разбавляли в 5 раз деионизированной водой (Direct-Q3, «Merck», Германия) и фильтровали (PTFE filter Clean 2, 0,45 мкм, «Thermo Fisher Scientific», США).
Для изучения состава фенольных соединений использовали ультра-эффективную жидкостную хроматографическую систему (УЭЖХ, Acquity UPLC® 2.9.0, «Waters Corporation», США), которая включала фотодиодный детектор (190-500 нм) и тройной квадрупольный масс-спектрометр Xevo TQ («Waters Corporation», США) (УЭЖХ-ДД-МС). В градиентной программе использовали 0,1 % муравьиную кислоту (А) и ацетонитрил (Б): 0-0,5 мин, 0,1 % Б в А; 0,5-5,0 мин, 0,1-30,0 % Б в А (линейный градиент); 5,0-6,0 мин, 30-35 % Б в А (линейный градиент). Скорость потока элюента 0,5 мл/мин, объем введенного образца — 5 мкл. Масс-спектрометр функционировал в режиме регистрации отрицательных ионов (33).
Полученные МС-данные анализировали с применением программы DataAnalysis 4.0 («Bruker Daltonik GmbH», Германия). При идентификации фенольных соединений использовали УФ- и МС-спектры, а также опубликованные данные (7, 34, 35).
Количество фенольных соединений определяли методом Фолина-Чокальтеу (36). В 96-луночных микропланшетах смешивали 10 мкл образца экстракта (1 мг/мл), 100 мкл реагента Фолина-Чокальтеу (разбавленного в 10 раз) и 80 мкл 1 М раствора карбоната натрия. Планшет встряхивали в течение 20 с. После 20-минутной инкубации в темноте при комнатной температуре измеряли оптическую плотность при λ = 630 нм (SPECTROstar Nano®, «BMG LABTECH», Германия). Общее содержание фенольных соединений определяли в мг-экв. галловой кислоты на 1 г сухой массы экстракта (мг ЭГК/г).
Для определения количества флавоноидов использовали метод, основанный на реакции комплексообразования флавоноидов с хлоридом трехвалентного алюминия (37). Реакционная смесь содержала 140 мкл H 2 O, 5 мкл водного 10 % AlCl 3 , 5 мкл 1 М ацетата натрия и 100 мкл образца экстракта 1 мг/мл. После 30-минутной инкубации при комнатной температуре поглощение измеряли при X = 415 нм (SPECTROstar Nano ® , «BMG LABTECH», Германия) и рассчитывали в мг-экв. кверцетина на 1 г сухой массы (мг ЭК/г).
Влияние метаболитов исследуемого экстракта из листьев A. rubra на активность а -амилазы, выделенной из поджелудочной железы свиньи («Nordmark Pharma GmbH», Германия), измеряли прямым колориметрическим методом (38). Метод основан на способности интактной панкреатической амилазы расщеплять субстрат 2-хлор-4-нитрофенол-олигосахарид с образованием свободного 2-хлор-4-нитрофенила (ХНФ). Положительный контроль — акарбоза (3 мкг/мл), отрицательный контроль (бланк) — вода.
Анализ проводили в 96-луночных микропланшетах при 37 ° С. В лунки последовательно добавляли 2,5 мкл раствора амилазы (O-4,6-дидезокси-4-{[4,5,6-тригидрокси-3-гидроксиметил-2-циклогексен-1-ил]амино}- a -D-глю-копиранозил-(1 ^ 4)-O- a -D-глюкопранозил-(1 ^ 4)-D-глюкоза) (50 Ед/мл) («Bayer Pharma», Индия), 95 мкл 50 ммоль/л MES-буфера (рН 6,0), содержащего моноклональные антитела против слюнной амилазы и 0,05 % азид натрия («Вектор Бест», Россия), и 5 мкл раствора образца экстракта (конечная концентрация 0,05, 0,1 и 0,2 мг/мл). После инкубации в течение 5 мин при интенсивном встряхивании добавляли раствор, содержащий субстрат ХНФ (23 мкл, 20 ммоль/мл) в MES-буфере (50 ммоль/мл, pH 6,0) и 0,09 % азида натрия («Вектор Бест», Россия). Интенсивность окрашивания измеряли при λ = 405 нм согласно протоколу к набору реагентов. Активность фермента выражали в процентах относительно отрицательного контроля с водой, активность которого принимали за 100 %.
Активность липазы, выделенной из поджелудочной железы свиньи («Nordmark Pharma GmbH», Германия), оценивали прямым колориметрическим методом на основе модифицированного протокола, разработанного ранее (39). Метод основан на том, что субстрат сложного эфира 1,2-О-ди-лаурил-рац-глицеро-3-глутаровой кислоты (6-метилрезоруфин) (DGGR) расщепляется липазой, в результате чего образуется нестабильный эфир дикарбоновой кислоты, который самопроизвольно гидролизуется с образованием глутаровой кислоты и метилрезоруфина — голубовато-фиолетового хромофора с максимумом поглощения при λ = 580 нм. Скорость образования метилрезоруфина прямо пропорциональна активности липазы в образце. Исследуемый экстракт разводили в диметилсульфоксиде (DMSO) до конечной концентрации в реакционной смеси от 0,05 до 0,2 мг/мл. В качестве положительного контроля использовали орлитстат (100 нг/мл). Отрицательный контроль (бланк) — вода. Анализ проводили в 96-луночном микропланшете при 37 ° С. В лунки последовательно добавляли 2 мкл раствора липазы поджелудочной железы свиньи в деионизированной воде (60 Ед/мл), 90 мкл раствора 1 (40 ммоль/л, Tris-буфер, pH 8,0, 1 мг/л коли-пазы, 6,4 ммоль/л дезоксихолата натрия, 3,4 ммоль/л тауродезоксихолата натрия, 0,09 % азида натрия, 7,4 ммоль/л хлорида кальция) («Вектор Бест», Россия) и 5 мкл раствора образца в DMSO с конечной концентрацией в реакционной смеси 0,2 мг/мл. После инкубации в течение 2 мин при встряхивании при 37 ° C добавляли 18 мкл раствора 2, содержащего субстрат DGGR (1 ммоль/л DGGR в 7,5 ммоль/л калий-натрий-тартратном буфере, рН 4,0) («Вектор Бест», Россия). Активность фермента выражали в процентах относительно отрицательного контроля с водой, активность которого принимали за 100 %.
Измерения проводили в трех повторностях. Статистическую обработку осуществляли в программе GraphPadPrism version 8.0.2 software («GraphPad Software», США). Данные представлены как средние значения ( M) и стандартные отклонения (±SD). Для анализа значимости различий применялся однофакторный дисперсионный анализ (ANOVA) с последующим тестом множественных сравнений Тьюки для групповых средних. Результаты считали статистически значимыми при p < 0,05.
Результаты. В результате проведенного анализа в экстракте из листьев A. rubra (рис. 1) было обнаружено 28 соединений (фенольные кислоты, проантоцианидины и флавоноиды) (табл., рис. 2).
Соединения 2, 3, 6 и 9 имели УФ-спектр, характерный для кофейной кислоты с максимумами поглощения в области 244, 297 плечо (пл), 325 нм (рис. 3, А). В масс-спектре соединений 2 и 3 присутствовал депротониро-550
ванный ион [М-Н] - с m/z 297 и его димер [2М-Н] - с m/z 595, а также характерный фрагмент с m/z 179, соответствующий иону [Кофейная кислота-H] - . Это позволило идентифицировать соединения как изомеры кофеои-лтреоновой кислоты. Анализ масс-спектров соединений 6 и 9 показал наличие основного депротонированного иона [M-H] - с m/z 353, иона [2М-Н] - с m/z 707 и фрагмента исходного иона с m/z 191, соответствующего хинной кислоте. Эти соединения были идентифицированы как изомеры кофеоилхин-ной кислоты. Ранее хлорогеновая кислота была обнаружена в A. rivularis (40).

Рис. 1. Растения Astilbe rubra Hook. f. & Thomson во время цветения в Ботаническом саду лекарственных растений ФГБНУ ВИЛАР (А) и лиофильно высушенные листья (Б) (г. Москва, 2023 год) .
Результаты ультра-эффективной жидкостной хроматографии с УФ-детектированием и масс-спектрометрией (УЭЖХ-УФ-МС) идентификации фенольных соединений в экстракте из листьев Astilbe rubra Hook. f. & Thomson (Ботанический сад лекарственных растений ФГБНУ ВИЛАР, г. Москва, 2023 год)
|
¹ |
Фенольные соединения |
РТ, мин |
УФ, нм |
m/z отрицательных ионов МС [M-H] - [2M-H] - |
Прочие фрагменты, m/z |
|
1 Не идентифицированное соединение 2 Кофеоилтреоновая кислота, изомер 1 |
2,54 2,69 |
197; 225 239; 322 |
331 297 |
595 |
177; 179; 251 |
|
3 Кофеоилтреоновая кислота, изомер 2 |
2,73 |
249; 326 |
297 |
595 |
177; 179; 251 |
|
4 Димер процианидина В-типа, изомер 1 |
2,82 |
199; 280 |
577 |
1155 |
289; 425; 452 |
|
5 Катехин |
2,94 |
212; 279 |
289 |
579 |
245 |
|
6 Кофеоилхинная кислота, изомер 1 |
2,96 |
235; 325 |
353 |
707 |
191 |
|
7 Тример процианидина В-типа, изомер 1 |
3,14 |
200; 279 |
865 |
- |
289; 451; 577 |
|
8 Димер процианидина В-типа, изомер 2 |
3,28 |
200; 279 |
577 |
1155 |
289; 425 |
|
9 Кофеоилхинная кислота, изомер 2 |
3,32 |
230; 283пл; 313 |
353 |
707 |
191 |
|
10 Эпикатехин |
3,37 |
224; 279 |
289 |
579 |
245 |
|
11 Тример процианидина В-типа, изомер 2 |
3,67 |
217; 279 |
865 |
- |
289; 577 |
|
12 Кумароилхинная кислота, изомер 1 |
3,74 |
216; 280; 310 |
337 |
- |
163; 191 |
|
13 Тример процианидина В-типа, изомер 3 |
3,74 |
865 |
- |
289; 425; 451; 577 |
|
|
14 Тетрамер процианидина В-типа, изомер 1 |
3,79 |
218; 279 |
1153 |
- |
289; 451; 576; 577; 865 |
|
15 Процианидин |
3,89 |
218; 279 |
- |
- |
289; 865; 1154 |
|
16 Тример процианидина А-типа, изомер 1 |
3,91 |
222; 279 |
863 |
- |
287; 289; 575; 573; 693 |
|
17 Рутин, изомер 1 |
3,97 |
255; 353 |
609 |
- |
163; 301 |
|
18 Кверцетин-гексозид, изомер 1 |
4,06 |
221; 268; 352 |
463 |
927 |
301 |
|
19 Тример процианидина В-типа, изомер 4 |
4,09 |
219; 281 |
865 |
- |
289; 577 |
|
20 Кверцетин-гексозид, изомер 2 |
4,11 |
219; 267; 353 |
463 |
927 |
301 |
|
21 Тетрамер процианидина В-типа, изомер 2 |
4,14 |
218; 282 |
1153 |
- |
289; 425; 451; 577; 865 |
|
22 Кверцетин-пентозид-гексозид, изомер 1 |
4,14 |
218; 265; 352 |
595 |
1191 |
301; 463 |
|
23 Кверцетин-пентозид, изомер 1 |
4,36 |
222; 267; 353 |
433 |
867 |
301 |
|
24 Кверцетин-рамнозид, изомер 1 |
4,48 |
255; 262; 349 |
447 |
895 |
301 |
|
25 Флавоноид |
4,61 |
255; 262; 349 |
579 |
1159 |
285; 417; 447 |
|
26 Хризоэриол-глюкуронид, изомер 1 27 Кверцетин-малонил-арабинофуранозид, изомер 1 |
4,68 |
255; 352 |
475 519 |
951 1039 |
299 301 |
|
28 Кемпферол-рамнофуранозид, изомер 1 |
4,85 |
232; 265; 344 |
431 |
- |
285 |
Примечание. Прочерки означают отсутствие данных.
Соединение 12 идентифицировали как изомер кумароилхинной кислоты. В его масс-спектре присутствовал депротонированный ион [М-Н] - с m/z 337, а также характерные фрагмент с m/z 163, соответствующий иону [р-Кумаровая кислота-H] - , и с m/z 191, соответствующий иону [Хинная кислота-H] - . Соединения 4, 5, 7, 8, 10, 11, 13-16, 19 имели УФ-спектр, характерный для флаван-3-олов (см. рис. 3, Б). Два соединения 5 и 10 были идентифицированы как катехин и эпикатехин (см. рис. 3, В) (7). Это подтверждается наличием в масс-спектре основного иона [M-H]- с m/z 289, а также его фрагмента с m/z 245 [M-H-CO 2 ] - .
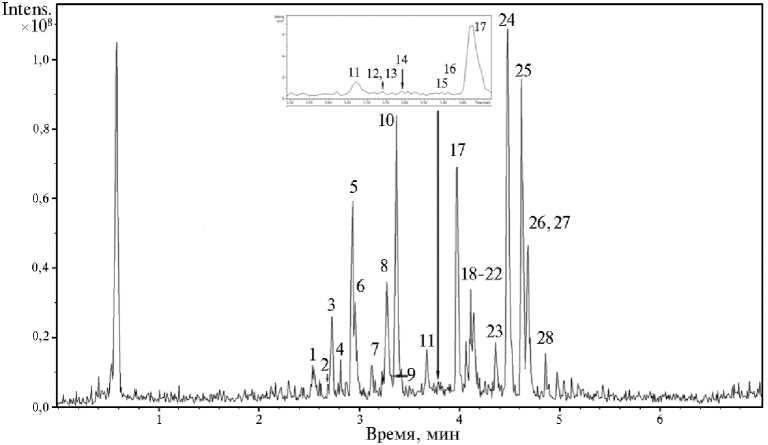
Рис. 2. Профиль фенольных соединений из экстракта листьев Astilbe rubra Hook. f. & Thomson, полученный методом УЭЖХ-МС (ультра-эффективная жидкостная хроматография с масс-спектрометрией; хроматограмма базового пика получена в режиме отрицательной ионизации) : 1 — неизвестное соединение; 2 — кофеоилтреоновая кислота, изомер 1; 3 — кофеоилтреоновая кислота, изомер 2; 4 — димер процианидина B-типа, изомер 1; 5 — катехин; 6 — кофеоилхинная кислота, изомер 1; 7 — тример процианидина В-типа, изомер 1; 8 — димер процианидина B-типа, изомер 2; 9 — кофеоилхинная кислота, изомер 2; 10 — эпикатехин; 11 — тример про-цианидина В-типа, изомер 2; 12 – кумароилхинная кислота, изомер 1; 13 — тример проциа-нидина В-типа, изомер 3; 14 — тетрамер процианидина В-типа, изомер 1; 15 — неизвестный процианидин; 16 — тример процианидина А-типа, изомер 1; 17 — рутин; 18 — кверцетин-гексозид, изомер 1; 19 — тример процианидина В-типа, изомер 4; 20 — кверцетин-гексозид, изомер 2; 21 — тетрамер процианидина В-типа, изомер 2; 22 — кверцетин-пентозид-гексозид, изомер 1; 23 — кверцетин-пентозид, изомер 1; 24 — кверцетин-рамнозид, изомер 1; 25 — флавоноид; 26 — хризоэриол-глюкуронид, изомер 1; 27 — кверцетин-малонил-арабинофура-нозид, изомер 1; 28 — кемпферол-рамнофуранозид, изомер 1 (Ботанический сад лекарственных растений ФГБНУ ВИЛАР, г. Москва, 2023 год).
Димеры процианидинов В-типа были представлены соединениями 4 и 8, идентифицированными на основании значений m/z ионов 577 [M-H] - и 1155 [2M-H] - , а также присутствия в масс-спектре характерных фрагментов с m/z 289, 425 и 451. Ион с m/z 289 образуется в результате расщепления межфлаваноидной связи, а фрагмент с m/z 451 [M-H-126 Да] - — при отщеплении молекулы флороглюцина (деление гетероциклического кольца). Еще один фрагмент спектра c m/z 425 образуется при потере 152 Да в результате ретро-фрагментация Дильса-Альдера (41).
Анализ масс-спектра соединений 7, 11, 13 и 19 показал наличие основного депротонированного иона [M-H]- с m/z 865 и характерных фрагментов исходного иона с m/z 577 и 289. В масс-спектре соединения 13 также присутствовали фрагменты с m/z 451 и 425. Эти соединения были идентифицированы как тримеры процианидина В-типа.
В листьях астильбы были обнаружены изомеры тетрамера проциа-нидина В-типа (соединения 14 и 21), которые идентифицировали на основании значений m/z 1153 иона [M-H] - и m/z 576 иона [M-H]2 - , а также фрагментов с m/z 865, 577, 451, 425 и 289.
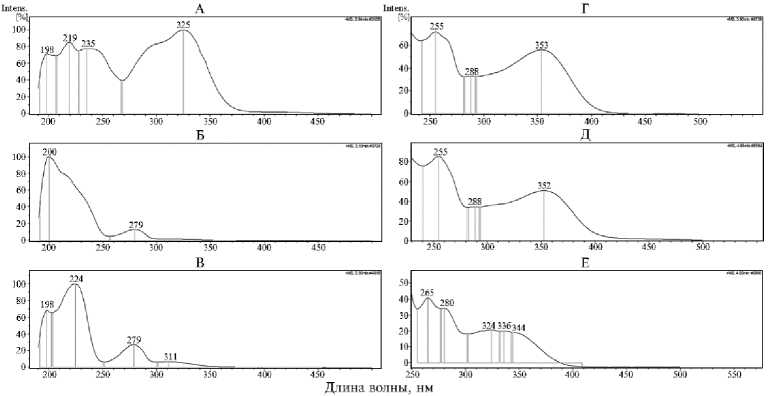
Рис. 3. Примеры УФ-спектров соединений ацетонового экстракта из листьев Astilbe rubra Hook. f. & Thomson: А — кофеоилхинная кислота, изомер 1; Б — тример процианидина В-типа, изомер 1; В — эпикатехин; Г — рутин, изомер 1; Д — кверцетин-малонил-арабинофуранозид, изомер 1; Е — кемпферол-рамнофуранозид, изомер 1 (Ботанический сад лекарственных растений ФГБНУ ВИЛАР, г. Москва, 2023 год).
Анализ масс-спектра соединения 15 не позволил определить m/z значение исходного иона [M-H] - . Однако присутствие фрагментов с m/z 865 и 289 характеризовало соединение как олигомер процианидина.
В масс-спектре соединения 16 наблюдали депротонированный ион с m/z 863, а также фрагменты, характерные для проантоцианидинов А-типа. Это соединение было идентифицировано как тример процианидина А-типа.
УФ-спектр соединений 17, 18, 20, 22-28 был характерен для флавоноидов (см. рис. 3, Г, Д, Е). Семь соединений имели УФ-спектр, характерный для кверцетина. Анализ их масс-спектра показал наличие фрагмента с m/z 301 [Кверцетин-Н] - . Соединение 17 было идентифицировано как кверцетин-рутинозид в соответствии со значением m/z основного иона 609 [M-H] - (7).
Соединения 18 и 20 имели m/z ионов [M-H]- и [2M-H]- соответственно 463 и 927, что характерно для кверцетин-гексозида (34). Анализ масс-спектра соединения 22 показал присутствие основного иона с m/z 595 и его димера со значением m/z 1191. Это соединение было идентифицировано как кверцетин-пентозид-глюкозид. Соединение 23 имело основной де-протонированный ион с m/z 433 и его димер с m/z 867 и было идентифицировано как кверцетин-пентозид (7, 35). Соединения 24 и 27 идентифицировали соответственно как кверцетин-рамнозид (m/z 447 [M-H] - ) и квер-цетин-малонил-арабинофуранозид (m/z 519 [M-H] - ). Соединения 17, 23, 24 и 27 ранее были выделены и идентифицированы в надземной части A. rubra (7).
Соединение 25 (m/z 579 [M-H]-) не было идентифицировано. Анализ его масс-спектра показал наличие фрагмента c m/z 285, что соответствует значениям ионов агликона кемпферола или лютеолина. Наблюдали также фрагменты с m/z 417 [агликон+пентоза-H]- и m/z 447 [агли- кон+гексоза-H]-.
В масс-спектре соединения 26 обнаружили ион [M-H] - с m/z 475 и [2M-H] - с m/z 951, что соответствует хризоэриол-глюкурониду или его изомеру. Идентификация подтверждается наличием фрагмента с m/z 299, соответствующего хризоэриолу.
УФ-спектр соединения 28 характерен для кемпферола (см. рис. 3, Е). Анализ масс-спектра показал наличие основного иона [M-H] - с m/z 431, а также фрагмента основного иона c m/z 285, соответствующего кемпферолу. Соединение 28 было идентифицировано как кемпферол-рамнофура-нозид.
Конденсированные таннины, или проантоцианидины, были ранее обнаружены в A. thunbergii (42). Это широко распространенные в природе полифенолы, присутствующие в различных органах растений и представляющие собой полимеры и олигомеры флаван-3-ола, связанные углерод-углеродными связями, с молекулярной массой до 28000 Да (43, 44). В зависимости от входящих в структуру проантоцианидина флаван-3-олов он будет относиться к процианидинам, пропеларгонидинам или продельфинидинам (45). Содержание и структура этих соединений в растениях могут варьировать в зависимости от окружающей среды, вида и фазы развития растения (46). Основная их функция — участие в защите растений от биотических и абиотических стрессов (47). Они ответственны за горечь и терпкость многих фруктов, чая и вина (48). Процианидины А-типа реже встречаются в растениях, чем процианидины В-типа (45). Однако у некоторых видов наблюдается преобладание этого типа процианидинов, например в перикарпии личи ( Litchi chinensis Sonn.) (49). Конденсированные таннины обладают широким спектром фармакологической активности — антибактериальной, противовирусной и противоопухолевой (50) и имеют потенциальное терапевтическое применение (51).
Общее содержание фенольных соединений в экстракте листьев A. rubra в нашем исследовании составило 276,8±9,2 мг ЭГК/г сухой массы (с.м.), содержание флавоноидов — 46,7±6,08 мг ЭК/г с.м. В листьях A. rivulari содержание фенольных соединений составляет 51±1,2 мг/г с.м. (52), а в экстракте коры A. rivularis — 183,11±0,50 мг ЭГК/г с.м. (53).
Несмотря на то, что, по данным R. Gon c alves с соавт. (54), различные процианидины, содержащиеся в растениях, способны ингибировать α -амилазу, в наших опытах экстракт из листьев A. rubra не влиял на активность α -амилазы in vitro и продемонстрировал слабый ингибирующий эффект в отношении этого фермента только при концентрации экстракта, равной 0,2 мг/мл (рис. 4). Однако, по данным H.-Y. Kim с соавт. (55), ингибирующая амилазу активность метанольного экстракта (10 мг/мл) из A. rubra составила 58,6 %, водного – 10,8 %. При этом не ясно, какая часть растения была использована для приготовления экстракта (55).
Экстракт из корня A. thunbergii способен ингибировать α -амилазу поджелудочной железы (42). Скорее всего, это связано со структурой соединений, содержащихся в экстракте. Так, наличие в структуре галлоильных групп положительно влияет на ингибирующий эффект в отношении амилазы. При этом катехины катехолового типа (катехин-галлат и эпикате-хин-галлат) в два раза сильнее проявляют ингибирующую способность в отношении амилазы, чем катехины пирогаллолового типа (галлокатехин-галлат и эпигаллокатехин-галлат) (56), а полимеры проантоцианидинов сильнее ингибируют α -амилазу, чем олигомеры (57). В структуре идентифици-554
рованных нами соединений галлоильные группы отсутствовали.
Изучаемый экстракт обладал способностью умерено ингибировать (в зависимости от концентрации) активность панкреатической липазы (см. рис. 4). Ингибирующий эффект составил 12 % при концентрации экстракта 0,05 мг/мл и 32 % при 0,2 мг/мл. Ранее проведенные исследования указывали на слабую антилипазную активность водных экстрактов астильбы (58) и отсутствие ингибирующего эффекта при использовании метанольных экстрактов (55).
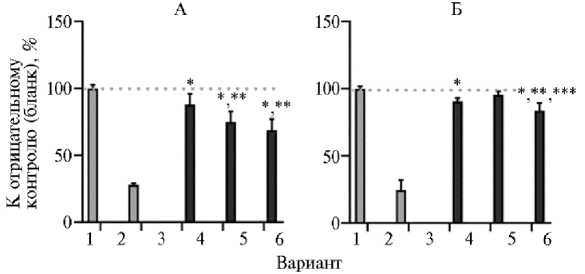
Рис. 4. Активность пищеварительных ферментов липазы (А) и α -амилазы (Б) под влиянием разной концентрации экстракта из листьев Astilbe rubra Hook. f. & Thomson: 1 — отрицательный контроль (вода), 2 — положительный контроль (А — акарбоза, 3,0 мкг/мл, Б — орлистат, 0,1 мкг/мл), 3 — 50 мкг/мл, 4 — 100 мкг/мл, 5 — 200 мкг/мл ( n = 3, M ±SD, Ботанический сад лекарственных растений ФГБНУ ВИЛАР, г. Москва, 2023 год).
*, ** и *** Статистически значимые отличия соответственно от отрицательного контроля, от 50 мкг/мл экстракта A. rubra , от 100 мкг/мл экстракта A. rubra (Tukey test, p < 0,05).
Таким образом, в результате анализа экстракта из листьев Astilbe rubra методом ультра-эффективной жидкостной хроматографии с УФ- и масс-спектрометрией мы идентифицировали 27 фенольных соединений: 10 конденсированных таннинов, 12 флавоноидов и 5 фенольных кислот. Конденсированные таннины были представлены 9 олигомерными процианиди-нами B-типа со степенью полимеризации до 4 и тримером процианидина А-типа. Суммарное содержание фенольных соединений в экстракте листьев составило 276,8±9,2 мг/г сухой массы, содержание флавоноидов — 46,7±6,08 мг/г с.м. Установлено in vitro, что изучаемый экстракт не обладал ингибирующим эффектом в отношении α -амилазы, но умерено ингибировал активность панкреатической липазы.


