Электронно-энергетические характеристики полиалициклических нанотрубок, содержащие функциональные группы с непереходными элементами
Автор: Калинкин Д.П., Литинский А.О.
Журнал: Математическая физика и компьютерное моделирование @mpcm-jvolsu
Рубрика: Химическая физика
Статья в выпуске: 8, 2004 года.
Бесплатный доступ
В рамках модели молекулярного кластера с замыканием нескомпенсированных валентностей атомами водорода и полуэмпирической расчетной схемы РМ3 исследованы электронное строение и спектры одноэлектронных состояний нанотрубок с насыщенными углерод-углеродными связями и их модификации, содержащие в качестве дефектов замещения наружных атомов водорода группы (O)2Mg, (O)2Zn, (O)2Al(OH), (O)2Si(OH)2, (O)2Si(Cl)2, (O)2Ge(OH)2, (O)2Ge(Cl)2, (O)2Sn(OH)2 и (O)2Sn(Cl)2 Обсуждены особенности зонной энергетической структуры данного класса нанотубуленов.
Короткий адрес: https://sciup.org/14968533
IDR: 14968533 | УДК: 539.2:530.145
Electronic and energy characteristics of polyalicyclic nanotubes containing functional groups with non-transitional elements
The model of a molecular cluster with closure of uncompensated valences by atoms of hydrogen and serr.iempirica! method PM3 are used for exploration an electronic structure and spectrums of one-electron states of nanotubes with saturated carbon-carbon connections and their modifications containing groups (O)2Mg, (O)2Zn, (O)2A1(OH), (O)2Si(OH)2, (O)2Si(Cl)2, (O)2Ge(OH)2, (O)2,Ge(Cl)2, (O)2,Sn(OH)2 and (O)2Sn(Cl)2 as substitute defects of outside atoms of hydrogen. The peculiarities of zonal energy structure of sectional class nanotubes are discussed.
Текст научной статьи Электронно-энергетические характеристики полиалициклических нанотрубок, содержащие функциональные группы с непереходными элементами
В рамках модели молекулярного кластера с замыканием нескомпенсированных валентностей атомами водорода и полуэмпирической расчетной схемы РМЗ исследованы электронное строение и спектры одноэлектронных состояний нанотрубок с насыщенными углерод-углеродными связями и их модификации, содержащие в качестве дефектов замещения наружных атомов водорода группы (O)2Mg, (O)2Zn, (O)jAl(OH), (O)2Si(OH)2, (O)2Si(Cl)2, (O)2Ge(OH)2, (O)2Ge(Cl)2, (O)2Sn(OH)2 и (O)2Sn(Cl)2. Обсуждены особенности зонной энергетической структуры данного класса нанотубуленов.
Исследовались алициклические углеводородные нанотрубки (АУН) типа (12,0), то есть «zig-zag», имеющие цилиндрическую симметрию и содержащие двенадцать гексагонов по окружности (диаметр равен 21,5 А для «наружных» атомов углерода и 20,1 А для «внутренних»), По окружности трубки система геометрически замкнута. Вдоль оси АУН размер кластера выбран L ~ 13,3 А (шесть циклов). Кластер содержит 168 атомов углерода и 192 атома водорода. Достаточно большая величина L отвечает локализованности дефекта (или дефектной группы) в случае наличия такового. Расстояния между ближайшими атомами углерода принимались равными ~1,53 -^ 1,55 А (следствие оптимизации чисто углеводородного нанотубулена). Нескомпен-сированные валентности замыкались атомами водорода (модель молекулярного кластера, МК). Расчеты проводились по схеме РМЗ [1—3] с использованием программного пакета GAMESS [4] с полной оптимизацией геометрических параметров. Кроме электронной структуры бездефектного АУН (расчет модели которого представлен в [5]), рассмотрим электронное строение и энергетический спектр тубуленов на его основе, имеющие дефекты замещения наружных атомов водорода в пределах одного центрального слоя вдоль окружности трубки на функциональные группы (O)2Mg, (O)2Zn, (О).Д1(ОН), (O)2Si(OH)2, (O)2Si(Cl)2, (O)2Ge(OH)2, (O),Ge(Cl)„ (O)2Sn(OH), и (O)2Sn(Cl)2 (рис. 1).'
---0\ Н—о т>—н
(ж)
(в)
Рис. 1. Функциональные группы замещения наружных атомов водорода вдоль окружности АУН центрального слоя трубки; введены следующие обозначения: (а) = (O)2Mg, (б) = (O)2Zn, (в) = (О)2А1(ОН), (г) (O)2Si(OH)2, (д) = (O)2Si(Cl)2, (е) ^ (O)2Ge(OH)2, (ж) (О)2Ое(С1)2, (з) = (O)2Sn(OH)2, (и) = (O)2Sn(Cl)2
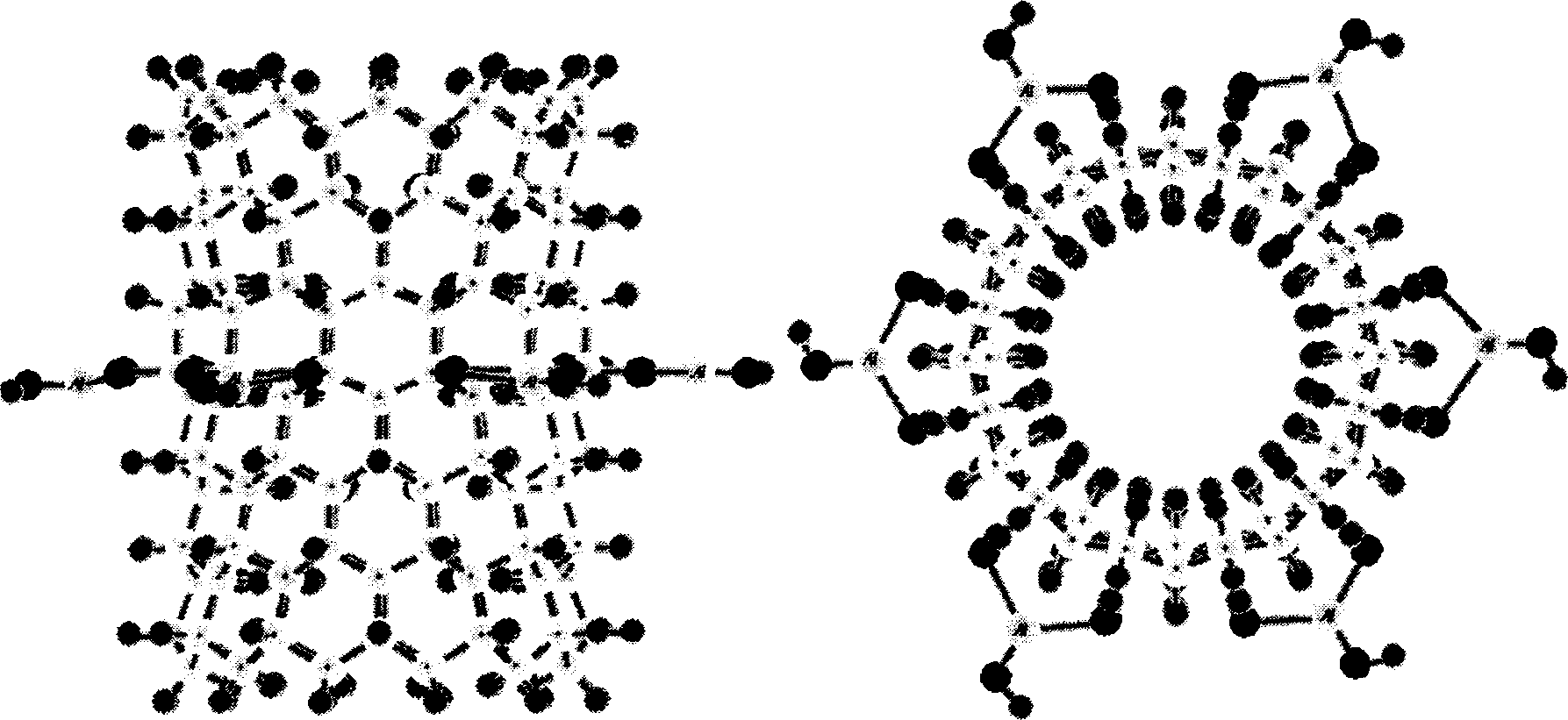
На рисунке 2 представлена модель МК алициклического углеводородного нанотубулена (12,0), содержащая дефектные группы (О)2А1(ОН).
(а)
(б)
Рис. 2. Модель молекулярного кластера АУН, содержащего дефектные группы (О)2А1(ОН) ((а) — вид сбоку, (б) — вид сверху; атомы углерода показаны светло-серыми шариками, атомы водорода — маленькими темными, кислорода — большими черными; подписанные шарики — атомы алюминия)
В таблице 1 приведены уровни энергии всех структур относительно границ валентной зоны И ЗОНЫ ПрОБОДИМОСТИ бСЗДСфСКТНОГО ВарИаНТа аЛИЦИКЛИЧССКОГО НаНОТубуЛСНа, а ТаКЖС ВСЛИЧИН запрещенной энергетической щели (ЗЭЩ) для АУН с рассмотренными выше типами дефектных групп. В таблице 2 продемонстрированы зарядовые распределения (в единицах заряда электрона) по атомам металлов функциональных групп.
Таблица 1
Уровни энергии, обусловленные дефектными группами, относительно границ зоны проводимости (Ес -Едеф) и валентной зоны (Едеф-Еу); здесь же приведены значения величины ЗЭЩ (АЕе)
|
Тип структуры |
м 5 О |
д N О |
Я О •< о |
Я о сю о |
и о |
Я О о о |
и и О о |
Я О СЮ О |
и "д' СЮ О |
|
(£деф-£и), эВ |
0,92 |
0,58 |
0,41 |
0,63 |
-0,14 |
0,22 |
-0,27 |
1,05 |
-0,57 |
|
(^С-^деф), эВ |
3,62 |
3,55 |
3,44 |
1,24 |
3,19 |
2,32 |
3,81 |
3,55 |
5,58 |
|
А£„, эВ |
7,92 |
8,33 |
8,61 |
10,58 |
9,41 |
9,93 |
8,92 |
7,86 |
7,45 |
Таблица 2
Заряды на атомах металлов дефектных групп
|
Тип структуры |
Ы) S О |
д N ri о |
К О < СМ О |
о сю о |
с сю СМ О |
И О СМ О |
и о о |
гм я о СЛ о |
и 'д' сю О |
|
Атом дефекта |
Mg |
Zn |
А1 |
S1 |
Si |
Ge |
Ge |
Sn |
Sn |
|
Заряд |
V) 40 o' + |
тТ о” + |
т т—Ч + |
+ |
+ |
о о + |
о ОО o' + |
о ОО + |
+ |
Данные таблиц 1 и 2 свидетельствуют о том, что с ростом порядкового номера в таблице Менделеева основного атома дефекта нанотрубки энергетическая щель между валентной зоной (ВЗ) и зоной проводимости (ЗП) сужается, то есть АУН становится более «металлическим» (в смысле электронной проводимости).
Диаграммы энергетических уровней электронов (каждая молекулярная орбиталь (МО) представлена в виде линии) исследуемых структур приведены на рисунке 3. Их анализ позволяет сформулировать следующие выводы.
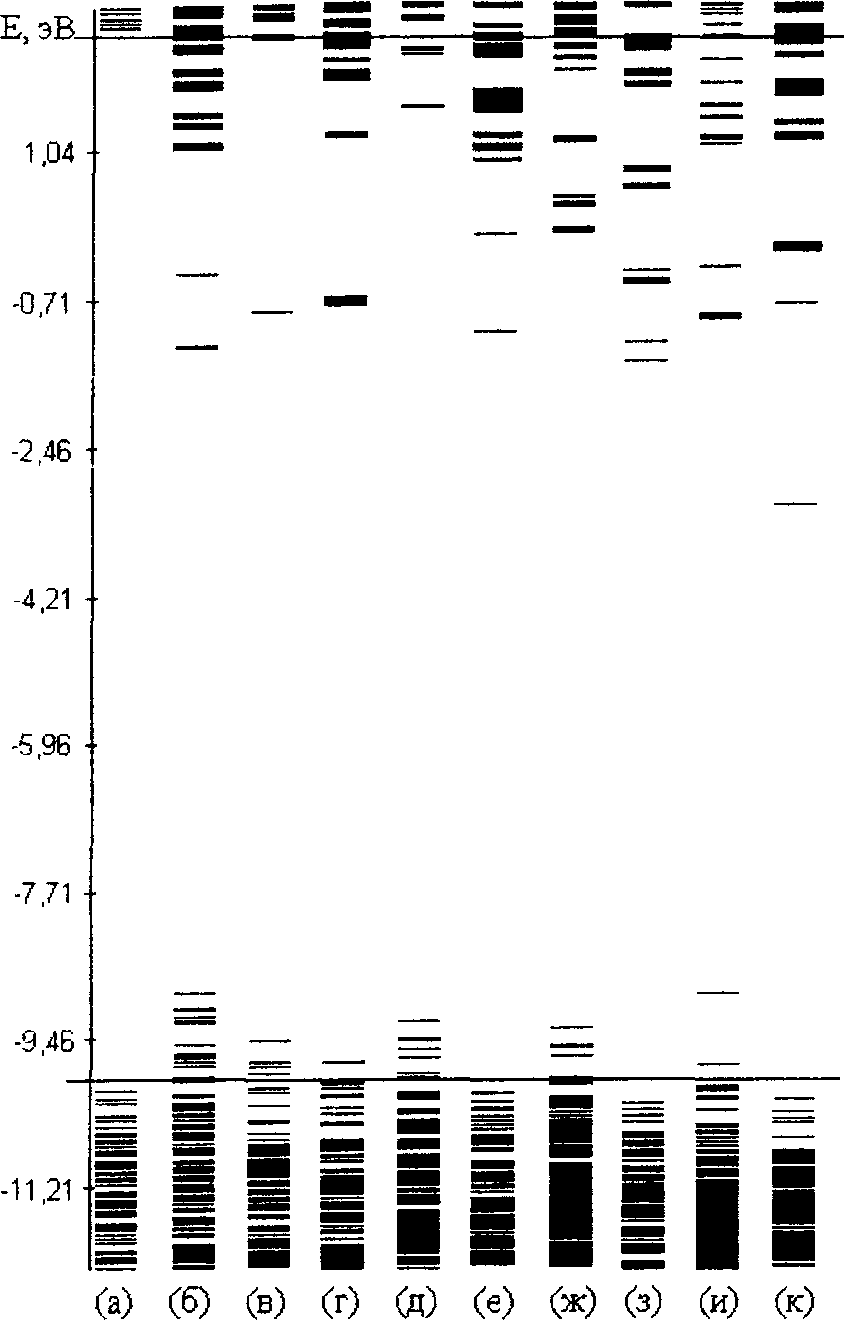
Рис. 3. Спектры одноэлектронных состояний бездефектного нанотубулена (а) и тубуленов с дефектами вдоль длины окружности исходной нанотрубки в пределах одного слоя, соответственно ((б) — (O)2Mg; (в) — (O)2Zn; (г) — (0)^1(011); (д) — (O)2Si(OH)2;
(е) - (O)2Si(Cl)2; (ж) - (O)2Ge(OH)2; (з) - (О)2Се(С1)2; (и) - (O)2Sn(OH)2 и (к) - (O)2Sn(Cl)2)
Замещение наружных атомов водорода вдоль длины окружности трубки в пределах одного слоя на группы (O)2Mg (рис. 1 а, рис. 3 б) приводит к достаточно заметному изменению энергетического спектра электронов. В запрещенной энергетической щели появляются уровни как над валентной зоной (отвечающие неподеленным парам электронов атомов кислорода (« 40 %) и связывающим орбиталям С-О связей (« 20—30 %)), так и под зоной проводимости, обусловленные атомами Mg (вклад в МО от соответствующих атомных орбиталей (АО) металла ® 60— 90 %). О степени «углубления» и тех и других уровней можно судить по рисунку 3 и таблице 1. Длины связей С-0 и Mg-О оказались равными 1,38 и 1,80 А, соответственно. На атоме Mg — достаточно большой положительный заряд (+0,65), на атоме кислорода — отрицательный (—0,45) (знаки зарядов на атомах дефектов соответствуют ожидаемым, то есть они обусловлены большей или меньшей электроотрицательностью по сравнению с атомами углерода).
Введение групп (O)2Zn (рис. 1 б, рис. 3 в) и (О)2А1(ОН) (рис. 1 в, рис. 2, рис. 3 г) также приводит к появлению уровней, примыкающих к ВЗ (соответствуют неподеленным парам электронов атомов кислорода и связывающим орбиталям С-0 связей (® 20—40 %) в обоих случаях) и более глубоко расположенных уровней под дном ЗП (основной вклад в эти уровни вносят аТОМЫ АП ^ти— и /и) и ш ^/v—/ j /и) с псимлвшмп примерши rw/ книлирида ^ди z,u /о)). причем наблюдается следующая тенденция в поведении последних: уровни, находящиеся у потолка валентной зоны, опускаются в область более низких энергий, а уровни, расположенные вблизи дна зоны проводимости, поднимаются в область более высоких энергий (то есть уменьшение А£ происходит за счет сдвигов границ возмущенных валентной зоны и зоны проводимости). Длины связей С-0 и Zn-О оказались равными 1,43 и 1,91 А, соответственно, для структуры (O)2Zn. На атоме Zn — положительный заряд (+0,47), на атоме кислорода — отрицательный (-0,38). Для структуры (О),А1(ОН) имеем: R(C-O) = 1,40 A, R(O-A1) = 1,77 А, R(A1-O) = 1,73 А и R(O-H) = 0,94 А, что хорошо согласуется с данными, приведенными в
-
[6] . На атоме алюминия — большой положительный заряд (+1,73), который в значительной степени компенсируется зарядами на соседних к нему атомах кислорода.
Качественно аналогичная ситуация имеет место во всех остальных структурах — (O)2Si(OH)2, (O)2Si(Cl)2, (O)2Ge(OH)2, (O)2Ge(Cl)2, (O)2Sn(OH)2 и (O)2Sn(Cl)2 — замещенных алициклических нанотубуленах. При этом верхним занятым состояниям отвечают орбитали неподеленных пар атомов кислорода функциональных групп с примесью орбиталей соседних атомов углерода и хлора (в структурах, содержащих хлор); до ~ 30 % от АО хлора в случае дефекта (O)2Si(Cl)2. Ниже приводятся величины вкладов соответствующих атомных орбиталей в нижние вакантные состояния. Здесь же указаны валентные длины связей (заряды на атомах металлов дефектных групп см. в табл. 2).
-
1. (O)2Si(OH)2 (рис. 1 г, рис. 3 д): Si ~ 50—60 %, 0-30 %; R(Si-O) = 1,7 А.
-
2. (O)2Si(Cl)2 (рис. 1 д, рис. 3 е): Si ~ 50—70 %, О ~ 10 %, С1 ~ 20—30 %; R(Si-Cl) = 2,1 А, R(Si-O) = 1,7 А.
-
3. (О) Ge(OH)2 (рис. 1 е, рис. 3 ж): Ge ~ 60 %, О ~ 30 %; R(Ge-O) = 1,8 А.
-
4. (O)2Ge(Cl)2 (рис. 1 ж, рис. 3 з): Ge ~ 55—60 %, С1 ~ 20—40 %; R(Ge-Cl) = 2,2 А, R(Ge-O) = 1,8 А.
-
5. (O)2Sn(OH)2 (рис. 1 з, рис. 3 и): Sn ~ 50—70 %, О ~ 40 %; R(Sn-O) = 1,9 А.
-
6. (O)2Sn(Cl)2 (рис. 1 и, рис. 3 к): Sn ~ 50—75 %, О ~ 10—20 %, О ~ 15—30 %; R(Sn-Cl) = = 2,3 A, R(Sn-O) = 1,9 А.
При введении атома хлора в дефектные группы структуры тубулена наблюдается следующая картина: уровни энергии как занятых, так и вакантных состояний опускаются в область более низких энергий (по сравнению с дефектами, содержащими группы О-Н). Состояния, преимущественный вклад в которые вносят орбитали атомов хлора, оказываются в глубине валентной зоны и на границе зоны проводимости. Переход к функционально замещенным структурам во всех случаях приводит к сужению запрещенной щели.
Проведенные модельные расчеты показали, что в результате замещения наружных атомов водорода только в пределах одного кольца в алициклических нанотубуленах с достаточно широкой величиной ЗЭЩ (такие АУН являются широкощелевыми диэлектриками) можно получить широкощелевые (и даже узкощелевые) полупроводники. То есть данные дефектные группы напрямую оказывают влияние на электронную проводимость тубулена, приближая полупроводниковую проводимость нанотрубки (12,0) к металлическому типу проводимости (что зависит от количества функциональных групп замещения). Итак, сделаем предположение о возможности создания на основе таких АУН одномерных наноструктур с требуемыми проводящими свойствами, что может найти соответствующее применение в элементах полупроводниковой техники.
Список литературы Электронно-энергетические характеристики полиалициклических нанотрубок, содержащие функциональные группы с непереходными элементами
- Thiel W. Semiempirical methods: current status and perspectives//Tetrahedron. 1988. V. 44 № 24. P. 7393-7408.
- Stewart J.J.P. Optimization of parameters for semiempirical methods. 1. Methods//J. Comput. Chem. 1989. V. 10. № 2. P. 209-220.
- Stewart J.J.P. Optimization of parameters for semiempirical methods. 2. Applications//J. Comput. Chem. 1989. V. 10. № 2. P. 221-264.
- Schmidt M.W., Baldridge K.K., Boatz J.A., Elbert S.T., Gordon M.S., Jensen J.H., Koseki S., Matsunaga N., Nguyen K.A., Su S.J., Windus T.L., Dupuis M., Montgomery J.A. General Atomic and Molecular Electronic Structure System//J. Comput. Chem. 1993. V. 14. P. 1347-1363.
- Калинкин Д.П., Литинский А.О. Электронно-энергетический спектр алициклических углеюдородных нанотубуленов с дефектами замещения, распределенными параллельно оси трубки//Вестник ВолГУ. Сер. 1: Математика. Физика. 2002. Вып. 7. С. 98-102.
- Краснов К.С. Молекулярные постоянные неорганических соединений: Справочник. Л.: Химия, 1979. 448 с.


