Эндопротезирование аневризм брюшной аорты как метод выбора у больных с высоким риском осложнений
Автор: Чупин Андрей Валерьевич, Колосов Роман Владимирович, Зайцев Максим Владимирович, Паршин Павел Юрьевич, Орехов Павел Юрьевич, Дерябин Сергей Владимирович, Кемеж Юлия Владимировна, Ситников Александр Владимирович, Лебедев Дмитрий Петрович
Журнал: Клиническая практика @clinpractice
Рубрика: Оригинальные исследования
Статья в выпуске: 3 (7), 2011 года.
Бесплатный доступ
Методика эндопротезирования аневризм брюшной аорты за последние десятилетия используется все более часто. Данное вмешательство показано пациентам с высоким хирургическим и анестезиологическим риском открытого оперативного пособия. Рассматривается опыт 29 эндопротезирований аневризм брюшной аорты EXLUDER Core у пожилых пациентов с высоким риском открытого оперативного вмешательства. В ближайшем и отдаленном периоде летальных исходов не отмечено. После эндопротезирования аневризмы брюшной аорты не отмечено кардиальных и дыхательных осложнений в ближайшие сроки после операции. При динамическом наблюдении (1, 6, 12 мес. после операции) пациентов при компьютерной томографии осложнений (миграции эндопротеза, увеличение диаметра аневризмы, эндоликов I типа) не отмечено. Таким образом, эндопротезирование аневризмы брюшной аорты является методом выбора для пациентов группы высокого риска.
Эндопротезирование, аневризма брюшной аорты, осложнения
Короткий адрес: https://sciup.org/14338574
IDR: 14338574
Endovascular aortic aneurysm repair as a choice method in patients with high risk of complications
The technique of endoprosthetics of aneurysms of the abdominal aorta has been used more and more often in recent decades. This intervention is indicated for patients with high surgical and anesthesia risk of open surgical manual. The experience of 29 endoprosthetical aneurysms of the abdominal aorta EXLUDER Core in elderly patients at high risk of open surgical intervention is considered. In the near and distant period, no lethal outcomes were noted. After endoprosthetics of the aneurysm of the abdominal aorta, cardiac and respiratory complications were not observed in the short term after the operation. With dynamic follow-up (1, 6, 12 months after surgery), patients with computed tomography of complications (endoprosthesis migration, aneurysm diameter increase, type I endolysis) were not observed. Thus, endoprosthetics of the aneurysm of the abdominal aorta is the method of choice for patients at high risk.
Текст научной статьи Эндопротезирование аневризм брюшной аорты как метод выбора у больных с высоким риском осложнений
В настоящее время социальная значимость и актуальность диагностики и лечения аневризм брюшной аорты (АБА) по-прежнему остается высокой.
В США ежегодно диагностируется приблизительно 200 000 АБА. В Великобритании ежегодно регистрируется 18 пациентов с АБА на 100 000 населения. В России, по данным статистики, выявляется около 1 случая АБА на 100 000 в год. Следует отметить, что эти показатели в нашей стране занижены по причине недостаточного скрининга АБА [1-4].
Консервативное лечение рассматриваемой патологии малоэффективно. Отмечено, что 90% больных погибают от разрыва аневризмы в течение года. Риск разрыва АБА увеличивается при артериальной гипертензии, наличии хронических заболеваний легких, мешковидной формы аневризматического мешка. Вопрос о лечении аневризм брюшной аорты давно и однозначно решен в пользу хирургического вмешательства, которое на настоящий момент считается наиболее эффективным.
Однако выполнение вмешательства у паци- ентов старшей возрастной группы, наличие сопутствующей кардиальной патологии, сахарного диабета, мультифокального атеросклероза влечет за собой высокий риск периоперационных осложнений [5-8].
Существует большое число работ, направленных на снижение операционного риска у больных данной категории, связанного как с самой техникой операций, так и анестезиологическим пособием, очередностью вмешательства, отбором пациентов.
Внедрение c 1991 г. (Володось Н.Л. и соавт., Parody H. et al.) эндопротезирования АБА позволило осуществлять хирургическое лечения пациентов с крайне высоким риском осложнений, которым ранее данное вмешательство возможно было выполнить только по витальным показаниям [9, 10]. Совершенствование техники, инструментария, конструкции эндопротезов также значительно снизили риски операции и улучшили результаты как в ближайшем, так и в отдаленном периоде наблюдения.
Количество открытых операций на брюшной аорте при АБА в США за последние десятилетия изменялось в широком диапазоне – от
17 000 до 46 000, эндоваскулярных операций – от 11 000 до 14 000 в год [1-4].
В России число плановых открытых операций в 2008 г. на брюшной аорте при АБА составило 1335, эндоваскулярных – 53. Общая летальность после открытых операций по поводу АБА за 2008 г в России составила 10,3%, после эндоваскулярных операций летальных исходов не отмечено [11].
Целью работы являлся анализ результатов эндопротезирования АБА у пациентов c высоким риском периоперационных осложнений при открытых оперативных вмешательствах.
Материал и методы
В отделении сосудистой хирургии Клинической больницы № 83 ФМБА России в период с декабря 2007 по июль 2011 г. выполнено 29 эндопротезирований АБА.
Средний возраст пациентов составил 69,5 лет (от 57 до 86 лет). 60% больных были старше 70 лет. В данной группе преобладали мужчины – 24 (82,7%), женщин – 5 (17,3%).
Сопутствующие заболевания у пациентов данной группы представлены в табл. 1.
Таблица 1
|
Сопутствующая патология |
Количество пациентов |
% |
|
Артериальная гипертензия |
28 |
96,5 |
|
ИБС |
22 |
75,8 |
|
Инфаркт миокарда в анамнезе |
9 |
31 |
|
Стенокардия напряжения 2 ф.к. |
7 |
24 |
|
Стенокардия напряжения 3 ф.к. |
5 |
17 |
|
Желудочковая экстрасистолия (частая) |
3 |
10 |
|
Мерцательная аритмия |
5 |
17 |
|
Сахарный диабет |
8 |
27,5 |
|
Поражение артерий нижних конечностей |
5 |
17 |
|
ХОБЛ, тяжелое течение |
2 |
6,9 |
|
ХПН, цистостомия |
2 |
6,9 |
|
Ожирение 3 ст. |
1 |
3,5 |
|
Онкология с планируемым оперативным лечением в течение 1 мес. |
2 |
6,9 |
Сопутствующие заболевания у больных с АБА
Предоперационное обследование включало эхокардиографию, при которой выявлено выраженное нарушение сократительной функции миокарда левого желудочка с наличием зон гипо- и акинеза у 7 пациентов (24%). Фракция выброса составила в среднем 57,9 ± 1,5% (минимальная 35%, максимальная 66%).
Пациентам выполнялось ультразвуковое дуплексное сканирование брюшной аорты. Средний диаметр аневризмы брюшной аорты составил 4,8 ± 0,3 см (минимальный 2,5 см, максимальный 7,4 см).
Всем пациентам проводилась контрастная мультиспиральная компьютерная томография (МСКТ) (рентгеновский мультиспиральный компьютерный томограф "Aquilion 64", Toshiba, Япония c наличием 64-рядного детектора) брюшной аорты и подвздошных артерий c выполнением 3D-реконструкции и определения параметров АБА (протяженность, длина «шейки», максимальный диаметра аневризмы), распространения на подвздошные артерии, наличия и выраженности пристеночного тромбоза (рис. 1).
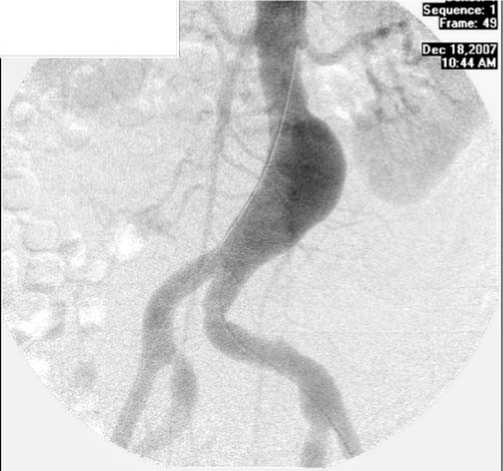
Рис. 1. Ангиография брюшной аорты с контрастированием до операции
Средний диаметр АБА, по данным МСКТ, составил 5,06 ± 0,22 см (колебания от 2,5 до 8,5 см). При этом аневризма с размерами 2,5 см имела мешотчатый характер с резким истончением передней стенки. Пристеночный тромбоз АБА выявлен у 23 (79%) пациентов. Распространение аневризмы на подвздошные артерии отмечено у 13 (45%) больных. У всех пациентов аневризмы брюшной аорты располагались инфраренально и имели «шейку» под почечными артериями для фиксации эндопротеза. У 2 (10%) пациентов потребовалось выполнение контрастной ангиографии для уточнения состояния и характера поражений подвздошных артерий и артерий нижних конечностей.
Критерием для выполнения эндопротезирования брюшной аорты было наличие инфраре-нальной АБА, наличия «шейки» аневризмы, технической возможности изготовления и имплантации эндопротеза. Также основными показаниями для эндопротезирования АБА являлось наличие тяжелой сопутствующей патологии пациента (прежде всего кардиальной и дыхательной), определяющей высокий хирургический и анестезиологический риск открытого оперативного вмешательства.
Результаты
Всем 29 пациентам выполнено эндопроте-зирвоание АБА с применением эндопротеза EXLUDER Gore. Операцию проводили стандартным способом, под эпидуральной анестезией осуществляли доступы к бедренным артериям обеих нижних конечностей. После поперечной артериотомии общих бедренных артерий устанавливали системы доставок эндопротеза. После выполнения ангиографии с использованием мобильного рентгеновского аппарата Zeim (С-дуга) определяли уровень позиционирования эндопротеза. Под контролем С-дуги позиционировался ствол с ипсилатеральной ножкой бифуркационного эндопротеза EXLUDER Gore, а затем контралатеральная ножка эндопротеза. Далее в обязательном порядке выполняли контрастную ангиографию с определением правильного позиционирования эндопротеза и наличия эндоподтекания.
У 3 пациентов выполняли сочетанную операцию. Двум больным перед эндопротезированием АБА эмболизировали внутреннюю подвздошную артерию в связи с распространением аневризмы на эту зону. Одному пациенту предварительно выполнена ангиопластика и стентирование наружной подвздошной артерии по поводу ее гемодинамически значимого стеноза. Другому пациенту после установки эндопротеза дополнительно потребовалась ангиопластика и стентирование наружной подвздошной артерии. У третьего больного потребовалось протезирование общей бедренной артерии в связи с ее выраженным атеросклеротическим пора- жением и невозможностью ушивания пункционного дефекта артерии.
Среднее время операции составило 142,1 ± 8,6 мин (минимальное 80 мин, максимальное 310 мин). Увеличение времени операции было связано с техническими трудностями при позиционировании контралатеральной ножки эндопротеза при значительном внутрипросветном диаметре АБА.
26 (89,7%) пациентов после операции были переведены под наблюдение в профильное отделение. 3 (10,3%) пациента наблюдались в отделении реанимации и интенсивной терапии в течение суток в связи с тяжелой сопутствующей кардиальной патологией.
Среднее время пребывания в стационаре составило 20,4 ± 1,3 сут, а среднее время послеоперационного периода – 12,3 ± 0,9 дня. У всех пациентов отмечалось гладкое течение послеоперационного периода. У одного больного развилось местное осложнение – расхождение краев послеоперационной раны на бедре с последующим вторичным заживлением.
У 5 (25%) пациентов интраоперационно отмечали наличие эндоподтекания (endoleak).
Endoleak I типа, интраоперационно выявленный у 3 пациентов, был устранен позиционированием дополнительной аортальной надставки у 2 пациентов, у одного пациента – с помощью аортального баллона. При контрольной МСКТ у этих больных данных за endoleak получено не было.
У двух пациентов интраоперационно выяв- лен endoleak II типа. Коррекция при данном типе endoleak не проводилась. При динамическом наблюдении через 1 мес. после эдопротези-рования АБА данных относительно наличия endoleak II типа не получено.
Послеоперационная летальность после эндопротезирования АБА не отмечена.
Все больные выписаны в удовлетворительном состоянии.
В алгоритм послеоперационного обследования включалось выполнение контрастной МСКТ в течение 1 мес. после операции, а также через 6, 12, 18, 24 мес. Данные обследования в ближайший и отдаленный период представлены в табл. 2 и 3. Свыше 69% пациентов обследованы в сроки более 6 и 12 мес. после операции (табл. 2).
Таблица 2
Послеоперационное обследования или МСКТ с контрастированием
|
Срок после операции |
Количество пациентов |
|
1 мес. |
29 |
|
1 и 6 мес. |
12 |
|
1, 6 ,12 мес. |
8 |
|
1, 6 ,12, 24 мес. |
3 |
Таблица 3
|
Результаты обследования |
Интраоперационно |
Через 1 мес. |
Через 6 мес. |
Через 12 мес. |
|
Нет подтекания |
24 |
28 |
22 |
11 |
|
Endoleak I типа |
3 |
- |
- |
- |
|
Endoleak II типа |
2 |
1 |
1 |
* |
|
Миграция стента |
- |
- |
- |
- |
Ближайшие и отдаленные результаты послеоперационного обследования
У всех больных отмечена полная проходимость эндопротеза EXLUDER Gore, отсутствие увеличения размеров аневризмы аорты и миграции эндопротеза (табл. 3, рис 2, 3.).
Endoleak II типа выявлен у одного пациента через 6 мес. после операции, требующий последующего планового динамического наблюдения при КТ.
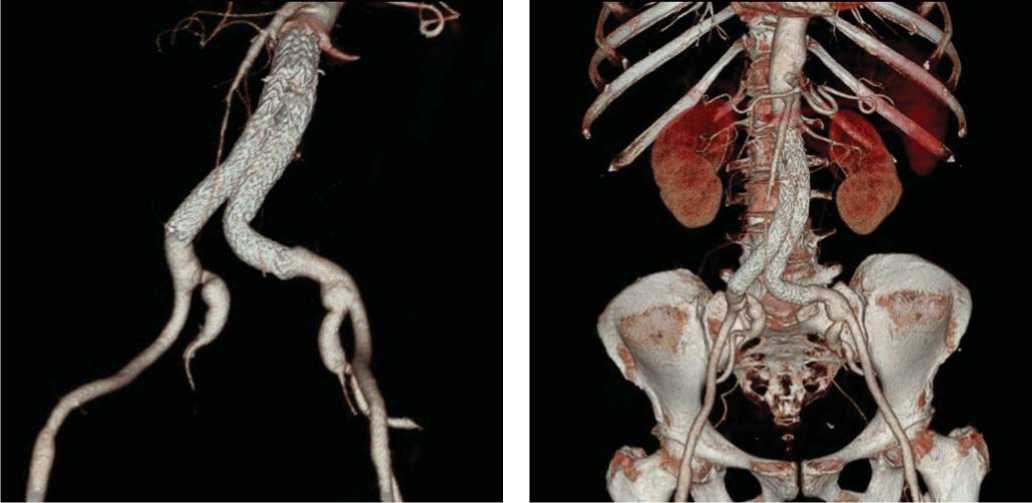
Рис. 2. КТ брюшной аорты после эндопротезирования Excluder через 3 мес. после операции
Заключение
Наш опыт применение методики эндопротезирования АБА EXLUDER Gore показал хорошие ближайшие и отдаленные результаты. Использование методики эндопротезирования АБА у пациентов с высоких риском открытого оперативного вмешательства позволило избежать тяжелых осложнений (в том числе кардиальных, дыхательных) в лечении аневризмы брюшной аорты. Данное вмешательство является методом выбора для лечения больных данной группы.
Совершенствование методики эндопротезирования, технических аспектов использования эндопротезов (применение фенестрированных эндопротезов, более совершенных элементов
Рис. 3. КТ брюшной аорты после эндопротезирования Excluder через 24 мес. после операции доставки эндопротеза и др.) способствует расширению показаний к применению данного вмешательства для лечения АБА. Накопление опыта эндопротезирования АБА способствует снижению осложнений (endoleak, миграция эндопротеза, увеличение аневризмы после операции) в ближайшем и отдаленном периоде, об этом свидетельствуют данные зарубежных центров, анализирующих результаты более 100 операций [1, 7, 8, 12].
Эндопротезирование АБА, несомненно, является перспективным направлением в лечении аневризм аорты. Дальнейшее изучение результатов оперативного лечения АБА методом эндопротезирования позволит снизить летальность и количество осложнений этого грозного заболевания.
Список литературы Эндопротезирование аневризм брюшной аорты как метод выбора у больных с высоким риском осложнений
- Lee W.A., Carter J.W., Upchurch G. et al. Perioperative outcomes after open and endovascular repair of intact abdominal aortic aneurysms in the United States during 2001//J. Vasc. Surg. 2004. Vol. 39 (3). P. 491-496.
- National Center for Health Statistics. National Vital Statistics Report 2002. 2002. Vol. 50 (16):14.
- Gillum R.F. Epidemiology of aortic aneurysm in the United States//J. Clin. Epidemiol. 1995. Vol. 48 (11). P. 1289-1298.
- Simoni G., Pastorino C., Perrone R. et al. Screening for abdominal aortic aneurysms and associated risk factors in a general population//Eur. J. Vasc. Endovasc. Surg. 1995. Vol. 10 (2). P. 207-210.
- Клиническая ангиология: Руководство/Под ред. А.В. Покровского. В двух томах. Т.2. М.: Медицина, 2004. 888 с.
- Спиридонов А.А., Аракелян В.С., Тутов Е.Г., Сухарева Т.В. Хирургическое лечение аневризмы брюшной аорты. М.: НЦССХ им. А.Н. Бакулева, 2005. 294 с.
- Schermerhorn M.L., O'Malley A.J., Jhaveri A. et al. Endovascular vs. open repair of abdominal aortic aneurysms in the Medicare population//N. Engl. J. Med. 2008. Vol. 358 (5). P. 464-474.
- EVAR trial participants. Endovascular aneurysm repair versus open repair in patients with abdominal aortic aneurysm (EVAR trial 1): randomized controlled trial//Lancet. 2005. Vol. 365 (9478). P. 2179-2186.
- Володось Н.Л., Карпович И.П., Троян В.И. и соавт. Новый метод лечения аневризм грудной, брюшной аорты и магистральных артерий с помощью самофиксирующегося синтетического протеза//Сб. науч. работ "Диагностика и хирургическое лечение аневризм аорты". Майкоп, 1992. C. 91-95.
- Parodi J.C., Marin M.L., Veith F.J. Transfemoral, endovascular stented graft repair of an of abdominal aortic aneurysms//Arch. Surg. 1995. Vol. 130 (5). P. 549-552.
- Покровский А.В. Состояние сосудистой хирургии в России в 2008 году. Российское общество ангиологов и сосудистых хирургов. М., 2009. С. 29
- Ghotbi R., Sotiriou A., Mansur R. New results with 100 Excluder cases//J. Cardiovasc. Surg. (Torino). 2010. Vol. 51 (4). P. 475-480.


