Эндопротезирование первого плюснефдлднгового сустава как один из методов лечения Hallux rigidus
Автор: Кавалерский Г.М., Сорокин А.А., Прохорова М.Ю.
Журнал: Московский хирургический журнал @mossj
Рубрика: Обзоры литературы
Статья в выпуске: 4 (32), 2013 года.
Бесплатный доступ
Статья представляет собой обзор литературных данных об этиологии, патогенезе, особенностях клинической картины и методах лечения Hallux rigidus. Отражены перспективы тотального эндопротезирования первого плюснефалангового сустава. Проанализированы результаты оперативного лечения 36 пациентов в ортопедическом отделении ГКБ № 67 г. Москвы с 2010 по 2012 года по поводу артроза первого плюснефалангового сустава 3 стадии. В 12 случаях выполнено тотальное эндопротезирование, в 24 - артродез первого плюснефалангового сустава. Полученные результаты показали, что для лечения hallux rigidus применение тотального эндопротезирования первого плюснефалангового сустава позволяет полностью устранить боль и восстановить движения в полном объеме.
Эндопротезирование, артродез
Короткий адрес: https://sciup.org/142211107
IDR: 142211107 | УДК: 61:796
Текст обзорной статьи Эндопротезирование первого плюснефдлднгового сустава как один из методов лечения Hallux rigidus
Задачи современной ортопедической хирургии в последние десятилетия значительно усложнились. Пациенты предъявляют более высокие требования к качеству и результатам лечения. Использование модельной обуви, гиподинамия и другие факторы обострили проблемы, связанные со сложными деформациями стоп [3]. В настоящее время ортопеды все чаще сталкиваются с проблемой дегенеративных заболеваний – артрозов первого плюснефалан-гового сустава [12]. Эти изменения в суставе происходят в результате нарушения обмена веществ в ткани хряща и недостаточной микроциркуляции крови в ней [15].
Актуальность проблемы диагностики и лечения hallux rigidus определяется высокой заболеваемостью и функциональной значимостью первого плюснефалангового сустава [1, 2]. В среднем от данной нозологии страдают примерно 15–18% населения [4]. Проблемы, вызываемые этим заболеванием, глобальнее, чем могли бы показаться. При ригидности первого плюснефалангового сустава, как следствие артроза, возникает боль и ограничение тыльного сгибания, что влечет за собой изменение плюснефаланговой оси, смещение точки опоры на наружные отделы стопы, а следовательно, и изменение биомеханической системы конечности со всеми вытекающими последствиями [7]. До сих пор при- чины возникновения деформирующего артроза до конца не выяснены, однако применительно к развитию hallux rigidus можно предположить большие и длительно действующие нагрузки, оказывающиеся для этого сустава чрезмерными, травмы и хронические микротравмы сустава, которые часто встречаются у спортсменов, переохлаждение стоп, ношение узкой сдавливающей обуви и т.п. [13]. Перечисленные факторы приводят к ухудшению кровообращения в первом плюснефаланговом суставе, что и ведет к развитию артроза [1, 4].
Наиболее типичными симптомами при артрозе первого плюснефалангового сустава являются боли в нем, некоторая отечность, умеренное покраснение и небольшое повышение температуры в области сустава [5, 17]. Движения в суставе обычно болезненные, ограничены, что проявляется прихрамыванием пациента при ходьбе [8].
Тактика лечения зависит от стадии процесса. В первую очередь необходимо обеспечить покой сустава, для чего применяется ортопедическая обувь и специальные стельки [9]. Лечение начинается с консервативных методов, которые включают применение нестероидных противовоспалительных препаратов, физиотерапевтические процедуры, местное введение стероидных препаратов в сустав, а также назначение препаратов, улучшающих обмен веществ в ткани суставного хряща [7, 16]. При неэффективности консервативного лечения ортопеды вынуждены применять хирургическую тактику. Оперативные методы лечения показаны больным с тяжелой (3 стадией) формой артроза первого плюснефалангового сочленения [3]. Основными оперативными методами лечения Hallux Rigidus является клиновидная остеотомия основной фаланги 1 пальца или шейки 1 плюсневой кости (Helfet, A., Lee D. 1980), операция Keller W. (1904), артродез 1 плюснефалангового сустава (Shereff M., Baumhauer J. 1988., McKeever, 1952.), хейлэктомия (Giannini S., Ceccarelli F., 2004; Mann R., Clanton O., 1988.). Однако большинство авторов отмечают, что резекционная артропластика дает положительный эффект лечения лишь при второй стадии заболевания [2].
В последнее время мнение ортопедов склоняется в пользу эндопротезирования, хотя эта проблема и остается спорной [11]. Показаниями к эндопротезированию первого плюсне-фалангового сустава являются не только Hallux Rigidus, но также идиопатический и посттравматический артроз, дегенеративный артроз, анкилоз сустава, постинфекционный артроз после полного санирования инфекции в кости [15]. Противопоказаниями к эндопротезированию первого плюс-нефалангового сустава являются альгодистрофия (системная рефлекторная дистрофия), остеопороз, занятие некоторыми видами спорта (бег, спортивная ходьба, теннис и т.д.), тяжелый физический труд, дистрофические изменения, ревматическая дезинтегративная деструкция сустава [12].
Несомненно, у эндопротезирования имеются определенные клинические преимущества: быстрое исчезновение болевых ощущений, сохранение и восстановление подвижности и отсутствие истирания сустава, а также оптимальная биосовместимость, бесцементная установка и простая хирургическая техника. Однако при выборе метода оперативного лечения обязательно следует учитывать противопоказания, особенно при эндопротезировании, и их немало [6]. Также пациент должен быть проинформирован о пределах возможной нагрузки на имплантат [11]. Необходимо помнить, что предельно допустимая нагрузка на имплантат не сопоставима с несущей способностью здоровой кости [3].
Принципиально эндопротезы для 1 плюснефалангового сустава делятся на связанные (Ti/Co-Cr/сталь и силиконовые спейсеры) и несвязанные (TiCoCr с полиэтиленовым вкладышем, пирокарбон и циркониевая керамика) [10]. Связанным эндопротезам характерны такие недостатки, как возникновение неправильных сил без амортизации [12]. Установка таких имплантов требует очень высокого качества кости [14]. При возникновении сил в каждом случае оказывают влияние дополнительные аксиальные силы тяги, которые в скором времени приводят к расшатыванию эндопротеза [18]. Силиконовые спейсеры выдерживают незначительные нагрузки, для них характерен достаточно бы-
Рис. 1. Связанный эндопротез (силиконовые спейсеры)

Рис. 2. Эндопротезы с парой трения керамика-керамика и полиэтилен-металл стрый износ материала [6, 19] (рис. 1).
Несвязанным эндопротезам присущи хорошая подвижность, способность выдерживать достаточные нагрузки, при их имплантации сохраняются структуры связок [5] (рис. 2). Так как эндопротез амортизирует нагрузки, происходит изменение направления сил и их перенос [6].
Целью нашего исследования стало улучшения результатов лечения пациентов, страдающих hallux rigidus , в связи с высокой частотой рецидивов и низкой удовлетворенностью результатами традиционного лечения (консервативное лечение, артродезирование, резекционная артропластика).
В данной работе представлены результаты лечения 36 пациентов (20 мужчин и 16 женщин) с hallux rigidus , находившихся в ортопедическом отделении ГКБ № 67 им. Л.А. Ворохобова ДЗ г. Москвы в период с 2010 по 2012 гг. Средний возраст пациентов составил 59,5 лет (минимальный возраст в группе пациентов 42 года, максимальный – 73). Для определения объема оперативного вмешательства проводили тщательное предоперационное планирование. Всем пациентам была произведена рентгенография обеих стоп, включая рентгенографию с нагрузкой и боковую проекцию оперированной стопы. Контроль осуществляли через 12 месяцев после операции. Отчет был сделан для каждой стопы с использованием истории болезни, шкалы Kitaoka [20], клинического и плантоскопического метода, рентгенографии перед операцией и контроля после. Эти данные включали в себя протоколы операций, осложнения и субъективные ощущения пациентов. Для субъективной оценки боли в раннем и отдаленном послеоперационном периоде использовалась визуально-аналоговая шкала боли (ВАШ).
Всего было установлено 12 тотальных эндопротезов первого плюснефалангового сустава, 4 из которых – с парой трения металл-полиэтилен Total Toe System (производства компании «Биомет»), и 8 – керамика-керамика MOLANA фирмы MOJE. При выборе эндопротеза предпочтение отдавали моделям несвязанного типа в связи с их подвижностью, способностью выдерживать достаточные нагрузки, сохранением структуры связок при имплантации. Из суще- ствующих видов несвязанных эндопротезов циркониевая керамика обладает рядом преимуществ, таких как хорошая способность врастания, отсутствие износа и реакций отторжения.
Операции выполняли под спинальной анестезией в положении пациентов на спине. Производили дорсомеди-альный разрез с отсепаровыванием капсулы сустава. Выполняли резекцию основания основной фаланги первого пальца стопы толщиной около 4 мм под углом 90 градусов. При сращении сесамовидных костей с первой плюсневой костью выполняли мобилизацию с помощью желобоватого долота. По шаблону выполняли резекцию головки 1 плюсневой кости, и на данном этапе подбирали правильный размер импланта. В каналы основной фаланги первого пальца и первой плюсневой кости по направителю и под контролем ЭОП устанавливали спицу Киршнера и рассверливали с помощью канюлированного сверла до метки. Вновь сформированный дистальный канал уплотняли под соответствующий размер ножки импланта. При необходимости использовали режущую поверхность компактора, позволяющую увеличить размер сформированного канала. Импактором устанавливали проксимальный компонент эндопротеза. С помощью пробного размера проверяли размер резекции, и в случае необходимости проводили дополнительный опил. Далее проводили ступенчатое уплотнение ложа импланта с помощью компактора. Устанавливали дистальный компонент. Важно обращать внимание на скошенность суставной поверхности: головка импланта должна указывать на подошвенную поверхность. Производили вправление сустава с ушиванием капсулы и наложением кожных швов. Гипсовую иммобилизацию не проводили, пациенты передвигались со следующего дня после операции без помощи костылей. Сложность послеоперационной реабилитации заключается в том, что, с одной стороны, нужно восстановить движения в оперированном суставе, с другой – избежать расшатывания эндопротеза или его частей, которые могут потерять свою функцию из-за больших или чрезмерных нагрузок. В послеоперационном периоде движения в суставе начинали в первый же день после операции сразу после удаления дренажа с помощью двигательной шины, позволяющей осуществлять безболезненное движение в диапазоне от исходной точки до 30 градусов включительно в плантарном направлении, и до 55 градусов – при дорсальной флексии. Активизацию начинали со второго дня после операции, при этом использовали специальную разгрузочную обувь, которую больной должен был носить в течение 4-х недель. Подъем по лестнице разрешали с 3-го дня после операции. Через две недели после операции проводили самомобилизацию согласно инструкциям (при необходимости). Через четыре недели разрешали осторожную ходьбу в твердой широкой стандартной обуви. После 6 недель проводили рентген-контроль, и при благоприятном течении разрешали полную нагрузку. Последующий рентген-контроль проводили через полгода после операции, и затем ежегодно. Перед операци-
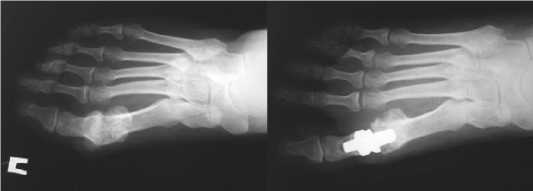
Рис. 3. Клинический пример ей пациента следует ознакомить с возможными специфическими рисками: риск просадки имплантата, расшатывания имплантов, повреждения в области комплекса сесамовидных костей, переломов протезов из-за образования моноклинного циркония, чрезмерных нагрузок вследствие большого спорта.
24 пациентам, отказавшимся от предложенного тотального эндопротезирования первого плюснефалангового сустава, за этот же временной период в клинике было выполнено оперативное лечение в объеме артродеза первого плюснефалангового сустава. Операцию выполняли под пневматическим кровоостанавливающим жгутом, наложенным в средней трети голени. Разрезом по медиальной поверхности стопы от плюснефалангового до плюснекли-новидного суставов осуществляли доступ к медиальной поверхности I плюсневой кости и прилежащим суставам. Выкраивали треугольный лоскут из медиального отдела капсулы плюснефалангового сустава, по линии Гейбаха выполняли резекцию экзостоза головки I плюсневой кости. Через разрез в I межплюсневом промежутке осуществляли доступ к латеральной поверхности плюснефалангового сустава и выполняли его латеральный релиз (выделяли и пересекали сухожилие поперечной головки мышцы, приводящей большой палец, рассекали капсулу сустава над латеральной сесамовидной косточкой, выполняли мобилизацию сесамовидного комплекса). Из медиального доступа вскрывали I плюснефаланговый сустав, освобождали суставные концы плюсневой и основной фаланги 1 пальца. Осцилляторной пилой резецировали суставной хрящ основания фаланги вместе с субхондральной пластинкой, выполняли резекцию головки плюсневой кости так, чтобы плоскость резекции была обращена вверх под углом 10 градусов. Фиксацию плюснефалангового сустава проводили 2 винтами Барука. Раны послойно ушивали наглухо. Послеоперационная реабилитация этой группе больных проводилась стандартно согласно общим рекомендациям.
В первой группе (эндопротезирование) у всех пациентов уже в раннем послеоперационном периоде наблюдался незначительный болевой синдром (0–2 баллов по ВАШ), восстановление объема движений и исправление деформации пальцев. Ранний послеоперационный период лишь у одного пациента с сопутствующей соматической патологией (сахарный диабет 2 типа, среднетяжелого течения, ожирение 2 ст.) осложнился развитием краевого кожного некроза. В послеоперационном периоде через 12 месяцев мы наблюдали удовлетворительные результаты оперативного лечения (до 98 баллов по шкале Kitaoka), что подтверждалось субъективным мнением пациентов и объективным клиническим обследованием. Болевой синдром был полностью купирован. Движения в суставе восстановлены в полном объеме у всех пациентов этой группы.
Во второй группе пациентов (артродез) в раннем послеоперационном периоде во всех случаях отмечался выраженный болевой синдром (5–7 баллов по ВАШ). В отдаленном периоде болевой синдром сохранялся у 30% пациентов, движения в суставе отсутствовали (76 баллов по шкале Kitaoka). В процессе отсроченного наблюдения только в 1 случае избыточная резекция головки привела к возникновению серьезной проблемы – ятрогенного варусного отклонения первого пальца, которое в дальнейшем потребовало хирургической коррекции. У трети пациентов имелись проблемы в подборе обуви (требовалось использование индивидуальных ортопедических изделий).
Несмотря на небольшое количество операций, в выборе хирургической тактики лечения, проводимых при Hallux rigidus , сохраняются разногласия относительно показаний к той или иной операции. Эндопротезирование первого плюснефалангового сустава – технически более требовательная операция, чем артродез, и требует тщательного планирования и специальной подготовки. Тем не менее, установка эндопротеза является единственным методом, позволяющим достоверно устранить болевой синдром и восстановить амплитуду движений в полном объеме. С целью подтверждения трибологических характеристик керамических протезов необходимо проведение дальнейших исследований. В свою очередь, для верификации повышенной износостойкости эндопротезов несвязанного типа (по сравнению с протезами полусвязанного типа) также необходим больший материал и сроки исследований.
Таким образом, среди известного множества операций по лечению артроза первого плюснефалангового сустава, операции Шеде-Брандеса и варианты резекции головки первой плюсневой кости, по своей сути, являются калечащими, так как лишает стопу адекватной опороспособности и по результатам отдаленных исследований не решают данной проблемы. Нельзя не отметить, что внедрение технологии эндопротезирования позволило уменьшить число осложнений и неудовлетворительных исходов лечения. Так как основной целью хирургического вмешательства при Hallux rigidus является улучшение качества жизни пациента, тотальное эндопротезирование представляется перспективой развития в оперативном лечении артроза плюснефаланго- вого сустава 3 стадии, требующей детального клинического изучения.
Список литературы Эндопротезирование первого плюснефдлднгового сустава как один из методов лечения Hallux rigidus
- Альбрехт, Г.А. К патологии и лечению hallucis valgi//Русский врач. 1911. Т. 10, № 1. С. 14-19.
- Васильев Н.А., Левченко В.О. Некоторые новые данные рентгенодиагностики поперечной распластанности переднего отдела стопы//Вестник рентгенологии и радиологии. 1984. № 3. С. 42-45.
- Карданов А.А. Оперативное лечение деформаций и заболеваний костей и суставов первого луча стопы. 2009. С. 1-7.
- Кузьмин В.И. Оперативное лечение больных с поперечным плоскостопием, Hallux Valgus: проектирование медицинского технологического процесса//Вестн. травматологии и ортопедии им. Н.Н. Приорова. 2003. № 1. С. 67-71.
- Мастер-класс по мелким суставам кисти и стопы «История и современные технические возможности эндопротезирования мелких суставов». Новосибирск: НИИТО, 2010.
- Пахомов И.А., Прохоренко В.М. Результаты хирургического лечения пациентов с поражениями 1 плюснефалангового сустава. Новосибирск, 2010.
- Юсевич, Я.С., Кисельков, А.В. Оперативная стабилизация скелета переднего отдела стопы при поперечном плоскостопии//Ортопедия, травматология и протезирование. 1966. № 6. С. 39-44.
- Coetzee C. The Lapidus procedure as salvage after failed surgical treatment of hallux valgus//J. Bone Jt. Surg. 2004. Vol. 86-A, № 1. P. 30-36.
- Couglhlin M.J. Juvenile hallux valgus: etiology and treatment (R. A. Mannaward)//Foot Ankle Int. 1995. Vol. 16, № 11. P. 682-697.
- David N. Townshend, Magdi Greiss, West Cumberland Hospital, Whitehaven, Cumbria UK (15.-18.09.2005 IFFAS Neapel)
- Dieter Werner//The Foot. 2001. Vol. 11. P. 24-27 (altes Implantat screw-fit).
- Ferrari J. A radiographic study of the relationship between metatarsus adductus and hallux valgus//Foot Ankle Surg. 2003. Vol. 42, № 1. P. 324-331.
- Faber F. Role of first ray hypermobility in the outcome of the Lapidus procedure//J. Bone Jt. Surg. 2004. Vol. 86-A, № 3. P. 486-495.
- Fadel G., Scripada S., Abbound R.J., Jain A.S. UK, 5th Congress of the EFAS in Montpellier, 2004.
- Grebing B. Evaluation of Morton's theory of second metatarsal hypertrophy//
- Omonbude O.D., Faraj A.A. Altrdale General Hospital, West Yorkshire UK//The Foot. 2004. Vol. 14. P. 204-206.
- Patrick Laing, Malviva, Makawana. UK 5th Congress of the EFAS in Montpellier, 2004.
- Talal Ibrahim, Grahame John Saint Clair Taylor Glenfield Hospital, Leicestrer UK//The foot. 2004. Vol. 14. P. 124-128.
- J. Bone Jt. Surg. 2004. Vol. 86-A, № 7. P. 1375-1386.
- Kitaoka H.B., Alexander I.J., Adelaar R.S., Nunley J.A., Myerson M.S., Sanders M. Clinical rating systems for the ankle-hindfoot, midfoot, hallux, and lesser toes//Foot Ankle Int. 1994. Vol. 15. P. 349-353.


