Эндоскопический эндоназальный транссфеноидальный доступ к краниофарингиомам
Автор: Матмусаев М.М., Кариев Г.М., Якубов Ж.Б., Асадуллаев У.М., Такеучи К., Сайто Р.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Клинические наблюдения
Статья в выпуске: 4 т.18, 2023 года.
Бесплатный доступ
Введение: Лечение краниофарингиом является сложной проблемой из-за их анатомического расположения. Расширенный эндоскопический эндоназальный транссфеноидальный доступ (РЭЭТД) показан при селлярных, супраселлярных, некоторых интравентрикулярных новообразованиях у взрослых и детей. Описание наблюдения: Больному 51 год. Он госпитализирован с жалобами на снижение зрения. Предоперационные КТ и МРТ продемонстрировали в основном солидное образование в супраселлярной области. Больному произведена РЭЭТД. Послеоперационное состояние у больного прошло без осложнений. Г истопатологический диагноз показал адамантоматозную краниофарингиому. Послеоперационная КТ, МРТ с контрастным усилением и без него демонстрируют тотальное удаление опухоли.
Эндоскопический транссфеноидальный доступ, краниофарингиомы, функции гипофиза, зрительные нарушения
Короткий адрес: https://sciup.org/140303488
IDR: 140303488 | DOI: 10.25881/20728255_2023_18_4_146
Endoscopic endonasal transsphenoidal approach to craniopharyngiomas
Introduction: The treatment of craniopharyngiomas is challenging due to their anatomical location. The extended endoscopic endonasal transsphenoidal surgery (EEETS) is indicated for sellar, suprasellar, and some intraventricular tumors in adults and pediatric patients. Case presentation: A 51-year-old male with visual disturbances was admitted to our hospital. Preoperative computed tomography (CT) and magnetic resonance imaging (MRI) demonstrated mainly a solid mass in the suprasellar region. The patient underwent EEETS. The patient’s postoperative course was uneventful. Histopathological diagnosis demonstrated adamantomatous craniopharyngioma. Postoperative CT, MRI with and without contrast enhancement demonstrated total removal of the tumour.
Текст научной статьи Эндоскопический эндоназальный транссфеноидальный доступ к краниофарингиомам
Краниофарингиомы (КФ) представляют собой одно из наиболее сложных опухолевых образований в нейрохирургии. Из-за критической расположенности рядом с важными нейроваскулярными структурами, операция является сложной и требует глубокого понимания анатомии супраселлярной области [1].
КФ — доброкачественные эпителиальные опухоли селлярной области, происходящие из остатков кармана Ратке. ВОЗ относит их к новообразованиям I степени [2]. Папиллярная форма встречается исключительно у взрослых, а ада-мантиноматозный подтип — в основном у детей [3; 4]. Наблюдается бимодальное возрастное распределение заболеваемости КФ с большей амплитудой в детском возрасте. Однако прогноз этих опухолей в первую очередь зависит от характера роста. Для планирования операции важна протяженность опухоли по отношению к зрительному нерву, гипофизу и его стеблю, гипоталамусу, сонной артерии и комплексу передних мозговых артерий, а также расположение опухоли по отношению к турецкого седлу и диафрагме. Помимо размеров опухоли и ее мульти-лобулярности с солидным и кистозным компонентами, значительный интерес представляет наличие или отсутствие распространения поражения на третий желудочек и его связь с ним. Для решения проблемы выбора правильной хирургической тактики в каждом конкретном случае параллельно с техническим прогрессом инструментария и оборудования в хирургическую практику были перенесены разнообразные топографические и клинические классификации КФ [3; 5–8]
РЭЭТД используется в течение последних 15 лет [9; 10]. Он обеспечивает прямой доступ к очагам поражения в супраселлярном, ретроселлярном и ретрокливальном отделах, что позволяет избежать обширной краниотомии и уменьшить осложнения, связанные с тракцией паренхимы мозга. Мы описываем хирургическую технику удаления КФ с помощью РЭЭТД.

Описание наблюдения
Мужчина, 51 год, поступил в клинику с нарушением зрения, которое продолжается на протяжении 7 месяцев. Офтальмологическое обследование показало остроту зрения 0,1 на обоих глазах. При обследовании поля зрения была выявлена битемпоральная гемианопсия (Рис. 1). Лабораторное исследование показало, что уровень гормонов гипофиза находится в пределах нормы. Предоперационная КТ и МРТ с контрастным усилением показали наличие образования диаметром 23 мм, в основном солидного, без кальцификатами в супраселлярной областях. Опухоль не инвазировала в кавернозный синус (Рис. 2). Поражение преимущественно локализовалось в супраселлярной области, и помимо аденомы гипофиза рассматривалась краниофарингиома в качестве возможного дифференциального диагноза. Учитывая большие размеры опухоли в супраселлярной области, был запланирован РЭЭТД как вариант прямого доступа к поражению.
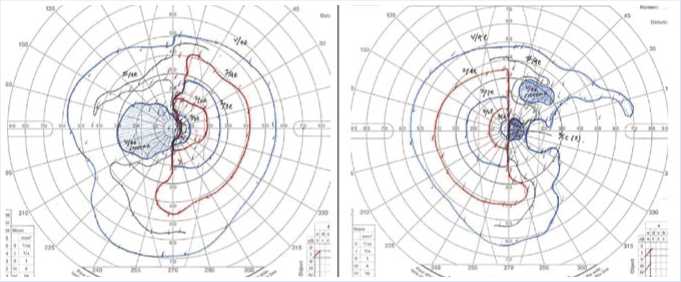
Рис. 1. При исследовании поля зрения были выявлены его дефекты в виде битемпоральной гемианопии.
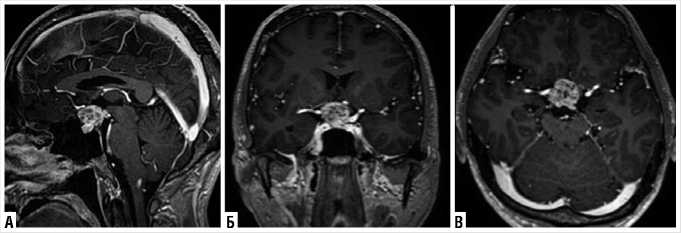
Рис. 2. Предоперационная МРТ головного мозга. A–В — МРТ с контрастным усилением демонстрирует солидную супраселлярную краниофарингиому.
Хирургическая техника
Назальный и сфеноидальный этап
Под общей анестезией пациента поместили в положение лежа с жесткой фиксацией головы с использованием скобы «Сугита» (Mizuho Medical Innovation, Токио). Голова была слегка повернута вправо, а верхняя часть туловища была поднята на 15 градусов. Нос и ноздри подготавливаются бетадином, а носовая полость заполняется пропитанными эпинефрином (1:1000) тампонами.
С помощью жесткого эндоскопа с пневматическим держателем выполнялся вертикальный разрез слизистой оболочки носовой перегородки. Проводилась подслизистая диссекция, и кость носовой перегородки была удалена. Используя подслизистый коридор, можно было достичь сфеноидальную пазуху с минимальными повреждениями интраназальных структур. Широкая сфенои-дотомия является ключевым моментом в данной операции, для получения со-ответствующеего хирургического поля, поэтому требовалось удалить достаточный объем передней стенки и перегородки сфеноидального синуса. Следующим этапом является трепанация турецкого седла (sellar floor), бугорок седла (tuberculum sellae) и площадки (planum sphenoidale) основной кости. Также трепанируется медиальный оптикокаротидный карман (medial optico-carotid recess) (Рис. 3).
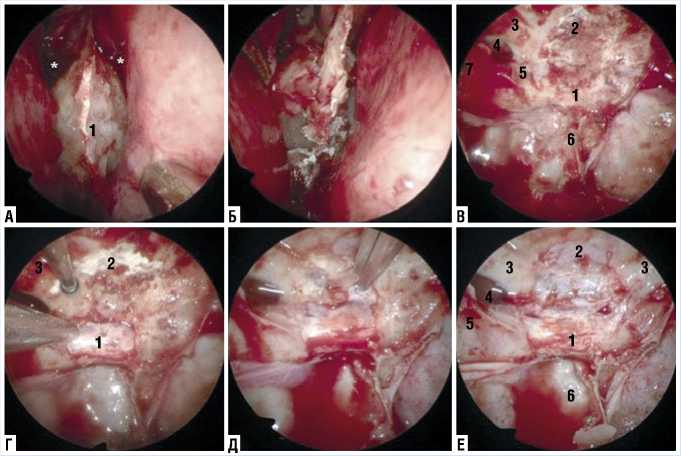
Рис. 3. Интероперационное фото. Этап сфеноидотомии и удаления костных структур. А — после резекции носовой перегородки. * — sphenoid ostium (соустья основной пазухи). 1 — передняя стенка основной пазухи. Б — передняя стенка основной пазухи резецируется и удаляется с использованием микродрели и костных кусачек. B — после сфеноидотомии и удаления межпазушных перегородок, мы можем выделить анатомические ориентиры основной пазухи: 1 — дно турецкого седла, 2 — площадка основной кости, 3 — костный выступ правого канала зрительного нерва, 4 — латеральный оптико-каротидный карман, 5 — медиальный оптико-каротидный карман, 6 — скат, 7 — костные выступы внутренних сонных артерий. Г–Е — трепанация дна турецкого седла и площадки основной кости. Данные костные структуры с помощью микродрели трепанируются до толщины «яичной скорлупы» (eggshell), а затем удаляются кусачками Керрисона. 1 — дно турецкого седла, 2 — площадка основной кости, 3 — костные выступы канала зрительных нервов, 4 — латеральный оптико-каротидный карман, 5 — костные выступы внутренних сонных артерий, 6 — скат.

Вскрытие твердой мозговой оболочки и резекция опухоли
Далее проводился разрез твердой мозговой оболочки (ТМО) в форме обратной буквы «Т», что облегчало раскрытие краев ТМО и позволило более удобно приблизить и ушивать. При расширенном транссфеноидальном доступе рассечение верхнего межкавернозного синуса часто сопровождался венозным кровотечением, которое устранялось путем нанесения двойного узлового шва на синус. Для расширения обзора параселлярных структур, наложенные нити на ТМО подвешивают к внешней стороне ноздри, чтобы расширить операционное поле (Рис. 4 А).
В турецком седле находился гипофиз, а в супраселлярной области была обнаружена опухоль, покрытая арахноидальной оболочкой. Диссекции опухоли от арахноидеи. Верхняя гипофизарная артерия (ВГА), питающая хиазму, была диссектирована от опухоли и сохранена. Питающие артерии опухоли от ВГА коагулированы биполярной электрока-утеризацией и рассечены. Сначала была выполнена внутренняя декомпрессия опухоли. После достаточной декомпрессии опухоль была отделена от хиазмы (Рис. 4 Б–Д). Удаление продолжалась путем повторения периферической диссекции и внутренней декомпрессии. Под опухолью и с левой стороны был обнаружен стебель.Опухоль частично инва-зировала в стебель, который тщательно был диссецирован с помощью микродиссекторов и микроножниц (Рис. 4 Е). После адекватной диссекции окружающих тканей и внутренней декомпрессии, опухоль стала подвижной. Верхняя поверхность опухоли была полностью отделена от серого бугора (tuber cinereum), мобилизирована, и стали видны сосцевидные тела (mammillary bodies). После тщательного иссечения перфораторов опухоли с сохранением жизненно важных нейроваскулярных структур была выполнена тотальная резекция опухоли, верифицирован окончательный гемостаз (Рис. 4 Ё–З).
Реконструкция дефектов основания черепа
После удаления опухоли, дефект ТМО закрывали с использованием коллагенового матрикса (DuraGen®; Integra LifeSciences, Plainsboro, NJ, USA) (Рис. 2 K, L), который укладывали интрадурально (трансплантат «inlay») и затем непрерывно сшивали по методу «Модифицированные ботинки с шнур-
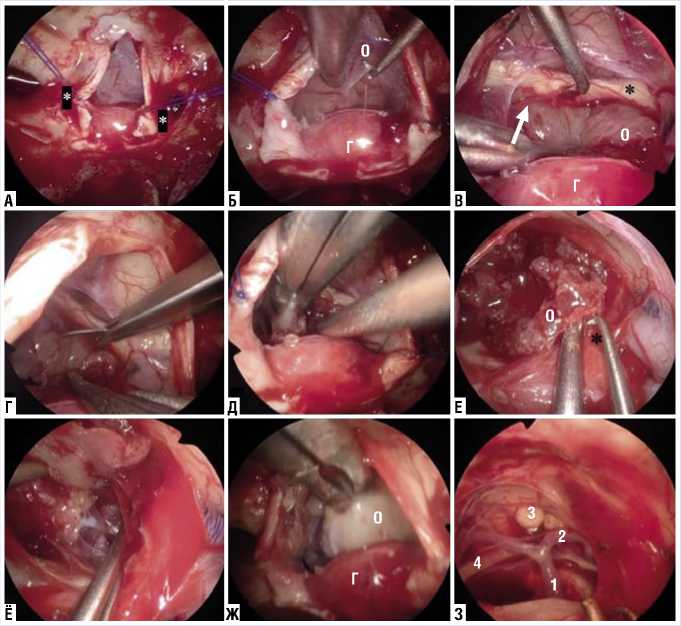
Рис. 4. Интероперационное фото. Этап вскрытия твердой мозговой оболочки (ТМО) и удаление краниофарингиом. А — ТМО вскрыта в форме обратной буквы «Т» и наложен двойной узловой шов на верхний межкавернозный синус. Наложенные нити на ТМО подвешивают к внешней стороне ноздри, чтобы расширить операционное поле. * — верхней межкавернозный синус. Б — обнаружены опухоли и гипофиз, который диссецирован из арахноидеи. Г — гипофиз, О — опухоль. В — отделение опухоли от верхней гипофизарной артерии (ВГА), хиазмы и зрительного нерва. Г — гипофиз, О — опухоль, * — зрительный нерв и хиазма, стрелка — ВГА. Г, Д — внутренняя декомпрессия и удаление опухоли, производились по частям с помощью щипцов. Е — отделение опухоли от стебелья. О — опухоль, * — стебель. Ё, Ж — после внутренней диссекции, опухоль отделялся от tuber cinereum и была полностью удалена. З — выявлена базиларная артерия, задняя мозговая артерия, верхняя мозжесковая артерия, третий черепно-мозговой нерв и сосцевидные тела. 1 — базиларная артерия, 2 — задняя мозговая артерия, 3 — сосцевидные тела, 4 — третий черепно-мозговой нерв.
Результаты
У больного не наблюдалась послеоперационная назальная ликворея. Значительно улучшились зрительные нарушения, включая остроту зрения (Vis OD = 0,9 OS = 0,8) и дефицит поля зрения (Рис. 6). Функции передней доли гипофиза полностью сохранены. После операции наблюдался легкий несахарный диабет (НД), который лечили пероральным введением антидиуретического гормона вазопрессина. Гистопатологический диагноз: адамантоматозная КФ. Послеоперационная КТ, МРТ с контрастным усилением и без него демонстрируют полное удаление опухоли (Рис. 7 A–Г). В течении 24-месячного послеоперационного периода рецидивов не было.
Обсуждение
Преимущества и недостатки РЭЭТД
Расширенная эндоназальная доступ обеспечивает прямой и безопасный путь к базальным структурам мозга, таким как ретрохиазматическая область, инфундибулум, дно третьего желудочка и верхний отдел межпедун-
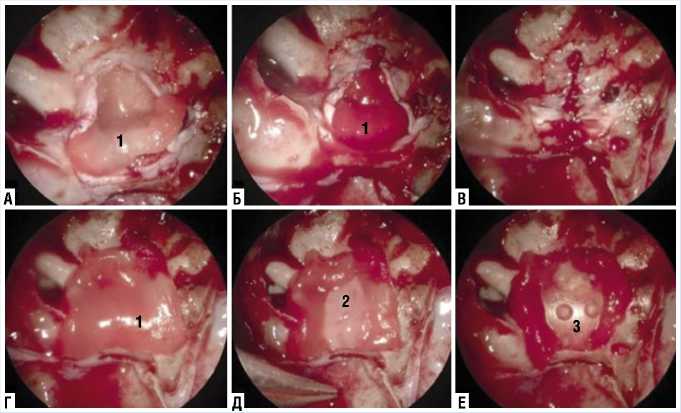
Рис. 5. Интероперационное фото. Реконструкция основания черепа. А–В — коллагеновую матрицу (Duragen) поместили субдурально (inlay collagen matrix) и зашивали методом «shoelace technique». Г — другой коллагеновый матрикс (onlay collagen matrix) устанавливается эпидурально в качестве накладного трансплантата и фиксируется путем помещения его краев под окружающую кость. Д — на коллагеновую матрицу «onlay» укладывается септальная кость. Е — затем выполняется жесткая реконструкция с использованием рассасывающейся фиксирующей сетки. 1 — коллагеновый матрикс, 2 — септальная кость, 3 — рассасывающейся фиксирующая сетки.
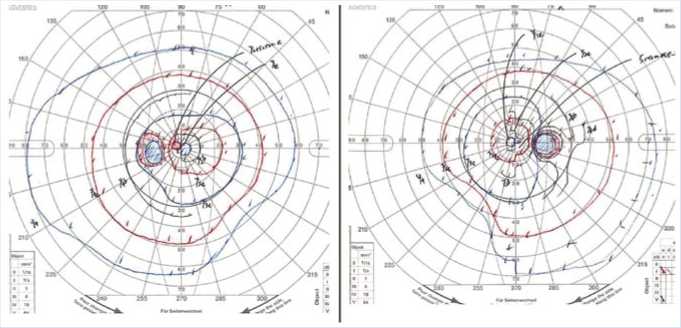
Рис. 6. Послеоперационное поле зрения показало улучшение битемпоральной гемианопии.
кулярной цистерны, представляющим собой основные зоны распространения КФ. Слепые зоны, которые трудно визуализировать при транскраниальном доступе, непосредственно и широко визуализируются снизу, что позволяет лучше контролировать такие важные нейроваскулярные структуры, как нижний аспект зрительного аппарата, мам-миллярные тела, дно и боковые стенки третьего желудочка, а также перфорирующие артерии от базилярной артерии. Анатомическими ограничениями РЭЭТД является, прежде всего, область латеральнее супраклиновидных сонных артерий, куда иногда могут распростра- няться КФ и которая не может быть достаточно безопасно достигнута эндоназальным путем. Вторым ограничением является ограниченная доступность ретроселлярного область, находящегося за спинкой турецкого седла (dorsum sellae). Это пространство можно визуализировать с помощью угловых эндоскопов, но из-за наличия гипофиза и костных структур спинки турецкого седла и задних накланенных отросков (posterior clinoid’s) его доступность ограничена. Еще одним ограничением эндоскопического подхода являются чисто интравентрикулярные КФ (КФ типа IV по Kassam et al) [7].
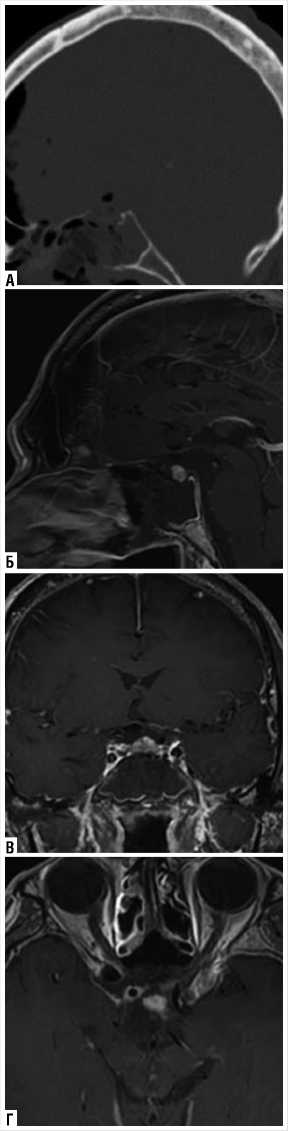
Рис. 7. Послеперационная КТ и МРТ головного мозга. А — сагиттальное КТ-изображение демонстрирует адекватное удаление кости из planum sphenoidale (площадка основной кости), tuberculum sallae (бугорка ту-рецкого седла), а также sellar floor (передней стенки турецкого седла) при рас-ширенном эндоскопическом эндоназальном транссфеноидальном доступе. Б–Г — послеоперационная МРТ с контрастным усилением демонстрирует тотальную резекцию краниофарингиомы.
Степень резекции опухоли
Концепция хирургии КФ характеризуется первоначальной внутренней декомпрессией опухоли и выявлением границы раздела между опухолью и прилежащими анатомическими структурами, особенно гипоталамусом, который часто представляет собой лишь тонкую бумажную мембрану [7; 9]. Неоднородное распространение опухоли, прикрепление или инфильтрация жизненно важных окружающих нейроваскулярных структур не позволяют провести явную линию иссечения, что затрудняет полную резекцию и потенциально опасно для жизненно важных областей мозга. Показатели тотальной резекции при различных доступах в литературе варьируют от 16% [12] до 90% [13]. Хотя Ya^argil и соавт. [13] сообщили о 90% частоте тотальной резекции, основывая этот показатель только на впечатлениях хирурга, поскольку послеоперационная МРТ в большинстве случаев была недоступна. Кроме того, интраоперационная/ранняя послеоперационная летальность составила 9%, а общая летальность — 16,7%. Yang и соавт. [14] обнаружили, что независимо от подхода, общий процент резекции после операции по поводу КФ составляет 58%. Koutourousiou и соавт. [15] в своей серии случаев добился общей частоты тотальной резекции — всего 37,5%. Однако тотальная резекция не считалась безопасной и, как следствие, выполнялась не у всех пациентов.
Основным ограничением при проведении тотальной резекции является наличие гипоталамической инвазии, которую можно определить как отсутствие хирургической плоскости (surgical plane) между опухолью и гипоталамусом. Это представляет собой важный предиктор послеоперационной инвалидизации и смертности [16], поскольку поддержание качества жизни после операции остается приоритетом. Если тотальная резекция опухоли не достигнута, рассматривается возможность проведения адъювантной лучевой терапии, такой как фракционированная лучевая терапия, радиохирургия или протонно-лучевая терапия. Эти методы лечения могут улучшить контроль над заболеванием. Субтотальная резекция в сочетании с лучевой терапией также может рассматриваться для сохранения оси гипофиза, хотя вопрос профилактики рецидивов остается спорным [17].
Решение о сохранении или пожертвовании стебля гипофиза принимается во время операции. Если у пациента до операции имеется нормальная функция гипофиза, то важно максимально со- хранить её [9]. Однако, при КФ трансинфундибулярного типа сохранение стебля гипофиза часто невозможно, так как опухоль инфильтрирует эту область [7].
Зрительные результаты
Нарушение зрения является наиболее частым симптомом КФ. В серии случаев, проведенной Mou и соавт. [18], было замечено, что после использования эндоназального эндоскопического доступа зрение улучшилось у 88.5% пациентов. Аналогичные показатели улучшения зрения, варьирующиеся от 75% до 90,2%, были отмечены в группе пациентов с КФ, которых пролечены с использованием эндоскопического эндоназального доступа в последние годы [15; 19; 20]. Другие исследования подтверждают, что этот доступ хирургического вмешательства дает лучшие результаты в восстановлении зрения по сравнению с традиционной краниотомией, и при этом снижает вероятность развития новых дефектов зрения [21; 22]. Использование эндоскопической эндоназальной хирургии для удаления опухоли основания черепа обеспечивает более эффективную декомпрессию хиазмы и уменьшает риск непосредственного повреждения хиазмы и поражения сосудистых перфораторов.
Эндокринологические результаты
По сравнению с транскраниальной операцией, для резекцией КФ, эндоназальный эндоскопический доступ также сопровождается проблемами в улучшении и сохранении нейроэндокринной функции [23; 24], и в этом контексте он не предоставляет существенных изменений [15; 25]. По данным Gardner et al., после транскраниальных операций у 24–66% пациентов наблюдается пангипопитуитаризм, а несахарный диабет встречается у 43–79% пациентов. В то же время, после транссфеноидальных операций пангипопитуитаризм отмечается у 18–67% пациентов, а несахарный диабет — у 8–48% [26].
Для пациентов, у которых есть шанс сохранить стебель гипофиза, Sasaki et al предполагают, что при хирургическом лечении КФ, двустороннее сохранение pSHA Ib (primary superior hypophyseal artery infundibular branch) благоприятно влияет на результат послеоперационной функции передней доли гипофиза [27].
Послеоперационая назальная ликворея
Послеоперационная назальная ликворея представляет собой одно из основных осложнений расширенной эндоскопической транссфеноидальной хирургии, которое может привести к серьезным осложнениям, таким как менингит. Адекватная реконструкция основания черепа имеет важное значение для предотвращения послеоперационной назальной ликвореи и связанных с ней жизнеугрожающих осложнений. Сообщалось о нескольких методах реконструкции основания черепа, направленных на предотвращение этого осложнения, включая «gasket seal» [28], васкуляризированный назасептальный флап [29].
Согласно некоторым авторам, ушивание ТМО считается наиболее безопасным и эффективным методом реконструкции основания черепа [11; 30; 31]. Метод непрерывного и плотного ушивания ТМО при реконструкции основания черепа эффективен и обычно не требует дополнительных процедур, таких как установка люмбального дренажа и на-зосептального флапа [32].
Заключение
Внедрение расширеннего эндоскопического эндоназального транссфеноидального доступа представляет собой значительное улучшение в лечении КФ. Панорамный обзор, обеспечиваемый эндоскопией и использование угловой оптики позволяют удалять поражения, распространяющиеся в супраселлярной области. На основании полученных результатов эндоскопическая эндоназальная хирургия может рассматриваться как альтернатива транскраниальной хирургии при лечении КФ.
Авторы заявляют об отсутствии конфликта интересов (The authors declare no conflict of interest).
Список литературы Эндоскопический эндоназальный транссфеноидальный доступ к краниофарингиомам
- Матмусаев М.М., Якубов Ж.Б., Асадуллаев У.М., и др. Современные аспекты хирургического лечения больных с краниофарингиомами головного мозга (обзор литературы) // Неврология. – 2022. – №1(89). – С.41-44. [Matmusaev MM, Yakubov JB, Asadullaev UM, et.al. Modern aspects of surgical treatment of patients with craniopharyngiomas (literature review). Neurology. 2022; 1(89): 41-44. (In Russ.)]
- Louis DN, Ohgaki H, Wiestler OD, et al. The 2007 WHO classification of tumours of the central nervous system. Acta Neuropathol. 2007; 114(2): 97-109. doi: 10.1007/ s00401-007-0243-4.
- Adamson TE, Wiestler OD, Kleihues P, et.al. Correlation of clinical and pathological features in surgically treated craniopharyngiomas. J Neurosurg. 1990; 73(1): 12-17. doi:10.3171/jns.1990.73.1.0012.
- Larkin SJ, Ansorge O. Pathology and pathogenesis of craniopharyngiomas. Pituitary. 2013; 16(1): 9-17. doi:10.1007/s11102-012-0418-4.
- Fukushima T, Hirakawa K, Kimura M, et al. Intraventricular craniopharyngioma: its characteristics in magnetic resonance imaging and successful total removal. Surg Neurol. 1990; 33(1): 22-27. doi: 10.1016/0090-3019(90)90220-j.
- Hoffman HJ, De SM, Humphreys RP, et al. Aggressive surgical management of craniopharyngiomas in children. J Neurosurg. 1992; 76(1): 47-52.
- Kassam AB, Gardner PA, Snyderman CH, et al. Expanded endonasal approach, a fully endoscopic transnasal approach for the resection of midline suprasellar craniopharyngiomas: a new classification based on the infundibulum. J Neurosurg. 2008; 108(4): 715-728. doi: 10.3171/JNS/2008/108/4/ 0715.
- Pascual JM, González-Llanos F, Barrios L, et al. Intraventricular craniopharyngiomas: topographical classification and surgical approach selection based on an extensive overview. Acta Neurochir (Wien). 2004; 146(8): 785-802. doi: 10.1007/s00701-004-0295-3.
- Baldauf J, Hosemann W, Schroeder HW. Endoscopic Endonasal Approach for Craniopharyngiomas. Neurosurg Clin N Am. 2015; 26(3): 363-375. doi: 10.1016/j.nec.2015.03.013.
- Cavallo LM, Solari D, Esposito F, et al. The role of the endoscopic endonasal route in the management of craniopharyngiomas. World Neurosurg. 2014; 82(6): 32-40. doi: 10.1016/j.wneu.2014.07.023.
- Nagata Y, Takeuchi K, Sasaki H, et al. Modified Shoelace Dural Closure with Collagen Matrix in Extended Transsphenoidal Surgery. Neurol Med Chir (Tokyo). 2022; 62(4): 203-208. doi:10.2176/jns-nmc.2021-0355.
- Karavitaki N, Cudlip S, Adams CB, et al. Craniopharyngiomas. Endocr Rev. 2006; 27(4): 371-397. doi: 10.1210/er.2006-0002.
- Yaşargil MG, Curcic M, Kis M, et al. Total removal of craniopharyngiomas. Approaches and long-term results in 144 patients. J Neurosurg. 1990; 73(1): 3-11. doi: 10.3171/ jns.1990.73.1.0003.
- Yang I, Sughrue ME, Rutkowski MJ, et al. Craniopharyngioma: a comparison of tumor control with various treatment strategies. Neurosurg Focus. 2010; 28(4): E5. doi: 10.3171/2010.1.FOCUS09307.
- Koutourousiou M, Gardner PA, Fernandez-Miranda JC, et.al. Endoscopic endonasal surgery for craniopharyngiomas: surgical outcome in 64 patients. J Neurosurg. 2013; 119(5): 1194-1207. doi: 10.3171/2013.6. JNS122259.
- Prieto R, Pascual JM, Rosdolsky M, et al. Craniopharyngioma adherence: a comprehensive topographical categorization and outcome-related risk stratification model based on the methodical examination of 500 tumors. Neurosurg Focus. 2016; 41(6): E13. doi: 10.3171/ 2016.9.FOCUS16304.
- Figueredo LF, Martínez AL, Suarez-Meade P, et al. Current Role of Endo-scopic Endonasal Approach for Craniopharyngiomas: A 10-Year Systematic Review and Meta-Analysis Comparison with the Open Transcranial Approach. Brain Sci. 2023; 13(6): 842. doi: 10.3390/ brainsci13060842.
- Mou J, Wang X, Huo G, et al. Endoscopic Endonasal Surgery for Cranio-pharyngiomas: A Series of 60 Patients. World Neurosurg. 2019; 124: e424-e430. doi: 10.1016/j.wneu. 2018.12.110.
- Cavallo LM, Frank G, Cappabianca P, et al. The endoscopic endonasal approach for the management of craniopharyngiomas: a series of 103 patients. J Neurosurg. 2014; 121(1): 100-113. doi: 10.3171/2014.3.JNS131521.
- Leng LZ, Greenfield JP, Souweidane MM, et al. Endoscopic, endonasal resection of craniopharyngiomas: analysis of outcome including extent of resection, cerebrospinal fluid leak, return to preoperative productivity, and body mass index. Neurosurgery. 2012; 70(1): 110-124. doi: 10.1227/NEU.0b013e31822e8ffc.
- Kim EH, Ahn JY, Kim SH. Technique and outcome of endoscopy-assisted microscopic extended transsphenoidal surgery for suprasellar craniopharyngiomas. J Neurosurg. 2011; 114(5): 1338-1349. doi: 10.3171/2010.11.JNS10612.
- Komotar RJ, Starke RM, Raper DM, et.al. Endoscopic endonasal compared with microscopic transsphenoidal and open transcranial resection of craniopharyngiomas. World Neurosurg. 2012; 77(2): 329-341. doi: 10.1016/j.wneu. 2011.07.011.
- Chakrabarti I, Amar AP, Couldwell W, et.al. Long-term neurological, visual, and endocrine outcomes following transnasal resection of craniopharyngioma. J Neurosurg. 2005; 102(4): 650-657. doi: 10.3171/jns.2005.102.4.0650.
- Honegger J, Buchfelder M, Fahlbusch R. Surgical treatment of craniopharyngiomas: endocrinological results. J Neurosurg. 1999; 90(2): 251-257. doi: 10.3171/jns.1999.90.2.0251.
- Yamada S, Fukuhara N, Oyama K, et al. Surgical outcome in 90 patients with craniopharyngioma: an evaluation of transsphenoidal surgery. World Neurosurg. 2010; 74(2-3): 320-330. doi: 10.1016/j.wneu.2010.06.014.
- Gardner PA, Prevedello DM, Kassam AB, et al. The evolution of the endonasal approach for craniopharyngiomas. J Neurosurg. 2008; 108(5): 1043-1047. doi: 10.3171/JNS/ 2008/108/5/1043.
- Sasaki H, Takeuchi K, Nagata Y, et al. The importance of preserving the superior hypophyseal artery infundibular branch in craniopharyngioma surgery. Acta Neurochir (Wien). 2023; 165(3): 667-675. doi: 10.1007/s00701-022-05415-3.
- Leng LZ, Brown S, Anand VK, et al. «Gasket-seal» watertight closure in minimal-access endoscopic cranial base surgery. Neurosurgery. 2008; 62(5-2): 342-343. doi: 10.1227/01.neu.0000326017.84315.1f.
- Hadad G, Bassagasteguy L, Carrau RL, et al. A novel reconstructive technique after endoscopic expanded endonasal approaches: vascular pedicle nasoseptal flap. Laryngoscope. 2006; 116(10): 1882-1886. doi: 10.1097/01.mlg. 0000234933.37779.e4.
- Matmusaev M, Watanabe T, Iwami K, et al. Endoscopic transnasal transsphenoidal management of sellar/suprasellar arachnoid cyst: A case report and literature review. Surg Neurol Int. 2023; 14: 131. doi: 10.25259/SNI_1102_2022.
- Nishioka H, Izawa H, Ikeda Y, et al. Dural suturing for repair of cerebrospinal fluid leak in transnasal transsphenoidal surgery. Acta Neurochir (Wien). 2009; 151(11): 1427-1430. doi: 10.1007/s00701-009-0406-2.
- Ishikawa T, Takeuchi K, Nagata Y, et al. Three types of dural suturing for closure of CSF leak after endoscopic transsphenoidal surgery. Journal of Neurosurgery JNS. 2019; 131(5): 1625-1631. doi: 10.3171/2018.4.JNS18366.


