Эндотелий как мишень патологического воздействия вирусной инфекции
Автор: Шевченко Ю.Л., Стойко Ю.М., Гудымович В.Г.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Редакционные статьи
Статья в выпуске: 2 т.17, 2022 года.
Бесплатный доступ
В обзорной статье подробно анализируются данные, полученные в результате экспериментальных и клинических исследований, посвященных взаимодействию различных вирусов с эндотелием и эндокардом. Рассмотрены вопросы воздействия вирусной инфекции на эндотелиальные клетки, возможные механизмы их повреждения, а также активации патологических каскадов внутрисосудистого тромбоза, острого респираторного дистресс-синдрома и неконтролируемого генерализованного воспалительного процесса. С учетом механизмов реализации данных процессов приведены пути коррекции этих нарушений с помощью эндотелиопротекторов, в частности, назначением препарата сулодексид.
Вирусная инфекция, эндотелий, эндокард, эндотелиальная дисфункция, сулодексид
Короткий адрес: https://sciup.org/140295050
IDR: 140295050 | DOI: 10.25881/20728255_2022_17_2_11
Endothelium as a target of pathological effects of viral infection
The review article analyzes in detail the data obtained as a result of experimental and clinical studies on the interaction of various viruses with the endothelium and endocardium. The issues of the impact of a viral infection on endothelial cells, possible mechanisms of their damage, as well as the activation of pathological cascades of intra-vascular thrombosis, acute respiratory distress syndrome, and an uncontrolled generalized inflammatory process are considered. Taking into account the mechanisms for the implementation of these processes, ways to correct these disorders with the help of endothelial protectors, in particular, by prescribing the drug sulodexide, are given.
Текст научной статьи Эндотелий как мишень патологического воздействия вирусной инфекции
Эндотелиальные клетки (ЭК) выстилают внутреннюю поверхность всех кровеносных и лимфатических сосудов, создавая полупроницаемый барьер между кровью, лимфой и окружающими их тканями. Это свойство обуславливает тот факт, что все возможные входные порты вирусной инфекции находятся в тесном контакте с ЭК. Микроциркуляторное русло, состоящее из артериол, капилляров и посткапиллярных венул, составляет наибольшую поверхность сердечно-сосудистой системы и является основной составляющей, где происходит большинство физиологических процессов, связанных с эндотелием. Именно здесь проявляется большинство вызванных вирусом сосудистых повреждений [1].
Воздействие вирусов на клетки эндотелиальной и эндокардиальной выстилки до последнего времени было весьма дискутабельным [2; 3]. Предположение о возможном воздействии вирусной инфекции на эндотелий высказывалось нами на протяжении многих лет [4] и основано было на клиническом анализе течения сепсиса и внутрисердечной инфекции, в частности. Вирусная инфекция является инициализирующим фактором, который, наряду с гемодинамическими изменениями (травматизация эндокарда патологически направленными потоками крови) запускает каскад изменений, который в присутствии тран-зиторной бактериемии приводит к фиксации бактерий на подготовленном и «взрыхленном» эндокарде [4].
Механизмы воздействия вирусов на эндотелий и эндокард
Общей чертой вирусов, поражающих ЭК, является их способность вызывать тяжелые полиорганные заболевания. Клинические признаки терминальной стадии течения вирусной инфекции часто сходны с гипоперфузией, отеком, кровотечением и тромбозом, что указывает на нарушение функции центральных сосудов [2].
Оценка патологической анатомии сосудов позволяет заподозрить тропность вирусов к ЭК. Ряд клинико-экспериментальных исследований как с ЭК, так и кардиомиоцитами, позволил сделать ряд выводов. Имплантированные культуры являлись прежде всего «мостом» к замещению их аутологичными клеточными структурами. Несмотря на полученную клиническую эффективность следует отметить достаточно высокую уязвимость этих «протезированных клеток» в период их замещения и подверженность вирусной инфекции [5].
ЭК — важная мишень для большинства вирусов человека, включая бета- и гамма-герпесвирусы. Инфекция эндотелия имеет серьезные последствия как для вируса, так и для хозяина. Для вируса заражение ЭК может стать воротами для распространения в органы и резервуаром для долговременной персистенции. У хозяина репликация вируса и последующий иммунный ответ в эндотелии увеличивают проницаемость тканей и воспаление, способствуя развитию сосудистых заболеваний и усугублению их тяжести.
Повреждение эндотелия играет важную роль в патогенезе тромбоза, атеросклероза, ДВС и васкулита. Ряд вирусов человека обладает способностью инфицировать культуры ЭК, полученных из пупочной вены человека или грудной аорты крупного рогатого скота [2]. Friedman H.M. и соавт. еще в 1981 г. в серии работ

показали с помощью иммунофлуоресцентных методов инфицирование как эндотелия вен, так и эндотелия аорты вирусами простого герпеса типа 1, аденовирусом типа 7, вирусом кори и вирусом парагриппа типа 3. Вирус же эпидемического паротита, полиовирус типа 1 и эховирус типа 9 росли только в культурах венозных ЭК, а вирус Коксаки В4 был способен инфицировать только культуры ЭК, полученных из артерий крупного рогатого скота. Авторы отмечают, что при репликации некоторые вирусы вызывали острые литические изменения. Это позволило сделать вывод о весьма важном значении репликация вируса в эндотелии в патогенезе вирусного заболевания, вызывающего повреждение стенки сосуда [2].
Goodrum F. и Bughio F. (2015) из Аризонского университета удалось выделить ряд важных генетических детерминант тропизма различных вариантов цитомегаловируса человека к ЭК. Он отличается способностью как инфицировать широкий спектр типов клеток, так и длительно персистировать в клетках (продуктивно реплицируется в фибробластах, в латентном состоянии находится в гемопоэтических клетках-предшественниках и клетках миелоидного происхождения, другие типы клеток являются местами долговременного выделения этого вируса, поддерживая хроническую инфекцию, прежде всего эндотелиальную). Выявление механизмов тропизма к ЭК может позволить разработать новые мишени для противовирусных препаратов, ограничивающие репликацию в ЭК [3].
Поражение эндотелия сосудов чаще вызывает весьма специфичную, схожую с тромбоэмболическим поражением, реакцию. В дополнение к прямым повреждающим кардиальным эффектам (миокардиты, аритмии, васкулиты), вирусное воздействие осуществляется и косвенно — в результате неконтролируемого системного воспалительного процесса [6; 7]. Это дополнительно вовлекает сосудистый эндотелий путем рекрутирования лейкоцитов, инициации провоспалительных компонентов, приводящих закономерно к повреждению тканей, высвобождению цитокинов и формированию заключительных каскадов — острого респираторного дистресс-синдрома (ОРДС), диссеминированного внутрисосудистого свертывания (ДВС) крови, неконтролируемой гиперэргической воспалительной реакции.
Эпителий бронхов и ЭК капилляров являются важнейшими барьерами противовирусной защиты при инфицировании респираторными вирусами. Инфицирование вирусами вызывает реакцию комплекса эпителий-эндотелий. Однако, направленность ее, степень выраженности, временные и морфологические характеристики, по-видимому, отличаются. При инокуляции обычных респираторных вирусов мишенью повреждения является, прежде всего, ЭК. Реакция же ЭК является вторым этапом противоинфекционного противодействия, преимущественно при тяжелом течении заболеваний и генерализации инфекционного про- цесса. Такая стадийность процесса, вероятно, позволяет выиграть время.
ЭК характеризуются тканеспецифическими и сосудистыми профилями, которые, вероятно, и регулируют их восприимчивость и переносимость вирусной инфекции [8]. Огромное их разнообразие возникает благодаря сочетанию морфологических характеристик, которые определяют фенотипы с переменной устойчивостью [9]. Некоторые фенотипы митотически относительно стабильны (например, эпигенетические модификации ЭК артериальных и венозных сосудов) [10]. Другие же, наоборот, обеспечивают память о различных стимулах (примером могут быть биологически активные белки с длительным периодом полураспада в тельцах Вейбеля-Паладе) [11].
Таким образом, поддержание текучести крови, регуляция кровотока, контроль трансэндотелиальной экстравазации белков плазмы и контроль переноса лейкоцитов — все это отвечает на сигналы, генерируемые во время гомеостаза, гипоксии, воспаления и восстановления [12].
Нарушение регуляции функции микроциркулятор-ного русла опосредует отек и геморрагию при вирусных заболеваниях. Компоненты гликокаликса, покрывающие люминальную поверхность ЭК — гликопротеины с кислыми олигосахаридами и терминальными сиаловыми кислотами — придают суммарный отрицательный заряд [13]. Cиаловые кислоты весьма часто используются вирусами для прикрепления к клеточной поверхности [14]. Поэтому, поддержание целостности микрососудов зависит от перекрестного взаимодействия ключевых компонентов ЭК — гликокаликса и межклеточных соединений [13].
Венулярные ЭК жестко контролируют миграцию лейкоцитов из крови в ткани и организуют локальные воспалительные реакции, например, при вирусной пневмонии. Чтобы лейкоциты могли пересечь стенку сосуда, они должны сначала прикрепиться к поверхности эндотелия. Этот процесс происходит в посткапиллярных венулах воспаленных тканей и получил название каскада многоступенчатой адгезии. Захват и катание лейкоцитов на эндотелиальных поверхностях опосредуется Р-, Е- и L-селектинами, которые связывают гликозилированные лиганды. Это происходит в динамическом процессе, формируя и разрывая связи, поддерживающие захват и прокатку под действием напряжения сдвига. Р- и Е-селектин, по-видимому, являются наиболее важными селектинами, экспрессируемыми на активированных посткапиллярных венулах в нелимфоидных тканях. Роллинг лейкоцитов позволяет осуществлять их тесный контакт с ЭК, активируя интегрины лейкоцитов хемокинами, представленными гликокаликсом [15].
ЭК являются важным барьером, регулирующим гомеостаз тканей. В ответ на вирусную инфекцию они инициируют каскад иммунного ответа [16]. Эндотелий и эпителий образуют клеточный монослой, соединен-
ный плотными контактами (TJ), которые регулируют проницаемость монослоя и адгезивных контактов (AJ), которые обеспечивают межклеточные адгезионные взаимодействия. Легочный эндотелий состоит из макро- и микрососудистых ЭК. Эти легочные микрососудистые клетки являются частью альвеолярно-капиллярного/ эпителиально-эндотелиального барьера [17].
Клетки легочного эпителия часто являются воротами, а повреждение альвеол в дальнейшем опосредовано путем активации цитокинов и хемокинов и рекрутирования клеток из иммунной системы [18]. Вирусная инфекция не является основной причиной повреждения тканей. Оно возникает в результате острого гипериммунного воспаления, приводящего к массированному высвобождению цитокинов (интерлейкин (IL) -1β, IL-6 и фактор некроза опухоли-α (TNF-α)) [19], воздействуя на клетки паренхимы легких, поглощение кислорода и ЭК, приводя к эндотелииту, тромбозу и ДВС [20]. Эпителиальные/эндотелиальные поражения, опосредованные цитокинами/хемокинами, приводят к нарушению целостность гемато-воздушного барьера, способствуя повышению проницаемости сосудов, аль- веолярному отеку, инфильтрации лейкоцитов (макрофагов, нейтрофилов) и, как следствие общей гипоксии организма [15; 21].
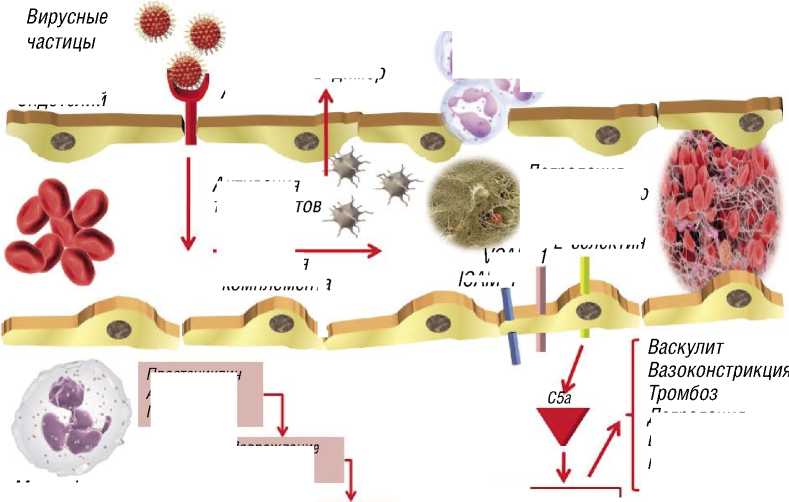
Интенсивное и непрерывное высвобождение про-воспалительных цитокинов лежит в основе неконтролируемого генерализованного воспалительного процесса, характерного для синдрома острого респираторного дистресс-синдрома (ОРДС) и ведущего к повреждению легких [21], активацию системы комплемента (C3, C4 и C5b-C9) [6; 15] (Рис. 1).
Большое количество нейтрофилов у пациентов с тяжелыми формами поражения также связано с высоким уровнем активных форм кислорода (АФК), которые активируют каскад реакций, ведущих к повреждению тканей, тромбозу и нарушениям гемостаза [22]. Здоровый эндотелий производит антитромботические молекулы, такие как оксид азота (NO) и простациклин (PGI2) [23]. Эндотелиальная дисфункция, наблюдаемая у пациентов с вирусной инфекцией, связана с окислением и снижением уровня NO, увеличением молекул протромботической адгезии [24]. Эндотелиальная дисфункция, воспаление, выработка АФК и повышенный риск тромбоэмболии
ЭНДОТЕЛИОЦИТЫ И ВИРУСНАЯ ИНФЕКЦИЯ
D-димер
АСЕ2
I1
Деградация внеклеточного матрикса
Е-селектин
VCAМ-1 селекти
ICAM
Макрофаг
Отек
Повреждение эндотелия
Простациклин
АФК NET
TNF α , IL-1 β , IL-6, IL-8
Рис. 1. ЭК и легочный эпителий при вирусной респираторной инфекции. Связывание вируса с рецептором ACE2 на эндотелиоцитах приводит к активации системы комплемента, набора белков плазмы с функциями опсонизации в иммунной системе. Активация системы комплемента вызывает высвобождение провоспалительных цитокинов (например, TNF α , IL-1 β , IL-6, IL-8) и рекрутирование фагоцитарных клеток. Высвобождение этих цитокинов способствует активации эндотелия, что приводит к экспрессии селектинов (E-селектин и P-селектин) и интегринов (ICAM и VCAM), а также способствует рекрутированию нейтрофилов и моноцитов, вызывая повреждение эндотелия через высвобождение АФК, производство NET, деградацию внеклеточного матрикса и высвобождение большого количества провоспалительных цитокинов. Повреждение эндотелия вызывает активацию каскада свертывания и активацию тромбоцитов, что приводит к гиперкоагуляции и тромбозу. Дальнейшая активация NLRP3, приводя к воспалению, усиливает выработку IL-1 β и TNF α , что приводит к накоплению нейтрофилов, повышенному образованию АФК и NET, вызывающих повреждение эндотелия, отек легких и гибель клеток (по [6]с изменениями).
Эндотелий
Активация
Активация комплемента
Захват лейкоцитов
Тромбоз
Деградация внеклеточно матрикса

неразрывно связаны. АФК стимулируют экспрессию тканевого фактора и ингибируют протеин С, главный антикоагулянт [23]. Во время вирусной инфекции активация рецептора ангиотензина 1 также вызывает повышенное высвобождение АФК, а также чрезмерную активацию инфламмасомы NLRP3 и гибель эндотелиоцитов легких в результате пироптоза [25].
Таким образом, респрираторная вирусная инфекция вызывает повреждение эпителиально-эндотелиального барьера и разрыв этой системы. Исследования, сравнивающие ткани легких у пациентов, умерших от вирусной инфекции, продемонстрировали значительные изменения в морфологии эндотелия: потери контакта с базальной мембраной, разрыв межклеточных контактов [26]. Воспаление достигает эндотелиального уровня, а затем усиливается. Однако, повреждение эндотелия в большей степени связано с воспалительной аутологичной реакцией, а не с репликацией вируса или повышенной вирусной нагрузкой [27]. Прямая или косвенная активация ЭК инфекцией приводит к отеку легких и запускает каскад гиперкоагуляции, который и приводит к тяжелым поражениям тканей.
Дисфункция ЭК вместе с воспалением, вызванным вирусной инфекцией, может привести к аномальной гиперкоагуляции и активно участвовать в тромбовоспалительных процессах, которые приводят к васкулопатии и сепсису [28]. Лабораторные исследования показали, что коагулопатии у этой категории больных характеризуется высоким уровнем D-димера, P-селектина и фибриногена [29].
Существуют многочисленные клинические исследования, продемонстрировавшие значительно более высокую частоту различных тромботических осложнений течения тяжелых форм вирусных инфекций: артериальный тромбоз — до 69% пациентов в критическом состоянии [30], тромбоз глубоких вен — до 50% больных [30]; ТЭЛА — до 31% пациентов [31]. Отмечается повышенная частота и ишемического инсульта, инфаркта миокарда или системной артериальной эмболии [32].
Ряд публикаций продемонстрировал спектр наиболее значимых сердечно-сосудистых заболеваний, осложняющих течение вирусной инфекции. Среди них острый коронарный синдром и инфаркт миокарда, миокардит и острое поражение миокарда [33], инфекционный эндокардит (ИЭ) [34; 35]. Ряд публикаций, посвященных этому вопросу, указывает, с одной стороны, на уменьшение количества зарегистрированных случаев ИЭ на пике пандемии, а с другой — на значительное увеличение госпитальной летальности [36], даже при отсутствии сопутствующих заболеваний.
Сходство симптоматики вирусной инфекции и ИЭ, наличие синдрома системного воспалительного ответа в сочетании с несвоевременностью обращения за медицинской помощью из-за ограничений и акцент учреждений на лечение конкурирующей инфекции являются весьма значимыми дополнительными факторами ухудшения прогноза и исходов ИЭ [37].
Кроме организационных факторов, на диагностику ИЭ оказали влияние и чисто клинические особенности вирусной инфекции. Так, в литературе описаны ряд отдельных случаев или наблюдения малых групп пациентов с ошибочной или поздней диагностикой как вирусной инфекции у больных ИЭ, так и позднего диагноза ИЭ у пациентов с установленной ранее вирусной инфекцией [35].
Хотя в литературе периодически обсуждаются случаи предполагаемой вирусной этиологии ИЭ, однако эта концепция еще пока требует доказательств: прямое цитопатическое действие вируса на эндокард и его включение в клетки не доказано. Наиболее вероятной причиной следует считать бактериальный генез развития внутрисердечной инфекции — и наиболее часто на фоне выраженной естественной или медикаментозно индуцированной иммуносупрессии [5; 35].
Множественные венозные тромбозы, повреждение микрососудистого русла и признаки системной гиперкоагуляции, системный васкулит характерны не только для SARS-CoV-2 и других вариантов вирусной инфекции, но и для ИЭ [5; 33; 35].
В первую очередь обращает на себя внимание тяжелое поражение миокарда (значительное снижение общей сократимости и широко распространенное нарушение локальной сократимости миокарда, очаговые изменения ЭКГ). Возможность такого поражения существует как при новой коронавирусной инфекции, так и при ИЭ, и однозначная интерпретация преобладающей роли того или иного заболевания в конкретном случае затруднена даже после морфологического исследования.
Повреждение эндотелия и тромбоз больших и малых ветвей коронарных артерий считаются ключевым механизмом повреждения миокарда при вирусной инфекции. Морфологически это может соответствовать миокардиту, кардиомиопатии Такоцубо и коронарогенному некрозу миокарда.
Лечебная тактика при вирусном поражении эндотелия и эндокарда
Развитие вирусной инфекции, особенно с поражением легких, часто сопровождается тромботическими осложнениями, инициатором которых является дисфункция эндотелия в ответ на воздействие вирусным агентом. Последующий каскад нарушений вовлекает прежде всего сосудистое звено с развитием микротромбозов, повреждением эндотелия сосудов и ткани легкого, системным воспалительным ответом и генерализацией процесса. Учитывая многофакторность и разнонаправленность процесса, медикаментозное воздействие не всегда оказывает решающее воздействие на его прерывание. Однако, ясно одно, антикоагулянтная терапия должна быть одним из основных компонентов в лечебной программе пациентов с вирусной инфекцией. Причем, раннее назначение препаратов этой группы позволяет предотвратить прогрессирование поражения.
Данные литературы об отсроченных тромботических и эмболических осложнениях подчеркивают важность пролонгированного их применения после перенесенной инфекции.
Схема лечения ДВС-синдрома во многом зависит от тяжести заболевания и кинических проявлений. В первую очередь необходимо сделать акцент на самой многочисленной группе пациентов — контактных, без симптомов заболевания или с минимально выраженными их проявлениями. Учитывая то, что в патогенезе развития вирусной инфекции значительное место занимают ДВС-синдром и повреждение эндотелия мелких и крупных сосудов самой различной локализации, применение су-лодексида может иметь существенное значение. Связано это с тем, что он оказывает комплексное воздействие на систему гемостаза и защищает эндотелий от различных видов патологической агрессии [38].
Сулодексид представляет собой комбинацию двух природных фракций гликозаминогликанов — дерматансульфата (20%) и высокоподвижной гепариноподобной фракции (80%). Сочетание этих фракций обладает анти-тромботическим и профибринолитическим действием.
В частности, посредством воздействия на фактор IIа (тромбин) препарат способен тормозить образование фибрина из фибриногена, активировать фибринолиз и тормозить агрегацию тромбоцитов. Ангиопротектор-ное действие сулодексида связано с восстановлением структурной и функциональной целостности клеток эндотелия сосудов.
Важнейшим для коррекции нарушений функции эндотелия является восстановление гликокаликса — поверхностного слоя эндотелия сосудов, который выступает в роли рецептора механического раздражения, участвует в регуляции тонуса сосудов и его проницаемости, а также контролирует взаимодействие циркулирующих клеток крови с клетками эндотелия. Сулодексид способен связываться с ЭК как в моделях in vitro, так и в моделях in vivo, увеличивая и восстанавливая отрицательный заряд и толщину гликокаликса.
Сулодексид подавляет ответную реакцию эндотелиальных клеток на воспалительные процессы. Так, в исследованиях из отдела патофизиологии Познаньского университета (Польша) Ciszewicz M, Polubinsk с соавт. (2009) и Suminska-Jasinska K, Polubinska с соавт. (2011), культивируемые ЭК пупочной вены человека, подвергшиеся воздействию высоких концентраций глюкозы, высвобождали свободные радикалы (активные формы кислорода), хемотаксический белок моноцитов-1 и интерлейкин-6. Эти изменения предотвращались при добавлении сулодексида в культуральную среду [39; 40].
Заключение
Таким образом, проведенные анализ литературных материалов, исследования клинических особенностей и личные наблюдения позволяют сделать ряд следующих выводов. Прежде всего, основной мишенью вирусной инфекции является эндотелий, причем чаще — эндотелий сосудов малого круга кровообращения (легочной локализации). Это позволяет постулировать мысль о гетерогенности эндотелия в различных органах и системах. Гетерогенность эндотелия, по-видимому, носит относительный характер, что объясняет поражение не только сосудов легких, но и других органов и локализаций — склонность к тромбозам вен нижних конечностей, миокардитам с периваскулитами, тромбозам артерий органов брюшной полости, частым инсультам, более частым развитием инфекционного эндокардита. В дальнейшем следует сконцентрировать внимание на патогенетической коррекции с использованием эндо-телиопротективных препаратов с учетом особенностей гетерогенности эндотелия.
Авторы заявляют об отсутствии конфликта интересов (The authors declare no conflict of interest).
Список литературы Эндотелий как мишень патологического воздействия вирусной инфекции
- Fosse JH., Haraldsen G, Edelmann R. Endothelial Cells in Emerging Viral Infections. Front. Cardiovasc. Med. 2021; 24(8): 619690. doi: 10.3389/ fcvm.2021.619690.
- Friedman HM, Macarak EJ, MacGregor RR, et al. Virus infection of endothelial cells. J. Infect. Dis. 1981; 143(2): 266-273. doi: 10.1093/infdis/ 143.2.266.
- Goodrum F, Bughio F. Viral infection at the endothelium. Oncotarget. 2015; 6(29): 26541–26542. doi: 10.18632/oncotarget.5246.
- Шевченко Ю.Л. Хирургическое лечение инфекционного эндокардита и основы гнойно-септической кардиохирургии. — 2-е изд. — М.: Династия, 2020. — 448 с.
- Шевченко Ю.Л., Матвеев С.А. Клеточные технологии в сердечно-сосудистой хирургии. — М.: Медицина, 2005. — 160 с.
- Barbosa LC, Gonçalves TL, Prudencio de Araujo L, et al. Endothelial cells and SARS-CoV-2: An intimate relationship. Vascul Pharmacol. 2021; 137: 106829. doi: 10.1016/j.vph.2021.106829.
- Evans PC, Rainger GE, Mason JC, et al. Endothelial dysfunction in COVID-19: a position paper of the ESC Working Group for Atherosclerosis and Vascular Biology, and the ESC Council of Basic Cardiovascular Science. Cardiovasc Res. 2020; 116(14): 2177-2184. doi: 10.1093/cvr/cvaa230.
- Jakab M, Augustin HG. Understanding angiodiversity: insights from single cell biology. Development. 2020; 147(15): 1-13. doi: 10.1242/dev.146621.
- Aird WC. Mechanisms of endothelial cell heterogeneity in health and disease. Circ Res. 2006; 98(2):159-162. doi: 10.1161/01.RES.0000204553. 32549.a7.
- Aitsebaomo J, Portbury AL, Schisler JC, Patterson C. Brothers and sisters: molecular insights into arterial-venous heterogeneity. Circ Res. 2008; 103(9): 929-939. doi: 10.1161/CIRCRESAHA.108.184937.
- Aird WC. Endothelial cell heterogeneity. Cold Spring Harb Perspect Med. 2012; 2(1): a006429. doi: 10.1101/cshperspect.a006429.
- Regan ER, Aird WC. Dynamical systems approach to endothelial heterogeneity. Circ Res. 2012; 111: 110-130. doi: 10.1161/CIRCRESAHA.111.261701.
- Weinbaum S, Tarbell JM, Damiano ER. The structure and function of the endothelial glycocalyx layer. Annu Rev Biomed Eng. 2007; 9: 121-167. doi: 10.1146/annurev.bioeng.9.060906.151959.
- Wasik BR, Barnard KN, Parrish CR. Effects of sialic acid modifications on virus binding and infection. Trends Microbiol. 2016; 24(12): 991-1001. doi: 10.1016/j.tim.2016.07.005.
- Шевченко Ю.Л., Гороховатский Ю.И., Азизова О.А., Замятин М.Н. Системный воспалительный ответ при экстремальной хирургической агрессии. — М.: РАЕН, 2009. — 273 с.
- Blume C, Reale R, Held M, et al. Cellular crosstalk between airway epithelial and endothelial cells regulates barrier functions during exposure to double-stranded RNA. Immun Inflamm Dis. 2017; 5(1): 45-56. doi: 10.1002/iid3.139.
- Millar FR, Summers C, Grif MJ, Proudfoot AG. The pulmonary endothelium in acute respiratory distress syndrome: insights and therapeutic opportunities. Thorax. 2016; 71: 462-473. doi: 10.1136/thoraxjnl-2015-207461.
- De Biasi S, Meschiari M, Gibellini L, et al. Marked T cell activation, senescence, exhaustion and skewing towards TH17 in patients with COVID-19 pneumonia. Nat. Commun. 2020; 11: 3434. doi: 10.1038/s41467-020-17292-4.
- Felsenstein S, Herbert JA, McNamara PS, Hedrich CM. COVID-19: immunology and treatment options. Clin. Immunol. 2020; 215: 108448. doi: 10.1016/j.clim.2020.108448.
- Noris M, Benigni A, Remuzzi G. The case of complement activation in COVID-19 multiorgan impact. Kidney Int. 2020; 98(2): 314-322. doi: 10.1016/j.kint.2020.05.013.
- Pelaia C, Tinello C, Vatrella A, et al. Lung under attack by COVID-19-induced cytokine storm: pathogenic mechanisms and therapeutic implications. Ther. Adv. Respir. Dis. 2020; 4: 1-9. doi: 10.1177/1753466620933508.
- Laforge M, Elbim C, Frère C, et al. Tissue damage from neutrophil-induced oxidative stress in COVID-19. Nat. Rev. Immunol. 2020; 20(9): 515-516. doi: 10.1038/s41577-020-0407-1.
- Panfoli I. Potential role of endothelial cell surface ectopic redox complexes in COVID-19 disease pathogenesis. Clin. Med. 2020; 20(5): e146-e147. doi: 10.7861/clinmed.2020-0252.
- Xavier AR, Silva JS, Almeida JP, et al. COVID-19: clinical and laboratory manifestations in novel coronavirus infection. J. Bras. Patol. E Med. Lab. 2020; 56:1-9. doi: 10.5935/1676-2444.20200049.
- Ratajczak MZ, Bujko K, Ciechanowicz A, et al. SARS-CoV-2 entry receptor ACE2 is expressed on very small CD45 − precursors of hematopoietic and endothelial cells and in response to virus spike protein activates the Nlrp3 inflammasome. Stem Cell Rev. Rep. 2020; 17(1): 266-277. doi: 10.1007/s12015-020-10010-z.
- Ackermann M, Verleden SE, Kuehnel M, et al. Pulmonary vascular endothelialitis, thrombosis, and angiogenesis in Covid-19. N.Engl. J. Med. 2020; 383(2): 120-128. doi: 10.1056/NEJMoa2015432.
- Kaur S, Tripathi DM, Yadav A. The enigma of endothelium in COVID-19. Front. Physiol. 2020; 11: 989. doi: 10.3389/fphys.2020.00989.
- Pons S, Fodil S, Azoulay E, Zafrani L. The vascular endothelium: the cornerstone of organ dysfunction in severe SARS-CoV-2 infection. Crit. Care. 2020; 24(1): 353. doi: 10.1186/s13054-020-03062-7.
- Grobler C, Maphumulo SC, Grobbelaar LM, et al. Covid-19: The rollercoaster of fibrin(ogen), D-dimer, Von Willebrand factor, P-selectin and their interactions with endothelial cells, platelets and erythrocytes. Int. J. Mol. Sci. 2020; 21(14): 5168. doi: 10.3390/ijms21145168.
- Gong JM, Du JS, Han DM. Implications of bed rest for patients with acute deep vein thrombosis: a qualitative study. Patient Prefer. Adherence. 2020; 14: 1659-1667. doi: 10.2147/PPA.S271481.
- Klok FA, Kruip MJ, van der Meer NJ, et al. Incidence of thrombotic complications in critically ill ICU patients with COVID-19. Thromb. Res. 2020; 191: 145-147. doi: 10.1016/j.thromres.2020.04.013.
- Stefanini GG, Montorfano M, Trabattoni D, et al. ST-elevation myocardial infarction in patients with COVID-19: clinical and angiographic outcomes. Circulation. 2020; 141(25): 2113-2116. doi: 10.1161/CIRCULATIONAHA. 120.047525.
- Fried JA, Ramasubbu К, Bhatt R, et al. The Variety of Cardiovascular Presentations of COVID-19. Circulation. 2020; 141(23): 1930-1936. doi: 10.1161/CIRCULATIONAHA.120.047164.
- Маев И.В., Шпектор А.В., Васильева Е.Ю. Новая коронавирусная инфекция COVID-19: экстрапульмональные проявления // Терапевтический архив. — 2020. — Т.92. — №8. — С.4-11. doi: 10.26442/00403660.2020.08.000767.
- Пономарева Е.Ю., Кошелева Н.А. Сочетание инфекционного эндокардита и инфекции COVID-19 у молодой пациентки // Архивъ внутренней медицины. — 2021. — Т.11. — №4. — С.297-302. doi: 10.20514/2226-6704-2021-11-4-297-302.
- Cosyns В, Motoc А, Arregle F, et al. Not to Forget Infective Endocarditis in COVID-19 Era. J Am Coll Cardiol Cardiovasc Imaging. 2020; 13(11): 2470-2471. doi: 10.1016/j. jcmg.2020.07.027.
- Hussain A, Roberts N, Oo A. Prosthetic aortic valve endocarditis complicated by COVID-19 and hemorrhage. J Card Surg. 2020; 35(6): 1348-1350. doi: 10.1111/jocs.14643.
- Кузнецов М.Р., Решетов И.В., Папышева О.В. и соавт. Основные направления антикоагулянтной терапии при COVID-19 // Лечебное дело. — 2020. — №2. — С.66-73. doi: 10.24411/2071-5315-2020-12213.
- Ciszewicz M, Polubinska A, Antoniewicz A. et al. Sulodexide suppresses inflammation in human endothelial cells and prevents glucose cytotoxicity. Transl Res. 2009; 153(3): 118-123. doi: 10.1016/j.trsl.2008.12.007.
- Suminska-Jasinska K, Polubinska A, Ciszewicz M, Mikstacki A. Sulodexide reduces senescence-related changes in human endothelial cells. International Medical Journal of Experimental and Clinical Research 17(4): CR222-6. doi:10.12659/MSM.881719.


