Энергетический спектр электронов поверхностной фазы оксида железа, взаимодействующей с макромолекулами фторполимеров при действии СО2-лазерного излучения
Автор: Литинский Аркадий Овсеевич, Новиков Сергей Игоревич, Петров Максим Владимирович
Журнал: Математическая физика и компьютерное моделирование @mpcm-jvolsu
Рубрика: Химическая физика
Статья в выпуске: 11, 2007 года.
Бесплатный доступ
В рамках метода теории функционала плотности типа B3LYP/LanL2DZ с использованием кластерных моделей взаимодействующих центров изучены и обсуждены особенности электронно-энергетических характеристик и спектров одноэлектронных состояний поверхностной фазы оксида железа и различных хемосорбционных контактов с остатками макромолекул фторполимера. Этому процессу способствует обработка взаимодействующих подсистем лазерным СO2-излучением, частота которого близка к частотам валентных колебаний связей, претерпевающих разрыв в процессе образования поверхностных структур.
Короткий адрес: https://sciup.org/14968603
IDR: 14968603 | УДК: 539.2:
Energy spectrum of electrons of ferric oxide surface phase interacting with fluorocarbon polymer macromolecules under the influence of CO2-laser radiation
Within the framework of density functional theory method of the type B3LYP/LanL2DZ and the cluster models of interacting centers peculiarities of the electronic-energy characteristics and one-electronic states spectra of the surface phase of ferric oxide and different chemisorptive contacts with radical of fluorocarbon polymer macromolecules were studied and discussed. The processing of the interacting subsystems by laser CO2-radiation with frequency similar to frequencies of stretching vibrations of the breaking bonds during the formation of surface structures promoted this process.
Текст научной статьи Энергетический спектр электронов поверхностной фазы оксида железа, взаимодействующей с макромолекулами фторполимеров при действии СО2-лазерного излучения
В рамках метода теории функционала плотности типа B3LYP/LanL2DZ с использованием кластерных моделей взаимодействующих центров изучены и обсуждены особенности электронно-энергетических характеристик и спектров одноэлектронных состояний поверхностной фазы оксида железа и различных хемосорбционных контактов с остатками макромолекул фторполимера. Этому процессу способствует обработка взаимодействующих подсистем лазерным CO2-излучением, частота которого близка к частотам валентных колебаний связей, претерпевающих разрыв в процессе образования поверхностных структур.
Оксидные пленки, а также композиционные материалы на их основе широко применяются в качестве материалов в элементах электронных приборов. Представляют интерес также материалы, получаемые покрытием оксидных пленок полимерами (оксид-полимерные композиции). Для их практического использования требуется знание как энергетических характеристик соответствующих контактов, так и особенностей энергетического спектра электронов соответствующих структур.
В данной работе изучены спектры одноэлектронных состояний оксида железа (ОЖ) Fe +2 (включая поверхность) и хемосорбционных комплексов поверхности ОЖ- Fe +2 с макромолекулами фторполимера (ФП). Рассчитаны также энергии образования соответствующих хемосорбционных связей.
На поверхности ОЖ всегда имеются гидроксидные группы (они обнаруживаются ИК-спек-троскопически, поскольку валентные колебания связей O-H являются характеристическими), поэтому за основу модели поверхности Fe +2 -оксидной фазы нами был выбран молекулярный кластер (МК), содержащий поверхностную OH-группу (рис. 1) [1–5].
Рис. 1. Кластер, моделирующий локальный фрагмент поверхности оксида железа
В этот кластер входят ближайшие к Fe +2 атомы кислорода (октаэдрическое окружение), которые замыкались атомами водорода, количество которых отвечало необходимой степени окисления иона железа (+2) и электронейтральности МК [6].
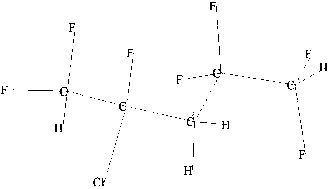
Макромолекула ФП (за основу принят фторкаучук СКФ-32), два элементарных звена кото-~ — рой изображены на рисунке 2, содержит 4 типа неэквивалентных атомов углерода (C*, C, C, С /), поэтому она моделировалась низкомолекулярными структурами, в центре которых располагался один из этих атомов углерода (рис. 3) (разорванные валентности макромолекулы ФП замыкались атомами водорода).
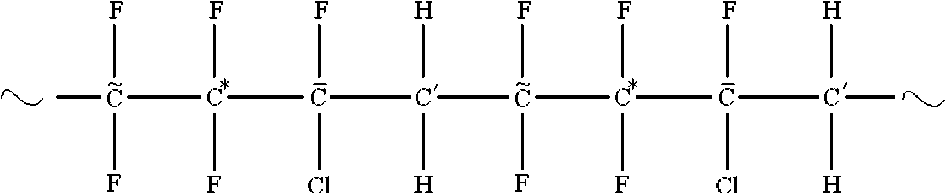
Рис. 2. Строение макромолекулы фторполимера (на примере фторкаучука СКФ-32)
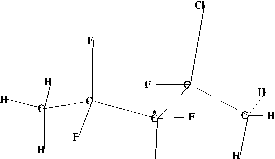
(а)
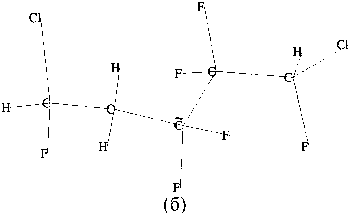
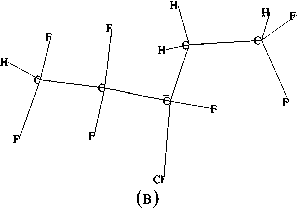
(г)
~ —
Рис. 3. Кластерные модели углеродных C *(а)-, C (б)-, C (в)- и С / (г)-центров макромолекулы фторполимера
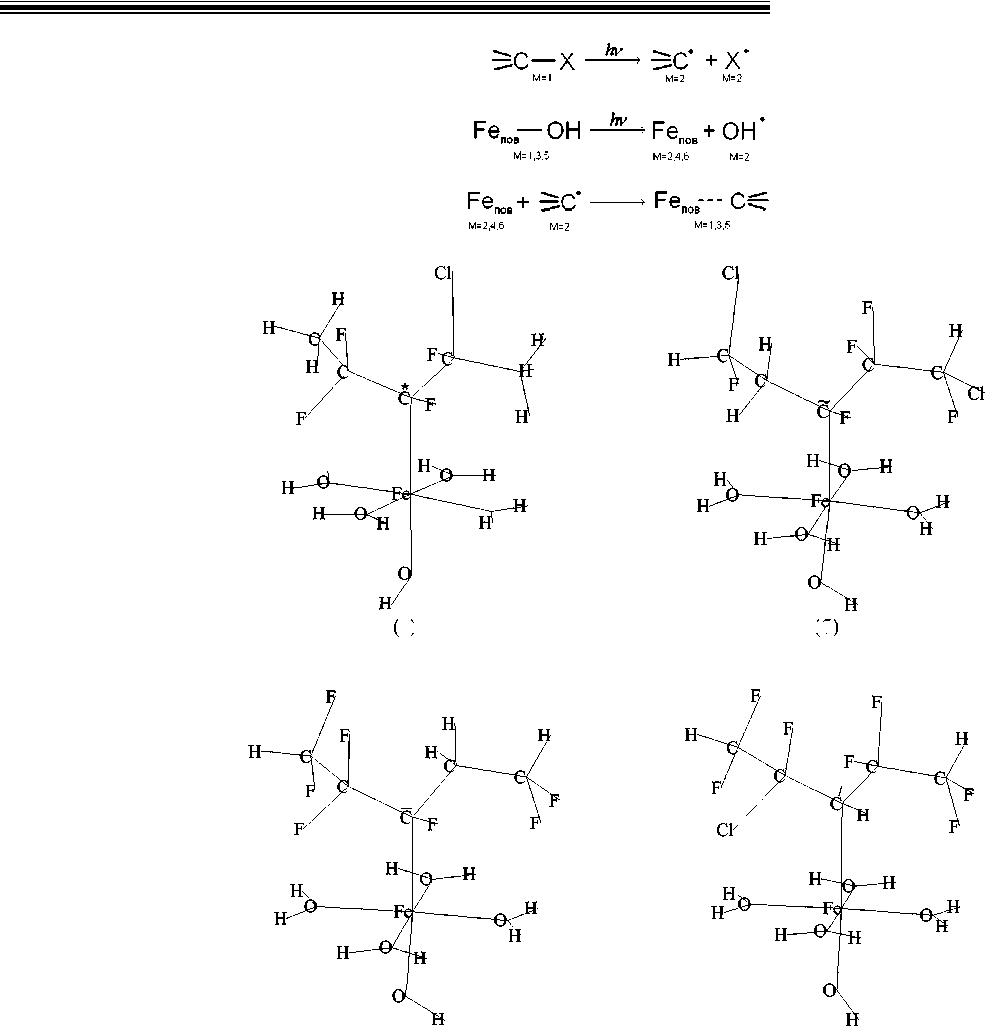
Частоты валентных колебаний связей , и лежат в области 900 ^ 1 100 см -1 [7], поэтому следует ожидать, что под воздействием излучения СО 2 -лазера (основная частота излучения которого v = 944 см -1 ) эти связи способны разорваться вследствие их резонансного «расшатывания». Образующиеся при этом радикалы ФП-макромолекулы и неполнокоординированные поверхностные Fe-центры могут рекомбинировать друг с другом с образованием соответствующего поверхностного соединения ( -контакт) (рис. 4). Таким образом, схема протекающих процессов имеет вид (M = 2 S + 1 – мультиплетность соответствующих структур, S – полный спин системы; X – F, Cl, или H):
(а)
(б)
(в)
(г)
Рис. 4. Кластерные модели адгезионных связей между Fe-центрами поверхности оксида железа ~- и C*(а)-, C(б)-, C(в)- и С /(г)-углеродными центрами макромолекулы фторполимера
Спектры одноэлектронных состояний соответствующих объемных и поверхностных фаз, а также энергии их образования рассчитывались в рамках вычислительной схемы теории функционала плотности типа B3LYP/LanL2DZ (трехпараметрический гибридный обменный функционал Беке [8] и корреляционный функционал Ли, Янга и Пара [9; 10]; валентно-расщепленный двухэкспоненциальный базис Даннинга-Хузинаги [11] для атомов первых двух периодов периодической системы и эффективный псевдопотенциал в сочетании с двухэкспоненциальным базисом для остальных атомов [12–14]).
Рассчитанные спектры *) , полученные для структур с различной мультиплетностью **) , оптимизированные значения межатомных расстояний и энергии разрыва (образования) соответствующих хемосорбционных связей приведены на рисунке 5 и в таблицах 1 и 2.
Оптимизированные длины связей R(C-F), R(C-Cl), R(C-H) и энергии разрыва ( Δ Ε ) этих связей
Таблица 1
|
^С—F |
^C-F |
^C-CI |
^с-н |
|
|
R, А |
1,42 |
1,40 |
1,86 |
1,096 |
|
A E , эВ |
4,05 |
3,98 |
2,43 |
4,510 |
В соответствии с результатами, приведенными в таблице 3 и на рисунке 6, более стабильными оказываются структуры с наибольшей мультиплетностью (это относится как к поверхности ОЖ, так и к его объемной фазе и хемосорбционным контактам). Наиболее значительное понижение энергии имеет место для высокоспиновых состояний Feпов- и Fe-OH-центров (при М = 6 и М = 5 соответственно). Для всех Fe--- С^-структур понижение энергии в ряду M = 1 ^ M = 3 ^ M = 5 примерно одинаково.
a)
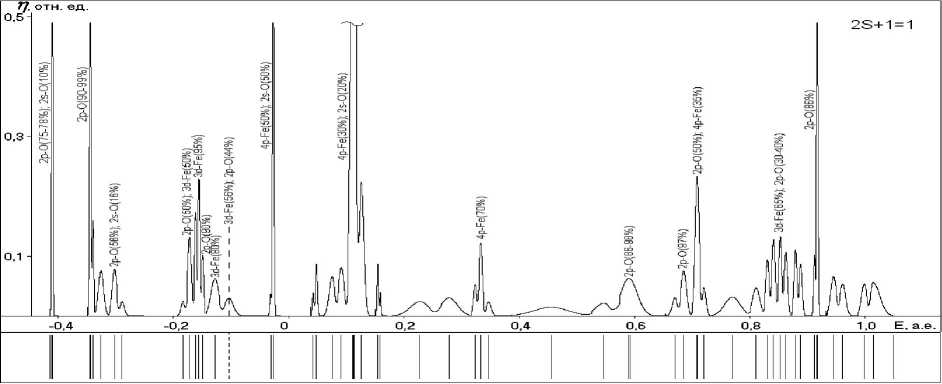
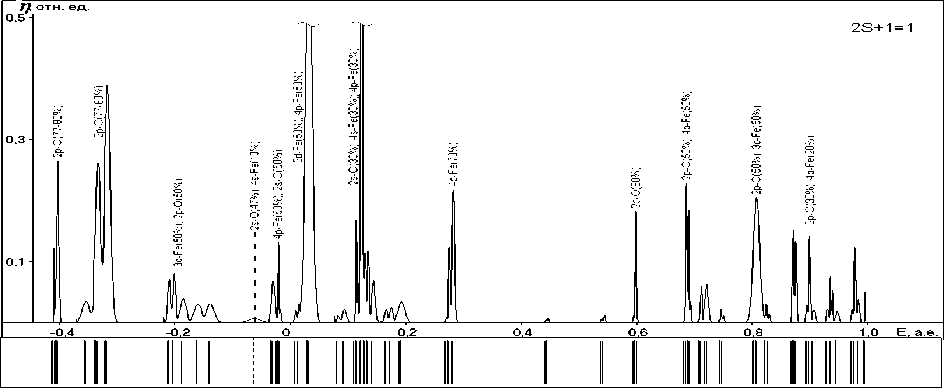
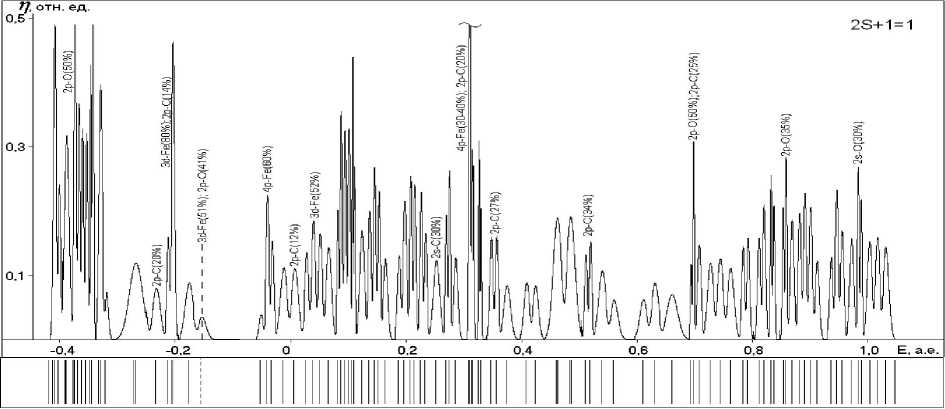
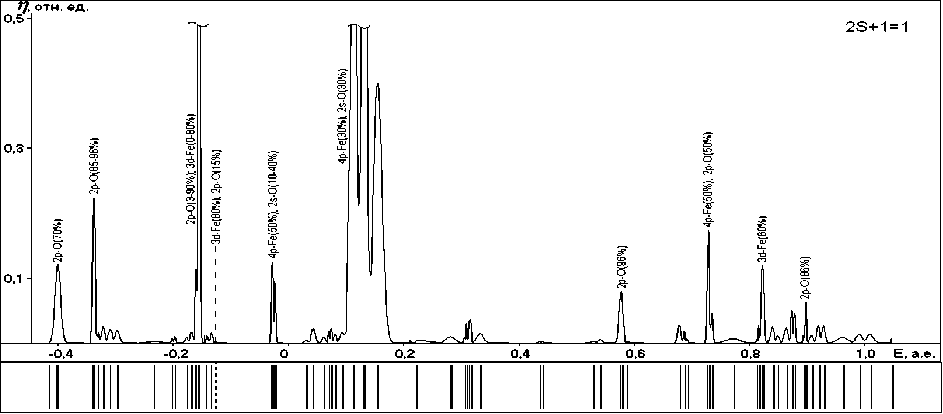
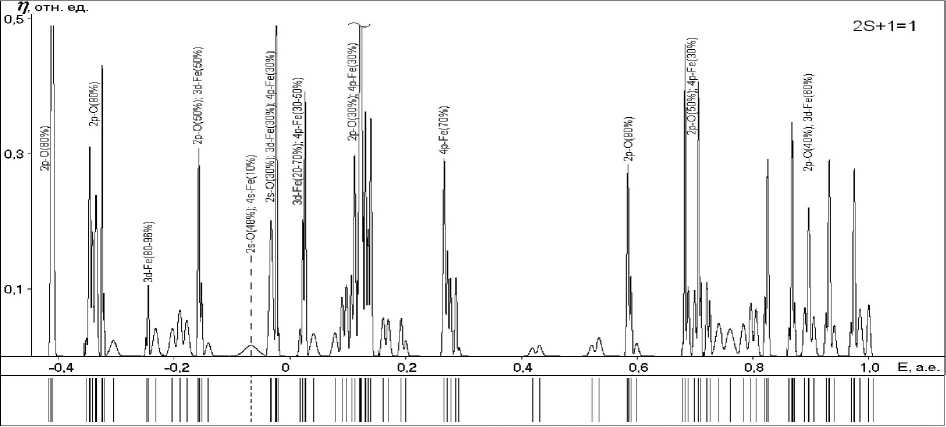
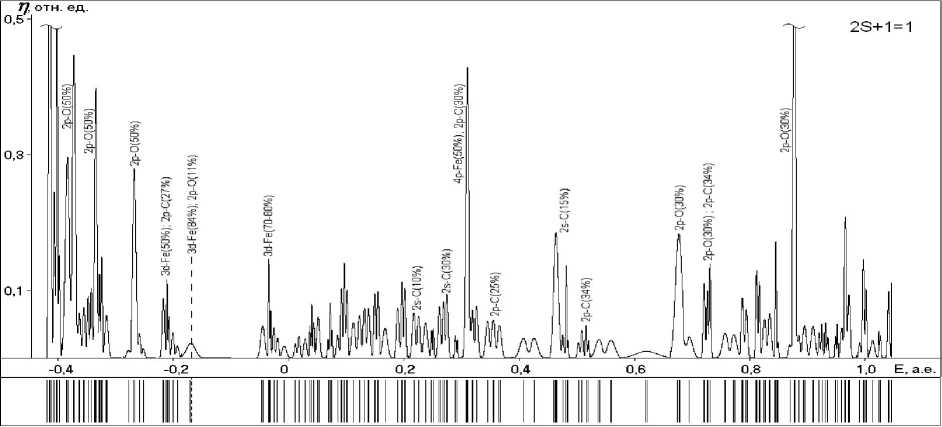
Рис. 5. Энергетические спектры и графики плотностей одноэлектронных состояний структур с различными мультиплетностями (указаны в верхнем углу):
а , г , ж – поверхностных гидроксидов; б , д , з – ОЖ-Fe2+-поверхностных структур;
в , е , и – хемосорбционных комплексов ; к, л – радикала и макромолекулы ФП соответственно
(см. также продолжение рисунка на последующих страницах)
б)
в)
г)
д)
е)
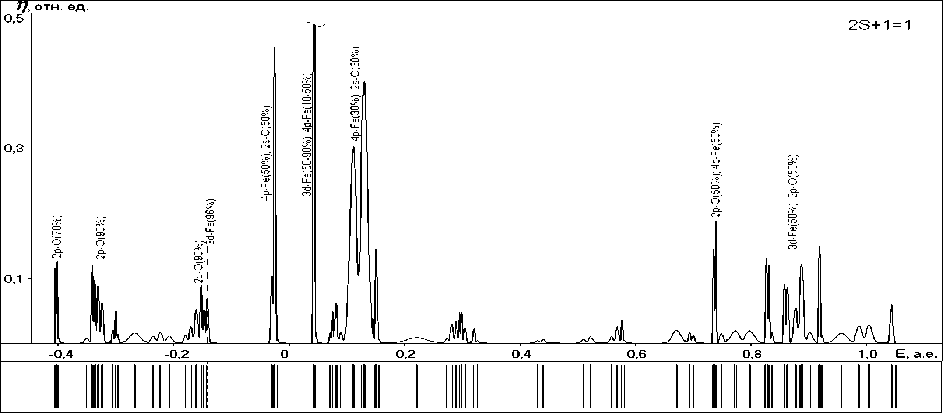
ж)
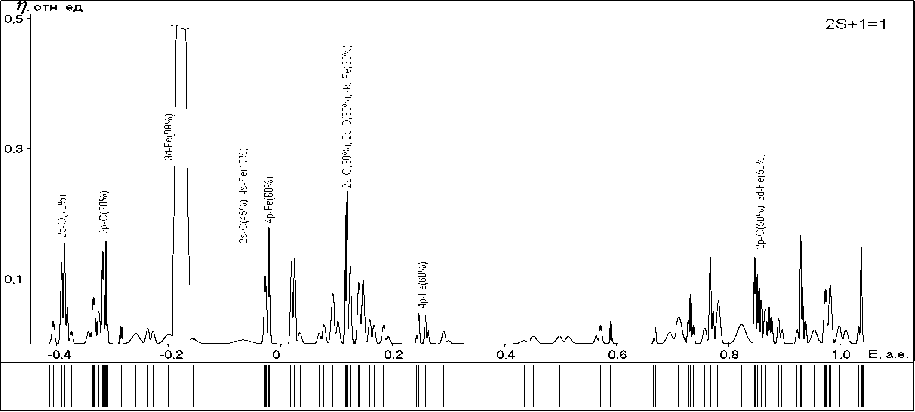
з)
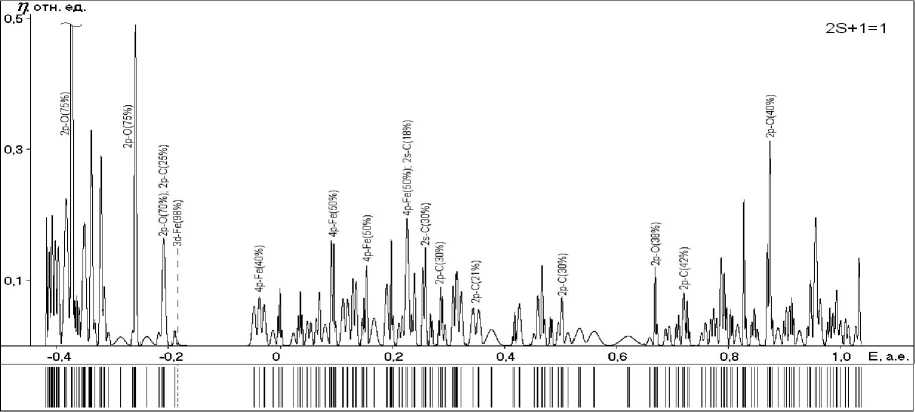
и)
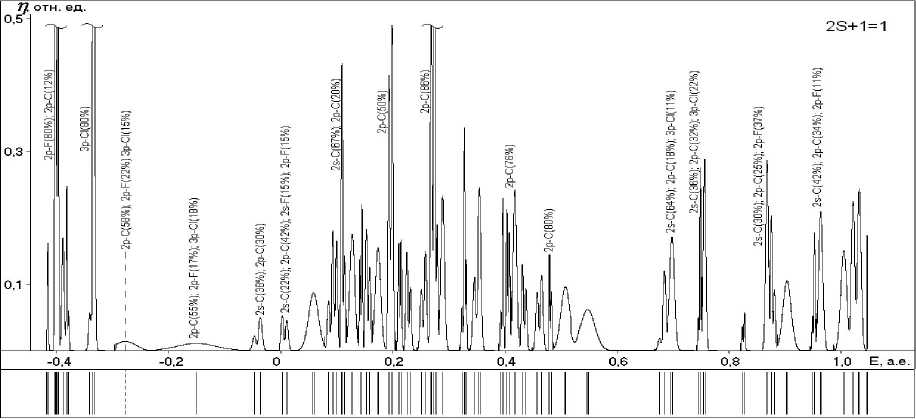
к)
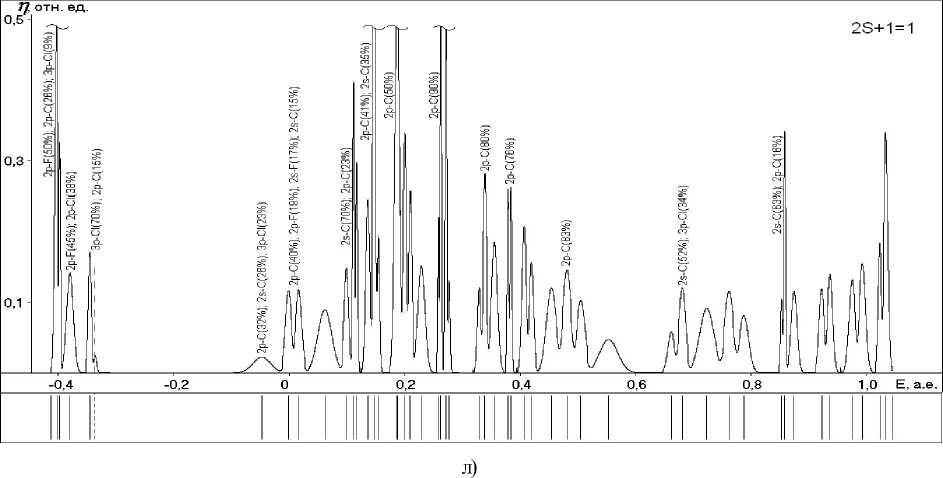
Рис. 5. Окончание
Что касается энергий разрыва АЕ связей Fe-OH и Fe---c^, характеризующих прочность этих связей, то она максимальна для структур с мультиплетностью М = 3. При этом для структур Fe-OH А Е (M = 1) > А Е (M = 5), а для всех структур типа Ре---Сё А Е (M = 1) < А Е (M = 5) (см. табл. 2, рис. 7).
Для контактов с одной и той же мультиплетностью а) в случае -центров энергия хемо-сорбционных связей выше, чем для других центров; б) для ^С - и ^с-центров величины А Е примерно одинаковы, а для -центра энергия разрыва несколько выше. Отметим также, что величины энергий разрыва связей не коррелируют с длинами этих связей.
Таблица 2
Оптимизированные значения межатомных расстояний R(Fe-OH) и R( ) и энергии разрыва (ΔE) этих связей в комплексах поверхности оксидной фазы железа с OH-группой или остатком макромолекулы фторполимера
|
2 S + 1 = 1 |
2 S + 1 = 3 |
2 S + 1 = 5 |
|||||
|
° R, А |
А Е , эВ |
° R, А |
А Е , эВ |
° R, А |
А Е , эВ |
||
|
Feпов-OH |
|||||||
|
2,02 |
3,67 |
2,09 |
3,98 |
2,13 3,57 |
|||
|
^епо"в" |
|||||||
|
« з к О 5 д Е н К |
C * |
2,25 |
3,32 |
2,26 |
3,73 |
2,45 |
3,18 |
|
~ C |
2,13 |
3,33 |
2,16 |
3,70 |
2,30 |
3,07 |
|
|
C |
2,14 |
3,74 |
2,17 |
4,09 |
2,33 |
3,47 |
|
|
С / |
2,38 |
3,87 |
2,40 |
4,25 |
*) |
*) *) |
|
Таблица 3
Разности энергий структур с различной мультиплетностью
[ A ' пов = Е пов ( М = 2) - Е „в ( М = 4) ; А" „о8 = E „o8 ( М = 4) - Е в ( М = 6); д ' = Е ( М = 1)- Е ( М = 3); А" = Е ( М = 3) - Е ( М = 5) ; см. рис. 6]
|
Структура |
A ' пов , эВ |
A '/ пов , эВ |
|
Fe пов |
0,10 |
1,58 |
|
Fe-OH |
0,41 |
1,16 |
|
Fe---C— |
0,51 |
1,02 |
|
Fe---C^ |
0,47 |
0,95 |
|
Fe---C^ |
0,45 |
0,95 |
|
Fe---c'^ |
0,47 |
*) |
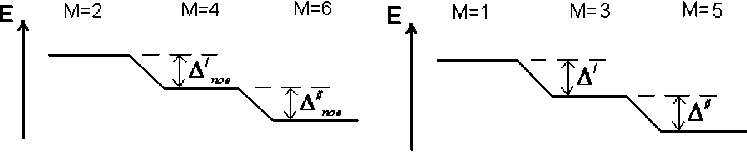
(а)
(б)
Рис. 6. Схема изменения полных энергий E структур с различной мультиплетностью (M = 2 S + 1, S – полный спин системы) для структур:
а) ОЖ-Fe2+ и б) или
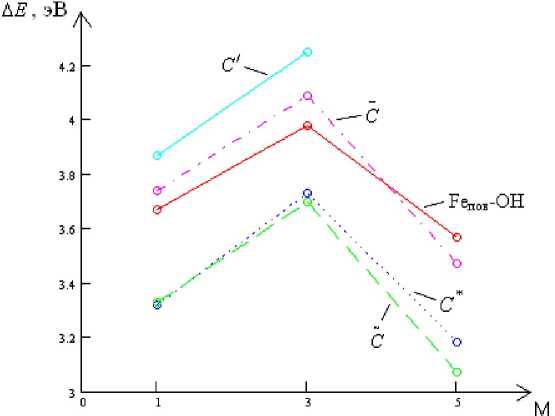
Рис. 7. Энергии разрыва связей А Е поверхностного ОЖ-Fe2+-центра с остатком макромолекулы ФП или группой OH при различных мультиплетностях хемосорбционных структур
Таблица 4
Энергии £ / аа ) , е"^а ) нескомпенсированных спинов электронов:
-
а) поверхностного ОЖ-Fe2+-центра для различных мультиплетностей М системы;
-
б) остатков макромолекулы фторполимера (М = 2)
Fe пов
а
М
2
4
6
е 'а ) ,эВ
–1,69
–1,83
–3,84 –4,15
–1,82 –4,24 –4,83
–4,84 –4,85
б
C *
~
C
C -
С /
е"а ) , эВ
–7,54
–7,28
–7,49
–8,59
Таблица 5
Смещения энергий верхних занятых состояний Д е для хемосорбционной структуры Feпов-OH для состояний с различной мультиплетностью М
|
Fe пов -OH |
|||||||
|
М |
1 |
3 |
5 |
||||
|
А е , эВ |
–1,13 |
–1,62 |
–1,81 |
–2,01 |
–2,07 |
–2,19 |
–2,31 |
Таблица 6
Смещения энергий верхних занятых состояний Де (эВ) при образовании контакта поверхности ОЖ-Fe2+ с остатком макромолекулы ФП для различных мультиплетностей М хемосорбционного комплекса
|
М |
1 |
3 |
5 |
|||||
|
5 О а § I 3 Я 3 м Р О Ь п ^ У 2 |
C * |
–2,48 |
–2,75 |
–2,84 |
–3,15 |
–3,30 |
–3,82 |
–3,84 |
|
~ C |
–2,13 |
–2,33 |
–2,41 |
–2,71 |
–2,93 |
–3,42 |
–3,55 |
|
|
C - |
–2,00 |
–2,24 |
–2,30 |
–2,57 |
–2,84 |
–3,32 |
–3,44 |
|
|
С / |
–2,69 |
–3,00 |
–3,08 |
*) |
*) |
*) |
*)*) |
|
Анализ приведенных на рисунке 5 спектров одноэлектронных состояний изученных систем позволяет сделать следующие выводы:
-
1) ОЖ-Fe 2+ - поверхностные структуры . Верхним занятым состояниям отвечают связывающие орбитали Fe-O-связей для состояний с мультиплетностью М = 2; 4; 6. А также зона занятых состояний содержит кроме связывающих состояний Fe-O-связей состояния, отвечающие неподеленным парам атомов кислорода и 3 d -орбиталям атомов железа в случае М = 4; 6) энергии последних превышают энергии электронов неподеленных пар атомов кислорода). Энергии верхних занятых орбиталей, спины электронов которых нескомпенси-рованы в рамках метода ТФП они соответствуют энергиям ионизации электронов), в целом увеличиваются по модулю) с увеличением мультиплетности поверхностной структуры табл. 4).
Вакантным состояниям отвечают состояния, соответствующие разрыхляющим орбиталям связей Fe-O, среди которых имеются также состояния, вклад в которые превносят преимущественно орбитали атомов железа.
-
2) В результате образования поверхностного гидроксида ПГ ) имеет место стабилизация структуры (см. табл. 5), одна из причин которой - уменьшение энергии А е верхнего занятого
состояния. Величина I A s | (табл. 5) нарастает с увеличением мультиплетности системы и в целом коррелирует с энергиями разрыва связей Fe-OH (табл. 2).
В верхние занятые состояния ПГ преимущественный вклад вносят 3 d -орбитали железа [для высокоспиновых систем (М = 3; 5)]; в случае М = 1 эти состояния оказываются несколько глубже, а верхним состояниям отвечают связывающие орбитали связей Fe-O. Для ПГ с М = 3 и 5 связывающие состояния связей Fe-O лежат энергетически глубже по сравнению с энергиями 3 d -Fe-орбиталей.
Вакантные состояния (ВС) ПГ подразделяются на группы, в каждую из которых входят состояния, преимущественный вклад в которые вносят разрыхляющие орбитали Fe-OH-связей либо только орбитали атомов железа. Состояния первой группы соответствуют нижней границе зоны ВС, а также могут иметь и более высокие энергии. Состояния второй группы – выше нижней границы зоны ВС (насколько выше, зависит от величины М).
2 +
-
3) - структуры . В верхние занятые состояния преимущественный вклад
вносят 3 d -состояния атома железа, причем в большей степени это относится к высокоспиновым системам. Состояниям с более глубокими энергиями отвечают связывающие орбитали хемосорбционных связей, а с еще более глубокими энергиями – связывающие орбитали Fe-O-связей и неподеленных пар электронов атомов кислорода; в нижние вакантные состояния основной вклад вносят 4 p - или 3 d -орбитали атомов железа, более высокоэнергетическим состояниям отвечают разрыхляющие орбитали хемосорбционных связей и связей Fe-O.
Список литературы Энергетический спектр электронов поверхностной фазы оксида железа, взаимодействующей с макромолекулами фторполимеров при действии СО2-лазерного излучения
- Эварестов Р.А. Квантово-химические методы в теории твердого тела. Л.: ЛГУ, 1982. 279 с.
- Жидомиров Г.М. Кластерные приближения в квантово-химических исследованиях хемосорбции и поверхностных структур//Итоги науки и техники. М.: ВИНИТИ, 1984. Т. 9. С. 3-161.
- Литинский А.О. Квазимолекулярные модели хемосорбции и поверхностных структур: Дис.... д-ра хим. наук. М.: МГУ, 1987. 344 с.
- Особенности воздействия лазерного излучения на фторэластомеры при формировании новых антифрикционных и защитных покрытий/Е.И Тескер [и др.]//Физика и химия обработки материалов. 2001. № 3. С. 28-33.
- Пенкаля Т. Очерки кристаллохимии. Л.: Изд-во «Химия», 1974. 496 с.
- Исследование механизма формирования адгезионных связей фторполимерных пленочных покрытий с металлической подложкой под действием излучения CO2-лазера/Е.И. Тескер [и др.]//Физика и химия обработки материалов. 2005. № 1. С. 70-77.
- Бранд Дж. Применение спектроскопии в органической химии/Дж. Бранд, Г. Эглинтон. М.: Мир, 1967. 279 с.
- Becke A.D. Density-functional thermochemistry. III. The role of exact exchange/A.D. Becke//Journal of Chemical Physics. 1993. Vol. 98. P. 5648-5652.
- Lee C. Development of the Colle-Salvetti correlation-energy formula into a functional of the electron density/С. Lee, W. Yang, R.G. Parr//Physical Review. 1988. Vol. 37. P. 785-789.
- Miehlich B. Chem. Phys. Lett./B. Miehlich, A. Savin, H. Stoll. 1989. Vol. 157. 200 p.
- Dunning T.H. Modern Theoretical Chemistry/T. H. Dunning, Jr. Hay, P. J. Hay. 1976. Vol. 3. P. 1-28.
- Hay P.J. Ab initio effective core potentials for molecular calculations. Potentials for the transition metal atoms Sc to Hg/P.J. Hay, W.R. Wadt//Journal of Chemical Physics. 1985. Vol. 82. P. 270-283.
- Wadt W.R. Ab initio effective core potentials for molecular calculations. Potentials for main group elements Na to Bi/W. R. Wadt, P. J. Hay//J. Chem. Phys. 1985. Vol. 82. P. 284-298.
- Hay P.J. Ab initio effective core potentials for molecular calculations. Potentials for K to Au including the outermost core orbitals/P. J. Hay, W. R. Wadt//J. Chem. Phys. 1985. Vol. 82. P. 299-310.


