Энтропийная составляющая в уравнении Гиббса-Гельмгольца для характеризации изменения степени усвоения кулинарных блюд
Автор: Позняковский В.М., Алексанян И.Ю., Нугманов А.Х.-Х., Фоменко Е.В.
Журнал: Вестник Красноярского государственного аграрного университета @vestnik-kgau
Рубрика: Технические науки
Статья в выпуске: 9, 2016 года.
Бесплатный доступ
В статье предлагается использовать термодинамический подход к определению ки-нетических коэффициентов внутреннего и внешнего массо- и энергопереноса, а также граничных условий в процессе кулинарной об-работки, необходимых для решения матема-тической модели переноса пищевых компо-нентов и энергетической ценности. Авторами изучаются теплообменные процессы при кон-струировании и приготовлении кулинарных блюд. Методами термодинамического анализа находятся показатели связи влаги с материа-лом, а также степени усвоения пищевых ком-понентов и калорий организмом человека. Вы-делены характерные особенности сорбции в зависимости от внутримолекулярного взаи-модействия углеводородных цепей, их длины, разветвленности и энергии. Авторами указы-вается на преобладание осмотического меха-низма сорбции, поскольку количество харак-терных участков и точек перегиба на изо-термах сорбции материалов связано с нали-чием ячеек, закрытых и открытых капилля-ров, клеточных оболочек и мицелл, свой-ственных растительным компонентам. При количественной оценки характера изменений термодинамических составляющих уравнения Гиббса-Гельмгольца авторами использовались положения статики процессов взаимодей-ствия с водой, а также приѐмы анализа изо-терм сорбции для изохорно-изобарно-изотерми-ческого процесса. В процессе иссле-дования, на основе выведенных зависимостей для кулинарных блюд получены значения эн-тропийной составляющей при влажности ма-териала до и после переработки. Рассмотре- ны зависимости вида и характера изотерм сорбции большинства пищевых продуктов, отличия численных значений термодинамиче-ских коэффициентов массопереноса и гигро-скопических характеристик. Для решения ма-тематической модели переноса пищевых ком-понентов и калорий авторами представлены результаты экспериментального определения кинетических коэффициентов внутреннего и внешнего массо- и энергопереноса, граничные условия в процессе обработки. Авторами предлагается на основе термодинамического анализа кривых равновесия определять сте-пень усвоения пищевых компонентов организ-мом человека, интенсивность их переноса и энергетическую ценность.
Термодинамический ана-лиз, термодинамическая энтропия, энергия свя-зи гиббса, уравнение гиббса - гельмгольца, энергетическая ценность
Короткий адрес: https://sciup.org/14084787
IDR: 14084787 | УДК: [641.
Entropy component in the equation of Gibbs-Helmholtz to characterize changes in the degree of assimilation of culinary dishes
In the article it is suggested to use the thermo-dynamics going near determination of kinetic coef-ficients internal and external mass- and ener-gytransfer, and also border terms in the process of culinary treatment, necessary for the decision of mathematical model of transfer of food components and power value. Authors are study heat-exchange processes at constructing and preparation of culi-nary dishes. The methods of thermodynamics anal-ysis are indexes of connection of moisture with ma-terial, and also degrees of mastering of food com-ponents and calories by the organism of man. The characteristic features of persorption are distin-guished depending on intramolecular cooperation of hydrocarbon chains, their length, ramified and energy. Specified authors on predominance of os-motic mechanism of persorption, as an amount of characteristic areas and inflectionpoints on the iso-therms of persorption of materials is related to the presence of cells, closed and open capillaries, cel-lular shells and micelles, peculiar to the vegetable components. At quantitative estimation of character of changes of thermodynamics constituents of equalization of Gibbs-Helmholtz authors positions of statics of processes of co-operating were used with water, and also receptions of analysis of iso-therms of persorption for isochoric- isobar- isother-mal processes. In the process of research, on the basis of the shown out dependences for culinary dishes the values of entropy constituent are got at humidity of material before and after processing. Dependences of kind and character of isotherms of persorption of most food products, difference of numeral values of thermodynamics coefficients of transfer of mass and hygroscopic descriptions are considered. For the decision of mathematical model of transfer of food components and calories authors are present the results of experimental determina-tion of kinetic coefficients internal and external mass- and energytransfer, border terms in the pro-cess of treatment. It is suggested authors on the basis of thermodynamics analysis of curves of equi-librium to determine the degree of mastering of food components the organism of man, intensity of their transfer and power value.
Текст научной статьи Энтропийная составляющая в уравнении Гиббса-Гельмгольца для характеризации изменения степени усвоения кулинарных блюд
Введение . Феноменологический подход в науке позволяет создавать теории для наблюдаемых явлений (феноменов), например, термодинамика в физике, где описание поведения макроскопических тел в тепловых процессах с помощью небольшого числа макроскопических параметров и некоторых функций от этих параметров оказывается достаточным для решения большого круга задач, представляющих технический интерес.
Основные положения термодинамики справедливы практически для любой системы и использование термодинамических методов (циклов и потенциалов) позволяет описывать даже сложные физические процессы.
Исследование статики тепломассообменных кулинарных процессов является базой для научно-обоснованного анализа правильности применения известных и создания оригинальных способов моделирования, проектирования и конструирования пищевых многокомпонентных смесей.
Цель исследования : определение степени усвоения пищевых компонентов организмом человека на основе термодинамического анализа кривых равновесия ингредиентов, входящих в пищевую систему до и после кулинарной обработки.
Исходя из цели исследования, становится необходимым решение следующего ряда задач: определение для кулинарных продуктов значения энтропийной составляющей при заданной влажности материала до и после переработки компонентов; определение энергии связи влаги с материалом до и после теплового воздействия; степени усвоения пищевой энергии организмом человека методами термодинамического анализа.
Объекты и методы исследования. В качестве объектов исследования являлись овощи (столовая свекла ГОСТ Р 51811-2001 «Свекла столовая свежая, реализуемая в розничной торговой сети», морковь ГОСТ Р 51782-2001 «Морковь столовая свежая, реализуемая в розничной торговой сети» и картофель свежий продовольственный ГОСТ Р 51808-2013 (ЕЭК ООН FFV-52:2010) «Картофель продовольственный. Технические условия») до и после варки на пару.
Активность воды определялась тензотер-мическим (эксикаторным) методом Ван-Бамелена, на экспериментальной установке, которая состоит из эксикатора, содержащего водный раствор серной кислоты, весов аналитических с погрешностью не более 0,1 % (второй класс точности по ГОСТ 24104-88), хро-мель-копелевой термопары ХК(L) ТП-011 с погрешностью не более 0,5 К (характеристики прибора регламентируются ГОСТ Р 8.585-2001), подсоединенной к мультиметру.
Степень усвоения кулинарной продукции организмом Квсв определяли, получив значение энтропийной составляющей при необходимой по технологии влажности материала до и после обработки (разница энтропийных составляющих).
Исследования проводились в 3–5-кратной повторности. Результаты исследований обрабатывались современными методами расчета статистической достоверности измерений, а также с помощью компьютерных программ и являются достоверными.
Термодинамический анализ на основе обработки изотерм сорбции (десорбции), зависимости между равновесными параметрами (относительной влажностью воздуха или активностью воды и влагосодержанием продукта Aw = f( Up)) определяет не только энергию связи влаги с материалом, но и степень усвоения пищевых компонентов и калорий организмом человека, так как энергия связи влаги с сухим веществом зависит от связи молекул, частиц или фракций между собой, т. е. эти силы взаимодействия между собой и водой взаимосвязаны и в большой степени определяются энергетической энтропийной составляющей, особенно при диспергировании продукта, его механической или тепловой обработке (измельчении, варке и т. п.) [1].
Совпадает вид и характер изотерм сорбции большинства пищевых продуктов. Незначительные расхождения между численными значениями термодинамических коэффициентов массо-переноса и гигроскопических характеристик можно объяснить разными видами тепловой обработки или гидролиза сырья. Поскольку продукты животного и растительного происхождения относятся к сложным биополимерным системам, то применимы некоторые положения физической химии полимерных и белковых веществ.
В зависимости от внутримолекулярного взаимодействия углеводородных цепей, их длины, разветвленности и энергии выделяются характерные особенности сорбции. Количество характерных участков и точек перегиба на изотермах сорбции материалов обусловлено наличием ячеек, закрытых и открытых капилляров, клеточных оболочек и мицелл (поскольку присутствуют растительные компоненты), которые предполагают преобладание набухания – осмотического механизма сорбции.
В случае нахождения диапазона влагосо-держаний, лимитирующего тепломассобменный процесс в гигроскопической области, механизм массопереноса при обезвоживании определяем формой и энергией связи влаги с материалом, а также частиц или фракций между собой [2].
Энергия связи влаги с материалом:
E =
( dAF' — Iе U p )
- R • T • In A w . (1)
Продифференцируем уравнение Гиббса – Гельмгольца:
A F = A E - T •A S (2) где - a s ; a e (соответственно изменения внутренней энергии (энтальпии) и энтропии, по Up при Р, T = const.
Получим:
dA F
— t5 Up
V p J T, P dAE —
[dUp v p J T, P
- T •
( dA S ^
I6 U p J
Для получения выражения по дифференциальному изменению энтропии связанной воды, частиц или фракций друг с другом, продифференцируем это выражение по Т:
d
(dAF ^
( dAS )
— dT dUn v p J t , P
( dAS } | d UD v p J t , P
d ( RT In A w ) ^
d T
II
—
UP )
\ p J T , P
Для количественной оценки характера изменений термодинамических составляющих уравнения Гиббса-Гельмгольца используем положения статики процессов взаимодействия с водой и приемы анализа изотерм сорбции для изохорно-изобарно-изотермического процесса, где
a(As ) „ _ - _ T •——- - энтропийная составляющая сво- dUp бодной энергии [4].
Характер изменения t •d(AS) свидетель-d Up ствует о значительной гибкости макромолекул, наличии полупроницаемых мембранных оболочек (клеточных оболочек, стенок мицелл) и ориентационном, структурном (иммобилизацион-ном) и осмотическом механизме их взаимодействия с водой.
Уравнение Гиббса-Гельмгольца базируется на правиле фаз Гиббса, определяющем число степеней свободы системы (число независимых параметров, которые можно выбирать произвольно, и они определяют значения всех остальных параметров): Sсс = k – f + 2, где k – число компонентов, f – число фаз.
При тепловой и механической обработке (диспергировании) системы (пищевых продуктов или смесей), на первый взгляд сохраняется число компонентов, а число подобных фаз, фракций, частиц, контактирующих между собой, возрастает, что по идее уменьшает число степеней свободы системы Sсс, однако при этом уменьшается связь между частицами, энтропия системы растет, следовательно растет и Sсс, а также степень усвоения компонентов диспергированных частиц организмом человека [3].
Этот парадокс можно объяснить тем, что k – это число переносимых компонентов, т. е., к примеру, при тонком измельчении, тепловой обработке (разваривании и т. п.) число компонентов возрастает, а перенос между подобными фазами, т. е. частицами с одинаковыми характеристиками (потенциалами) отсутствует. Иными словами, в аспекте массопереноса число компонентов при обработке материала увеличивается, а число фаз не меняется, что и приводит к росту энтропии и числа степеней свободы системы, и, как следствие, степени усвоения ценных компонентов пищевых продуктов организмом индивидуума.
Особенно отметим, что энтропийная составляющая в уравнении Гиббса-Гельмгольца для определения свободной энергии характеризует, в основном, состояние структурной, иммобили-зационной – внутриклеточной влаги, энтропия которой растет при разрушении ячеек, замкнутых микро- и макрокапилляров, клеток, что и происходит при механической и тепловой обработке пищевых продуктов [4]. При этом растет энтропия и числа степеней свободы системы, и, как следствие, степень усвоения переносимых компонентов пищевых продуктов, пищевых калорий, витаминов и другого организмом индивидуума.
Определив из полученных зависимостей для любого продукта значение энтропийной составляющей при необходимой по технологии влажности материала до и после обработки (разница энтропийных составляющих), можно определить степень усвоения переносимых компонентов пищевых продуктов, пищевых калорий (изменение калорийности), витаминов и другого организмом индивидуума, а также изменение энергетической и пищевой ценности продукта в процессе обработки.
Данная разница энтропийных составляющих позволит определить кинетические коэффициенты внутреннего и внешнего массо- и энергопереноса, а также граничные условия в процессе обработки, необходимые для решения математической модели переноса пищевых компонентов и калорий. Учитывая, что влажность продукта до и после, а также при различной степени обработки может быть варьируемой, необходимо получить кривые равновесия и их математическую интерпретацию для определения диапазонов влияющих факторов и определения коэффициентов и параметров при любой влажности и степени обработки исследуемого материала.
Учитывая, что пищевая энергетическая ценность не равна общей энергии потребляемых продуктов, степень усвоения энергии организмом можно оценить критерием (симплексом) – отношением пищевой калорийности или энтропийной составляющей в уравнении Гиббса-Геймгольца к общей энергии Гиббса, т. е.
Эу Эу
К усв = о = ад?
Э общ RTI nA w + T^j-
Эу
= djF д д- д Up + 1 д Up или j^L
Если в знаменатель данных уравнений подставить разность калорийности или энтропийной составляющей продукта до и после переработки, то получим величину, характеризующую изменения степени усвоения в процессе реализации кулинарной технологии.
Результаты исследования и их обсуждение. По экспериментальным и расчетным данным построены графики изотерм сорбции картофеля, свеклы и моркови до и после тепловой и механической обработки (рис. 1).
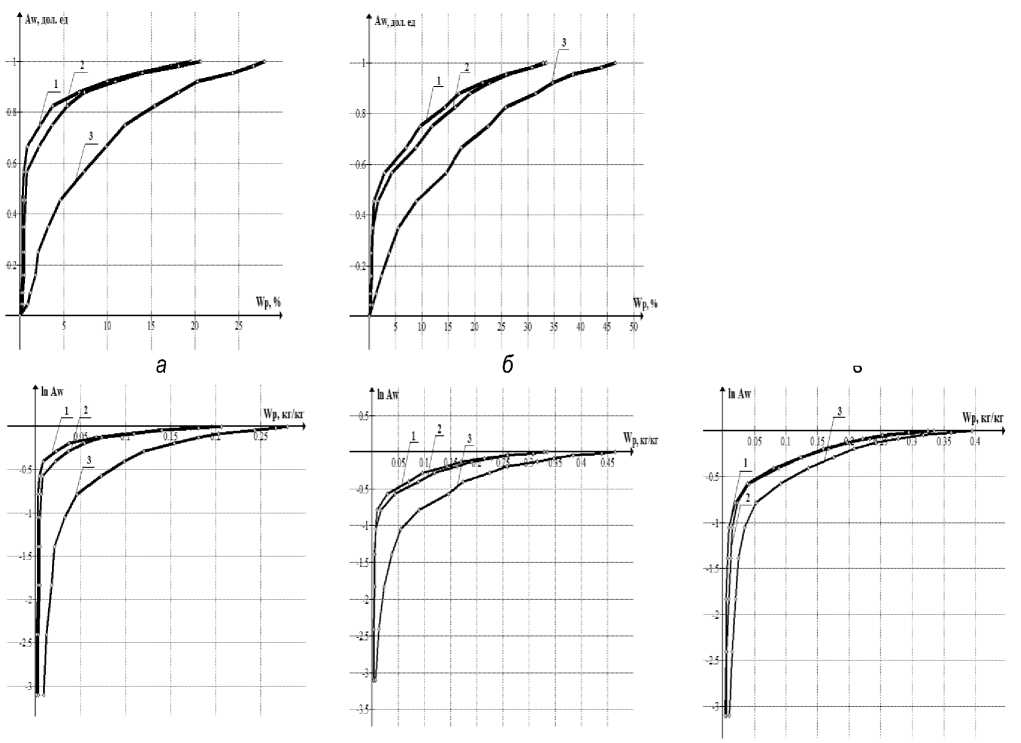
а
б
в
Рис. 1. График изотерм сорбции: а – картофеля; б – свеклы и в – моркови до и после тепловой и механической обработки при температуре 25 °С; 1 – продукт отварной измельченный;
2 – продукт отварной целый; 3 – продукт свежий
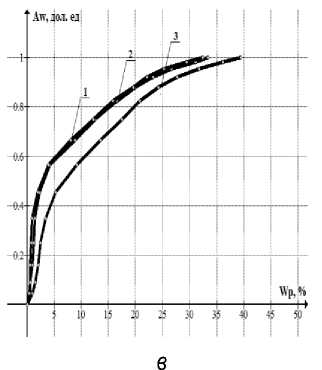
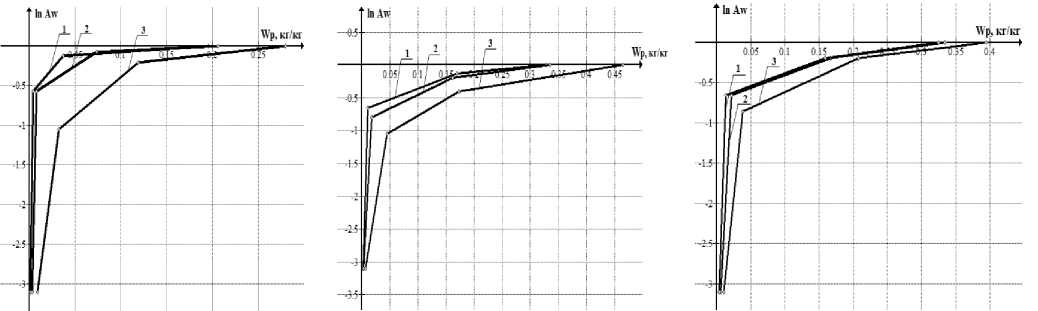
Проведена аппроксимация кривых изотерм сорбции овощей линейными уравнениями по зонам (рис. 2), что позволит получить необходимые данные для выявления закономерностей изменения калорийности продуктов в результа те обработки и степени усвоения ценных компо нентов пищи организмом человека.
кусв для случая варки картофеля, свеклы и моркови на пару и его дальнейшей протирки (измельчение) равен соответственно 0,25; 0,30; 0,14.
Полученные данные, как и комплекс зависимостей структурно-механических и теплофизических характеристик пищевых продуктов и смесей от влияющих факторов, необходимы для физико-математического моделирования процессов обработки продуктов питания и проникновения энергетически ценных компонентов в материалы и организм индивидуума.
Термодинамический анализ может использоваться для решения вопросов устойчивости отдельных фаз и соединений, а также для установления наиболее общих закономерностей протекания энергетического взаимодействия в пищевых материалах. Выяснение последовательности перераспределения энергии, ее термодинамической вероятности в тех или иных пищевых системах помогает объяснять процессы, происходящие в системе и находить пути совершенствования технологии.
а б в
Рис. 2. Линейно аппроксимированные графики изотерм сорбции: а – картофеля; б – свеклы; в – моркови до и после тепловой и механической обработки при температуре 25 °С;
1 – продукт отварной измельченный; 2 – продукт отварной целый; 3 – продукт сырой
Выводы . Формализованное математическое описание технологии, направленное на создание оригинальных пищевых систем, основанное на теплофизическом и термодинамическом эк-сергетическом подходе (с учетом энтропии системы) позволит достигнуть рациональных решении поставленных задач. Ведь абстрактное понятие энтропии, как и понятие энергия, искусственно введенное, но полезное для термодинамических расчетов, стало часто использоваться не только в границах термодинамики, но и в статистике, информационных технологиях, математике, лингвистике, интеллектуальной области и др.
Термодинамический анализ может использоваться для решения вопросов устойчивости отдельных фаз и соединений, а также для установления наиболее общих закономерностей протекания энергетического взаимодействия в пищевых материалах. Выяснение последова- тельности перераспределения энергии, её термодинамической вероятности в тех или иных пищевых системах помогает объяснять процессы, происходящие в системе, и находить пути совершенствования технологии, опираясь на феноменологические исследования. Первым шагом определения последовательности и термодинамической вероятности перераспределения энергии в пищевых системах и является степень усвоения компонентов организмом человека.
Список литературы Энтропийная составляющая в уравнении Гиббса-Гельмгольца для характеризации изменения степени усвоения кулинарных блюд
- Титова Л.М., Алексанян А.И., Прямухин С.В. и др. Развитие методов моделирова-ния процессов тепломассообмена в поли-дисперсных системах на основе комплекс-ного анализа их сорбционных свойств//Вестн. Астрахан. гос. техн. ун-та. -2014. -№ 1 (57). -С. 115-118.
- Вода в пищевых продуктах: пер. с англ.//под ред. Р.Б. Дакуорта. -М.: Пищевая промышленность, 1980. -575 с.
- Нугманов А.Х.-Х. Научно-практические под-ходы к конструированию многокомпонент-ных пищевых систем в технологии обще-ственного питания. -Астрахань, 2016. -88 с.
- Осипов А.И., Уваров А.В. Энтропия и ее роль в науке//Соросовский образователь-ный журнал. -2004. -№ 1. -С. 70-79.


