Этапное хирургическое лечение с временной лапаростомией у больных послеоперационным перитонитом
Автор: Жариков Андрей Николаевич, Лубянский Владимир Григорьевич, Алиев Александр Руштиевич, Омаров Н.Б., Власов К.Е., Сероштанов Василий Владимирович, Иваницкая Е.А.
Журнал: Московский хирургический журнал @mossj
Рубрика: Клинические исследования
Статья в выпуске: 1 (41), 2015 года.
Бесплатный доступ
Проведен анализ хирургического лечения 19 больных с послеоперационным перитонитом, возникшим вследствие множественных перфораций тонкой кишки и несостоятельности энтероэнтероанастомозов. Тяжесть состояния по шкале APACHE II составила 17,3±1,4 баллов, тяжесть перитонита, согласно индексу брюшной полости (В.С. Савельев с соавт., 2009), - 22,6±0,2 балла. Всем пациентам выполнялись резекции тонкой кишки с отсроченным межкишечным анастомозированием в процессе плановых санаций брюшной полости. Расположение перфорированных полимерных пленок для формирования временной лапаростомы под края передней брюшной стенки показало эффективность у 9 (47,4%) больных с преобладанием флегмоны передней брюшной стенки и у 5 (26,3%) пациентов при фиксации ее к коже при наличии компартмент-синдрома. Окончание программированных реалапаротомий, наложение отсроченного межкишечного анастомоза и закрытие лапаростомной раны осуществлялось при улучшении состояния больного (APACHE II
Послеоперационный перитонит, отсроченный анастомоз, релапаротомия, лапаростомия
Короткий адрес: https://sciup.org/142211195
IDR: 142211195 | УДК: 616.381-002-089.168.1-06-089.85
Текст научной статьи Этапное хирургическое лечение с временной лапаростомией у больных послеоперационным перитонитом
В последнее время продолжают обсуждаться вопросы хирургической тактики с применением программированных санаций брюшной полости у больных с распространенным перитонитом [8, 9, 17]. Показаниями к их выполнению служат трудности в устранении источника перитонита (панкреонекроз, абсцессы живота, массивные плотно фик- сированные наложения фибрина и т.д.) [4, 11, 14]. Использование кишечных швов при ушивании дефектов полых органов или формирование первичных тонкокишечных анастомозов при распространенном перитоните сопряжено с высокой частотой их несостоятельности [4, 6]. С учетом этих позиций в настоящее время восстановление непрерывности тонкого кишечника после резекции сегментов ди- гестивного тракта в условиях тяжелого распространенного перитонита может быть отложено, а межкишечный анастомоз может быть наложен в отсроченном порядке [13]. Наряду с этим, при использовании тактики этапного хирургического лечения лапаростомия продолжает оставаться одним из эффективных способов открытого ведения перитонита [2, 5, 12, 15, 17]. Все большую актуальность и развитие она приобретает при наличие синдрома внутрибрюшной гипертензии (абдоминальный компартмент-синдром) и его влияния на прогрессирование полиорганной недостаточности [1, 3, 10]. Ранее было отмечено, что при формировании лапаростомы с использованием марлевых салфеток, быстро наступает раневое истощение, суперинфицирование, прогрессирование явлений острого висцерита, образование наружных кишечных свищей, обширных вентральных грыж [4]. В настоящее время широко внедряются новые способы и материалы в формировании лапаростом у больных с перитонитом, включающие мешки «Богота» [11], сэндвич-технологии [17], вакуумное дренирование [7, 16]. Однако на сегодняшний день вопрос об оптимальном варианте завершения операций при программированных санациях брюшной полости, временном или окончательном способе закрытия срединной раны у больных с послеоперационным перитонитом остается открытым.
Материалы и методы исследования
Основу работы составили 19 больных с послеоперационным перитонитом (ПП), поступивших в клинику госпитальной хирургии с 2011 по 2014 год. Мужчин было 14 (73,7%), женщин — 5 (26,3%). Средний возраст составил 52,5±1,4 года. Послеоперационный перитонит возник после операций по поводу острой спаечной кишечной непроходимости, травм брюшной полости, инфицированного панкреонекроза и являлся следствием множественных (от 2 до 5) перфораций стенки тонкой кишки и несостоятельности межкишечных анастомозов. Количество операций на предыдущих этапах до поступления в клинику составило 2,1±0,3. Тяжесть состояния пациентов по шкале APACHE II достигала 17,3±1,4 баллов, тяжесть перитонита (индекс брюшной полости В.С. Савельева) — 22,6±0,2 балла. Оперативное лечение включало в себя проведение обструктивных резекций тонкой кишки с кишечной интубацией приводящих отделов без наложения анастомоза (E.Г. Григорьев, 1996). Во время первой релапаротомии после уточнения характера, распространенности воспалительного процесса в брюшной полости, причины образования дефекта в стенке тонкой кишки или правой половины ободочной кишки (острая перфорация, несостоятельность кишечных швов, некроз) выполняли резекцию пораженного участка тонкой кишки (и правостороннюю гемиколэктомию) с формированием культей тонкой кишки, или тонкой и ободочной кишки путем погружения в 2 кисетных шва.
Заглушенные участки кишки не выводили на переднюю брюшную стенку, а оставляли в брюшной полости. Декомпрессию тонкой кишки осуществляли с помощью назоинтестинальной интубации ее приводящих отделов с последующей активной аспирацией кишечного содержимого после операции.
В дальнейшем восстановление непрерывности желудочно-кишечного тракта выполнялось в процессе программированных санаций брюшной полости, режим которых определялся после первой релапаротомии с формированием временных лапаростом после каждой санации. Для этого использовались полимерные перфорированные пленки, располагаемые в различных позициях (под переднюю брюшную стенку, путем фиксации к коже), в зависимости от наличия флегмоны передней брюшной стенки или абдоминального компартмент-синдрома. Критерием к наложению отсроченного межкишечного анастомоза во время программированных санаций служило стихание острого воспаления в брюшной полости (светлый экссудат, единичные налеты фибрина, уменьшение отека и инфильтрации кишечной стенки, блестящий серозный покров). Если мы отмечали прогрессирование тяжелого послеоперационного перитонита, появление острых перфораций на фоне ишемических изменений кишки вследствие мезентериального тромбоза, развитие полиорганной недостаточности, мы отказывались от наложения соустья и выводили энтеростому на переднюю брюшную стенку. При благоприятном течении после купирования перитонита и наложения отсроченного межкишечного анастомоза проводили окончательное закрытие лапаростомной раны вторичными швами, в ряде случаев с использованием сетчатых имплантов.
Результаты и обсуждение
Основными проблемами в лечении больных послеоперационным перитонитом были флегмона передней брюшной стенки и абдоминальный компартмент-синдром. Использование марлевых тампонов для формирования лапаростомы обуславливало нарушение дренажной функции и образование плотных сращений марли с подлежащими кишечными петлями, а применение дренажных трубок или материалов из пластмассы — к повышенной травматизации кишечной стенки с риском ее перфорации и образования несформи-рованных кишечных свищей. В начале нашей работы для изоляции петель кишечника от внешней среды, тканей передней брюшной стенки, а также для создания адекватного оттока гнойного экссудата в качестве материала для формирования временной лапаростомы были использованы полиэтиленовые пленки (пакеты для инфузионных растворов) с множественными отверстиями (рис. 1а). Пленка свободно располагалась над петлями кишечника, хорошо отграничивая их от краев раны передней брюшной стенки, легко удалялась при выполнении программированной санации брюшной полости. В ряде случаев формирование временной лапаростомной раны заканчивали наложением редких лигатур (2–3) только на кожные края передней брюшной стенки без захвата апоневроза. Однако используемая пленка была достаточно плотной, плохо расправлялась, могла часто мигрировать в нижние отделы брюшной полости, расположение ее под передней брюшной стенкой ограничивало перспективы снижения внутрибрюшного давления. Учитывая вышеуказанные недостатки, для временного формирования лапаростомных ран были использованы другие синтетические материалы, и в частности, хорошо себя зарекомендовавшее «Полимерное покрытие для лапаростомии при перитоните» из материала реперен. Указанное полимерное покрытие представляет собой полимерную пленку толщиной 100–400 мкм с отверстиями для оттока экссудата. Одна ее поверхность (париетальная) имеет рельефный рисунок и обладает способностью к адгезии брюшной стенки, что препятствует дислокации. Другая поверхность (висцеральная) является сверхгладкой, неровности составляют до 10–20 нм. Эти качества материала обеспечивали свободное скольжение под пленкой петель кишечника, отсутствие тенденции к образованию спаек, легкое ее отделение от органов брюшной полости при выполнении программированной санации брюшной полости. Указанное полимерное покрытие мы вначале располагали под края раны передней брюшной стенки при ее флегмоне (рис. 1б).
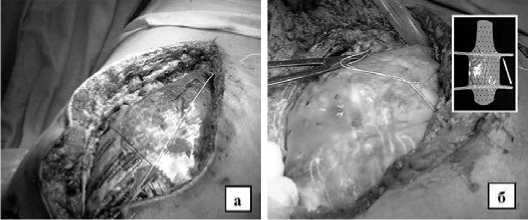
Рис. 1. Использование перфорированных полиэтиленовых и полимерных материалов для формирования лапаростомных ран у больных с ПП, осложненным флегмоной передней брюшной стенки: а – стерильный перфорированный пакет для инфузионных растворов; б – полимерное покрытие из материала реперен
Наряду с этим, у 5 больных послеоперационным перитонитом с высокими показателями внутрибрюшного давления (более 14 мм рт. ст.) эти временные перфорированные полимерные эндопротезы были апробированы с расположением их на передней брюшной стенке, что способствовало увеличению объема брюшной полости. Круговая фиксация пленки узловыми швами к коже препятствовала ее дислокации и выпадению кишечных петель (рис. 2 а, б).
Кроме того, для борьбы с абдоминальным компартмент-синдромом в клинике широко применяется кишечная ин-
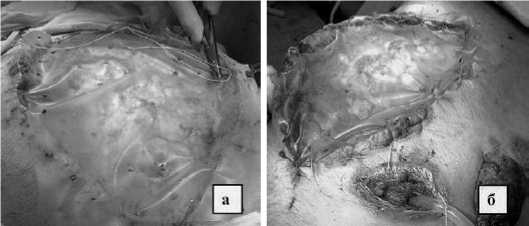
Рис. 2. Использование временных полимерных эндопротезов для формирования лапаростомы при послеоперационном перитоните с наличием синдрома внутрибрюшной гипертензии: а – фиксация пленки к коже, б – окончательный вид лапаростомы тубация (Ю.М. Дедерер, 1962). Мы в своей работе на протяжении многих лет использовали назоинтестинальную интубацию [6]. Интраоперационное опорожнение кишечника позовляло не только лучше сформировать лапаро-стому, но и осуществлять в послеоперационном периоде кишечный лаваж, энтеросорбцию (ФишантС) и раннее энтеральное питание. Для кишечной интубации использовались как стандартные зонды, так и зонды оригинальной конструкции.
Количество программированных санаций брюшной полости у больных с послеоперационным перитонитом варьировало от 2 до 4 и в среднем составило 2,8±0,8. Интервал между санациями был равен 36–48 часов. Отсроченный межкишечный энтероэнтероанастомоз был наложен 7 (38,9%) больным, а анастомоз с ободочной кишкой (эн-теротрансверзоанастомоз) —у 10 (52,6%) больных. В 2 наблюдениях тяжесть послеоперационного перитонита не позволила выполнить отсроченное анастомозирование, что послужило основанием к выведению энтеростомы.
Расположение перфорированного полимерного покрытия в положении под брюшную стенку для временного формирования лапаростомной раны на этапах санаций брюшной полости показало свою эффективность у 9 (47,4%) больных послеоперационным перитонитом, осложненным флегмоной передней брюшной стенки. Использование полимерных пленок с фиксацией к коже передней брюшной стенки было востребовано у 5 (26,3%) больных послеоперационным перитонитом с преобладанием синдрома внутри-брюшной гипертензии (рис. 3 а, б).
Длительность открытого ведения брюшной полости при послеоперационном перитоните составила 14,6±1,2 суток. Критериями к окончанию этапа программированных санаций брюшной полости и переходу к полузакрытому методу ведения брюшной полости явилось купирование полиорган-ной недостаточности (APACHE II), клинико-лабораторные признаки снижения системной воспалительной реакции, уменьшение его тяжести по основной бальной шкале (индекс брюшной полости В.С. Савельева), восстановление
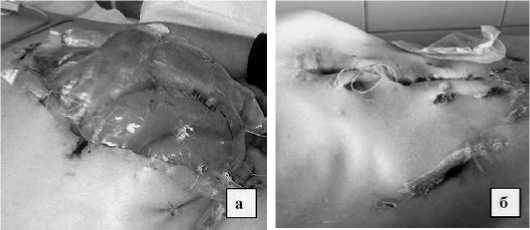
Рис. 3. Больной с послеоперационным перитонитом и абдоминальным компартмент-синдромом: а – формирование временной лапа-ростомы с использованием полиэтиленовой пленки, б – купирование перитонита, окончательное закрытие лапаростомы вторичными швами пассажа по кишечнику, нормализация показателей внутри-брюшного давления (табл. 1.)
Завершение программы этапного хирургического лечения послеоперационного перитонита проиходило в основном при снижении тяжести состояния пациента по шкале APACHE II менее 10 баллов, тяжести перитонита (индекс брюшной полости) менее 12 баллов и уменьшения уровня внутрибрюшного давления менее 12 мм рт. ст. В этот период разарабатывались мероприятия по окончательному закрытию лапаростомной раны. Они осуществлялись в более ранние сроки, не дожидаясь зрелых грануляций в ране и ригидности краев передней брюшной стенки. Наряду с традиционным подходом в окончательном закрытии лапаростомных ран (наложение вторично-отсроченных швов при гранулирующих ранах), в стремлении к формированию каркаса передней брюшной стенки в области лапаростомы мы использовали оригинальные решения. У 2 (10,5%) пациентов с послеоперационным перитонитом после последней программированной санации брюшной полости на лапаротомную рану устанавливали сетчатые импланты (Эслан — лавсан, Фторекс — лавсан с гидрофобным покрытием) (рис. 4).
Таблица 1
Критерии к временному наложению лапаростомы и ее окончательному закрытию у больных послеоперационным перитонитом
|
Показатели |
Временное наложение лапаростомы |
Окончательное закрытие лапаростомы |
p |
|
M±m |
M±m |
||
|
APACHE II (баллы) |
17,3±2,5 |
9,6±1,8 |
<0,05 |
|
Индекс брюшной полости (баллы) |
21,6±3,7 |
12,3±2,4 |
<0,05 |
|
Внутрибрюшное давление (мм рт. ст.) |
20,6±3,6 |
12,1+1,9 |
<0,05 |
Примечание: p – значимость различий между временным формированием и окончательным закрытием лапаростомы.
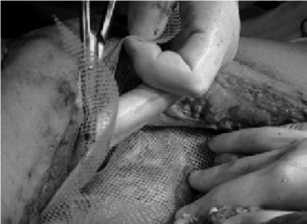
Рис. 4. Послеоперационный перитонит. Завершение этапа плановых санаций брюшной полости. Установка сетчатого импланта для окончательного закрытия лапаростомной раны
Как показали последующие наблюдения, установленные сетчатые импланты в лапаростомных ранах хорошо покрывались грануляционной тканью и были успешно закрыты дополнительными вторичными кожными швами.
В результате проведенного лечения удалось добиться выздоровления у 14 (73,7%) больных с послеоперационным перитонитом. Несостоятельности используемых 17 отсрочненных межкишечных анастомозов не было. Однако, несмотря на проводимое этапное хирургическое лечение, умерло 5 (26,3%) пациентов. Смерть наступила вследствие прогрессирования абдоминального сепсиса, по-лиорганной недостаточности.
Выводы
-
1. Тяжесть больного с послеоперационным перитонитом, распространенность воспалительного процесса в брюшной полости могут служить основанием к выполнению резекции тонкой кишки без наложения первичого межкишечного анастомоза.
-
2. Формирование временной лапаростомы является обязательным элементом этапа программированных са-нанций у больных послеоперацинным перитонитом. В качестве материалов могут быть использованы современные перфорированные полимерные пленки с расположением их под края передней брюшной стенки при ее флегмоне или путем фиксации к коже при наличии абдоминального компартмент-синдрома.
-
3. Окончание режима программированных санаций брюшной полости и отсроченнное межкишечное анастомозирование осуществляется при снижении показателей шкалы APACHE II менее 10 баллов, индекса брюшной полости менее 12 баллов, внутрибрюшного давления менее 12 мм рт. ст. и подразумевает раннее закрытие лапаро-стомной раны, в том числе с использованием сетчатых имплантов, увеличивающих каркасные свойства передней брюшной стенки.
Список литературы Этапное хирургическое лечение с временной лапаростомией у больных послеоперационным перитонитом
- Абакумов М.М., Смоляр А.Н. Значение синдрома высокого внутрибрюшного давления в хирургической практике//Хирургия. 2003. №12. С. 66-72.
- Быков А.Д., Жигаев Г.Ф., Цыбиков Е.Н. Лапаростомия при распространенном гнойном перитоните и ведение послеоперационной раны брюшной стенки//Бюллетень ВСНЦ СО РАМН. 2009. №3 (67). С. 313-314.
- Гареев Р.Н., Тимербулатов Ш.В., Тимербулатов В.М., Фаязов Р.Р. Интраабдоминальная гипертензия//Медицинский вестник Башкортостана. 2012. №4, (7). С. 66-73.
- Григорьев Е.Г., Коган А.С., Колмаков С.А. Хирургия тяжелых и осложненных форм распространенного гнойного перитонита//Бюллетень Восточно-Сибирского научного центра СО РАМН. 2005. №3. С. 228-229.
- Зубарев П.Н., Врублевский Н.М., Данилин В.И. Способы завершения операций при перитоните//Вестник хирургии им. И.И. Грекова. 2008. №6. С. 110-113.
- Лубянский В.Г., Жариков А.Н. коррекция синдрома энтеральной недостаточности у больных с послеоперационным перитонитом//Вестник национального медико-хирургического центра им. Н.И. Пирогова. 2010. №3,(5). С. 106-110.
- Оболенский В.Н., Ермолов А.А., Оганесян К.С., Аронов Л.С. Вакуум-ассистированная лапаростома в комплексном лечении больного с перитонитом и внутренним желчным свищом//Хирургия. 2013. №12. С. 91-94.
- Савельев В.С., Филимонов М.И., Гельфанд Б.Р. и др. Программированные релапаротомии в лечении распространенного перитонита, варианты тактических решений//Инфекции в хирургии. 2009. №4,(7). С. 26-31.
- Шуркалин Б.К., Горский В.А., Фаллер А.Л. Пролонгированная санация брюшной полости при лечении перитонита//Альманах клинической медицины. 2006. №11. С. 176-179.
- Ari K. Leppäniemi. Laparostomy: why and when?//Crit Care. 2010. Vol. 14(2). P. 216.
- Kirshtein B., Roy-Shapira A., Lantsberg L, Mizrahi S. Use of the «Bogota bag» for temporary abdominal closure inpatients with secondary peritonitis//Am Surg. 2007. Vol. 73. P. 249-52.
- López-Cano M., Pereira J.A., Armengol-Carrasco M. «Acute postoperative open abdominal wall»: Nosological concept and treatment implications//World j. Gastrointest. Surg. 2013. Vol. 5(12). P. 314-320.
- Ordoñez C.A., Puyana J.C. Management of peritonitis in the critically ill patient//Surg. Clin. North Am. 2006. Vol. 86(6). P. 1323-1349.
- Regner J.L., Kobayashi L., Coimbra R. Surgical strategies for management of the open abdomen//World j. Surg. 2012. Vol. 36(3). P. 497-510.
- Steinberg D. On leaving the peritoneal cavity open in acute generalized suppurative peritonitis//Am. j. Surg. 1979. Vol. 137(2). P. 216-220.
- Stevens P. Vacuum-assisted closure of laparostomy wounds: a critical review of the literature//Int. Wound j. 2009. Vol. 6(4). P. 259-266.
- Wittmann D.H. Newer methods of operative therapy for peritonitis: open abdomen, planned relaparotomy or staged abdominal repair (STAr)/In: Tellado j.M., Christou N.V. editors. Intraabdominal infections. Madrid (Spain): Harcourt, 2000. P. 153-192.


