К проблеме связи иммунотерапии у пациентов, страдающих рецидивирующим рассеянным склерозом, с риском тяжелого течения COVID-19
Автор: Якобей Э., Бострум И., Жуковская К., Бернтссон Ш.Г., Ландтблом А.-М.
Журнал: Анализ риска здоровью @journal-fcrisk
Рубрика: Оценка риска в организации здравоохранения
Статья в выпуске: 3 (35), 2021 года.
Бесплатный доступ
Иммуномодулирующие лекарства являются важным элементом контроля заболевания у пациентов с рецидивирующе-ремиттирующим рассеянным склерозом. Анти-CD20-терапия является одним из таких методов лечения. В Швеции было зарегистрировано широкое нерегламентированное применение ритуксимаба (РТКС) у пациентов с рассеянным склерозом; в настоящее время его прописывают более чем половине из них. Основной причиной для этого (в дополнение к финансовым аспектам) явились результаты второй фазы исследования лекарства, а также данные наблюдения, подтверждающие его высокую эффективность и безопасность. Приведены сведения по использованию препаратов, изменяющих течение рассеянного склероза, в Швеции и риску тяжелого течения COVID-19, ассоциированного с применением РТКС в данной группе пациентов. Национальный шведский реестр пациентов с рассеянным склерозом (SMSreg) призван учитывать всех таких больных в стране (примерно 18 тысяч). После того как в Швеции началась пандемия COVID-19, в нем появился новый раздел для регистрации клинических и демографических параметров пациентов с рассеянным склерозом, заразившихся COVID-19. Все данные, приведенные в настоящем исследовании, были получены из реестра SMSreg. 85 человек из примерно 6 тысяч пациентов с рассеянным склерозом в Швеции, которые получали лечение РТКС, были госпитализированы с COVID-19 (согласно данным SMSreg на 16 июня 2021 г.), и скорректированный анализ выявил повышение риска госпитализации в 2-3 раза (OR = 2,89; p = 0,001) для пациентов, получающих анти-CD20-терапию. Практики лечения были изменены в Швеции весной 2020 г., в результате чего большинство больных стали получать вливания РТКС через более длительные промежутки времени. Это было сделано для снижения риска тяжелого течения COVID-19. В настоящее время данные Шведского реестра по рассеянному склерозу указывают, что применение РТКС для лечения пациентов с рассеянным склерозом может повлиять на клиническое течение COVID-19. Эти наблюдения привели к быстрому изменению практики использования иммуномодулирующих препаратов для лечения таких больных в Швеции.
Рассеянный склероз, иммуномодуляционная терапия, инфекция, covid-19, анти-cd20-терапия, ритуксимаб, национальные реестры здоровья, шведский реестр рассеянного склероза
Короткий адрес: https://sciup.org/142231424
IDR: 142231424 | УДК: 616.8-616.9, | DOI: 10.21668/health.risk/2021.3.14
The risk of COVID-19 severity in patients with ms appears to be associated with immunotherapy
Immunomodulatory drugs are important to control disease activity in relapsing-remitting multiple sclerosis (MS). Anti-CD 20-therapy is one of such medications. In Sweden, extensive off label prescription of rituximab (RTX) in MS has been documented; it is presently prescribed for more than half of all treated MS patients. The rationale for the increasing prescription of RTX was previous data from phase II and observational studies supporting high efficacy and safety, in addition to the financial aspect. We report national data on usage of disease modifying therapies in MS patients and risk of severe COVID-19 in association with RTX exposure within this group. The Swedish National MS Registry (SMSreg) aims to cover all patients with MS in the country, (n=approximately 18,000). After COVID-19 pandemic started in Sweden, a new section was established in it to register clinical and demographic parameters in COVID-19-infected patients. Data presented in the current report were obtained from the SMSreg. A total of 85 out of approximately 6,000 RTX-treated Swedish MS patients had been hospitalized with COVID-19 (as reported from the SMSreg, June 16, 2021) and adjusted analyses showed a 2-3 fold increase in a risk (OR = 2.89; p = 0.001) of hospitalization for anti-CD20 treated patients. A change of praxis was introduced in Sweden in spring 2020, resulting in a majority of patients receiving RTX infusions with extended intervals in order to reduce the risk of severe COVID-19 infection. Current Swedish registry data suggest that exposure to RTX in MS may affect the clinical outcome of COVID-19 infection. These observations have rapidly impacted use of immunomodulatory drugs in Swedish MS patients.
Текст научной статьи К проблеме связи иммунотерапии у пациентов, страдающих рецидивирующим рассеянным склерозом, с риском тяжелого течения COVID-19
Жуковская Кристина – аспирант кафедры неврологии (e-mail: ; тел.: +46 18 611 00 00; ORCID: .
Бернтссон Шала Гадери – доктор медицинских наук, доцент, старший консультант отдела неврологии отделения неврологии (e-mail: ; ORCID: .
Ландтблом Анна-Мария – профессор отделения неврологии (e-mail: ; тел.: 460 705 59 16 70; ORCID: .
При этом доступные методики лечения крайне разнообразны и имеют разные цели [4]. Что касается больных с рецидивирующе-ремиттирующим РС (РРРС), то для их лечения применяются препараты как первой, так и второй линии в зависимости от течения болезни и реакции на лечение. Один из препаратов второй линии – ритуксимаб (РТКС), который в первую очередь используется для лечения ревматоидного артрита (РА), стал широко и зачастую нерегламентированно применяться в Швеции для лечения РС [4–8]. Механизм действия ритук-симаба основан на анти-CD20-моноклональных антителах (mABs), которые являются посредниками в разрушении клеток, отвечающих за экспрессию CD20. Это разрушение происходит путем апоптоза, дополнительной активации и опосредованной клеточно-зависимой цитотоксичности антител [7, 9]. В исследовании, проведенном в Швеции, в стране отмечалась тенденция к увеличению числа случаев непрерывного применения РТКС для лечения пациентов с РС в период с 2011 по 2016 г. [5]. В Швеции ритуксимаб назначался 53,3 % всех пациентов с РС, которые начали получать терапию, изменяющую течение болезни, в 2017 г. [5]. Эту тенденцию частично объясняли как эффективностью препарата и его относительной безопасностью, так и невысокими затратами, связанными с его применением, – это отмечалось в случаях лечения как ревматоидного артрита, так и рассеянного склероза [5, 7]. По крайней мере в системе здравоохранения в Швеции различия в затратах просто поразительны. По сравнению с финголимодом и натализумабом, применение которых стоит примерно 200 тысяч шведских крон на одного пациента в год, затраты на ритуксимаб составляют всего 25 тысяч шведских крон [10]. Этот препарат нерег-ламентированно применяется не только в Швеции; подобные случаи отмечены в Норвегии, Дании и, реже, в России [8, 11, 12].
Потенциальное воздействие, которое ритук-симаб может оказывать на гуморальный иммунитет, вызвало определенную тревогу. В нескольких исследованиях было показано, что у некоторых пациентов, получающих лечение данным препаратом, развивалась гипогамма-глобулинемия, а это может вызывать повышенный риск тяжелых инфекций [13]. В 2020 г. в исследовании, проведенном в Швеции Luna et al. [14], анализировали ри-туксимаб и другие высокоэффективные препараты для иммунотерапии, применяемые для лечения РС, и пришли к выводу, что использование ритуксима-ба было связано с самым высоким риском тяжелых инфекций. Инфекции могут вызывать как более тяжелые клинические обострения, так и псевдорецидивы с развитием обратимого или необратимого ухудшения неврологического состояния пациентов с рассеянным склерозом. Помимо данных, связывающих неврологические проявления и COVID-19, можно упомянуть еще и интересный обзор о вме- шательстве иммуномодулирующей терапии в течение данной инфекции, а также о том, могут ли различные методики лечения повлиять на исход COVID-19 в текущей ситуации пандемии [14, 15].
Цель исследования – описать методы терапии, изменяющей течение болезни, применяемые в данное время в Швеции для лечения пациентов с рассеянным склерозом, а также привести данные о возможном течении COVID-19, связанном с использованием методов терапии для лечения пациентов с РС, заразившихся COVID-19.
Материалы и методы. Шведский реестр пациентов с РС (SMSreg) был основан с целью обеспечения высококачественной неврологической помощи и лечения [16]. Он используется неврологическими отделениями в клиниках по всей стране вот уже 20 лет и учитывает примерно 80 % людей в Швеции, страдающих РС, что составляет примерно 18 тысяч пациентов. Реестр SMSreg содержит данные о клинических и демографических переменных, течении болезни и иммуномодулирующих методах терапии, назначенных пациентам с РС. Данный реестр регулярно используется врачами и медсестрами в стационарах и клиниках и часто служит основой для принятия решений о необходимом лечении. После начала пандемии COVID-19 в реестр был встроен модуль, призванный аккумулировать данные о клинических параметрах инфекции COVID-19 у пациентов с РС. Модуль COVID-19 был разработан для получения более широких знаний о влиянии инфекции на пациентов с РС в Швеции [17]. Этот модуль позволяет неврологам регистрировать данные о пациентах с РС с подтвержденным (положительный ПЦР-тест или позитивный тест на антитела) COVID-19 или подозрением на него (согласно критериям ВОЗ). Переменные, которые необходимо зарегистрировать в реестре, включают пол, возраст, дату заболевания COVID-19, клинические симптомы, продолжительность COVID-19, текущую иммунотерапию, последнее известное число лейкоцитов, потребность в госпитализации / интенсивной терапии / ИВЛ и исход болезни (выздоровление / смерть). Все данные, приведенные в настоящем исследовании, доступны на веб-сайте реестра SMSreg и на платформе визуализации и анализа данных (VAP) в реестре SMSreg [16].
Результаты и их обсуждение. 10 962 пациента с РС из 18 тысяч зарегистрированных в реестре SMSreg получали в качестве лечения терапию, изменяющую течение болезни; более половины из них (52 %) принимали ритуксимаб. Другие препараты, назначенные в рамках терапии, включали диметил-фумарат (11 %), натализумаб (12 %), интерферон-бета (7 %), финголимод (7 %), глатирамер ацетат (4 %), терифлуномид (4 %), кладрибин (1 %), алем-тузумаб (1 %) и окрелизумаб (1 %) (сведения доступны на платформе визуализации и анализа данных в SMSreg, июнь 2021 г.) (рис. 1).
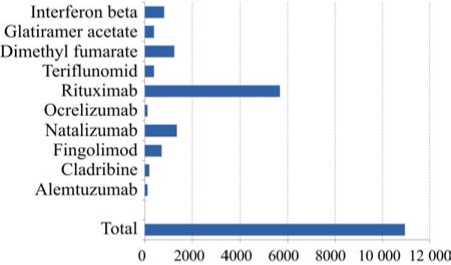
Рис. 1. Непрерывная терапия, изменяющая течение болезни: препараты, принимаемые пациентами с РС в Швеции. Данные получены с помощью платформы для визуализации и анализа (VAP), Шведский реестр пациентов с РС (SMSreg), июнь 2021 г.
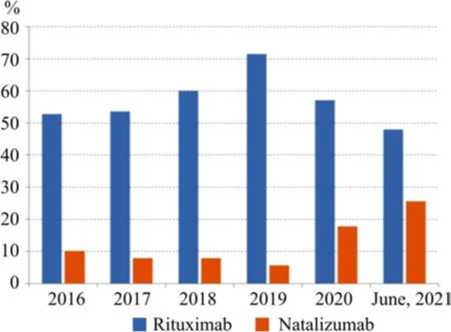
Рис. 2. Количество пациентов с РС, использующих ритуксимаб и натализумаб, по отношению к принимающим прочие препараты, назначаемые в рамках ТИТБ, за период с января 2016 г. по июнь 2021 г. Данные получены с помощью платформы для визуализации и анализа (VAP), Шведский реестр пациентов с РС (SMSreg), июнь 2021 г.
По состоянию на 16 июня 2021 г. из примерно 18 тысяч пациентов с рассеянным склерозом, зарегистрированных в SMSreg, 971 были также отмечены как зараженные COVID-19, 127 из них проходили лечение в стационаре [16], причем 26 – в палатах интенсивной терапии, а пять человек скончались.
85 пациентов с рассеянным склерозом из примерно 6 тысяч, принимавших ритуксимаб, были госпитализированы с COVID-19. Уточненный анализ данных по параметрам возраста, пола, продолжительности заболевания, расширенной шкалы оценки степени инвалидизации (EDSS) и прогрессирования заболевания выявил в 2–3 раза более высокий риск госпитализации ( OR = 2,89; p < 0,001) для пациентов, получающих анти-CD20-терапию (включая РТКС и окрелизумаб) (данные доступны на веб-сайте SMSreg) [16].
Количество пациентов с рассеянным склерозом в Швеции, для лечения которых использовалась терапия, изменяющая течение болезни, варьировалось с течением времени. В связи с пандемией возникла тенденция к уменьшению применения ритуксимаба и к увеличению случаев применения натализумаба (данные доступны на платформе визуализации и анализа данных в SMSreg, июнь 2021 г.) (рис. 2).
Предполагалось, что современная высокоэффективная иммуномодулирующая терапия, например анти-CD20-терапия, может повлиять на течение и последствия COVID-19 у пациентов с рассеянным склерозом. Взаимосвязь в Швеции между анти-CD20-терапией и риском госпитализации для пациентов с данным заболеванием, согласно реестру SMSreg, была подтверждена и результатами международного исследования, в котором использовались регистрационные сведения из нескольких стран [18]. Положительная взаимосвязь между анти-CD20-тера-пией и риском как госпитализации, так и необходимости интенсивной терапии была выявлена на примере большой интернациональной когорты пациентов с рассеянным склерозом, состоящей из более чем двух тысяч зараженных COVID-19 [18]. Сопоставимые результаты, полученные в ходе исследования в Италии с участием 844 пациентов, страдающих рассеянным склерозом, описаны в работе [19]. Еще одно исследование, проведенное в Северной Америке, показало, что пациенты с исследуемым заболеванием, принимающие ритуксимаб, были подвержены более высокому риску заражения COVID-19 и более тяжелому течению заболевания по сравнению с больными, не получающими иммуномодулирующего лечения [19, 20].
Таким образом, отдельное исследование показало, что лица с рассеянным склерозом, принимающие ритуксимаб, подвержены более высокому риску тяжелого течения COVID-19 в среднем в течение 2,5 месяцев после вливания лекарства по сравнению с населением в целом [21]. Высокая доза ритукси-маба (1000 мг) была также взаимосвязана с более тяжелыми последствиями COVID-19 [21]. Более того, обширное глобальное исследование с участием более чем 2800 пациентов с РА, зараженных COVID-19, выявило корреляцию между экспозицией ритуксимаба и более тяжелыми последствиями инфекции, чем в случае применения ингибиторов фактора некроза опухоли альфа. Последнее вполне согласуется с результатами, полученными в международном исследовании с участием нескольких национальных когорт пациентов с рассеянным склерозом [22].
Накопление данных, подтверждающих повышенный риск более тяжелых последствий COVID-19 для пациентов, принимающих ритуксимаб, вызвало необходимость как можно скорее выработать новые клинические решения по выбору препарата терапии и времени его приема для таких больных. В Швеции весной 2020 г. было рекомендовано продлить промежутки времени между вливаниями ритуксимаба с целью сокращения продолжительности истощения В-клеток, что, возможно, могло бы снизить риск тяжелого течения COVID-19. Эта стратегия получила подтверждение данными исследования, проведенного в Швеции, авторы которого отметили от- сутствие рецидива болезни у пациентов с РС после прекращения приема РТКС [23]. Кроме того, сведения, полученные из реестра SMSreg, выявили новые тенденции в Швеции в назначении препаратов для лечения рассеянного склероза, включая уменьшение использования ритуксимаба и увеличение применения натализумаба.
Подводя итоги, можно отметить, что доступные данные реестра SMSreg и объединенные данные, полученные из реестров других стран, указывают на повышенный риск более тяжелого течения и последствий COVID-19 для пациентов, получающих анти-CD20-терапию. Выбирать иммуномодулирующую терапию следует только при условии тщательного изучения прочих общих факторов риска и специфических факторов риска для пациентов с рассеянным склерозом, включая степень инвалидизации, с целью снижения риска тяжелого течения COVID-19.
Финансирование. Исследование не имело финансовой поддержки.
Список литературы К проблеме связи иммунотерапии у пациентов, страдающих рецидивирующим рассеянным склерозом, с риском тяжелого течения COVID-19
- Rising prevalence of multiple sclerosis worldwide: Insights from the Atlas of MS, third edition / C. Walton, R. King, L. Rechtman, W. Kaye, E. Leray, R.A. Marrie, N. Robertson, N. La Rocca [et al.] // Mult. Scler. – 2020. – Vol. 26, № 14. –P. 1816–1821. DOI: 10.1177/1352458520970841
- Boyko A., Melnikov M. Prevalence and Incidence of Multiple Sclerosis in Russian Federation: 30 Years of Studies // Brain. Sci. – 2020. – Vol. 10, № 5. – P. 305. DOI: 10.3390/brainsci10050305
- Tullman M.J. Overview of the epidemiology, diagnosis, and disease progression associated with multiple sclerosis // Am. J. Manag. Care. – 2013. – Vol. 19, suppl. 2. – P. S15–20.
- Hauser S.L., Cree B.A.C. Treatment of Multiple Sclerosis: A Review // Am. J. Med. – 2020. – Vol. 133, № 12. – P. 1380–1390.e2. DOI: 10.1016/j.amjmed.2020.05.049
- Rapidly increasing off-label use of rituximab in multiple sclerosis in Sweden – Outlier or predecessor? / S.G. Berntsson, A. Kristoffersson, I. Boström, A. Feresiadou, J. Burman, A.M. Landtblom // Acta. Neurol. Scand. – 2018. – Vol. 138, № 4. – P. 327–331. DOI: 10.1111/ane.12963
- Garg N., Smith T.W. An update on immunopathogenesis, diagnosis, and treatment of multiple sclerosis // Brain. Behav. – 2015. –Vol. 5, № 9. – P. e00362. DOI: 10.1002/brb3.362
- Clinical Pharmacokinetics and Pharmacodynamics of Monoclonal Antibodies Approved to Treat Rheumatoid Arthritis / D. Ternant, T. Bejan-Angoulvant, C. Passot, D. Mulleman, G. Paintaud // Clinical. Pharmacokinetics. – 2015. – Vol. 54, № 11. – P. 1107–1123. DOI: 10.1007/s40262-015-0296-9
- Safety and efficacy of rituximab as first- and second line treatment in multiple sclerosis – A cohort study / H.M. Torgauten, K.-M. Myhr, S. Wergeland, L. Bø, J.H. Aarseth, Ø. Torkildsen // Multiple Sclerosis Journal – Experimental, Translational and Clinical. – 2021. – Vol. 7, № 1. – P. 2055217320973049. DOI: 10.1177/2055217320973049
- Rituximab for the treatment of multiple sclerosis: a review / C.G. Chisari, E. Sgarlata, S. Arena, S. Toscano, M. Luca, F.Patti // J. Neurol. – 2021. – Jan. 8. – P. 1–25. DOI: 10.1007/s00415-020-10362-z
- Hedlund F. Multiple sclerosis a newly interpreted disease [Электронный ресурс] // Medicinsk Vetenskap. – 2016. – № 4. – URL: https://ki.se/forskning/multipel-skleros-en-nytolkad-sjukdom (дата обращения: 16.04.2021).
- Заявление о разработке проекта клинических рекомендаций «Рассеянный склероз у взрослых и детей, (код по МКБ-10: G35)» [Электронный ресурс]. – 2020. – URL: https://centrems.com/downloads/Clinical_recommendations_of_the_RS-Project_submitted_to_the_MHRF.pdf (дата обращения: 13.04.2021).
- Anti-CD20 antibody therapy and risk of infection in patients with demyelinating diseases / N.R. Oksbjerg, S.D. Nielsen, M. Blinkenberg, M. Magyari, F. Sellebjerg // Mult. Scler. Relat. Disord. – 2021. – Vol. 52. – P. 102988. DOI: 10.1016/j.msard.2021.102988
- Association of Immunoglobulin Levels, Infectious Risk, and Mortality With Rituximab and Hypogammaglobulinemia / S. Barmettler, M.S. Ong, J.R. Farmer, H. Choi, J. Walter // JAMA Netw Open. – 2018. – Vol. 1, № 7. – P. e184169. DOI: 10.1001/jamanetworkopen.2018.4169
- Infection Risks Among Patients With Multiple Sclerosis Treated With Fingolimod, Natalizumab, Rituximab, and Injectable Therapies / G. Luna, P. Alping, J. Burman, K. Fink, A. Fogdell-Hahn, M. Gunnarsson, J. Hillert, A. Langer-Gould [et al.] // JAMA Neurol. – 2020. – Vol. 77, № 2. – P. 184–191. DOI: 10.1001/jamaneurol.2019.3365
- Garg R.K. Spectrum of Neurological Manifestations in Covid-19: A Review // Neurol. India. – 2020. – Vol. 68, № 3. – P. 560–572. DOI: 10.4103/0028-3886.289000
- Multipel skleros [Электронный ресурс] // Svenska neuroregister. – URL: https://www.neuroreg.se/multipel-skleros/ (дата обращения: 17.04.2021).
- Iacobaeus E., Burman J., Landtblom A.M. Multiple Sclerosis and COVID-19 – Still limited knowledge // Lakartidningen. – 2020. – Vol. 117.
- Associations of DMT therapies with COVID-19 severity in multiple sclerosis [Электронный ресурс] / S. Simpson-Yap, W. De Brouwer, T. Kalincik, N. Rijke, J. Hillert, C. Walton, G. Edan, Y. Moreau [et al.] // medRxiv. – 2021. – URL: https://www.medrxiv.org/content/10.1101/2021.02.08.21251316v1 (дата обращения: 21.04.2021).
- Disease modifying therapies and Coronavirus Disease 2019 severity in Multiple Sclerosis / M.P. Sormani, N. De Rossi, I. Schiavetti, L. Carmisciano, C. Cordioli, L. Moiola, M. Radaelli, P. Immovilli [et al.] // Ann. Neurol. – 2021. – Vol. 89, № 4. – P. 780–789. DOI: 10.1002/ana.26028
- COVID-19 in Patients with Multiple Sclerosis: Associations with Disease-Modifying Therapies / A.T. Reder, D. Centonze, M.L. Naylor, A. Nagpal, R. Rajbhandari, A. Altincatal, M. Kim, A. Berdofe [et al.] // CNS Drugs. – 2021. – Vol. 35, № 3. – P. 317–330. DOI: 10.1007/s40263-021-00804-1
- Multiple sclerosis, rituximab, and COVID-19 / A. Langer-Gould, J.B. Smith, B.H. Li, K.M.S. Group // Ann. Clin. Transl. Neurol. – 2021. – Vol. 8, № 4. – P. 938–943. DOI: 10.1002/acn3.51342
- Associations of baseline use of biologic or targeted synthetic DMARDs with COVID-19 severity in rheumatoid arthritis: Results from the COVID-19 Global Rheumatology Alliance physician registry / J.A. Sparks, Z.S. Wallace, A.M. Seet, M.A. Gianfrancesco, Z. Izadi, K.L. Hyrich, A. Strangfeld, L. Gossec [et al.] // Ann. Rheum. Dis. – 2021. – Vol. 80, № 9. – P. 1137–1146. DOI: 10.1136/annrheumdis-2021-220418
- Interrupting rituximab treatment in relapsing-remitting multiple sclerosis; no evidence of rebound disease activity / A. Juto, K. Fink, F. Al Nimer, F. Piehl // Mult. Scler. Relat. Disord. – 2020. – Vol. 37. – P. 101468. DOI: 10.1016/j.msard.2019.101468


