К вопросу о применении бипортальной баллонной кифопластики при агрессивных гемангиомах позвоночника
Автор: Мизюров С.А., Островский В.В., Зарецков В.В., Арсениевич В.Б., Лихачев С.В., Степухович С.В., Папаев А.В.
Журнал: Кафедра травматологии и ортопедии @jkto
Рубрика: Оригинальное исследование
Статья в выпуске: 1 (47), 2022 года.
Бесплатный доступ
Цель исследования. Изучить целесообразность применения бипортальной баллонной кифопластики при хирургическом лечении агрессивных гемангиом позвоночника.Материал и методы. 20 пациентам с агрессивными гемангиомами грудного и поясничного отделов позвоночника выполнена кифопластика с использованием бипортального транскутанного транспедикулярного доступа под контролем электронно-оптического преобразователя. Проведены МРТ- и КТ-исследования.Результаты. В предоперационном периоде интенсивность болевого синдрома по визуально-аналоговой шкале (ВАШ) составляла 8,3 ± 1,7 баллов, после оперативного вмешательства - 1,6 ± 1,4 балла. Средний общий балл по опроснику Освестри (ODI) до хирургического вмешательства составлял 18,0±4,0 баллов, после операции - 5,8±2,2 балла. Через 1 месяц после оперативного лечения показатели ВАШ и ОDI соответствовали 0 баллам. Осложнений в послеоперационном периоде не отмечалось. КТ-исследование проводили всем пациентам в 1-е сутки после хирургического вмешательства. По КТ-данным в 100% случаев удалось добиться полного заполнения костного дефекта полиметилметакрилатом, миграции костного композита за пределы тела позвонка не было. Повторное КТ-исследование через 6 и 12 месяцев после операции не выявило признаков рецидива опухоли. Заключение. Применение бипортальной баллонной кифопластики не только снижает риск экстравертебрального выхода костного композита,но и препятствует развитию рецидива опухоли. Однако, в настоящее время не существует общепринятых критериев и показаний, объединенных в алгоритм для применения одно- и бипортальной баллонной кифопластики в лечении агрессивных гемангиом позвоночника, в связи с чем многие вопросы по ее использованию дискутабельны и нуждаются в дальнейшем изучении.
Позвоночник, агрессивная гемангиома, бипортальная баллонная кифопластика
Короткий адрес: https://sciup.org/142235276
IDR: 142235276 | УДК: 616.71-006 | DOI: 10.17238/2226-2016-2022-1-31-37
To a question of the using biportal balloon kyphoplasty in aggressive spinal hemangiomas
Research objective. To study the feasibility of using biportal balloon kyphoplasty in the surgical treatment of aggressive spinal hemangiomas.Material and methods. Kyphoplasty using biportal transcutaneous transpedicular access under the control of an electron-optical converter was performed for 20 patients with aggressive hemangiomas of the thoracic and lumbar spine. MRI and CT researches were conducted.Results. In the preoperative period, the intensity of the pain syndrome according to the visual-analog scale (VAS) was 8.3 ± 1.7 points, after surgery - 1.6± 1.4 points. The average overall score on the Oswestry questionnaire (ODI) before surgery was 18.0 ±4.0 points, after surgery - 5.8± 2.2 points. In one month after the surgical treatment, the indicators of VAS and ODI were 0 points. There were no complications in the postoperative period. CT research was performed for all patients on the 1st day after surgery. According to CT data, in 100% of cases, it was possible to achieve complete filling of the bone defect with polymethylmethacrylate, there was no outflow bone composite outside the vertebral body. Repeated CT research in 6 and 12 months after surgery revealed no signs of tumor recurrence.Conclusion. The use of biportal balloon kyphoplasty not only reduces the risk of extravertebral outflow bone composite, but also prevents the development of tumor recurrence. However, currently there are no generally accepted criteria and indications combined into an algorithm for the use of single- and biportal balloon kyphoplasty in the treatment of aggressive spinal hemangiomas, and therefore many questions about its using are debatable and need further study.
Текст научной статьи К вопросу о применении бипортальной баллонной кифопластики при агрессивных гемангиомах позвоночника
Введение. Гемангиома позвоночника (ГП) выявляется у 10% взрослого населения, чаще у лиц трудоспособного возраста (30-60 лет) [1]. Гистологически гемангиомы подразделяются на три типа: капиллярная, по частоте встречаемости составляет 15,8%, кавернозная - 29,2% и смешанная, наиболее часто встречающийся тип гемангиом, - 55% [2,3]. Единичные ГП обнаруживаются у 55% больных, поражение тел 2-3 позвонков встречается у 25% обследуемых, у 15% – до 5 позвонков, а у 5% выявляется поражение более 5 позвонков, причем частота их выявления увеличивается с возрастом [4].
Основным, а порой и единственным симптомом заболевания, является локальный болевой синдром [2,5]. Наиболее эффективным методом диагностики ГП считается компьютерная томография (КТ), точность и чувствительность которого достигают 100% [1,6]. Вторым по точности (94,7%) является метод магнитно-резонансной томографии (МРТ), его чувствительность составляет 96,7% [2,6]. ГП в 0,9% - 4% случаев проявляют себя как агрессивные и сопровождаются выраженной клинической симптоматикой [7]. «Агрессивность» ГП служит одним из основных показаний к хирургическому лечению [2]. С целью повышения объективности оценки агрессивности гемангиом позвонков М. Н. Кравцовым и соавт., (2012) была разработана «Балльная шкала оценки агрессивности гемангиом позвонков», включающая 9 радиологических и клинических критериев [7].
На основании применяемой шкалы агрессивной следует считать гемангиому при сумме весовых значений признаков, равной 5 баллам и более [2,7]. По мере роста гемангиомы обычно происходит и процесс постепенной перестройки костной ткани пораженного позвонка, что приводит к снижению его опоро-способности и повышает риск патологического перелома [8].
В настоящее время при лечении агрессивных ГП широко применяется пункционная вертебропластика (ПВ) [9]. Осложнения ПВ возникают в 0,5 - 76% случаев [10], из них клинически значимые – у 2,5% пациентов [11]. Наиболее частые (40-87,5% случаев) осложнения связаны с миграцией полиметилметакрилата за пределы позвонка [12].
По информации, в основном из зарубежных источников, баллонная кифопластика (БК) может стать методикой, позволяющей при лечении агрессивных ГП снизить риск экстравер-тебральной миграции костного композита [13]. В частности, БК снижает риск экстравертебрального истечения костного композита за счет уплотнения костной ткани по периферии от расправленного баллона, что при введении цемента высокой вязкости снижает риск его проникновения в позвоночный канал [14]. Несмотря на имеющиеся сообщения об использовании методики БК при лечении агрессивных ГП [13,15-20], нам не удалось обнаружить критериев и показаний, объединенных в алгоритм применения бипортальной баллонной кифопластики, в связи с чем многие вопросы по ее использованию дискута-бельны и нуждаются в дальнейшем изучении.
Цель исследования – изучить целесообразность применения бипортальной баллонной кифопластики при хирургическом лечении агрессивных гемангиом позвоночника.
Материалы и методы. Баллонная кифопластика из бипор-тального транскутанного транспедикулярного доступа выполнена у 20 пациентов с агрессивными ГП. Лиц мужского пола было 6, женского – 14. Большинство больных (12 пациентов) были трудоспособного (30-55 лет) возраста, у которых имеющееся поражение приводило к ограничению работоспособности. У всех пациентов было выявлено одноуровневое поражение: Th10 позвонок – 1 случай, Th11 – 2, Th12 – 6, L1 – 5, L2 – 2, L3 – 1, L4 - 2 и L5 – 1 случай.
При КТ-исследовании диагностированы следующие особенности поражения: у 7 больных было выявлено тотальное поражение тела позвонка, у 1 – тотальное поражение сопровождалось патологическим переломом тела позвонка, у 7 пациентов - 65% поражения с деструкцией кортикального слоя, у оставшихся 5 пациентов было диагностировано 50% поражение гемангиомой с истончением задней кортикальной пластинки тела позвонка. Диагноз «агрессивная ГП» формулировался с учетом «Балльной шкалы оценки агрессивности ГП» [2,7]. Степень выраженности болевого синдрома определяли по ВАШ, а показатель ограничения жизнедеятельности из-за боли - по опроснику Освестри (ODI).
Баллонную кифопластику выполняли в положении больного на животе из бипортального транскутанного транспедикулярного доступа. При помощи электронно-оптического преобразователя (ЭОП), при корректной прямой проекции, определяли траекторию транспедикулярного доступа путем визуализации корня дуги пораженного гемангиомой позвонка. Под контролем ЭОП визуализировали прохождение иглы заднего кортикального слоя позвонка. Далее через иглу, после удаления стилета, устанавливали спицу-проводник и продвигали ее до передней четверти тела позвонка. После установки проводника иглу доступа удаляли и по проводнику проводили рабочую канюлю таким образом, чтобы ее передняя часть лишь пересекала кортикальный слой позвонка в боковой проекции. Далее извлекали спицу-проводник и по рабочей канюле формировали костный канал для введения баллона. В подготовленный костный канал в «сжатом» состоянии устанавливали баллон. Затем проводили заполнение шприца расширителя баллона рентгено‐контрастной жидкостью. Подготовленный шприц расширитель присоединяли к баллону и вращательными движениями рукоятки шприца повышали давление в установленном баллоне. При помощи ЭОП пошагово осуществляли контроль увеличения объема баллона в двух проекциях, не допуская контакт баллона с кортикальной стенкой позвонка. После сформирования полости баллон «сдували» и удаляли. Далее приступали к подготовке костного композита с последующим заполнением им пломбировочных устройств
(филлеров). При достижении цементом рабочей фазы филлер устанавливали в рабочую канюлю и проводили пошаговое заполнение костной полости тела позвонка под контролем ЭОП. По окончании аугментации позвонка рабочую канюлю удаляли. При кифопластике использовали костный цемент повышенной вязкости.
Результаты. В предоперационном периоде интенсивность болевого синдрома по визуально-аналоговой шкале (ВАШ) составляла 8,3 ± 1,7 баллов, после оперативного вмешательства – 1,6 ± 1,4 балла. Средний общий балл по опроснику Освестри (ODI) до хирургического вмешательства составлял 18,0±4,0 баллов, после операции - 5,8±2,2 балла. Через 1 месяц после оперативного лечения показатели ВАШ и ОDI соответствовали 0 баллам. Осложнений в послеоперационном периоде не отмечалось. КТ-исследование проводили всем пациентам в 1-е сутки после хирургического вмешательства. По КТ-данным в 100% случаев удалось добиться тотального заполнения костного дефекта полиметилметакрилатом, миграции костного композита за пределы тела позвонка у всех прооперированных больных не выявлено. Период пребывания пациентов в стационаре составлял от 3 до 5 дней. Повторное КТ-исследование через 6 и 12 месяцев с момента операции признаков рецидива опухоли не обнаружило.
Клинический пример №1. Пациентка С., 52 лет, в октябре 2020 года обратилась в поликлинику института с жалобами на боль в нижне-грудном отделе позвоночника, которая носила стойкий и интенсивный характер, усиливалась при физической нагрузке и в положении стоя. Из анамнеза: пациентка страдала от боли на протяжении последних 2-х лет, при этом последний год отмечала значительное усиление болевого синдрома, что привело к постоянному приему обезболивающих препаратов. При пальпации остистого отростка Th12 позвонка - резкое усиление боли. Степень выраженности болевого синдрома составило 10 баллов по ВАШ, индекс ОDI – 17 баллов. При МРТ-исследовании грудного отдела позвоночника была обнаружена гемангиома тела Th12 позвонка. Дополнительно выполнена КТ, которая выявила тотальное поражение тела Th12 позвонка с деструкцией задней кортикальной пластинки (рис. 1).
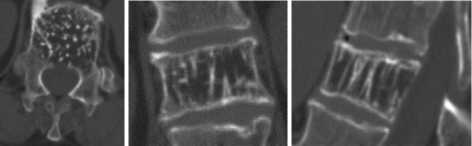
Рис. 1 КТ- сканы Th12 позвонка больной С. до операции
В связи с высоким риском экстравертебральной миграции полиметилметакрилата и обширностью поражения пациентке была выполнена БК Th12 позвонка из бипортального транспедикулярного доступа. В тело позвонка введено 12 мл костного цемента. В 1-е сутки после операции отмечен регресс болевого синдрома до 2 баллов по ВАШ, показатель ОDI составлял – 6 баллов. На послеоперационных КТ-снимках определялось тотальное заполнение костного дефекта позвонка, экстраверте-бральной миграции композита не выявлено (рис. 2). Пациентка выписана на 3-е сутки после вмешательства. Последующий КТ-контроль через 6 и 12 месяцев показал отсутствие рецидива опухоли.
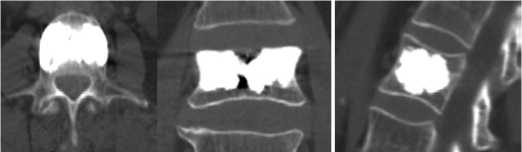
Рис. 4 КТ- сканы L2 позвонка больного М. после операции
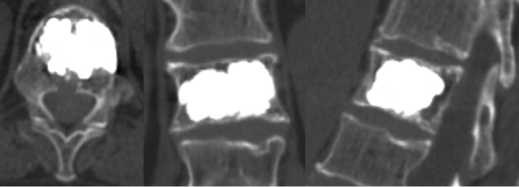
Рис. 2 КТ- сканы Th12 позвонка больной С. после операции
Клинический пример №2. Пациент М., 60 лет, обратился с жалобами на постоянную ноющую боль в поясничном отделе позвоночника. При пальпации остистого отростка L2 позвонка отмечено резкое усиление боли. Степень выраженности болевого синдрома составила 9 баллов по ВАШ, индекс ОDI – 19 баллов. При МРТ-исследовании поясничного отдела позвоночника была обнаружена гемангиома тела L2 позвонка. Дополнительно была выполнена
КТ, которая выявила 50% поражения тела L2 позвонка слева с признаками гемангиоматозного поражения (около 15%) справа, а также истончение задней кортикальной пластинки (рис. 3).
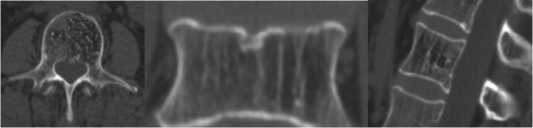
Рис. 3 КТ- сканы L2 позвонка больного М. до операции
В связи с высоким риском экстравертебральной миграции полиметилметакрилата в сторону позвоночного канала за счет истончения задней кортикальной пластинки позвонка и риска рецидива опухоли справа пациенту была выполнена БК L2 позвонка из бипортального транспедикулярного доступа. В тело позвонка введено 10 мл костного цемента. На 1-е сутки после операции отмечен регресс болевого синдрома до 2 баллов по ВАШ, показатель ОDI составлял – 7 баллов. На послеоперационных КТ-снимках определялось тотальное заполнение костного дефекта позвонка, экстравертебраль-ной миграции композита не выявлено (рис. 4). Пациент выписан на 5-е сутки после вмешательства. Последующий КТ-контроль через 6 и 12 месяцев подтвердил отсутствие рецидива опухоли.
Обсуждение. Осложнения, связанные с миграцией полиметилметакрилата за пределы тела позвонка при выполнении ПВ, встречаются в 40 - 87,5% случаев [12]. Lotfinia I. et al., (2010) провели анализ результатов ПВ, который выявил миграцию костного композита в межпозвонковые диски в 23,3% случаев, в 20% случаев эпидуральную и фораминальную миграцию полимера, экстравертебральное распространение по сегментарным сосудам в 6,7% случаев [21]. Описывая результаты хирургического лечения агрессивных ГП с использованием ПВ, Климов В. С. и соавт., (2018) также указывают на осложнения, обусловленные миграцией костного цемента за пределы тела позвонка [22]. Для снижения риска миграции костного полимера при выполнении ПВ используются различные методы аугментации пораженного позвонка. В частности, этапное его введение с использованием полиметилметакрилата вязкой консистенции, позиционирование пункционной иглы с максимальной конвергенцией к передним отделам тела позвонка, а также введение костного цемента под минимальным давлением [23,24]. Однако, несмотря на все эти применяемые методики, риск экстравертебрального выхода костного композита остается высоким и составляет от 2 до 11% случаев [12].
Впервые результаты применения БК при лечении агрессивных ГП, имеющих высокий риск экстравертебральной миграции полиметилметакрилата, были представлены Noez S. et al., (2006) [25] и Atalay B. et al., (2006) [26]. Основное отличие БК от ПВ заключается в предварительном введении по пункционной игле в тело пораженного позвонка специального «раздувающегося» баллона, способствующего уплотнению костной ткани по периферии от него [13]. Zapalowicz K. et al., (2008), сообщая о положительном результате применения БК в лечении агрессивной гемангиомы С7 позвонка, подтверждают, что введение под низким давлением полиметилметакрилата высокой вязкости в полость, образованную принудительно расправленным баллоном, уменьшает риск экстравертебраль-ной миграции полимера за счет того, что композит идет по пути наименьшего сопротивления в сформированную «альтернативную» полость [15]. В дальнейшем докладывая о двух случаях успешного лечения агрессивных ГП с использованием БК Jones J. O. et al., (2009) подтвердили мнение, высказанное Zapalowicz K. et al., (2008), что предлагаемая методика снижает риск миграции костного цемента по сравнению с ПВ за счет формирования «альтернативной» внутренней полости в теле пораженного позвонка [27]. Авторский коллектив Jones J. O.
еt al., (2009) высказались о целесообразности применения БК в лечении агрессивных ГП осложнившихся патологическим переломом тела пораженного позвонка с целью восстановления его высоты и опороспособности [27]. Giorge P. et al., (2020) была предложена оригинальная методика проведения БК с одновременным выполнением предоперационной эмболизации патологического сосудистого русла опухоли [17]. По мнению авторов, следует учитывать, что объем вводимого полиметилметакрилата не должен превышать объемов полностью расправленных баллонов [17].
Таким образом, анализируя представленные в зарубежной литературе случаи использования БК при агрессивных ГП и собственные результаты можно прийти к выводу, что основными и первоочередными критериями выбора для применения методики БК служат гемангиомы позвонков с тотальным поражением или с наличием дефекта кортикальной пластинки тела пораженного позвонка. С свою очередь при анализе литературных источников не удалось выявить показаний для выполнения одно- или бипортальной БК, в связи в чем данный вопрос нуждается в обсуждении. Данная проблема поднимается в сообщении Hadjipavlou A. et al., (2007), которые проспективно изучили данные 6 пациентов, прооперированных с использованием методики БК [13]. Наблюдение за одним из пациентов, которому была выполнена правосторонняя БК, показало, что через полгода боли возобновились и они были связаны с ростом гемангиомы в левой половине тела прооперированного позвонка. В связи с этим больному была выполнена повторная БК из транспедикулярного левостороннего доступа. Авторы сделали вывод о целесообразности полной аугментации гемангиомы полиметилметакрилатом с помощью двухпортальной БК [13]. Однако, авторами в сообщении не была проанализирована причина рецидива опухоли после выполнения однопортальной БК. По нашему мнению, причиной рецидива опухоли могла послужить непосредственно методика выполнения БК, так как для снижения риска рецидива опухоли при выполнении БК нужно придерживаться основного принципа – полноты заполнения пораженного позвонка при аугментации костного дефекта. Тем самым бипортальная БК должна применяться при невозможности полной аугментации пораженного позвонка из однопортального доступа. Применение однопортального доступа по всей видимости более целесообразно при выполнении БК на шейных и верхне-грудных позвонках.
В связи с вышесказанным использованная в нашем исследовании бипортальная БК была выполнена при выявленных у пациентов особенностях по КТ-данным (тотальное поражение тел позвонков с дефектами кортикального слоя, патологический переломом тела позвонка, 50% поражение с одной стороны и до 15% поражения тела позвонка с другой стороны, одностороннее поражение с истончением задней кортикальной пластинки тела позвонка), что способствовало регрессу не только болевого синдрома и восстановлению опороспособности пораженного позвонка, но и отсутствию эпизодов эпидурального выхода костного цемента и рецидивов опухоли. Отдельно следует отметить, что, несмотря на эффективность БК при лечении ГП, данная методика может иметь ограничение при выполнении операции, зависящее от особенностей анатомии позвонков. В частности, «тонкие» ножки пораженного позвонка затрудняют выполнение данной манипуляции, осложнением которой может стать травматизация (перелом) ножки позвонка. В таких случаях, предпочтение следует отдавать ПВ с использованием цемента более высокой вязкости и с достаточным «рабочим» временем для снижения риска экстравертебральной миграции.
Также следует отметить возможность применения би-портальной БК в комплексе с другими методиками лечения агрессивных ГП. Moore J. M. еt al., (2012) представили 2 случая успешного использования БК в сочетании с транспедикулярной фиксацией при лечении осложненных агрессивных ГП [16]. Авторы сообщают, что сочетание БК с транспедикулярной фиксацией снижает риск развития постламинэктомического кифоза и рекомендуют использовать БК в случаях, когда задние элементы позвонка дестабилизированы после декомпрессивной ламинэктомии [16]. Подтверждением вышесказанного может служить наблюдение Armaganian G. et al., (2013), представивших результат лечения патологического перелома тела L1 позвонка на фоне поражения гемангиомой [28]. Syrimpeis V. et al., (2014), считают, что сочетание задней декомпрессии, аугментации позвонка методом БК с последующей задней фиксацией у пациентов с неврологическим дефицитом сводит к минимуму дальнейшее развитие симптоматики и позволяет проводить раннюю реабилитацию [29]. Применение комбинированного хирургического лечения осложненных агрессивных ГП также нашло отражение и в работе Yu B. et al., (2014) [30].
Заключение. Применение бипортальной БК может являться методом выбора при хирургическом лечении агрессивных гемангиом с высоким риском миграции костного цемента. Кроме того, бипортальная БК эффективно применяется в комплексе с другими методиками лечения агрессивных ГП [16,28-30]. Также можно констатировать, что в настоящее время не существует показаний, объединенных в алгоритм применения одно- и би-портальной баллонной кифопластики в лечении агрессивных ГП, в связи с чем многие вопросы по ее применению остаются дискутабельны и нуждаются в дальнейшем изучении.
Список литературы К вопросу о применении бипортальной баллонной кифопластики при агрессивных гемангиомах позвоночника
- Кавалерский Г. М, Ченский А. Д., Макиров С. К. и др. Гемангиомы позвоночника: диагностика, лечение // Врач. 2007. №. 8. С. 19-22. [Kavalerskii G. M., Chenskii A. D., Makirov S. K. et. al. Hemangiomas of the spine: diagnosis, treatment // Doctor. 2007. 8: 19-22 (in Russ.).]
- Кравцов М. Н., Мануковский В. А., Манащук В. И. и др. Диагностика и лечение агрессивных гемангиом позвонков // Клинические рекомендации. Москва. 2015. С. 35. [Kravtsov M. N., Manukovsky V. A., Manashchuk V. I. et al. Diagnosis and treatment of aggressive vertebral hemangiomas//Clinical guidelines. Moscow. 2015: 35. (in Russ.).]
- Слынько Е. И. Хирургическое лечение сосудистых опухолей позвоночника и спинного мозга // Український нейрохірургічний журнал. 2000. №1(9). С. 55-64. [Slynko E. I. Surgical treatment of vascular tumors of the spine and spinal cord //Ukrainian neurosurgical journal. 2000. 1(9): 55-64 (in Russ.).]
- Козубаев У. У., Качиев Н. Т., Шамшиев А. Т. Эпидемиология первичных опухолей спинного мозга (обзор литературы) //Наука, новые технологии и инновации Кыргызстана. 2020. №. 3. С. 54-59. [Kozubaev U. U., Kachiev N. T., Shamshiev A. T. Epidemiology of the primary spinal cord tumors (review of literature). Science, new technologies and innovations of Kyrgyzstan. 2020. 3: 54-59 (in Russ.).]
- Грушина Т. И., Титов А. А. Современные представления о гемангиоме позвонка // Вестник травматологии и ортопедии им. Н. Н. Приорова. 2020. №1. С. 77-83. [Grushina T. I., Titov A. A. Current view on vertebral hemangioma. N. N. Priorov Journal of Traumatology and Orthopedics. 2020; 27(1): 77–83 (In Russ.).] DOI: 10.17816/vto202027177-83
- Гарматина О. Ю. Лучевая диагностика гемангиомы позвонка. Український радіологічний журнал. 2014. 22 (3). С. 60-63. [Garmatyna O. Yu. Radiological imaging of vertebral hemangioma. Ukrainian radiological journal. 2014. 22 (3): 60-63 (in Russ.).]
- Кравцов М. Н., Мануковский В. А., Жаринов Г. М. и др. Агрессивные гемангиомы позвонков: оптимизация тактики лечения //Вопросы нейрохирургии им. Н. Н. Бурденко. 2012. 76(2). С. 23-32. [Kravtsov M. N., Manukovskii V. A., Zharinov G. M. et al. Aggressive vertebral hemangiomas: optimization of management tactics. Burdenkos Journal of Neurosurgery. 2012; 76 (2): 23-32 (in Russ.).]
- Gajaseni P. et al. A child with a rare extraosseous extension and pathologic fracture from a vertebral hemangioma: a case report //JBJS case connector. 2017. 7(4): e86. DOI: 10.2106/JBJS.CC.17.00057
- Курамшин А. Ф., Сафин Ш. М., Нагаев Р. Я. и др. Особенности проведения вертебропластики при гемангиомах шейного отдела позвоночника. Хирургия позвоночника. 2015. Т. 12. №4. С. 80–83. [Kuramshin A. F., Safin Sh. M., Nagaev R. Y. et al. Vertebroplasty for cervical spine hemangioma //Spine surgery. 2015. 12 (4): 80-83. (In Russ.).]
- Kaso G., Horvath Z., Szenohradszky K. Comparison of CT characteristics of extravertebral cement leakages after vertebroplasty performed by different navigation and injection techniques // Acta Neurochir. 2008. 150: 677- 683.
- Jensen M. E., McGraw J. K., Cardella J. F. Position Statement on Percutaneous Vertebral Augmentation: A Consensus Statement Developed by the American Society of Interventional and Therapeutic Neuroradiology, Society of Interventional Radiology, American Associationof Neurological Surgeons. In: Congress of Neurological Surgeons, and American Society of Spine Radiology // Am. J. Neuroradiol. 2007. 28: 1439 –1443.
- Chotivichit A., Korwutthikulrangsri E., Churojana A., Songsaeng D. Complications in vertebroplasty. J. Med. Assoc. Chotmaihet thangphaet. 2012. 95: 75-81.
- Hadjipavlou A., Tosounidis T., Gaitanis I. et al. Balloon kyphoplasty as a single or as an adjunct procedure for the management of symptomatic vertebral haemangiomas. J Bone Joint Surg Br. 2007. 89(4):495-502. DOI: 10.1302/0301-620X.89B4.18121
- Cui Zhiyong M. D. et al. Unilateral versus bilateral balloon kyphoplasty for osteoporotic vertebral compression fractures: a systematic review of overlapping meta-analyses //Pain physician. 2019. 22: 15-28.
- Zapalowicz K., Skora P., Myslinski R. et al. Balloon kyphoplasty for painful C-7 vertebral hemangioma. J Neurosurg Spine. 2008. 8(5): 458-461. DOI: 10.3171/SPI/2008/8/5/458
- Moore J. M., Poonnoose S., McDonald M. Kyphoplasty as a useful technique for complicated hemangiomas. J. Clin. Neurosci. 2012. 19 (9): 1291–1293. DOI: 10.1016/j.jocn.2011.12.012
- Giorgi P., Compagnone D., Gallazzi E., Schirò G.R. Early percutaneous treatment of an aggressive vertebral hemangioma: A case report with a 5-year follow-up. // J. Craniovertebr. Junction. Spine. 2020. 11(2): 139-142. DOI: 10.4103/jcvjs.JCVJS_31_20
- Лихачев С. В., Зарецков В. В., Арсениевич В. Б и др. Агрессивные гемангиомы тел позвонков: Особенности регионарного кровотока. Диагностика и хирургическое лечение. Кремлевская медицина: Клинический вестник. 2015. 4: 107–115. [Likhachev S. V., Zaretzkov V. V., Arsenievich V. B. et al. Aggressive hemagiomas of the vertebral bodies. Peculiarities of the regional blood flow. Diagnostics and surgical treatment//The Kremlin medicine. Clinical Herald. 2015. 4: 107-115 (in Russ.).]
- Зарецков В. В., Лихачев С. В., Арсениевич В. Б. и др. Гемангиомы позвоночника. Особенности диагностики и хирургического лечения. Успехи современного естествознания. 2015. 6: 22-27. [Zaretskov V. V., Likhachev S. V., Arsenievich V. B. et al. Vertebral hemangiomas: Diagnostics and surgical treatment //Advances in current natural sciences. 2015. 6: 22–27. (in Russ.).]
- Зарецков В. В., Арсениевич В. Б., Лихачев С. В. и др. К вопросу об использовании баллонной кифопластики в хирургическом лечении агрессивных гемангиом позвоночника (клинические наблюдения) // Гений ортопедии. 2020. Т. 26. № 2. С. 234-237. [Zaretskov V. V., Arsenievich V. B., Likhachev S. V. et al. To the question of using balloon kyphoplasty in surgical treatment of aggressive vertebral hemangioma (case report). 2020. 26(2): 234-237. (in Russ.).] DOI 10.18019/1028-4427-2020-26-2-234-237
- Lotfinia I., Sayyahmelli S. Complications of Percutaneous Vertebroplasty: A Clinical Study and Literature Review // Neurosurg. Quarter. 2010. 20(2): 241-246.
- Климов В. С., Косимшоев М. А., Евсюков А. В. и др. Результаты дифференцированного хирургического лечения агрессивныхгемангиом позвонков //Хирургия позвоночника. 2018. Т. 15. №. 1. С. 79-90. [Klimov V. S., Kosimshoev M. A., Evsyukov A. V. et al. Results of differentiated surgical treatment of aggressive vertebral hemangiomas //Spine surgery. 2018. 15 (1): 79-90 (in Russ.).]
- Laredo J. D., Hamze B. Complications of percutaneous vertebroplasty and their prevention // Semin. Ultrasound, CT and MRI, WB Saunders. 2005. 26(2): 65-80.
- W. Chu et al. Decompressed percutaneous vertebroplasty: A secured bone cement delivery procedure for vertebral augmentation in osteoporotic compression fractures // Injury. 2013. 44(6):813-818. DOI: 10.1016/j.injury.2012.10.017
- Noez S. et al. Traitement par kyphoplastie d’un hémangiome vertébral douloureux //Revue Médicale de Liège. 2006. 61(2): 91-6.
- Atalay B. et al. Sacral kyphoplasty for relieving pain caused by sacral hemangioma //Spinal Cord. 2006. 44(3): 196-199.
- Jones J.O., Bruel B.M., Vattam S.R. Management of Painful Vertebral Hemangiomas with Kyphoplasty: A Report of Two Cases and a Literature Review // Pain Physician. 2009. 12: 297–303.
- Armaganian G., Adetchessi T., Pech-Gourg G. еt al. L1 burst fracture with associated vertebral angioma // Orthop Traumatol Surg Res. 2013. 99(2): 241-246. DOI: 10.1016/j.otsr.2012.12.016
- Syrimpeis V., Vitsas V., Korovessis P. Lumbar vertebral hemangioma mimicking lateral spinal canal stenosis: Case report and review of literature. The journal of spinal cord medicine. 2014. 37 (2): 237-242. DOI: 10.1179/2045772313Y.0000000135
- Yu B. et al. Noncontiguous lumbar vertebral hemangiomas treated by posterior decompression, intraoperative kyphoplasty and segmental fixation: Case report //Journal of Neurosurgery: Spine. 2014. 20 (1): 60-66. DOI: 10.3171/2013.10.SPINE13499


