К вопросу о структуре продуктов карамелизации D-мальтозы в водно-этанольных средах
Автор: Черепанов Игорь Сергеевич
Рубрика: Актуальные проблемы развития пищевых и биотехнологий
Статья в выпуске: 2 т.6, 2018 года.
Бесплатный доступ
Исследование процессов карамелизации в углеводных системах традиционно осложняется сравнительно жесткими условиями проведения реакций, приводящими к значительному количеству продуктов, при этом прогнозируемые свойства карамелей являются биологически важными, в связи с чем представляется перспективным изучение формирования определяющей их структуры. На основании анализа данных производной ИК-спектроскопии произведено отнесение основных полос поглощения в области колебаний эфирных связей, показано присутствие в структуре карамелей гликозидных фрагментов, являющихся как остатками мальтозы, так и новообразованиями, формирующимися в процессе карамелизации. Данные выводы были сделаны на основании факта появления дополнительных полос поглощения в интервалах 1200-1000 и 990-930 см-1. Формирование олигоструктур реализуется при термическом воздействии в сравнительно мягких условиях термостатирования в смешанном растворителе и активирующем действии малых количеств щелочи. Механизмы возникновения промежуточных продуктов начальных стадий можно представить как щелочной сольволиз мальтозы, либо как рециклизацию с элиминированием и образованием дикарбонильных редуктонов; в первом случае вероятно образование способных к дальнейшим термическим превращениям ангидроформ, второй путь является ключевым для формирования окрашенных продуктов карамелизации. Совокупность реализующихся в общем случае начальных неселективных процессов приводит к образованию на поздних стадиях смесей продуктов, способных к фракционированию посредством диализа. Анализ ИК-спектров в карбонильной области показывает наличие в продуктах полных реакционных систем полос поглощения β-дикарбонильных и сопряженных β-гидрокси-α,β-еноновых фрагментов (1600, 1625, 1720 см-1), которые не фиксируются в ИК-спектрах недиализуемых продуктов. На этом основании можно отнести значительную часть окрашенных продуктов к низкомолекулярным структурам, тогда как сравнительно «бедный» сигналами ИК-спектр недиализуемого продукта представляет олигомерную составляющую карамелей.
D-мальтоза, карамелизация, водно-этанольные среды, производная ик-спектроскопия, олигогликозидные фрагменты, окрашенные продукты, диализ, ангдироформы, дикарбонильные структуры
Короткий адрес: https://sciup.org/147233229
IDR: 147233229 | УДК: 664.1:543.4 | DOI: 10.14529/food180202
To the problem of structure of D-maltose caramelization products in aqueous-ethanolic media
The research of caramelization processes in carbohydrate systems is traditionally complicated by rather rigid conditions of carrying out reactions resulting in the significant amount of products, at the same time the predicted caramels properties are biologically important, in this connection studying of the formation structure defining them is perspective. Based on the analysis of derivative IR-spectroscopy data reference of the main absorption bands in the either-linkage vibration region is made, presence of the glycoside fragments which are both maltose fragments in caramel structure and new oligomers forming via caramelization is shown. In is concluded based on the fact of registration of side absorption bands in intervals of 1200-1000 and 990-930 cm-1. Formation of oligoglycosides is implemented at thermal influence in rather weak conditions of a thermostatting in the mixed solvent and following activating effect of alkali. Mechanisms of intermediate products formation at incipient states can be presented as alkaline solvolysis of maltose, or recyclization with elimination and formation of dicarbonyl reductons; formation capable to further thermal conversions anhydroforms is in case of the former probable, the second pathway is a key one for formation of colored caramelization products. Amount of the initial non-selective processes leads to formation at late stages the products mixture capable to fractionating by dialysis. The analysis of IR spectrums in carbonyl area shows existence in the complete reaction systems products of absorption bands, assigned to β-dicarbonyl and the conjugated β-hydroxy-α,β-enone fragments (1600, 1625, 1720 cm-1), which are not fixed in IR-spectrums of nondialyzable products. On this basis it is possible to refer the considerable proportion of the colored products to low-molecular structures, whereas the IR-spectrum of nondialyzable product rather "poor" in bands represents an oligomeric component of caramels.
Текст научной статьи К вопросу о структуре продуктов карамелизации D-мальтозы в водно-этанольных средах
Продукты термодеструкции углеводов (карамели) являются одними из наиболее широко известных веществ в пищевой индустрии; при этом в последнее время появились работы [1], детально описывающие карамелизованные углеводы как потенциальные высокоактивные антиоксиданты. Процессы карамелизации углеводов протекают как в растворах, так и в процессах «сухой» термодеструкции, каталитически ускоряясь кислотами, щелочами [2], солями аминокислот [3]. Важность изучения закономерностей данных процессов и структуры формирующихся продуктов неоднократно подчеркивалась вследствие их существенной зависимости от внешних и внутренних факторов; недавними исследованиями [4] было показано, что основными процессами, приводящими к образованию ка- рамелей, являются гликозирование и раскрытие углеводных циклов. Механизм образования О-гликозидов как результата поликонденсации низкомолекулярных углеводов известен давно [5], к настоящему времени в химии гликозидов разработан ряд синтетических методов [6] их получения, но структура формирующихся продуктов авторами цитируемых работ [1–3, 5] не обсуждается.
Колебательные спектры углеводов, как известно, содержат большое количество полос и зачастую трудно поддаются полной расшифровке, при этом отдельные области спектра содержат слаборазрешенные участки, детальный анализ которых практически невозможен. Для увеличения разрешения сигналов применяются различные способы обработки спектров, в частности использование производной ИК-спектроскопии [7] и Фурье- деконволюции [8]. Несмотря на ряд ограничений, данные методы позволяют решать многие задачи в части установления характера структурных фрагментов природных соединений и их производных анализом преобразованных спектров.
В настоящей работе представлены результаты изучения строения структурных фрагментов продуктов карамелизации D -мальтозы в водно-этанольной среде методом нормальной и производной ИК-спектро-скопии с целью установления и детализации характера гликозидных фрагментов карамелей и природы окрашенных продуктов.
Объекты и методы исследований
Целевые продукты были получены термостатированием водно-этанольного (62 %) раствора мальтозы (0.002 моль) в присутствии щелочи (NaОН, 3·10–4 моль) в течение 1,5 часа при 90 °С, ИК-спектры выделенных и высушенных карамелей снимались на ИК-Фурье спектрометре ФСМ 2201. Дополнительно карамели выдерживались в диализаторе в течение 48 часов, недиализуемый продукт также спектроскопически исследовался. Для подтверждения ряда выводов в аналогичных условиях были получены и исследованы карамели на основе моносахаридов ( D -глюкозы и D -галактозы).
Результаты и их обсуждение
Ранее был проведен детальный анализ полос поглощения ряда углеводов в области 1200–960 см–1 [9] и показано, что наличие в структуре олигосахаридов гликозидных связей надежно идентифицируются в областях 990–960 и 1170–1130 см–1. Вторые производные ИК-спектров продуктов карамелизации мальтозы в указанных областях представлены на рис. 1.
Анализ спектров показывает наличие ряда полос, характерных как для дисахаридов, так для олигосахаридов. Поглощение при 1151 см–1, которое достаточно четко выражено для обоих продуктов, относится к асимметричным колебаниям α(С 1 -О-С 4 ) [10], что может свидетельствовать о сохранении некоторой части структуры мальтозы в составе карамелей, хотя следует отметить, что отнесение данной полосы активно дискутируется в других работах [8]. В обоих случаях регистрируются несколько полос, в частности 1078, 1109 см–1 для продукта полной реакционной системы и 1051, 1091 см–1 для недиализуемого продукта, что может свидетельствовать об образовании новых структурных связей. Подтверждением этому являются дополнительные полосы в области 930–990 см–1, которые обычно не фиксируются в ИК-спектрах большинства простых углеводов[8] и служат косвенным доказательством наличия олигоглико-зидных фрагментов [9].В частности, для продуктов карамелизации D -глюкозы и D -галактозы в указанной области (рис. 2) кроме традиционно регистрируемого поглощения 915–920 см–1, отвечающего колебаниям пиранозных колец (тип I), хорошо видны незави-
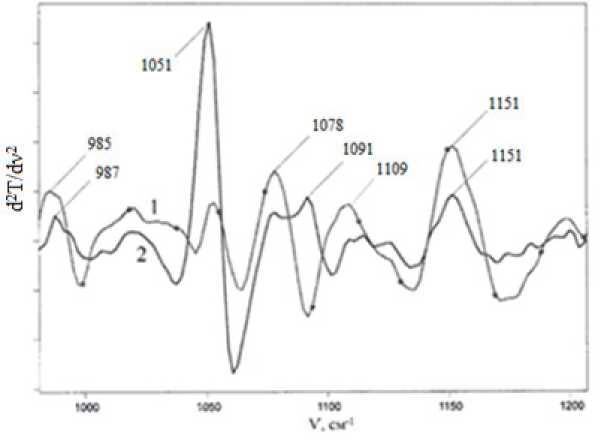
Рис. 1. Вторая производная ИК-спектра продукта карамелизации D -мальтозы в водно-этанольной среде в области 990–1200 см–1: 1 – спектр продукта, выделенного по окончании синтеза; 2 – спектр недиализуемого продукта
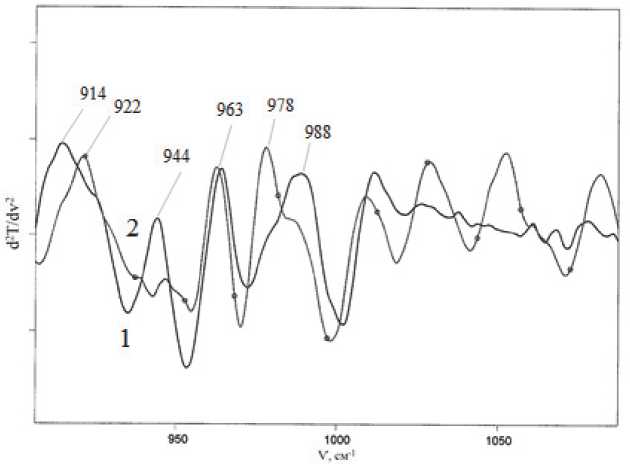
Рис. 2. Вторая производная ИК-спектров продуктов карамелизации в водно-этанольной среде: 1 – D -глюкозы; 2 – D -галактозы
сящие от типа углевода сигналы при 963 см–1, а также 978 см–1 для производных глюкозы и 988 см–1 для производных галактозы. Аналогичная практически постоянная по частоте полоса при 985–987 см–1 видна в спектре продуктов карамелизации мальтозы и описана авторами [9] для ряда олигоструктур.
Механизмы образования структуры карамелей несмотря на значительное количество идентифицированных летучих продуктов [2] представляются изученными в малой степени. Наиболее вероятными можно считать два основных направления:
В первом случае (I) происходит щелочной сольволиз мальтозы с одновременным образованием 1,2-ангидроциклов (1), которые впоследствии могут трансформироваться в 1,6-ангидроструктуры (2) [11], при этом, по мнению авторов [4], описанные превращения могут протекать в сформированных предварительно олигогликозидных цепях. Данный вариант развития процессов, вероятно, более характерен для «сухой» карамелизации. В основе второй схемы (II) лежит механизм рециклизации и элиминирования («peeling off» [12, 13]) с образованием дикарбонильных со-
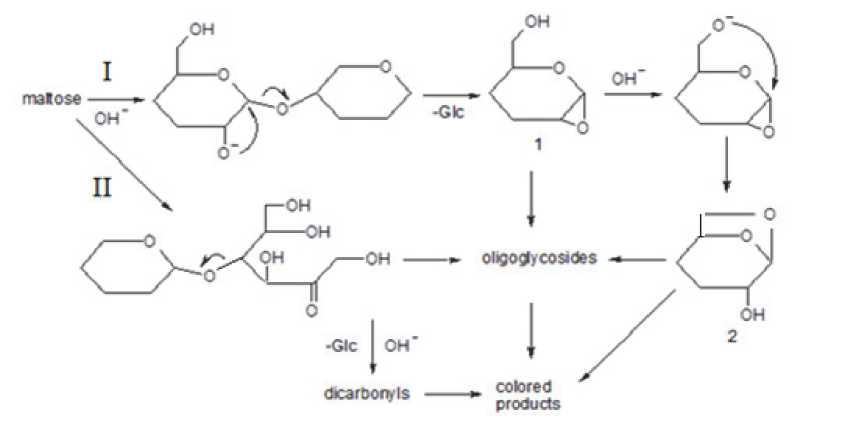
единений, конденсация которых приводит к окрашенным продуктам. Не исключается также, что окрашенные продукты могут образоваться непосредственно из ангидропроизводных [2].
Анализ поглощения в карбонильной области (рис. 3) показывает, что в процессе разделения составляющие карамелей, содержащие сопряженные системы кратных связей (полосы 1595, 1625, 1720 см–1), оказываются в диализате, т. е. являются низкомолекулярными производными – продуктами конденсации. По всей видимости комбинация указанных полос поглощения является следствием присутствия в структуре карамелей β-дикарбо-нильных и β-гидрокси-α,β-енон-фрагментов [13]. Следует отметить, что структура традиционных карамелей, полученных из сахарозы, отличается от таковых, синтезированных из восстанавливающих дисахаридов вследствие склонности фруктоз к образованию диангидридов [14]. Недиализуемый продукт не показывает аналогичную тонкую структуру в данной области поглощения (одна составная полоса при 1640 см–1), что свидетельствует о преобладании хромофоров в структуре низкомолекулярных составляющих карамелей.
Результаты проведенных исследований показывают протекание карамелизации мальтозы в водно-этанольных средах по нескольким возможным механизмам, приводящим к различным типам продуктов – преимущест- венно низкомолекулярным окрашенным веществам карбонильной природы и нерегулярным олигомерным структурам, которые, тем не менее, могут быть при необходимости фракционированы. Полученные данные могут быть полезны при разработке методик направленного получения целевых продуктов переработки углеводного сырья, обладающих биологически важными свойствами.
Список литературы К вопросу о структуре продуктов карамелизации D-мальтозы в водно-этанольных средах
- Benjakul S., Visessanguan W., Phonghanpai V., Tanaka M. Antioxidative activity of caramelization products and their preventive effect on lipid oxidation in fish mince // Food Chem., 2005, vol. 90, pp. 231-239. DOI: 10.1016/j.foodchem.2004.03.045
- Kroh L. Caramelisation in food and beverages // Food Chem, 1994, vol. 51, pp. 373-379. DOI: 10.1016/0308-8146(94)90188-0
- Fadel H.H., Farouk A. Caramelization of maltose solution in the presence of alanine // Amino Acids, 2002, vol. 22, pp. 199-213. 10.1007/ s007260200 DOI: 10.1007/s007260200
- Golon A., Kuhnert N. Unraveling the chemical composition of caramels // J. Agric Food Chem, 2012, vol. 60, pp. 3266-3272. DOI: 10.1021/jf204807z
- Hohno H., Adachi S. Disaccharide formation in thermal degradation of lactose / H. Honho // J. Dairy Sci., 1982, vol. 65, pp. 1421-1427. DOI: 10.3168/jds.S0022-0302(82)82364-3
- Yamamori A., Okada H., Kawazoe N., Muramatsu K., Onodera S., Shiomi N. Characteristics of α-D-fructofuranosyl-(2→6)-D-glucose synthesized from D-glucose and D-fructose by thermal treatment // J. Appl. Glycosci, 2014, vol. 61, pp. 99-104. 10.5458/ jag.jag.JAG-2014_001
- DOI: 10.5458/jag.jag.JAG-2014_001
- Matsuhiro B., Rivas P. Second-derivative Fourier transform infrared spectra of seaweed galactans // J. Appl. Phycol., 1993, vol. 5, pp. 45-51.
- DOI: 10.1007/BF02182421
- Nikolaenko N.A., Buslov D.K., Sushko N.I., Zhbankov R.G. Investigation of stretching vibration of glycosidic linkages of disaccharides and polysaccharides with use of IR spectra deconvolution // Biopolymers, 2000, vol. 57, pp. 257-262.
- DOI: 10.1002/1097-0282(2000)57:4
- Kacurakova M., Mathlouthi M. FTIR and laser-Raman spectra of oligosaccharides in water: characterization of the glycosidic bond // Carbohydr. Res., 1996, vol. 284, pp. 145-157.
- DOI: 10.1016/0008-6215(95)00412-2
- Sekkai M., Dincq V., Legnard P., Huvenne J.P. Investigation of the glycosidic linkages in several oligosaccharides using FT-IR and FT Raman spectroscopies // J. Mol. Struct., 1995, vol. 349, pp. 349-352.
- DOI: 10.1016/0022-2860(95)08871-P
- Cerny M., Stanek J. 1,6-anhydro derivatives of aldohexoses // Adv. Carbohydr. Chem. Biochem, 1977, vol. 34, pp. 24-178.
- Hollnagel A., Kroh L. Degradation of oligosaccharides in nonenzymatic browning by formation of α-dicarbonyl compounds via a «peeling off» mechanism // J. Agric. Food Chem., 2000, vol. 48, pp. 6219-6226.
- DOI: 10.1021/jf9906127
- Lewin M., Ziderman I., Weiss N., Basch A., Ettinger A. Chromogen formation during the alkaline degradation of hydrocellulose and cellobiose // Carbohydr. Res., 1978, vol. 62, pp. 393-398. 10. 1016/ S0008-6215(00)80890-3
- DOI: 10.1016/S0008-6215(00)80890-3
- Chi Y.D., Berglund K.A. Kinetics of difructosedianhydrides formation under fructose crystallization conditions // Starch, 1990, vol. 42, pp. 112-117. DOI: 0038-9056/90/0303-0112


