Кардиоваскулярные осложнения третичного сифилиса: разрыв аневризмы нисходящего отдела грудной аорты с последующим формированием аорто-пищеводного свища
Автор: Черная Н.Р., Лосева В.В., Горшков Н.С., Селяев В.С., Николаева Е.Б., Коков Л.С.
Журнал: Вестник медицинского института "РЕАВИЗ": реабилитация, врач и здоровье @vestnik-reaviz
Рубрика: Клинический случай
Статья в выпуске: 6 т.15, 2025 года.
Бесплатный доступ
Актуальность. У 30% пациентов, заражённых сифилисом и не получающих лечение, спустя длительный период течения болезни выявляются осложнения, характеризуемые как третичный сифилис. Сосудистые поражения чаще всего манифестируют спустя 15–30 лет после установления носительства инфекции. Аневризма аорты – одно из редких проявлений кардиоваскулярного сифилиса. Ввиду того, что аневризма аорты является редко встречаемым осложнением у пациентов с сифилисом, важными являются своевременные диагностика и лечение. Цель исследования: проанализировать особенности диагностики, тактику хирургического лечения пациентов с сифилитической аневризмой аорты. Материалы и методы. Описано клиническое наблюдение пациента с сифилитической аневризмой нисходящего отдела грудной аорты с признаками разрыва и формирования аорто-пищеводного свища. Анализ данных клинического наблюдения выполнен ретроспективно. Результаты. Пациент П. доставлен в клинику в апреле 2024 года по экстренным показаниям. В течение двух недель пациента беспокоил кашель и ноющие боли в эпигастральной области. По результатам обследования установлен диагноз – аневризма грудной части аорты разорванная (I71.1). Пациенту выполнено сонно-подключичное шунтирование слева, эндопротезирование грудной аорты. При повторной госпитализации спустя полгода по данным эндоскопических исследований и компьютерной томографии установлено наличие аорто-пищеводной фистулы. Выводы. Выявление больных с сосудистыми осложнениями на фоне течения сифилиса представляет сложность. Отличительной особенностью сифилитической аневризмы аорты является её длительное бессимптомное течение, что затрудняет раннее выявление патологии и своевременное лечение.
Аневризма грудной аорты, третичный сифилис, разрыв аневризмы, аортопищеводный свищ, сосудистые осложнения, эндоваскулярная коррекция, гематома средостения, кардиоваскулярный сифилис, стент-графт, сифилитический аортит
Короткий адрес: https://sciup.org/143185459
IDR: 143185459 | УДК: 616.13-007.64-002.5:616.329-007.253 | DOI: 10.20340/vmi-rvz.2025.6.CASE.2
Cardiovascular complications of tertiary syphilis: rupture of the aneurysm of the descending thoracic aorta, followed by the formation of an aortoesophageal fistula
Relevance. 30% patients who infected syphilis during the long time have got complications characterized as tertiary syphilis. Vascular complications often manifest after 15–30 years. An aortic aneurysm is one of the rare cardiovascular syphilis manifestation. Due to the fact that it is a rare complication, timely diagnosis and the correct treatment choice for such patients are important. The aim of the study. To analyze the diagnosis’ features and surgical treatment tactics for patients with syphilitic aortic aneurysm. Materials and methods. This paper describes a clinical case of a patient with ruptured syphilitic descending thoracic aortic aneurysm and signs of aortoesophageal fistula formation. The data analysis was performed retrospectively. Results. Patient P. was admitted to the clinic in April 2024. For two weeks he had been complaining of cough and epigastric pain. The examination revealed ruptured thoracic aortic aneurysm (I71.1). The patient underwent left carotid subclavian bypass surgery and thoracic endovascular aortic aneurysm repair. Six months later according to endoscopic examinations and computer tomography an aortoesophageal fistula was established. Conclusion. Identification of patients with syphilitic vascular complications is difficult. A syphilitic aortic aneurysm feature is its long-term asymptomatic course, which makes it difficult to early detection and treatment.
Текст научной статьи Кардиоваскулярные осложнения третичного сифилиса: разрыв аневризмы нисходящего отдела грудной аорты с последующим формированием аорто-пищеводного свища
По данным Всемирной организации здравоохранения численность заболевших сифилисом в мире составляет более 8 миллионов человек в возрасте от 15 до 49 лет. Последние опубликованные данные, собравшие статистику по России, сообщают о более чем 2500 заболевших в год. Ежегодно число носителей инфекции увеличивается, что требует внимания со стороны системы здравоохранения в вопросах диагностики и лечения основного заболевания и его осложнений.
В ряде случаев сифилис может протекать бессимптомно, что впоследствии становится причиной тяжёлых осложнений спустя 10–15 лет с момента попадания возбудителя в организм человека. Вместе с этим более 30% лиц с установленным диагнозом сифилиса являются ВИЧ-позитивными, что также усугубляет течение болезни и ещё больше снижает уровень иммунной защиты [1].
Установлено, что среди лиц с первичным сифилисом у 10% заболевание долгое время остаётся невыявленным. При отсутствии лечения это ведёт к осложнениям со стороны нервной и сердечнососудистой систем [1]. Аневризма аорты – одно из редких проявлений кардиоваскулярного сифилиса. Она встречается у трети пациентов с сосудистыми осложнениями в результате персистенции возбудителя сифилиса в организме. Сосудистые поражения чаще всего манифестируют спустя 15–30 лет после установления наличия инфекции. Помимо возник- новения аневризмы аорты могут быть выявлены стенозы магистральных сосудов шеи (10–20%), а также поражения сердечных клапанов (20–30%) [1, 2].
Основной сложностью диагностики сифилитических аневризм аорты является их бессимптомное течение. Проявления заболевания возникают чаще всего только при достижении аневризмой размера более 10–15 см в диаметре [3]. Причиной формирования патологического расширения аорты служит тропность спирохет к vasa vasorum, a также к слою адвентиции, что вызывает хроническое воспаление сосудистой стенки и ведёт к формированию локальных очагов некроза [3–5]. Ишемия среднего слоя сосудистой стенки становится причиной гибели мышечных клеток и потери тканью эластических свойств, а иммунный ответ в виде диффузного лим-фоцитоидного и плазмоцитоидного воспаления ведёт к развитию фиброза, формированию кальцифи-катов и расширению диаметра сосудов [6]. Ввиду большого размера и тонкой стенки, не способной к сопротивлению току крови при большом давлении, формируются гигантские аневризмы аорты, склонные к разрывам [3, 7]. Особенности молекулярного профиля клеток, формирующих разные отделы аорты, обусловливают тот факт, что тропность возбудителя сифилиса к тканям в различных участках сосуда меняется. Увеличению объёма поражения дополнительно способствует гематогенное распространение инфекции, а также присоединение условно- патогенной флоры к воспалительному процессу в условиях выраженной иммуносупрессии.
Чаще аневризма формируется в области дуги аорты (35%) и затрагивает нисходящий отдел грудной аорты (50%). Крайне редко поражаются брюшная аорта и отходящие от неё ветви, питающие органы брюшной полости [4, 5, 8]. Прогрессирование заболевания приводит к последующему формированию недостаточности аортального клапана и клиническим проявлениям острого коронарного синдрома [2, 9].
В исследовании учёных из Тайваня была проведена статистическая оценка базы данных более 28 000 пациентов с установленным диагнозом сифилиса. В расчёт были включены пациенты с осложнениями на фоне течения основного заболевания. В сравнении с данными более 20 000 пациентов с сосудистыми заболеваниями, но не имеющими в анамнезе сифилитической инфекции, было установлено, что инфицированные больные имеют статистически значимый больший риск развития осложнений со стороны сердечно-сосудистой системы. У таких больных в несколько раз выше частота развития инфаркта миокарда, аортальной недостаточности, фибрилляции предсердий и ишемического инсульта (p<0,001, a=95%), однако риск развития аневризмы аорты у пациентов старшей возрастной группы одинаков, независимо от наличия или отсутствия инфекции [9].
Ввиду того, что аневризма аорты является тяжёлым и редко встречаемым осложнением у пациентов с сифилисом, важными являются своевременная диагностика и корректный выбор тактики лечения таких больных. При достижении больших размеров аневризма вызывает сдавление рядом расположенных органов и проявляется затруднением дыхания, глотания, сухим кашлем и синдромом сдавления верхней полой вены [10]. Отличительной особенностью сифилитической аневризмы аорты является то, что для неё не характерно расслоение сосудистой стенки ввиду выраженного фиброза [11], поэтому основной причиной гибели пациентов с указанным диагнозом является именно разрыв аорты. По мнению многих авторов, течение сосудистых осложнений третичного сифилиса непредсказуемо [2], что заставляет обращать на себя внимание врачей в плане настороженности к выявлению инфекции.
Летальность пациентов с данным диагнозом составляет 80% за период двухлетних наблюдений [6]. На текущий момент стандартом для определения наличия инфекции являются лабораторные методы диагностики (выявление антител к Treponema pallidum), однако по результатам нескольких крупных исследований было выявлено, что серологические тесты у пациентов с сосудистыми осложнениями чаще отрицательны [12]. Причины снижения чув- 183
ствительности лабораторных маркеров к сифилису при наличии сосудистой патологии не выявлены, однако это говорит о том, что для установления точного диагноза предпочтительно использовать комбинацию лабораторных и инструментальных методов исследования [13, 14]. При проведении компьютерной томографии (КТ) на генез аневризмы аорты, связанный с сифилисом, может указывать значительное утолщение стенки, формирование множественных гематом, а также переход воспаления и патологического расширения на более мелкие ветви сосудов, отходящих непосредственно от аорты [13]. По данным китайских исследований, при обнаружении мешотчатых аневризм во время проведения инструментальных исследований прогноз для жизни пациента может быть более неблагоприятным [15].
Безусловно, пациентам с сифилитической аневризмой аорты требуется проведение оперативного вмешательства. На данный момент дискуссионным является вопрос выбора типа операции. Многократно описано сочетание консервативной терапии, направленной на лечение основного заболевания, и хирургических методик с целью коррекции сосудистых осложнений. Не менее эффективным способом коррекции сифилитической аневризмы аорты являются гибридные методы хирургического вмешательства, требующие протезирования корня и восходящего отдела аорты. В результате прогрессирования сифилитического аортита аневризма аорты часто сочетается с недостаточностью аортального клапана. В таком случае оправданным является применение гибридной хирургии. Текущие возможности сочетания как эндоваскулярной, так и открытой хирургии позволяют комбинировать различные способы вмешательств для достижения положительных результатов лечения таких пациентов [5].
Различные варианты вмешательства, в первую очередь, обусловлены факторами пола, возраста и наличия сопутствующих заболеваний. Также значимым критерием при выборе открытого, эндоваскулярного вмешательства или их сочетания является оценка тяжести состояния пациента при поступлении в стационар, данных лабораторных и инструментальных исследований [6, 16]. Показатель выживаемости пациентов с сифилитической аневризмой аорты низкий, но, вероятно, эти данные могут быть улучшены при большем внимании к описываемому инфекционному заболеванию и более частом наблюдении в динамике пациентов с подтверждённым диагнозом для раннего выявления осложнений и их своевременного лечения [6].
наиболее подходящих под запрос публикаций в базе данных PubMed (MEDLINE) применены алгоритмы поиска с использованием терминов MeshTerms – «aortic aneurysm/diagnostic imaging» [MeSH], «aortic aneurysm/microbiology» [MeSH], «syphilis, cardiovascular/complications» [MeSH], «syphilis, cardiovascular/surgery» [MeSH], «heart disease risk factors» [MeSH].
РЕЗУЛЬТАТЫ
Пациент П., 36 лет, был доставлен в клинику в апреле 2024 года с жалобами на затруднение дыхания и глотания. До этого в течение двух недель предъявлял жалобы на сухой кашель. К врачу по поводу указанной жалобы не обращался, самостоятельно принимал различные препараты от кашля, улучшения состояния при этом не наблюдалось. За два дня до госпитализации пациент стал ощущать боли в эпигастральной области ноющего характера, не связанные с приёмом пищи. В связи с этим пациент обратился в поликлинику по месту жительства, назначена консервативная терапия, назвать препараты больной затрудняется.
Вечером в день, предшествующий госпитализации, пациент употреблял крепкие алкогольные напитки. Ночью почувствовал отёчность в горле, затруднение дыхания. Самостоятельно была вызвана скорая медицинская помощь, пациент госпитализирован по экстренным показаниям. При обследовании в стационаре выявлены признаки синдрома системной воспалительной реакции (лейкоциты – 18,62*109/л, С-реактивный белок – 192,4 мг/л).
Установлен диагноз:
Основной: аневризма грудной части аорты разорванная (I71.1).
Хронические заболевания: хронический га стродуоденит.
Жалобы при поступлении: отёчность в горле, затруднённое дыхание, глотание, сухой кашель, ноющие боли в эпигастральной области, не связанные с приёмом пищи.
Объективно: общее состояние пациента тяжёлое, обусловлено основной диагностированной патологией. Сознание ясное. Температура тела 36,6 °C. Дыхание самостоятельное, с ингаляцией кислорода объёмом 6 л/мин. Дыхание регулярное, частота дыхательных движений (ЧДД) составила 16/мин., SpO 2 =96%, аускультативно – дыхание проводится равномерно во все отделы лёгких, хрипов нет. Гемодинамика со склонностью к гипертензии, артериальное давление (АД)=103/68 мм рт.ст. Пульс – 76 уд./мин., умеренного наполнения, ритм не нарушен. Живот не вздут, в дыхании участвует, при пальпации – мягкий, безболезненный. Симптомы раздражения брюшины отрицательные. Индекс массы тела (ИМТ) – 19,8 кг/м2. Мочеиспускание осуществ- 184
ЦЕЛЬ ИССЛЕДОВАНИЯ: проанализировать особенности диагностики и тактики хирургического лечения больных с сифилитической аневризмой аорты на примере демонстрации клинического наблюдения пациента с указанным диагнозом.
ЗАДАЧИ
-
1. Выполнить ретроспективный анализ клинического наблюдения пациента с сифилитической аневризмой нисходящей части грудной аорты с признаками разрыва (I71.1) с последующим формированием аорто-пищеводного свища.
-
2. Изучить литературные данные, рассматривающие вопросы диагностики кардиоваскулярных осложнений третичного сифилиса, и подходы к лечению таких пациентов.
-
3. Проанализировать применяемые тактики оперативного лечения больных с сифилитической аневризмой аорты, а также пациентов с осложнениями в виде формирования патологического сообщения между аортой и пищеводом на основе опубликованных международных исследований.
МАТЕРИАЛЫ И МЕТОДЫ
В данной работе рассмотрен вопрос выбора тактики ведения пациентов с сифилитической аневризмой аорты и её осложнениями. Изучены статистические данные о частоте выявления инфекции и её перехода в третичный сифилис, вызывающий осложнения со стороны не только иммунной системы, но и других систем и органов. Рассмотрены современные мнения о механизмах патогенеза аневризмы аорты при попадании в организм T. pallidum, а также механизмы повреждения сосудистой стенки.
Описано клиническое наблюдение пациента с аневризмой нисходящего отдела аорты с признаками разрыва и формированием медиастинальной гематомы. По данным лабораторных исследований у пациента выявлены антитела (IgG, IgM) к T. pallidum. Ранее диагноз сифилиса не был установлен. При повторной госпитализации у пациента выявлены признаки формирования аортопищеводного свища. Анализ данных клинического наблюдения выполнен ретроспективно.
Литературные данные, рассмотренные в работе, преимущественно опубликованы в период с 2020 по 2025 гг. Поиск информации осуществлён в российских и международных базах данных – в публикациях, включённых в Российский индекс научного цитирования, а также в работах, размещённых на PubMed (MEDLINE), Elsevier, Scopus, Cochrane Library, Research Gate, с использованием ключевых слов «thoracic aortic aneurysm», «tertiary syphilis», «mediastinal haematoma», «aneurysm rupture», «vascular complications», «TEVAR». Для отбора ляется по катетеру. Жалобы на своё состояние пациент активно не предъявлял на фоне инфузии морфина (доза на приём – 20 мг).
Данные лабораторных исследований:
Общий анализ крови: эритроциты – 3,72*1012/л, тромбоциты – 331,0*109/л, гемоглобин – 102,0 г/л, лейкоциты – 15,20*109/л, лимфоциты – 5,7%, моноциты – 2,5%, нейтрофилы – 91,2%, эозинофилы – 0,5%.
Биохимический анализ крови: общий белок – 75,82 г/л, креатинин – 93,87 мкмоль/л, мочевина – 9,83 ммоль/л, Cl- – 93,09 ммоль/л, Na+ – 134,77 ммоль/л, K+ – 5,37 ммоль/л, глюкоза – 9,98 ммоль/л, общий билирубин – 4,35 мкмоль/л, АСТ – 33,74 ед/л, АЛТ – 8,06 ед/л, КФК – 1214,92 ед/л.
Коагулограмма: концентрация протромбина – 66,9%, международное нормализованное отношение (МНО) – 1,28, протромбиновое время – 15,2 с, активированное частичное тромбопластиновое время (АЧТВ) – 21,6 с, концентрация фибриногена – 6,24 г/л.
Антитела IgG, IgM к T. pallidum – положительный результат.
При ультразвуковом исследовании выявлен неокклюзионный тромбоз внутренней яремной вены слева. Показатели скорости кровотока во внутренних сонных артериях с двух сторон снижены.
При ультразвуковом исследовании вен верхних конечностей обнаружены ЭХО-признаки гематомы мягких тканей шеи слева по типу геморрагического пропитывания.
При выполнении обзорной рентгенографии органов грудной клетки лёгочные поля без свежих и инфильтративных теней, корни лёгких структурные, не расширены. Диафрагма чёткая. Тень средостения не смещена, несколько расширена на уровне сосудистого пучка. Тень сердца не расширена. Аорта расширена на уровне дуги.
При проведении эндоскопического исследования трахеи и бронхов в просвете бронхиального дерева визуализируется небольшое количество слизистой мокроты. Левый главный бронх щелевидно сужен до 0,1*1,5 см за счёт сдавления извне гематомой.
По данным КТ, выполненной при поступлении, по правому контуру аорты визуализирован затёк контрастного препарата размерами 17*24 мм с формированием медиастинальной гематомы с распространением в ретрофарингеальное пространство общими размерами 72*49*200 мм.
После проведения полного обследования пациент был экстренно подан в операционную. Выполнено сонно-подключичное шунтирование слева с последующим эндопротезированием аорты.
Ход операции: под эндотрахеальным наркозом надключичным доступом с левой стороны выделены левая общая сонная артерия (ОСА) и левая подключичная артерия (ПА). Отмечено выраженное им-бибирование кровью мягких тканей и мышц вследствие разрыва грудной аорты. Артерии не изменены. Диаметр ОСА – 7 мм, ПА – 6 мм. Левая ПА выделена в дистальном направлении, сосуд лигирован в проксимальном отделе и от устья левой внутриг-рудной артерии. Мобильность левой ПА ограничена, сосуд расположен глубоко, ввиду чего было принято решение воздержаться от транспозиции.
После предварительного введения гепарина (5 тыс. ед.) наложен зажим на левую ПА. Выполнен анастомоз левой ПА со свободным краем синтетического протеза диаметром 6 мм по типу конец в бок нитью пролен 6/0. Зажим с артерии снят, анастомоз состоятелен. Наложен зажим на левую ОСА, выполнена продольная артериотомия длинной 1 см. Наложен анастомоз конец в бок между дистальным концом сосудистого протеза и левой ОСА нитью пролен 6/0. Перед наложением последнего шва проведена контрольная проверка кровотока – получен хороший пульсирующий центральный кровоток и удовлетворительные ретроградные кровотоки. Зажимы сняты, анастомоз герметичен. Проведены гемостаз, дренирование, рана послойно ушита.
Время пережатия левой ОСА – 20 минут.
Вторым этапом выполнено эндопротезирование аорты (рис. 1, 2). Катетер для инвазивного измерения артериального давления в левой лучевой артерии. В правой лучевой артерии установлен интро-дьюсер 6F. Мобилизирована правая общая бедренная артерия (ОБА), произведена пункция правой ОБА, установлен интродьюсер 6F, выполнена катетеризация восходящего отдела грудной аорты. Через трансрадиальный интродьюсер по проводнику заведён катетер Pigtail в восходящий отдел аорты. Выполнена ангиография грудного отдела аорты, визуализирована аневризма нисходящего отдела грудной аорты. По диагностическому катетеру в восходящий отдел аорты поведён проводник Lunderquist. Стент-графт Ankura TAA3428B180 позиционирован и имплантирован в нисходящий отдел грудной аорты ниже отхождения левой ОСА. Выполнена контрольная ангиография, стент полностью расправлен, эндолик под протезом отсутствует, брахиоцефальный ствол, левая ОСА и сонноподключичный анастомоз проходимы, свободно контрастируются.
Наложен сосудистый шов на правую ОБА, рана послойно ушита, наложена асептическая повязка. Интродьюсер из правой лучевой артерии удалён, наложен асептическая давящая повязка, место пункции без особенностей.
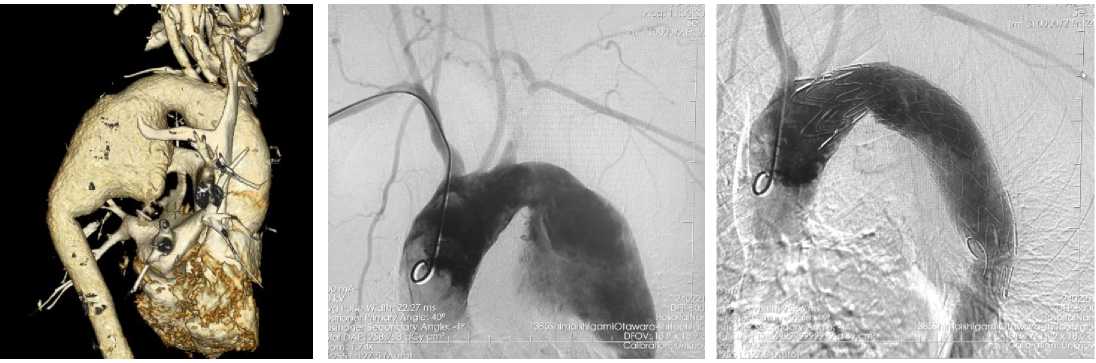
Рисунок 2. Данные интраоперационной ангиографии
Figure 2. Intraoperative angiography data
Рисунок 1. Данные 3D-реконструкции
Figure 1. 3D reconstruction data
После оперативного вмешательства пациент пе-реведё н в отделении реанимации. Общее состояние – тяжёлое, обсусловленное объёмом и характером оперативного вмешательства. Поддержка дыхательной функции осуществлена аппаратом искусственной вентиляции лёгких (ИВЛ). Гемодинамика со склонностью к гипертензии, АД=145/65 мм рт. ст., пульс – 110 уд/мин.
По данным КТ-ангиографии на вторые сутки:
Грудная аорта: восходящий отдел – 36 мм, дуга – 34 мм, нисходящий отдел – 32 мм.
От уровня восходящего отдела дуги аорты (уровень отхождения плечевого ствола) до уровня Th8 в просвете аорты определяется стент. Контуры грудной аорты чёткие, ровные на всём протяжении, просвет однородный. Признаков затекания контрастного вещества не выявлено. Плотно прилегая к дуге аорты и к нисходящему её отделу, определяется ограниченное жидкостное скопление – вероятнее всего, лизированная кровь, неоднородной структуры за счёт наличия сгустков, объемом 180 см3. Вышеописанное образование тесно прилегает к пищеводу, чётко не дифференцируясь от него, оттесняет пищевод и трахею вправо, деформирует левую лёгочную артерию и левый главный бронх, стенозируя его просвет максимально до 3*9 мм. Размер левого главного бронха до стеноза – 8*18 мм, несколько деформирован, дистальнее стеноза – 6*14 мм. В просвете пищевода определяется зонд. В полости перикарда содержимого не выявлено.
На третьи сутки госпитализации на фоне полного пробуждения и восстановления уровня сознания до ясного и нормального мышечного тонуса, компенсированного анализа кислотно-щелочного состояния пациент был экстубирован. На фоне выраженной компрессии трахеи и левого бронха у больного отмечено стридорозное дыхание, десатурация, гиперкапния, повышенный уровень возбуждения, признаки гипоксемии, в связи с чем пациент был экстренно переведён на ИВЛ. Продолжена симптоматическая терапия, по решению врачебного консилиума, учитывая устранённый дефект аорты путём эндоваскулярной имплантации стент-графта, показаний для открытого оперативного вмешательства не установлено.
При проведении эндоскопического исследования трахеи и бронхов выявлены признаки слизистогнойного трахеобронхита.
Пациенту проведена медиастинотомия с целью эвакуации гематомы средостения – под эндотрахе-альным наркозом в положении пациента на левом боку выполнен доступ в пятом межреберье по передней подмышечной линии, установлен порт ручного ассистирования, дополнительно установлен торакопорт №10 в седьмом межреберье по средней подмышечной линии. При ревизии плевральной полости подтверждено наличие гематомы средостения. Выполнено рассечение медиастинальной плевры над и под v. azygos длиной 4 см. При помощи аспиратора эвакуировано 150 мл сгустков и жидкой крови, полость промыта физиологическим раствором. Через доступ в седьмом межреберье установлена дренажная трубка до купола плевры по задней поверхности лёгкого. Рана послойно ушита.
При проведении рентгенографии лёгких справа визуализирован пневмоторакс в нижних отделах шириной до 0,7 см. Слева слабоинтенсивное снижение прозрачности за счёт жидкости, усиление лёгочного рисунка в нижних отделах. Правый корень лёгкого структурный, левый – малоструктурный. Диафрагма слева не дифференцируется. Конец дренажной трубки визуализирован на уровне Th5.
Выявлены рентгенологические признаки пневмоторакса, гиповентиляции справа, а также гидроторакса и воспалительной инфильтрации слева.
При проведении КТ на восьмые сутки: мягкие ткани грудной клетки и шеи с множественными включениями газа, преимущественно справа. Средостение не смещено, расширено. От уровня восходящего отдела дуги аорты до уровня Th8 в просвете аорты определяется стент-графт. Плотно прилегая к дуге аорты и к её нисходяшему отделу, не дифференцируясь от парапротезного пространства и пищевода, определяется ограниченное скопление лизированной крови неоднородной структуры за счёт наличия сгустков объёмом около 100 см3. Вышеописанное образование тесно прилегает к пищеводу, чётко не дифференцируясь от него, оттесняет пищевод и трахею вправо, деформирует левый главный бронх, стенозируя его просвет максимально до 4 мм. В заднебазальных отделах лёгких определяются участки уплотнения лёгочной ткани клиновидной формы с визуализацией просветов бронхов на этом фоне. В плевральных полостях минимальное количество жидкостного содержимого.
Отмечены КТ-признаки тромбированного пара-протезного пространства без формирования эндоликов, сохраняющейся подострой гематомы верх-ние-заднего средостения с некоторым уменьшением объёма.
Спустя неделю после госпитализации отмечена положительная динамика в состоянии пациента, по данным инструментальных исследований снижена интенсивность воспалительной инфильтрации, минимальный гидроторакс слева.
По данным эндоскопического исследования трахеи и бронхов на 15 сутки в просвете трахеи визуализировано небольшое количество слизистого секрета, слизистая трахеи гиперемирована с наложением светлого фибрина различной плотности на уровне трахеостомы. Установлены эрозивноязвенный трахеит, ненапряженная гематома носоглотки.
По данным микробиологического исследования в бронхов-альвеолярном лаваже выделена Pseudomonas aeruginosa (4*104 КОЕ/мл). С целью коррекции инфекционных осложнений пациенту был назначен меропенем (1 г каждые 8 часов в/в), ванкомицин (1 г 2 раза/сутки в/в). Через неделю проведения антибиотикотерапии при консультации с клиническим фармакологом меропенем был заменен на цефепим (2 г 2 раза/сутки в/в), сульбактам (1 г 2 раза/сутки в/в).
Данные лабораторных исследований оценены в динамике на протяжении всего периода наблюдения за пациентом (табл. 1).
Таблица 1. Данные лабораторных исследований
Table 1. Laboratory test data
|
Исследуемый показатель |
1 сутки |
4 сутки |
8 сутки |
12 сутки |
16 сутки |
|
Эритроциты (кл/л) |
3,72*1012 |
3,64*1012 |
4,17*1012 |
3,58*1012 |
3,42*1012 |
|
Тромбоциты (кл/л) |
331,0*109 |
197,0*109 |
344,0*109 |
304,0*109 |
379,4*109 |
|
Гемоглобин (г/л) |
102,0 |
106,0 |
120,0 |
100,0 |
100,9 |
|
Лейкоциты (кл/л) |
15,20*109 |
12,00*109 |
15,82*109 |
11,30*109 |
17,92*109 |
|
Лимфоциты (%) |
5,7 |
5,0 |
14 |
18,20 |
8 |
|
Моноциты (%) |
2,5 |
3,0 |
10,5 |
8,40 |
2 |
|
Нейтрофилы (%) |
91,2 |
91,6 |
73,10 |
71,20 |
86,84 |
|
Эозинофилы (%) |
0,5 |
0 |
2 |
0,20 |
0 |
|
Общий белок (г/л) |
75,82 |
60,71 |
67,60 |
58,83 |
63,48 |
|
Креатинин (мкмоль/л) |
93,87 |
63,50 |
65,80 |
55,56 |
65,40 |
|
Мочевина (ммоль/л) |
9,83 |
6,99 |
5,88 |
5,15 |
3,16 |
|
АСТ (ед/л) |
33,74 |
18,50 |
39,20 |
22,30 |
19,30 |
|
АЛТ (ед/л) |
8,06 |
6,30 |
26,90 |
20,37 |
15,20 |
|
МНО |
1,28 |
0,97 |
1,13 |
1,32 |
1,18 |
|
Протромбиновое время (с) |
15,2 |
11,3 |
13,3 |
15,6 |
13,9 |
|
АЧТВ (с) |
21,6 |
29,1 |
26,7 |
28,0 |
32,9 |
|
С-реактивный белок (мг/л) |
192,4 |
202,0 |
157,0 |
94,9 |
61,6 |
Пациент был переведён в отделение торакальной хирургии, на фоне последующего улучшения состояния выписан под наблюдение хирурга по месту жительства.
В октябре пациент был повторно экстренно госпитализирован в клинику. Начиная с 1 июня больной ежедневно регистрировал подъём температуры тела до 39–40 °C, самостоятельно принимал левофлоксацин, без эффекта. С середины июня на протяжении 3 недель пациент проходил лечение в ин- фекционной клинической больнице по поводу тубулоинтерстициального нефрита, ассоциированного с Escherichia coli. С августа пациент отмечал появление слабости, была вызвана бригада скорой помощи, зафиксированы показатели АД 80/40 мм рт. ст. Пациент был госпитализирован, установлен диагноз – клостридиальный колит. После выписки больной стал вновь предъявлять жалобы на повышение температуры тела, слабость, задержку мочеиспускания, онемение ног с последующим отсутствием движе- ния в ногах. При эзофагогастродуоденоскопии диагностирован аорто-пищеводный свищ.
Прогрессирующее ухудшение состояния больного непосредственно связано с проявлениями позднего кардиоваскулярного сифилиса (мезаортит, осложненный аневризмой грудного отдела аорты с формированием гематомы, стенозируюшей просвет левого главного бронха) и позднего нейросифилиса.
При поступлении: объективно общее состояние пациента средней тяжести, обусловлено основной диагностированной патологией и осложнениями третичного сифилиса. Сознание ясное. Дыхание самостоятельное, регулярное, ослабленное, поверхностное. ЧДД составила 17/мин. АД=115/70 мм рт. ст. Пульс – 82 уд./мин., умеренного наполнения, ритм не нарушен, тоны сердца приглушены. Живот не вздут, в дыхании участвует, при пальпации – мягкий, безболезненный. Симптомы раздражения брюшины отрицательные. Мочеиспускание нарушено.
Данные лабораторных исследований:
Общий анализ крови: эритроциты – 3,09*1012/л, тромбоциты – 361,0*109/л, гемоглобин – 81,0 г/л, лейкоциты – 10,14*109/л, лимфоциты – 20,1%, моноциты – 5,3%, нейтрофилы – 65,9%, эозинофилы – 4,5%.
Биохимический анализ крови: общий белок – 66,53 г/л, креатинин – 76,4 мкмоль/л, мочевина – 4,5 ммоль/л, глюкоза – 4,4 ммоль/л, общий билирубин – 6,7 мкмоль/л, АСТ – 26,3 ед/л, АЛТ – 10,3 ед/л.
Коагулограмма: концентрация протромбина – 66,3%, МНО – 1,32, протромбиновое время – 15,7 с, АЧТВ – 33,1 с, концентрация фибриногена – 4,84 г/л.
По данным КТ органов грудной клетки: определяется дефект стенки пищевода слева на уровне Th6. В прилегающей клетчатке на данном уровне определяется включение газа, прилегающее к протезу аорты. Лимфоузлы средостения увеличены до 11 мм. Затёка контрастного вещества за пределы аорты не выявлено. Восходящий отдел аорты расширен до 21 мм. Сонно-подключичный шунт проходим. В заднебазальных отделах обоих лёгких определяются фиброзные тяжи. Слева имеется минимальный гидроторакс и повышение плотности лёгочной ткани в S10 с этой же стороны.
Учитывая наличие инфекции протеза (рис. 3) и развития высокого риска протезного кровотечения из аорты, принято решение о проведении оперативного вмешательства.
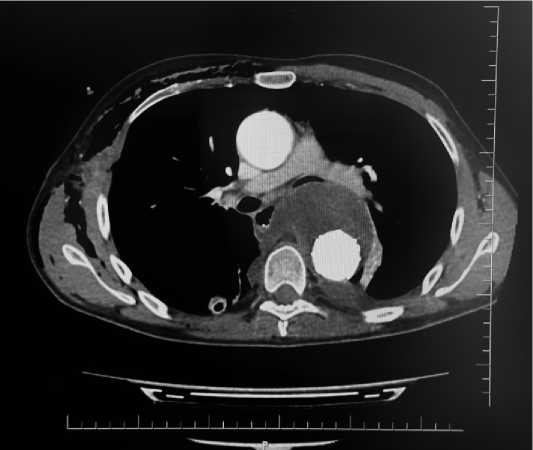
Рисунок 3. Данные КТ при повторной госпитализации Figure 3. CT data on readmission
В первые сутки произведено оперативное вмешательство. Выполнена боковая торакотомия справа в пятом межреберье протяжённостью 20 см. Произведён пневмолиз, взята на держалки непарная вена, с помощью аппарата JQA сосуд пересечён. С помощью аппарата Lotus рассечена лёгочная связка до нижней лёгочной вены. Рассечена медиастинальная плевра. Выделена нижняя треть пищевода, нижний и верхний концы пищевода пересечены, после чего проведено выделение пищевода в средней трети в зоне проекции аорты-пищеводного свища. Полость свища вскрыта, визуализирован аортальный стент-графт. Пищевод удалён. Выполнена боковая цервикотомия слева, заглушённый конец пищевода был извлечён и выведен на левую поверхность шеи, фиксирован к коже отдельными узловыми швами.
При гистологическом исследовании эпителия пищевода выявлено наличие рассеянной и очаговой лимфоплазмоклеточной инфильтрации. Ближе к адвентиции визуализирована полость, выстланная грануляционной тканью с диффузной лейкоцитарной инфильтрацией и выраженным ростом сосудов. Местами отмечено формирование мелких гранулём, в просвете обнаруженной полости визуализируется некротический детрит. На отдельных участках стенки пищевода визуализируется щелевидный ход, выстланный многослойным плоским неороговевающим эпителием с очагами воспалительной инфильтрации. Гистологическая картина предположительно соответствует просвету свищевого хода, не исключается наличие сифилитических гранулём, а также наличие дивертикула пищевода с минимальными признаками воспаления.
В первые сутки госпитализации было выполнено протезирование дистального отдела дуги и нисходящего отдела грудной аорты линейным сосудистым протезом InterGard 24*10 в условиях искусственного кровообращения (ИК) и циркуляторного ареста. В ходе оперативного вмешательства выявлены множественные разрывы адвентиции аорты, через которые визуализировался стент-графт, из пространства между аортой и протезом отмечалось отделение гнойного содержимого. Стент-графт удалён, сформирован анастомоз между аортой и телом линейного сосудистого протеза. Длительность ИК - 206 минут. Циркуляторный арест с перфузией нижней половины тела и антеградной перфузией головного мозга - 6 минут. Температура тела - 24,1 °C.
В раннем послеоперационном периоде состояние пациента оценено как тяжёлое, проводилась ИВЛ. На вторые сутки была отмечена нестабильная гемодинамика, начата вазопрессорная поддержка. На третьи сутки при рентгенографии визуализированы признаки воспалительной инфильтрации лёгочной ткани с обеих сторон, подъём температуры тела до 39 °C. При отключении седации пациент находился в поверхностном оглушении с элементами энцефалопатии.
На восьмые сутки после оперативного вмешательства при проведении рентгенологического исследования выявлены признаки свободной жидкости в брюшной полости, гастростаза, толсто- и тонкокишечной непроходимости. По жизненным показаниям была проведена лапаротомия, выполнена гастростомия по Штамму-Кадеру. К концу первых суток после оперативного вмешательства при сохранении крайне тяжёлого состояния больного произошла остановка сердечной деятельности с неэффективными реанимационными мероприятиями, констатирована смерть пациента.
При патолого-анатомическом исследовании выявлены признаки сифилитического аортита, сифилитические гранулемы в стенке пищевода в зоне аорто-пищеводного свища. Выявлены следующие признаки позднего третичного сифилиса: сифилитический мезаортит с деструктивным гуммозным поражением, нейросифилис с поперечным миелитом на уровне Th4-L2. Выявлены очаги метаболических повреждений миокарда левого желудочка, что привело к развитию лёгочно-сердечной недостаточности и явилось непосредственной причиной смерти пациента.
ОБСУЖДЕНИЕ
Согласно опубликованным данным в отношении пациентов с аневризмой аорты, образованной в результате осложнённого течения сифилиса, может быть применимо как открытое, так и эндоваскуляр- 189
ное вмешательство. Значимыми факторами в выборе тактики лечения таких больных является размер аневризмы, состояние пациента, в частности особенности гемодинамики, и выраженность иммунной дисфункции [17].
Разрыв аорты является неотложным состоянием. Статистически доказано, что риск летального исхода при такой патологии у пациентов без выраженных нарушений функций иммунной системы приближается к 70% [17]. В ходе семилетнего турецкого исследования были проанализированы данные 116 пациентов с разрывом аневризмы аорты. Две группы пациентов были подверженных либо открытому, либо эндоваскулярному вмешательству. Отмечено, что внутрипросветные методики лечения наиболее подходящи для гемодинамически нестабильных пациентов [17]. Если же обратить внимание на показатели выживаемости пациентов с разрывом аневризмы аорты, ассоциированной с сифилитическим повреждением сосуда, то уровень смертности у них значимо выше.
Стоит отметить, что диаметр аневризмы отмечается многими авторами как один из ключевых факторов риска разрыва аорты. У пациентов с сифилитической аневризмой аорты его значимость повышается в связи с длительным бессимптомным увеличением размеров патологического расширения сосуда. Вместе с этим риск разрыва повышается при сочетании инфекционного заболевания с воздействием стресса, внутрипросветным тромбозом, тонкостью аортальной стенки и метаболическими нарушениями [18, 19]. Многие авторы склоняются к тому, что аневризмы с бессимптомным течением следует оперировать открыто при превышении ими диаметра 5,5 см [20-22].
Как уже было ранее сказано, применение эндоваскулярных методик лечения разрыва аневризмы аорты может применяться и в отношении гемодинамически нестабильных пациентов с верифицированным диагнозом сифилиса. В данном случае выбор такой тактики обусловлен необходимостью более быстрой стаблизации состояния иммуноком-прометированного больного. Европейские клинические рекомендации также содержат рекомендации по выбору эндоваскулярного вмешательства в случае разрыва аневризмы независимо от её генеза [20].
При этом вопрос выбора метода лечения остаётся спорным при рассмотрении особенностей роста сифилитической аневризмы. Её более быстрое увеличение в диаметре становится возможной причиной осложнений у пациентов, прооперированных эндоваскулярно, в позднем послеоперационном периоде. Вместе с этим осложнения невозможно полностью исключить и после открытого вмешательства. Дальнейшее повреждение стенки аорты
-
T. pallidum часто является причиной формирования псевдоаневризм в области проксимального анастомоза [6]. Очевидно, что появление осложнений у обсуждаемой категории пациентов может быть отсрочено при проведении антибиотикотерапии и лечении основного заболевания.
При повторной госпитализации у рассматриваемого пациента отмечено прогрессирующее ухудшение тяжести состояния на фоне инфекционных осложнений и формирования аорто-пищеводного свища. Данное осложнение является редко встречаемым у пациентов, оперированных по поводу аневризмы аорты. Частота его развития равна 7 человек на 1 миллион [23].
Аорто-пищеводные свищи составляют 10% от общего числа патологических сообщений аорты с внутренними органами [24, 25]. Лидирующей причиной формирования свищей, фиксируемой на протяжении более чем 30 лет, является аневризма аорты (более 54%), меньший процент приходится на иные патологические состояния, прежде всего на опухоли с инфильтрирующим ростом (17%) [24, 26]. Безусловно, описываемое осложнение серьёзно и приводит к гибели более 90% пациентов с установленным диагнозом, несмотря на проведение эзофагэктомии и замену стент-графта на протез при выполнении открытого вмешательства [26-28].
Формирование свища сопряжено с наличием инфекционных осложнений у пациентов. По результатам оценки исходов лечения 409 пациентов после эндоваскулярного вмешательства в клиниках Оксфорда, частота системных воспалительных осложнений у таких больных составляет 3,7%. Пациенты, вошедшие в исследуемую группу, находились под наблюдением врачей в течение 11 лет. Отмечено, что сочетание инфекции с соединительнотканными нарушениями или нарушением функций иных органов и систем ведёт к росту летальности с 3,9% до 18,2% в течение 8 лет [29].
Аорто-пищеводный свищ, так же как и аортобронхиальная фистула, являются редко возникающими осложнениями у пациентов, ранее оперированных по поводу аневризмы аорты [30–32]. Частота возникновения патологического сообщения между аортой и пищеводом по данным литературы составляет не более 0,56–2% от общего числа больных с аневризмой аорты [33, 34]. Указанное осложнение чаще всего диагностируется посредством КТ-исследования [24, 27] и проявляется наличием полостей, заполненных воздухом, в аневризматическом мешке, тромбозом полости аневризмы, скоплением жидкости в парааортальном пространстве и последующей компрессией пищевода.
Наиболее частым механизмом формирования аорто-пищеводного свища является развитие некроза стенок сосуда и пищевода, близко приле- 190
жащих друг к другу, по причине действия механического фактора [26]. Ввиду нарушения питания стенки пищевода возникает вторичная эрозия, а также возрастает давление на органы заднего средостения. Начало процесса запускает развитие локального, а позднее и системного воспалительного ответа с формированием ложной аневризмы [28]. В группу риска возникновения описываемого осложнения зачастую относятся пациенты, не получающие на систематической основе гипотензивную терапию при установленной артериальной гипертензии, а также имеющие соединительнотканные дисплазии, в том числе низкой степени выраженности, и сопутствующие инфекционные заболевания [30, 35].
Международными исследованиями отмечено, что частота формирования аорто-пищеводных свищей стала возрастать с развитием эндоваскулярных вмешательств [24, 27, 33]. Выявленная взаимосвязь обусловлена высокими значениями радиальной силы, которую оказывает протез на стенку нативного сосуда. Изменения геометрии дуги аорты и её нисходящей части в данном случае также являются причиной ишемии и формирования вторичных осложнений. Безусловно, формирование фистулы – процесс, требующий времени. Её образование занимает не менее 90 дней, и с большей частотой она возникает у пациентов, которые пренебрегают лечением. Отмеченные взаимосвязи были выявлены в группе из 36 пациентов в возрасте 56-75 лет [33], что не позволяет однозначно судить о полученных выводах и требует дополнительных более крупных исследований.
Единственной признанной тактикой лечения пациентов с аорто-пищеводными свищами является открытое вмешательство. Данный вариант позволяет заменить ранее установленный стент-графт и не допустить дальнейшего распространения инфекции в окружающие ткани. Многие авторы рассматривают ранее установленные протезы как источник бактериальной диссеминации, требующий удаления, в связи с чем эндоваскулярное вмешательство в случае формирования свища не может рассматриваться как верный выбор [36]. Говоря же о тактике лечения разрывов аневризм аорты, стоит отметить, что в данном случае установка стент-графта является бридж-терапией для сохранения жизни пациента до этапа открытого вмешательства.
ВЫВОДЫ
В ходе ретроспективного анализа клинического наблюдения пациента с сифилитической аневризмой нисходящей части грудной аорты изучены вопросы своевременной диагностики сифилиса и его сосудистых осложнений. Рассмотрены наиболее часто применяемые тактики лечения пациентов с сифилитическими аневризмами аорты. Многие ав-
торы опубликованных исследований, посвящённых указанной тематике, склоняются к обязательному сочетанию лабораторных и инструментальных методов диагностики, но при этом не имеют единого мнения относительно типа хирургического вмешательства, которое стоит выполнить.
По-прежнему спорным остаётся вопрос выбора открытого или эндоваскулярного вмешательства для лечения пациентов с сифилитической аневризмой аорты. Каждый из указанных типов имеет ряд рассмотренных выше преимуществ и недостатков. Это, безусловно, говорит о необходимости индивидуального подхода в работе с пациентами с указанной патологией и о потребности постоянного анализа врачом соотношения риска и пользы от выбранного типа операции, исходя из состояния больного.
ЗАКЛЮЧЕНИЕ
Подводя итог вышесказанному, можем отметить, что сосудистые осложнения у пациентов с третичным сифилисом являются редкой, но крайне тяжёлой патологией. Раняя диагностика описываемых осложнений на данный момент – одна из первоочередных задач, стоящих перед профессиональным сообществом. Число пациентов с сифилитическими аневризмами не велико, в сравнении с общим количеством больных с указанной патологией аорты. Однако течение заболевания у них отличается более острым характером и быстрой скоростью прогрессирования от аневризмы больших размеров до формирования патологических сообщений между аортой и пищеводом, бронхами, что неизбежно ведёт к летальному исходу.


