Каррагинаны как новые субстанции для лекарственных средств с радиопротекторным действием
Автор: Подкорытова Елена Алексеевна, Хожаенко Елена Владимировна, Ковалев Валерий Владимирович
Рубрика: Коррекция экологического неблагополучия
Статья в выпуске: 5-2 т.16, 2014 года.
Бесплатный доступ
Каррагинаны - природные полисахариды, получаемые из красных водорослей. Одним из их важнейших биологических свойств является способность связывать ионы металлов. Это свойство позволяет рассматривать каррагинаны как основу для разработки лекарственных препаратов с радиопротекторным действием. Металлсвязывающая активность различных типов каррагинанов была изучена в системах, содержащих ионы стронция или церия. По результатам эксперимента установлено, что k- и i-каррагинаны эффективно связывают ионы стронция и церия, при этом наибольшая активность наблюдалась у i-каррагинана.
Каррагинаны, сорбция, радионуклиды, стронций, церий
Короткий адрес: https://sciup.org/148101814
IDR: 148101814 | УДК: 612.396.11:
Carrageenans as new substances for drugs with radioprotective effect
Carrageenans - the natural polysaccharides received from red seaweed. One of their major biological properties is ability to connect ions of metals. This property allows to consider carrageenans as a basis for development drugs with radioprotective effect. Metals connecting activity of various types of carrageenans was studied in the systems containing ions of strontium or cerium. By results of experiment it is established that k-and i-carrageenans effectively connect ions of strontium and cerium, thus the greatest activity was observed at i-carrageenan.
Текст научной статьи Каррагинаны как новые субстанции для лекарственных средств с радиопротекторным действием
– ферроцианиды, бария сульфат, полисурьмин, цеолиты, комплексообразователи и другие соединения, многие из которых являются довольно токсичными веществами и не предназначены для длительного применения [3, 11, 13]. Это обстоятельство делает актуальным поиск новых безопасных и эффективных средств обеспечения фармакологической защиты человека от воздействия источников внутреннего облучения. В качестве таких перспективных средств защиты могут рассматриваться некоторые некрахмальные полисахариды, так как они не вызывают токсических и выраженных побочных эффектов и при этом обладают достаточной сорбционной емкостью в отношении вышеприведенных металлов [7, 8, 12, 15]. В нашем исследовании использовали полисахариды красных водорослей – каррагинаны. В химическом плане каррагинаны представляют собой сульфатированные галактаны, состоящие из повторяющихся дисахаридных звеньев D-галактозы и ее производных, соединенных регулярно чередующимися β-(1→4)- и α-(1→3)-гликозидными связями. Для каррагинанов характерно большое структурное разнообразие, обусловленное тем, что 4-О-замещенный моносахаридный остаток может быть остатком как галактозы, так и ее 3,6-ангидропроизводного, а гидроксильные группы могут быть сульфатированы [1]. Характерной особенностью каррагинанов является их способность образовывать комплексы с ионами некоторых металлов, при этом катионы металлов взаимодействуют с сульфатными группами соседних участков молекул каррагинана с образованием межмолекулярных «мостиков», за счет которых происходит форми- рование и стабилизация структуры каррагинанового геля [10]. Способность каррагинанов к образованию комплексов с металлами зависит, в первую очередь, от индивидуальных особенностей их структуры. Несмотря на многочисленные работы, посвященные взаимодействию каррагинанов с металлами и проведенные детальные исследования структуры образующихся комплексов, в литературе практически отсутствуют сведения о взаимодействии каррагинанов c радионуклидами [4, 9].
Цель работы: проведение сравнительной оценки связывающей способности разных типов каррагинанов по отношению к ионам стронция и церия.
Материалы и методы. В экспериментальной работе были использованы коммерческие образцы ι-каррагинана (CAS номер 79062 07-1, тип II, Sigma), κ-каррагинана (CAS номер 11114-20-8, тип II, Aldrich), λ-каррагинана (CAS номер 9064-57-7 , тип I, Aldrich). Эти каррагинаны являются линейными полисахаридами, построенными из чередующихся остатков 1,3-связанной α -D-галактопиранозы и 1,4-связанной 3,6-ангидро-β-галактопиранозы и отличаются различным содержанием сульфатных групп. ι-каррагинан и κ-каррагинан относятся к желирующим типам, а λ-каррагинан желирующей способностью не обладает.Хлорид стронция (CAS номер 10476-85-4) и сульфат церия (CAS номер 13590-82-4) были произведены фирмой Aldrich.
Способность каррагинанов связывать ионы стронция и церия in vitro при разных значениях рН среды определялась по схеме, описанной нами ранее для пектинов [7]. Количество связавшихся с каррагинаном ионов металлов вычисляли по формуле:
Q=V(Ci-Cе)/M, где Q – количество ионов стронция или церия, связанных каррагинаном, мг/г; V – общий объем инкубационной смеси, л; Сi – начальная концентрация ионов металла в растворе, мг/л; Сe – равновесная концентрация ионов металла в растворе, мг/л; М – масса каррагинанов, г.
Для изучения кинетики связывания изотопов стронция и церия образцами каррагинанов в емкость, снабженную магнитной мешалкой, вносили 10 мл 0,1 М растворов хлорида стронция или сульфата церия и 10 мл 1,0 М ацетатного буфера со значением рН 4,0. При интенсивном перемешивании добавляли 100 мл 0,5% раствора ι-каррагинана, κ-каррагинана или λ-каррагинана и доводили объем смеси дистиллированной водой до 200 мл. Смесь инкубировали при перемешивании и через заданные промежутки времени отбирали из нее по 20 мл, в отобранной пробе определяли равновесную концентрацию церия или стронция по формуле представленной выше.
Результаты и обсуждение. Графики кинетики связывания каррагинана с ионами металла строили следующим образом: максимальную сорбционную емкость, зарегистрированную в ходе исследования, принимали за 100%, а количество связанных ионов стронция или церия в течение определенного времени инкубации выражали в процентах от максимальной сорбционной емкости. Кинетические кривые связывания стронция каррагинанами различных типов свидетельствуют, что для достижения сорбционного равновесия ι-каррагинану и κ-каррагинану требуется 90 мин и 120 мин соответственно (рис. 1).
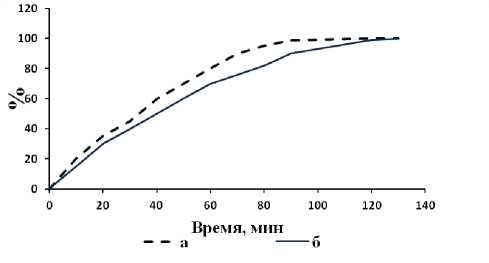
Рис. 1. Кинетика связывания ионов стронция каррагинанами при рН 4,0: а) ι-каррагинан, б) κ -каррагинан
Исследование кинетики сорбции ионов церия показало, что они взаимодействовали с каррагинанами достоверно быстрее, чем ионы стронция. Так, 50%-й уровень сорбции церия для ι -каррагинана, κ -каррагинана достигался через 17-20 мин, а максимальный – через 50-60 мин (рис. 2). Сорбционную активность у λ-каррагинана обнаружить не удалось, поэтому кривые связывания не были построены и показатели сорбционной активности не были рассчитаны.
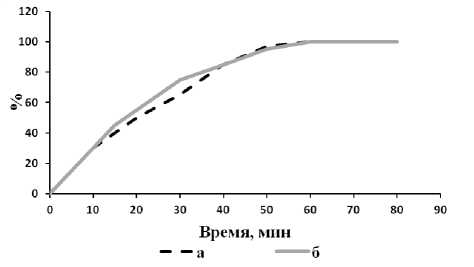
Рис. 2. Кинетика связывания ионов церия каррагинанами при рН 4,0: а) ι-каррагинан, б) κ -каррагинан
На основе экспериментальных данных по связыванию стабильных изотопов стронция и церия образцами каррагинанов были построены изотермы сорбционного равновесия (зависимость сорбции каррагинанами ионов металла от их равновесной концентрации). Форма полученных кривых позволила отнести их к классу изотерм Лэнгмюра. Следовательно, для определения коэффициентов сродства сорбентов к ионам стронция и церия, а также для нахождения максимальной сорбционной емкости исследуемых каррагинанов использовали сорбционную модель Лэнгмюра:
Q=Qmax×b×Ce/1+b×Ce, где Q – связывание стабильных изотопов, мг/г сухой массы каррагинанов; Qmax – максимальное связывание сорбата (церия или стронция) в данных условиях, мг/г каррагинанов; b – коэффициент сродства сорбента к сорбату, л/мг; Се – равновесная концентрация ионов металла в растворе, мг/л. Показатель Qmax является математическим отображением количества активных центров в структуре каррагинанов, которые могут взаимодействовать с молекулами сорбата. Коэффициент сродства (аффинитета) указывает на прочность возникающих связей и скорость образования комплекса сорбент-сорбат.
По результатам экспериментов с ι -каррагинаном не было обнаружено строгой зависимости его связывающей активности от рН среды. Максимум сорбции церия и стронция ι -каррагинаном был зарегистрирован при рН 4,0. При понижении рН до 2,0, а также при ее повышении до 6,0 связывающая активность снижалась незначительно, в целом, оставаясь на высоком уровне (табл. 1, 2). κ -каррагинан выделяется своей способностью активно сорбировать церий и стронций из растворов в диапазоне рН от 2,0 до 4,0, при этом при повышении рН до 6,0 его связывающая активность падала, в среднем, в 1,45 раза.
Таблица 1. Экспериментальные константы Лэнгмюра для связывания ионов стронция различными типами каррагинанов
|
i -каррагинан |
к -каррагинан |
|||||
|
pH 2,0 |
pH 4,0 |
pH 6,0 |
pH 2,0 |
pH 4,0 |
pH 6,0 |
|
|
Q max , мг/г |
40,9±0,8181 |
49,6±0,1489 |
46,5±0,2341 |
40,0±0,6280 |
50,0±0,8982 |
35,0±1,411 |
|
b, л/мг |
0,0263±0,0052 |
0,0633±0,0002 |
0,0548±0,0011 |
0,0172±0,0041 |
0,0430±0,0003 |
0,0074±0,0009 |
|
R2 |
0,995 |
0,999 |
0,996 |
0,998 |
0,997 |
0,988 |
Таким образом, при сорбции стабильных изотопов стронция и церия каррагинанами различных типов не наблюдается такой строгой зависимости от рН среды, как в случае с другими полисахаридами [7, 8]. Сорбционная активность каррагинанов снижается в ряду ι-каррагинан > κ-каррагинан > λ-каррагинан. Более высокие сорбционные характеристики ι-каррагинана в сравнении с κ-каррагинаном позволяют сделать предположение, что с увеличением количества сульфатных групп в молекуле каррагинанов возрастает их сорбционная активность. В то же время содержащий максимальное количество сульфатных групп λ-каррагинан не обладает связывающей активностью. То есть, можно сделать вывод, что образовывать прочные связи с ионами церия и стронция могут только каррагинаны, содержащие ангидрогалактозные звенья и способные в присутствии металлов формировать упорядоченную структуру геля с оптимальным пространственным размещением сульфатных и гидроксильных групп.
Таблица 2. Экспериментальные константы Лэнгмюра для связывания ионов церия различными типами каррагинанов
|
i -каррагинан |
к -каррагинан |
|||||
|
pH 2,0 |
pH 4,0 |
pH 6,0 |
pH 2,0 |
pH 4,0 |
pH 6,0 |
|
|
Q max , мг/г |
107,5±0,7527 |
128,2±0,7692 |
126,5±0,6329 |
90,9±0,5454 |
92,1±0,7272 |
62,5±1,411 |
|
b, л/мг |
0,0848±0,0059 |
0,5591±0,0033 |
0,0320±0,0016 |
0,0152±0,0060 |
0,0301±0,0023 |
0,0513±0,0009 |
|
R2 |
0,999 |
0,997 |
0,999 |
0,998 |
0,994 |
0,996 |
При исследовании влияния рН среды на активность каррагинанов было обнаружено, что ι-каррагинан активно связывает ионы церия и стронция во всем исследованном диапазоне рН среды. Снижение связывающей активности κ-каррагинана при сдвиге рН в щелочную сторону в данном эксперименте труднообъяснимо, особенно принимая во внимание высокую сорбционную активность ι-карраги-нана при тех же условиях и учитывая, что оба каррагинана образуют схожие гелевые структуры. Вместе с тем устойчивость комплексов церия и стронция с ι- и κ-каррагинанами при низких значениях рН может быть связана со стабилизацией данных комплексов за счет дополнительных донорно-акцепторных связей катиона с кислородными атомами галактопираноз-ного кольца и молекулами воды, входящими в структуру комплексов. Наличие таких связей в структуре комплекса металл-карагинан ранее было установлено в работах других авторов, в частности, для кальциевой соли ι-каррагинана [6].
Выводы: ι - и κ -каррагинаны характеризуются способностью прочно и эффективно связывать ионы стронция и церия. Сорбционная активность каррагинанов зависит от их структуры, в том числе от наличия сульфатных групп. ι -каррагинан является наиболее эффективным сорбентом стронция и церия, и может быть использован при создании новых лекарственных препаратов для лечения и профилактики состояний, связанных с поражением радионуклидами.
Работа выполнена в рамках государственного задания Министерства образования и науки РФ, код проекта 413.
Список литературы Каррагинаны как новые субстанции для лекарственных средств с радиопротекторным действием
- Усов, А.И. Проблемы и достижения в структурном анализе сульфатированных полисахаридов красных водорослей//Химия растительного сырья. 2001. №.2. С. 7-20.
- Яблоков, А.В. Миф о безопасности и эффективности мирных подземных ядерных взрывов. -М.: ЦЭПР, 2003. 176 с.
- Ahmadpour, A. Effect of adsorbents and chemical treatments on the removal of strontium from aqueous solutions/A. Ahmadpour, M. Zabihi, M. Tahmasbi, T.R. Bastami//Journal of Hazardous Materials. 2010. Vol. 182 (1-3). P. 552-556.
- Cuppo, F. Non-equilibrium processes of interchain association induced by Cs+ions in κ-carrageenan aqueous solutions/F. Cuppo, H. Reynaers, S. Paoletti et al.//International Journal of Biological Macromolecules. 2004. Vol. 34 (1-2). P. 43-47.
- Imanaka, T. Width and center-axis location of the radioactive plume that passed over Dolon and nearby villages on the occasion of the first USSR A-bomb test in 1949/T. Imanaka, S. Fukutani, M. Yamamoto et al.//Journal of Radiation Research. 2005. Vol. 46 (4). P. 395-399.
- Kara, S. Monovalent and divalent cation effects on phase transitions of i-carrageenan/S. Kara, E. Arda, O. Pekcan//Journal of Bioactive and Compatible Polymers. 2007. Vol. 22 (1). P. 42-61.
- Khotimchenko, M.Y. Cerium binding activity of different pectin compounds in aqueous solutions/M.Y. Khotimchenko, E.A. Kolenchenko, Y.S. Khotimchenko et al.//Colloids and Surfaces B: Biointerfaces. 2010. Vol. 77 (1). P. 104-110.
- Khotimchenko, M.Y. Removal of cesium from aqueous solutions by sodium and calcium alginates/M.Y. Khotimchenko, E.A. Podkorytova, V.V. Kovalev et al.//Journal of Environmental Science and Technology. 2014. Vol. 7 (1). P. 30-43.
- Khotimchenko, Y.S. Carrageenans as a new source of drugs with metal binding properties/Y.S. Khotimchenko, E.V. Khozhaenko, M.Y. Khotimchenko et al.//Marine Drugs. 2010. Vol. 8 (4). P. 1106-1121.
- Lázaro, N. Heavy metal biosorption by gellan gum gel beads/N. Lazaro, A.L. Sevilla, S. Morales, A.M. Marqués//Water research. 2003. Vol. 37 (9). P. 2118-2126.
- Manos, M.J. Layered metal sulfides: exceptionally selective agents for radioactive strontium removal/M.J. Manos, N. Ding, M.G. Kanatzidis//Proceedings of the National Academy of Sciences of the USA. 2008. Vol. 105 (10). P. 3696-3699.
- Nesterenko, V.B. Reducing the 137Cs-load in the organism of “Chernobyl” children with apple-pectin/V.B. Nesterenko, A.V. Nesterenko, V.I. Babenko et al.//Swiss Medical Weekly. 2004. Vol. 134 (1-2). P. 24-27.
- Quinn, K.A. Sorption of yttrium and rare earth elements by amorphous ferric hydroxide: influence of temperature/K.A. Quinn, R.H. Byrne, J. Schijf//Environmental Science and Technology. 2007. Vol. 41 (2). P. 541-546.
- Sakaguchi, A. Radiological situation in the vicinity of Semipalatinsk nuclear test site: Dolon, Mostik, Cheremushka and Budene settlements/A. Sakaguchi, M. Yamamoto, M. Hoshi et al.//Journal of Radiation Research. 2006. Vol. 47 (А). P. A101-A116.
- Wang, M. Adsorption and desorption of Sr(II) ions in the gels based on polysaccharide derivates/M. Wang, L. Xu, J. Peng et al.//Journal of Hazardous Materials. 2009. Vol. 171 (1-3). P. 820-826.


