Кинетические закономерности реакции гексахлорциклотрифосфазатриена с N-оксидом пиридина в смеси органических растворителей в присутствии воды
Автор: Вапиров Владимир Васильевич, Зайцев Дмитрий Олегович
Журнал: Ученые записки Петрозаводского государственного университета @uchzap-petrsu
Рубрика: Физико-математические науки
Статья в выпуске: 6 (151), 2015 года.
Бесплатный доступ
В реакции гексахлорциклотрифосфазатриена (фосфазена) с N-оксидом пиридина в органическом растворителе образуется «ониевая» соль. «Ониевая» соль является промежуточным продуктом в реакции гидролиза фосфазена. Реакция между фосфазеном и N-оксидом пиридина характеризуется первым порядком по фосфазену и N-оксиду. Вода оказывает каталитическое действие на данную реакцию. Каталитическая роль воды заключается в сольватации уходящей группы, что способствует ее более легкому отщеплению.
Фосфазен, химическая кинетика, механизмы реакции
Короткий адрес: https://sciup.org/14750942
IDR: 14750942 | УДК: 547.16:547.823:544.43
Kinetic characteristics of hexachlorocyclotriphosphazatriene and pyridine N-oxide reaction in mixed organic solvents in presence of water
Hexachlorocyclotriphosphazatriene reacts with pyridine N-oxide to form onium salt. This salt is an intermediate product of hexachlorocyclotriphosphazatriene hydrolysis. The reaction is characterized as a first-order reaction with respect to both phosphazene and N-oxide. The water produces a catalytic effect on the investigated process. The catalytic role of the water consists in the solvation of the leaving group, which helps in its disintegration.
Текст научной статьи Кинетические закономерности реакции гексахлорциклотрифосфазатриена с N-оксидом пиридина в смеси органических растворителей в присутствии воды
Циклический тример фосфонитрилхлорида – гексахлорциклотрифосфазатриен (фосфазен) (I) – является наиболее интересным, изучаемым и представляющим наибольшую практическую значимость соединением в ряду циклических фосфонитрилгалогенидов.
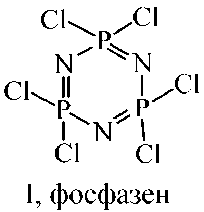
Это соединение может быть достаточно легко синтезировано, к тому же на его основе получен целый ряд производных, которые применяются в различных областях промышленности, физической электронике, медицине и т. д. [1], [3].
Интерес к фосфазену и в настоящее время достаточно широк, о чем свидетельствуют публикации [4], [5], [6], [8], [9], [10].
Преимущественными реакциями фосфазена являются реакции нуклеофильного замещения, которые в зависимости от условий протекают по механизмам SN1 или SN2. Установлено, что реакции замещения с участием высокоосновных нуклеофилов протекают в мягких условиях и практически с количественным выходом. Что же касается реакций фосфазена с низкоосновными нуклеофильными реагентами, то они возможны только в присутствии органических оснований, в качестве которых используются легкодоступные пиридин или триэти-ламин.
В [2] изучены кинетические закономерности реакций фенолиза и гидролиза фосфазена в присутствии триэтиламина и трибутиламина. Установлено, что роль органического основания в этих процессах заключается не только в связывании выделяющегося в ходе реакции хлороводорода, но и в увеличении органическим основанием нуклеофильных свойств субстрата за счет переноса протона. Например, гидролиз (I) в этих условиях протекает по схеме:
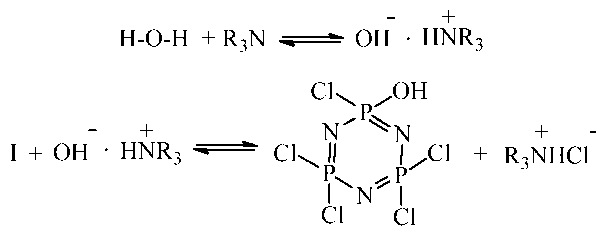
В реакции соединения (I) с пиридином, N-ме-тилимидазолом, диазобициклооктаном и рядом гетероароматических N-оксидов с достаточно высокими выходами выделяются соединения «ониевой» структуры [1], получение которых, на примере N-оксида пиридина, может быть представлено схемой:
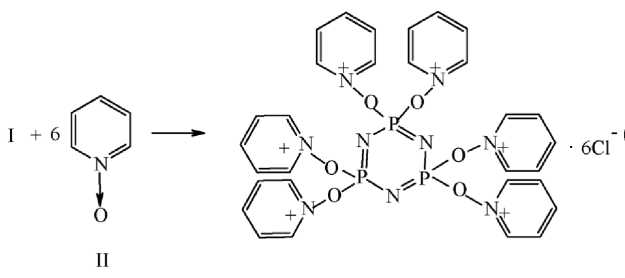
Что же касается стерически затрудненного триэтиламина, то для него неизвестны продукты реакции с соединением (I).
Выделенные и охарактеризованные современными методами физико-химического анализа соединения «ониевой» структуры фосфазена с рядом перечисленных гетероциклических соединений различной основности и N-оксидами пиридинового ряда неоднократно постулировались в качестве промежуточных продуктов в реакциях нуклеофильного замещения галогена в соединении (I). Подтвердить участие этих солей в качестве промежуточных продуктов в реакциях нуклеофильного замещения в соединении (I) оказалось очень сложно, так как выделяемые соли практически нерастворимы в органических растворителях. Оказалось, что единственным растворителем, в котором они растворяются, является вода. Для установления возможного участия «ониевых» солей как промежуточных продуктов в процессе гидролиза нами проведен следующий эксперимент. В раствор фосфазена в ацетонитриле добавлялся раствор N-оксида в этом же растворителе. Динамику процесса оценивали по полосе поглощения N-оксида пиридина. При сливании указанных растворов во времени наблюдается уменьшение полосы поглощения N-оксида, при этом реакция проходит практически до конца. Наиболее вероятным процессом при этом с учетом выделяющихся солей можно считать процесс солеобразования. После дальнейшего добавления в ацетонитрильный раствор избытка воды наблюдается увеличение во времени полосы поглощения N-оксида пиридина. Этот процесс наиболее вероятно связан с гидролизом образующейся соли фосфазена с N-оксидом пиридина (3), в результате чего выделяется N-оксид, который как слабое основание практически не связывает выделяющуюся хлороводородную кислоту в водном растворе.
/=\
^р<0”кС7
N -
II |Х1С1 + Н20---* I + Ц+НС1 (3) С1—р
СГ \N<^ "Cl
ш
Полученные данные свидетельствуют о том, что в реакциях нуклеофильного замещения в фосфазене с участием N-оксида пиридина первоначально образуется соль, которая лежит на координате реакции гидролиза (I) в присутствии N-оксида пиридина.
Ранее в [7] были изучены кинетические закономерности реакций соединения (I) c некоторыми N-оксидами. Эти процессы нашли отражение и в диссертационной работе [1], однако в этих работах не изучалось влияние воды на исследуемый процесс.
Целью настоящего исследования явилось изучение количественных закономерностей реакции фосфазена с N-оксидом пиридина в органическом растворителе в присутствии воды.
Наличие шести реакционных центров в соединении (I) предусматривает возможность замещения шести атомов галогена. Для того чтобы упростить задачу кинетического исследования, нами изучался только процесс монозамещения. В этом случае реакция между фосфазеном и N-оксидом описывается уравнением:
I + II → III (4)
Процесс монозамещения в субстрате обеспечивался условиями проведения реакции, когда концентрация фосфазена на несколько порядков превышала концентрацию N-оксида.
Кинетику расходования N-оксида пиридина проводили в смеси CCl 4 -CH 3 CN (15 об.% CH 3 CN). Такое соотношение растворителей обеспечивало скорость реакции, которая могла легко фиксироваться спектрально. Концентрация воды была в избытке по отношению к N-оксиду, однако соизмерима с концентрацией фосфазена. В общем условия проведения реакции соответствовали следующему соотношению реагентов: [H2O] ≈ [I] > [II].
Контроль за ходом процесса осуществлялся спектрофотометрически по убыли полосы поглощения N-оксида пиридина в области 280 нм. В указанных условиях проведения эксперимента наблюдаемая константа скорости псевдопервого порядка (k набл , с–1) постоянна по ходу процесса (таблица), что указывает на первый порядок реакции по N-оксиду пиридина.
Наблюдаемая константа скорости реакции (с–1), рассчитанная по кинетической кривой «оптическая плотность – время»
|
Время, с |
Оптическая плотность |
k, с–1 |
|
210 |
0,938 |
1,248∙10–4 |
|
510 |
0,906 |
1,252∙10–4 |
|
810 |
0,878 |
1,210∙10–4 |
|
1110 |
0,848 |
1,225∙10–4 |
|
1410 |
0,821 |
1,215∙10–4 |
|
1710 |
0,79 |
1,249∙10–4 |
|
2010 |
0,768 |
1,218∙10–4 |
|
2310 |
0,745 |
1,250∙10–4 |
Зависимость k набл (с–1) от концентрации фосфазена (I) представлена на рис. 1.
Прямая в координатах k набл – [I] исходит из начала координат, что соответствует первому порядку реакции по фосфазену. Первый порядок по фосфазену подтверждается и значением тангенса угла наклона в координатах lg k набл – lg [I].
Было установлено, что наблюдаемая константа скорости псевдопервого порядка также зависит и от концентрации воды. Эта зависимость также
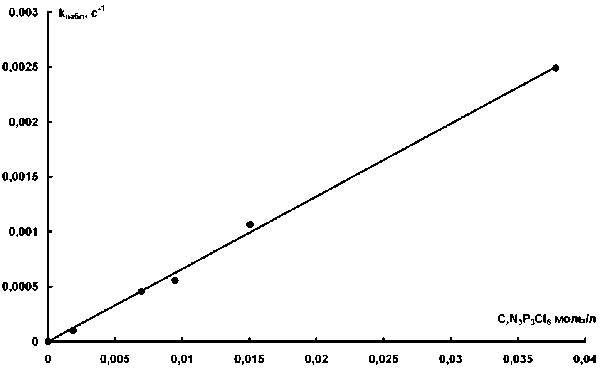
Рис. 1. Зависимость k набл (с–1) от концентрации фосфазена (I) в реакции с N-оксидом пиридина, r = 0,9987
Скорость расходования N-оксида в некаталитической стадии (5) с учетом условий проведения реакции описывается уравнением:
d(II) dt
= k1[I] o [II] t .
Скорость каталитической стадии (7) определяется как:
^
линейна, однако прямая не исходит из начала координат, отсекая на ординате соответствующий отрезок (рис. 2).
dI) = к 1[Цо [П] , [Н20] о . dt
Общее расходование N-оксида в стадиях (5) и (7) равно:
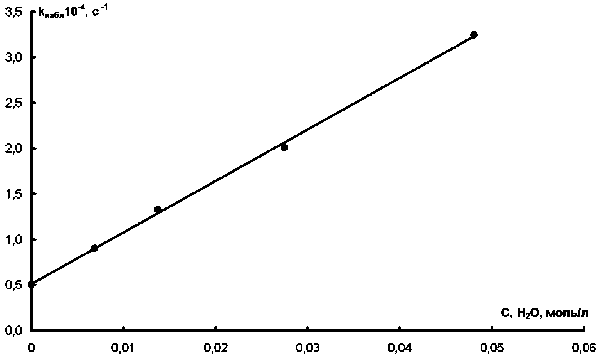
Рис. 2. Зависимость наблюдаемой константы (k набл ) от концентрации воды, r = 0,9992
При этом порядок по воде, определенный по зависимости lg kнабл – lg [H2O], меньше единицы и равен 0,72 ± 0,02.
Постоянство по ходу процесса наблюдаемой константы скорости реакции и в то же время ее зависимость от концентрации воды не могут быть связаны с возможным протеканием процесса гидролиза соли, образующейся на первой стадии (6):
.
Наблюдаемая константа скорости в этом случае определяется уравнением:
к набл = k i [I] o + k2[I] o [H20].
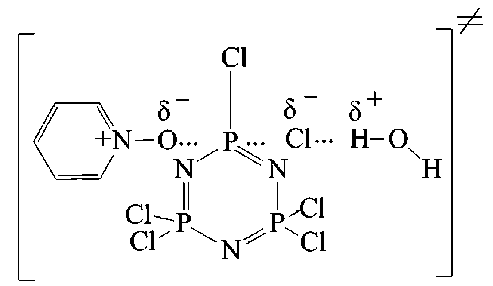
Представленные формально-кинетические закономерности получают объяснение в рамках предложенного механизма, в соответствии с которым наиболее вероятно предположить образование соли по механизму SN2 замещения. Каталитическая роль воды в процессе солеобразования может быть сведена к сольватации уходящей группы в переходном состоянии:
СГ \N^ XC1
Наиболее вероятно зависимость k наб. (c–1) от концентрации воды может быть объяснена протеканием реакции солеобразования по двум потокам – некаталитическому и при каталитическом участии воды:
Таким образом, на основании полученных экспериментальных данных можно считать, что «ониевая» соль фосфазена (I) с N-оксидом пиридина может выступать в роли интермедиата в процессах замещения галогена в фосфазене (I). Этот процесс может осуществляться при каталитическом действии воды. Роль воды может быть сведена к сольватации полярного переходного состояния и облегчению разрыва связи фосфора с уходящим галогеном.
* Статья подготовлена в рамках Программы стратегического развития ПетрГУ на 2012–2016 гг.
KINETIC CHARACTERISTICS OF HEXACHLOROCYCLOTRIPHOSPHAZATRIENE AND PYRIDINE N-OXIDE REACTION IN MIXED ORGANIC SOLVENTS IN PRESENCE OF WATER
Список литературы Кинетические закономерности реакции гексахлорциклотрифосфазатриена с N-оксидом пиридина в смеси органических растворителей в присутствии воды
- Вапиров В. В. Реакционная способность гексахлорциклотрифосфазатриена в реакциях нуклеофильного замещения: Автореф. дисс.. д-ра химич. наук. СПб.; Петрозаводск, 2000. 40 с.
- Вапиров В. В., Зайцев Д. О. Кинетические закономерности гидролиза гексахлорциклотрифосфазатриена в водном ацетонитриле в присутствии триэтиламина//Журнал общей химии. 2006. Т. 67. № 8. С. 1282-1285.
- Олкок Г. Фосфазотистые соединения. М.: Мир, 1976. 563 с.
- Терехов И. В., Филатов С. Н., Орлов А. И., Савельева А. В., Заузина Е. А. Синтез отвердителей фенолформальденидных смол на основе арилоксициклотрифосфазенов//Успехи в химии и химической технологии. 2013. Т. 27. № 3. С. 112-114.
- Терехов И. В., Чистяков Е. М., Филатов С. Н., Дерновая Е. С., Заузина Е. А. Синтез арилоксициклотрифосфазенов с амино-и гидроксогруппами//Успехи в химии и химической технологии. 2012. Т. 26. № 4. C. 106-109.
- Тупиков А. С., Чистяков Е. М., Киреев В. В. Синтез ß-дикетона на основе гекса-параметилкарбоксифеноксициклотрифосфазена//Успехи в химии и химической технологии. 2012. Т. 26. № 4. С. 114-117.
- Шумейко А. Е., Тицкий Г. Д., Вапиров В. В., Курченко Л. П. Исследование кинетики взаимодействия гексахлорциклотрифосфазатриена с 4-метилпиридин-Ы-оксидом//Журнал общей химии. 1987. Т. 57. № 5. С. 1051-1054.
- Allcock H. R., Hartle T. J., Taylor J. P., Sunderland N. J. Organic polymers with cyclophosphazene side groups: influence of the phosphazene on physical properties and thermolysis//Macromolecules. 2001. Vol. 34. № 12. P. 3896-3904.
- Huang Woei-Kae, Yeh Jen-Taut, Chen Kwei-Ju, Chen Kan-Nan. Flame retardation improvement of aqueous-based polyurethane with aziridinyl phosphazene curing system//J. Appl. Polym. Sci. 2001. Vol. 79. № 4. P. 662-673.
- Vaugeois Y., Mazzah A., De Jaeger R., Habimana J. Cyclic phosphonitrilic compounds bearing -N=PCl3 group as homogenous catalyst towards the silanol condensation//Phosph., Sulfur and Silicon and Relat. Elem. 2004. Vol. 179. № 9. P. 1819-1840.


