Клеточные механизмы хронического нейровоспаления
Автор: Сергеева Татьяна Николаевна, Сергеев Валерий Георгиевич, Чучков Виктор Михайлович
Журнал: Морфологические ведомости @morpholetter
Рубрика: Оригинальные исследования
Статья в выпуске: 4 т.22, 2014 года.
Бесплатный доступ
Нейровоспаление, которое рассматривается как ключевое звено патогенеза нейродегенеративных заболеваний, как правило, развивается задолго до гибели нейронов. Для выявления молекулярных и клеточных механизмов, обеспечивающих персистирование нейровоспаления, предшествующее нейродегенерации, мы исследовали отсроченные эффекты однократного введения бактериального эндотоксина (липополисахарида) в область черной субстанции мозга крыс. Через 8 недель, в области введения наблюдалось увеличение количества микроглиоцитов с высокой экспрессией MHC II, и астроцитов, интенсифицирующих экспрессию глиального фибриллярного кислого белка. Ярко выраженная сосудистая реакция сопровождалась индукцией синтеза в клетках стенки кровеносных сосудов фактора некроза опухоли-а, и миграцией лимфоцитов в паренхиму мозга. Полученные результаты обсуждаются с точки зрения системной организации сетевых взаимодействий между описанными клетками.
Нейровоспаление, нейродегенерация, микроглиоциты, астроциты, лимфоциты, перициты
Короткий адрес: https://sciup.org/143177009
IDR: 143177009
Cell mechanisms of chronic neuroinflamation
Neuroinflammation can develop long before the death of neurons. We investigated the deferred effects of a lipopolysaccharide single injection in the rat substantia nigra to identify the molecular and cellular mechanisms of persistent neuroinflammation. After 8 weeks, there was a large number of microglia and astrocytes with high expression of MHC II and glial fibrillary acidic protein, respectively. The observed reaction is accompanied by the induction tumor necrosis factor-а in the walls of blood vessels and migration of lymphocytes into the brain parenchyma. These results are discussed in terms of the systemic organization of the cells network.
Текст научной статьи Клеточные механизмы хронического нейровоспаления
Введение. Нейровоспаление – ключевое звено патогенеза нейродегенеративных заболеваний [1, 2]. Ведущую роль в процессах нейровоспаления играют активированные микроглиоциты [3-7]. Секретируемые ими провоспалительные факторы, такие как цитокины (интерлейкин-1, фактор некроза опухоли-α), монооксид азота, простагландины, специфические протеазы и свободнорадикальные производные кислорода, [8,9] индуцируют окислительный стресс в нейронах, который ведет к их повреждению и гибели.
Экспериментальные и клинические наблюдения свидетельствуют о том, что манифестации многих нейродегенеративных заболеваний, предшествует длительный этап хронического нейровоспаления [10,11] Остается открытым вопрос о молекулярных и клеточных механизмах, обеспечивающих персистирование нейровоспаления в нервной ткани в течение длительного времени. С учетом данных о том, что в процесс нейровоспаления могут быть вовлечены, помимо микроглиоцитов, и другие клетки: астроциты, эндотелио-циты и перициты кровеносных сосудов, а также лимфоциты, мигрирующие в нервную ткань [1214], логично полагать, что в основе хронического нейровоспаления лежат самоподдерживающиеся патофизиологические циклы, обусловленные взаимодействием этих клеток.
Для выявления паттерна активирующихся при хроническом нейровоспалении клеток, и идентификации возможных молекулярных механизмов, лежащих в основе такого рода активации, мы исследовали отсроченные эффекты однократного введения бактериального эндотоксина в область черной субстанции (ЧС) мозга крыс. Выбор этой области представляет интерес с точки зрения исследования патофизиологических процессов, лежащих в основе гибели дофаминергических нейронов и развития болезни Паркинсона.
Цель исследования - выяснить молекулярные и клеточные механизмы персистирующего нейровоспаления в головном мозге крыс.
Материал и методы исследования. Эксперименты проведены на 16 самцах крыс линии Вистар, весом 220 - 300 г., которые содержались в стандартных условиях Все экспериментальные манипуляции осуществлялись в соответствии с международными нормами этического обращения с животными. Крыс наркотизировали диэтиловым эфиром, освобождали поверхность черепа от мягких тканей, и при помощи бормашины высверливали отверстие по координатам: 5,2 мм каудальней брегмы и 2 мм латеральней осевого шва. При помощи стереотаксического аппарата вводили стеклянную микроканюлю с диаметром кончика 100 мкм на глубину 7,2 мм вентральней уровня твердой мозговой оболочки. Инъецировали 2 мкл липополисахарида Escherichia Coli (Sigma, USA) в концентрации 0,01мкг/мкл (8 животных) или 2 мкл стерильного физиологического раствора (8 животных). Через 8 недель животных наркотизировали диэтиловым эфиром, перфузировали через восходящую аорту физиологическим раствором на фосфатном буфере, затем 4% парафармальдегидом, приготовленном на забуференном физиологическом растворе (рН 7,2-7,4). Извлекали мозг, переносили на сутки в 25% раствор сахарозы и замараживали на сухом льду. При помощи криотома (Shandon Cryotom E; Eng) получали серийные срезы мозга толщиной 14 мкм и монтировали их на предметных стеклах Superfrost Plus (Fisher Scientific, USA).
О провоспалительных реакциях нервной ткани судили по результатам рутинного окрашивания срезов крезиловым фиолетовым и иммуногистохимического окрашивания с использованием первичных антител к тирозингидроксилазе (мышинные IgG, 1:2000; SantaCruz), молекулам главного комплекса гистосовместимости второго класса (мышиные IgG, 1:1000; Abcam), глиальному фибриллярному кислому белку (мышиные IgG, 1:1000; SantaCruz), кластеру дифференцировки лимфоцитов (мышиные IgG, 1:1000; Abcam), транскрипционному фактору FoxP3 (мышиные IgG, 1:1000; Abcam), фактору некроза опухоли - α (мышиные IgG, 1:1000; Abcam). Подсчет количества меченых клеток в ЧС производили при помощи флуоресцентного микроскопа Nikon Eclipse E200, совмещенного с цифровой камерой MicroPublisher 3,0 (USA), и компьютерной программы ImagePro Insight 8.0 (Media Сybernetics, USA). Результаты исследований проверяли на нормальность распределения значений с помощью W-теста Шапиро-Вилкоксона. Сравнение выборок проводили с помощью t- критерия Стьюдента. Различия считали достоверными при уровне статистической значимости P < 0,05. Результаты представляли, как M±m (среднее ± стандартное отклонение). Статистический анализ проводили в компьютерной программе Statistiсa 10.0.
Результаты исследования и их обсуждение. Через 8 недель после однократной инъекции ЛПС в область ЧС мы не обнаруживали в ней па- дения количества дофаминергических нейронов, но наблюдали целый ряд морфофункциональных изменений, свидетельствующих о наличии нейровоспалительного процесса. На срезах, окрашенных крезиловым фиолетовым, область введения ЛПС отличалась выраженной сосудистой реакцией (рис.1) и цитозом, наблюдаемым как в ретикулярной (ЧСр), так и компактной (ЧСк) части черной субстанции. Кровеносные сосуды имели увеличенный диаметр; в просвете сосудов и в непосредственной близости от них локализовались в большом количестве небольшие клетки с округлым ядром и узким ободком цитоплазмы, фенотип которых был схож с лимфоцитарным.
Иммуногистохимическое исследование срезов с использованием антител против молекул МНС II продемонстрировало увеличение в ЧС количества микроглиоцитов, интенсивно экспрессирующих этот маркер (+178,2±24,2%), относительно животных, которым в ЧС вводился стерильный физраствор. Введение ЛПС приводило также к значительному увеличению количества клеток, интенсивно экспрессирующих глиальный фибриллярный кислый белок (+255,2±43,2%), что свидетельствовало о реактивном астроглиозе, сохраняющемся в нервной ткани через 8 недель после однократной инъекции бактериального эндотоксина.
В клетках стенки кровеносных сосудов и периваскулярной области ЧС экспериментальных животных выявлялись клетки, интенсивно синтезирующие фактор некроза опухоли (ФНО-α). Иммунореактивные клетки в стенке сосудов имели вытянутую форму с отростками, преимущественно ориентированными по окружности сосуда. Такая форма и тот факт, что они не контактировали с внутренним просветом сосуда, позволили предположить, что данные клетки могли быть перицитами. Известно, что перициты в ответ на инфицирование, стимуляцию ЛПС и цитокинами способны синтезировать хемокины и провоспалительные цитокины, в том числе ФНО-α [15, 16].
Особенно интересным представляется обнаружение вокруг сосудов клеток с высокой экспрессией ФНО-α, фенотип которых был схож с микроглиоцитарным. Как известно, активированные микроглиоциты, способны синтезировать наряду с другими провоспалительными цитокинами и ФНО-α [17]. Расположение в непосредственной близости друг от друга вышеописанных клеток позволяет говорить о наличии взаимных стимулирующих влияний, опосредуемых прово-спалительными цитокинами.
Сосудистая реакция, индукция синтеза ФНО-α клетками стенки кровеносных сосудов, и значительное усиление интенсивности свечения иммунореактивного глиального фибриллярного
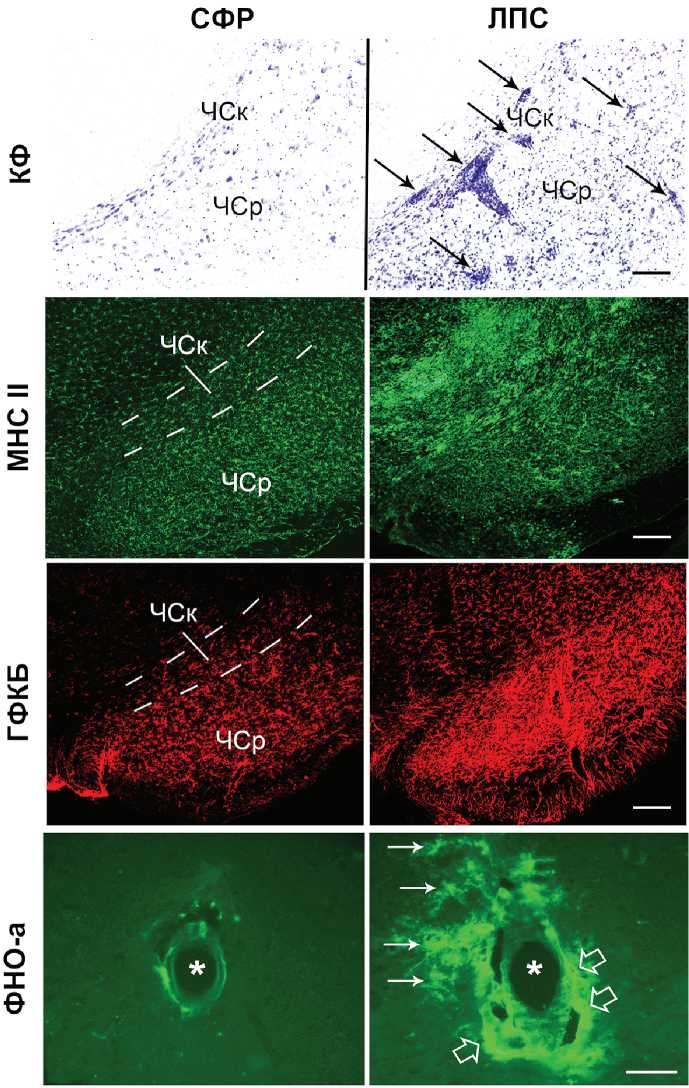
Рис. 1. Морфофункциональные изменения черной субстанции головного мозга крыс через 8 недель после введения в нее стерильного физиологического раствора (СФР) и липополисахарида (ЛПС). На срезах, окрашенных крезиловым фиолетовым (КФ), стрелками выделены расширенные сосуды, содержащие большое количество клеток с лимфоцитарным фенотипом. Иммуногистохимическое мечение свидетельствует об увеличении количества и интенсивности экспрессии иммунопозитив-ного сигнала в клетах, иммунореактивных к молекулам главного комплекса гистосовместимости (МНС II) и глиальному фибриллярному кислому белку (ГФКБ) после введения ЛПС. Эндотоксин индуцирует синтез фактора некроза опухоли-α (ФНО-α) в клетках микроглиоцитарного (тонкие стрелки) и перицитарного (контурные крупные стрелки) фенотипа. Обозначения: ЧСк – компактная часть черной субстанции; ЧСр – ретикулярная часть черной субстанции; звездочки – просвет кровеносных сосудов. Длина линии для КФ = 200 мкм; для МНС II и ГФКБ = 220 мкм; для ФНО-α = 100 мкм.
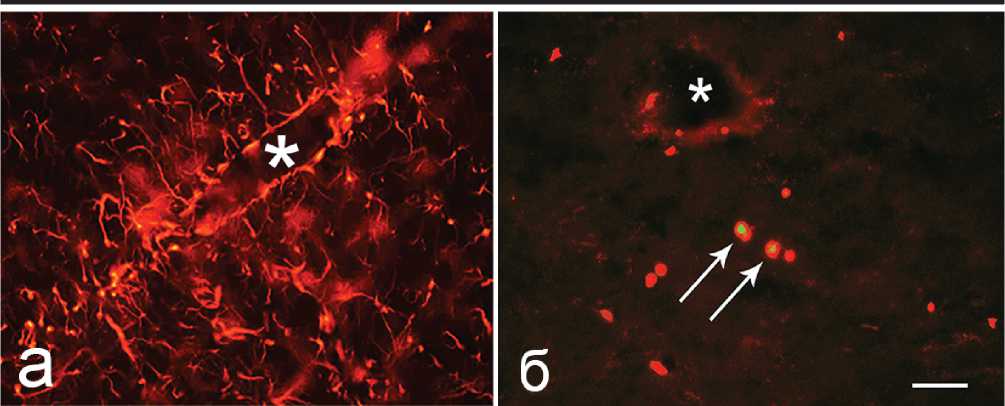
Рис. 2. Экспрессия иммунореактивного глиального фибриллярного кислого белка в астроцитарных отростках, контактирующих с кровеносными сосудами (а), и двойное иммуногистохимическое мечение клеток, экспрессирующих лимфоцитарный маркер CD3 (красное окрашивание) и FoxP3 (зеленое окрашивание) в черной субстанции через 8 недель после введения ЛПС. Стрелками обозначены клетки с двойной меткой. звездочками - просветы сосудов. Длина линии = 100 мкм.
кислого белка в отростках астроглиоцитов, образующих своеобразную муфту вокруг сосудов (рис. 2а), позволило предположить, что в описываемых экспериментальных условиях повышается проницаемость гематоэнцефалического барьера. В пользу этого свидетельствовало наличие клеток, экспрессирующих лимфоцитарный маркер (CD3) не только в просвете сосудов, но и паренхиме нервной ткани (Рис. 2б). Ранее исследователями было показано, что микроглиальная активация в повреждаемых областях мозга ведет к локальному повышению пропускной способности ГЭБ и инфильтрации в эти области лимфоцитов [18]. Недавние исследования показали, что, в свою очередь, инфильтрирующие нервную ткань T-лимфоциты оказывают стимулирующее воздействие на микроглиоциты, усиливая нейровоспаление и нейродегенерацию [19].
Вместе с тем, двойное иммуногистохимическое мечение позволило нам выявить в ядрах части лимфоцитов, мигрировавших в нервную ткань, транскрипционный фактор FoxP3 (Рис.2б), являющийся маркером регуляторной популяции лимфоцитов (Трег), активность которых, как свидетельствуют данные литературы, направлена на ингибирование воспалительного процесса. Ранее было показано, что Трег способны мигрировать в область повреждения и через прямое взаимодействие с локальной глией, снижать нейровоспаление и, таким образом, оказывать нейропротекцию. В частности, Трег могут супрессировать опосредованное микроглиоцитами нейровоспаление посредством снижения производства в них ре- активных форм кислорода и активности NF-κB, а также индуцировать Fas-FasL-опосредованный апоптоз активированных микроглиоцитов [20].
Таким образом, полученные результаты позволяют сделать вывод о том, что однократное введение ЛПС в ЧС, индуцирует в этой области персистирующее нейровоспаление, в которое вовлекаются перициты, микроглиоциты, астроциты и, мигрирующие в нервную ткань лимфоциты. Наличие описанных в литературе прямых межклеточных контактов и дистантной паракринной регуляции между ними, позволяет рассматривать совокупность клеток, участвующих в реакциях на действие повреждающего фактора как функциональную систему (которую мы предлагаем обозначить как нейроглиоваскулярная единица). Активность такой микросистемы изначально направлена на обеспечение защиты нейронов в условиях угрозы их повреждения и гибели. Однако наличие большого количества петель обратной связи между элементами нейроглиоваскуляр-ной единицы (рис. 3) ведет к персистированию воспалительного процесса в ней, даже после однократной стимуляции. Такое провоспалителное состояние может служить предрасполагающим фактором для инициации гибели нейронов при дополнительном воздействии внешних повреждающих факторов. Становится очевидным, что поиск новых подходов к терапии нейродегенеративных заболеваний должен базироватся на рассмотрении в качестве терапевтической мишени не отдельных клеток, а интегральной нейроглиова-скулярной системы.
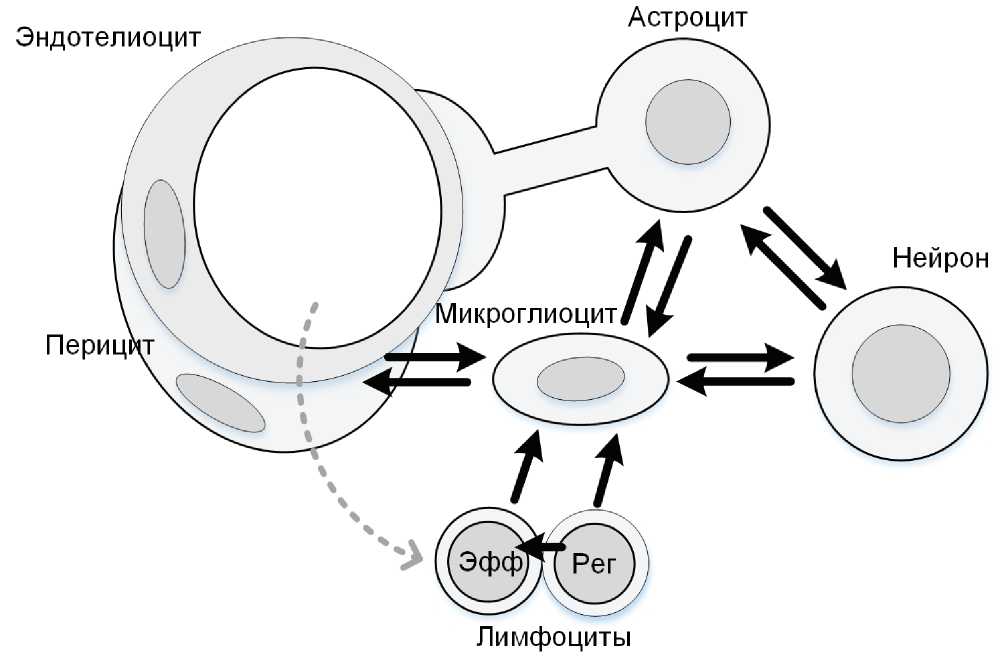
Рис. 3. Схема взаимодействий клеток, формирующих нейроглиоваскулярную единицу.
Заключение. Через 8 недель после однократного введения ЛПС в ЧС, в ней отсутствуют признаки выраженной нейродегенерации, но обнаруживаются признаки нейровоспаления: астро-цитоз и микроглиоцитоз, повышенная экспрессия этими клетками, соответственно, молекул МHC II и глиального фибриллярного кислого белка, индукция синтеза в стенке кровеносных сосудов фактора некроза опухоли - α, и интенсивная миграция в нервную ткань лимфоцитов. Хронический характер нейровоспаления, вызванный однократной инъекцией ЛПС, свидетельствует о наличии в изучаемой области мозга самоподдерживающе-гося патофизиологического механизма активации, основанного на взаимодействии этих клеток.
Список литературы Клеточные механизмы хронического нейровоспаления
- Vivekanantham S., Shah S., Dewji R., Dewji A., Khatri C., Ologunde R. Neuroinflamation in Parkinson's disease: role in neurodegeneration and tissue repair //Int J Neurosci. 2014. Vol.3. P. 1-17.
- Ellwardt E., Zipp F. Molecular mechanisms linking neuroinflammation and neurodegeneration in MS// Exp Neurol. 2014. Vol.262. P.8-17
- Orr C.F., Rowe D.B., Halliday G.M. An inflammatory review of Parkinson 's disease // Prog Neurobiol. 2002. Vol. 68, №5. Р.325-340.
- McGeer P.L., McGeer E.G. Glial reactions in Parkinson's disease // Mov Disord. 2008. Vol.23, №4. P. 474-483.
- Gao H.M., Hong J.S. Why neurodegenerative diseases are progressive: uncontrolled inflammation drives disease progression // Trends Immunol. 2008. Vol.29, №8. Р.357-365.
- Hirsch E.C., Hunot S. Neuroinflammation in Parkinson's disease: a target for neuroprotection? // Lancet Neurol. 2009. Vol. 8, №4. Р.382-397.
- Griffin W.S. Inflammation and neurodegenerative diseases // Am J Clin Nutr. 2006. Vol.83, №2. P. 470-474.
- Jha M.K., Suk K. Management of glia-mediated neuroinflammation and related patents // Recent Pat Inflamm Allergy Drug Discov. 2014. Vol.8, №2. P. 118-124.
- Suk K. Glial proteins and peptides: implications in neuroinflammation // Curr Protein Pept Sci. 2013. Vol.14, №1. P.2-10.
- Majde J.A. Neuroinflammation resulting from covert brain invasion by common viruses - a potential role in local and global neurodegeneration // Med Hypotheses. 2010. Vol.75,№2. P.204-213.
- Lyman M., Lloyd D.G., Ji X., Vizcaychipi M.P., Ma D. Neuroinflammation: the role and consequences // Neurosci Res. 2014. Vol.79. P. 1-12.
- Niranjan R. The role of inflammatory and oxidative stress mechanisms in the pathogenesis of Parkinson's disease: focus on astrocytes //Mol Neurobiol. 2014. Vol.49,№1. P.28-38.
- Monahan A.J., Warren M., Carvey P.M. Neuroinflammation and peripheral immune infiltration in Parkinson's disease: an autoimmune hypothesis // Cell Transplant. 2008. Vol.17,№4. P.363-372.
- Winkler E.A., Bell R.D., Zlokovic B.V. Central nervous system pericytes in health and disease // Nat Neurosci. 2011. Vol.11, P. 1398-1405.
- Alcendor D.J., Charest A.M., Zhu W.Q., Vigil H.E., Knobel S.M Infection and upregulation of proinflammatory cytokines in human brain vascular pericytes by human cytomegalovirus // J Neuroinflammation. 2012. Vol.9, P.95-104.
- Jansson D., Rustenhoven J., Feng S., Hurley D., Oldfield R.L., Bergin P.S., Mee E.W., Faull R.L., Dragunow M. A role for human brain pericytes in neuroinflammation // J Neuroinflammation. 2014. Vol.11, P.104-112.
- Gayle D.A., Ling Z., Tong C., Landers T., Lipton J.W., Carvey P.M. Lipopolysaccharide (LPS)-induced dopamine cell loss in culture: roles of tumor necrosis factor-alpha, interleukin-1beta, and nitric oxide // Brain Res Dev Brain Res. 2002. Vol.133, №1. P. 27-35.
- Racke M.K., Ratts R.B., Arredondo L., Perrin P.J., Lovett-Racke A. The role of costimulation in autoimmune demyelination//J Neuroimmunol. 2000. Vol.107, №2. P. 205-215.
- Brochard V., Combadiere B., Prigent A., Laouar Y., Perrin A., Beray-Berthat V., Bonduelle O., Alvarez-Fischer D., Callebert J., Launay J.M., Duyckaerts C., Flavell R.A., Hirsch E.C., Hunot S. Infiltration of CD4 lymphocytes into the brain contributes to neurodegeneration in a mouse model of Parkinson disease // J Clin Invest. 2009. Vol.119, P. 182-192.
- Reynolds A. D., Banerjee R., Liu J., Gendelman H.E., Mosley R.L. Neuroprotective activities of CD4 CD25 regulatory T cells in an animal model of Parkinson's disease// J Leukoc Biol. 2007. Vol. 82, №5. P. 1083-1094.


