Клиническая и электромиографическая характеристики нейромышечного статуса у недоношенных детей
Автор: Зарипова Юлия Рафаэльевна, Мейгал Александр Юрьевич
Журнал: Ученые записки Петрозаводского государственного университета @uchzap-petrsu
Рубрика: Медицинские науки
Статья в выпуске: 8 (129) т.2, 2012 года.
Бесплатный доступ
При помощи клинических и электромиографических критериев охарактеризован нейромышечный статус у недоношенных детей в течение первых 6 недель жизни. В ходе клинического осмотра выявлена положительная динамика неврологического статуса. Установлено, что у недоношенных детей в первые 6 недель постнатального периода интерференционная электромиограмма (иЭМГ) имеет сходство с иЭМГ доношенного новорожденного первых дней жизни и характеризуется «упрощенной» временной структурой, низкой амплитудой и частотой, замедленной динамикой параметров ЭМГ.
Недоношенные дети, нейромышечный статус, электромиография, нелинейные и линейные параметры
Короткий адрес: https://sciup.org/14750289
IDR: 14750289 | УДК: 612.741.16:612.65+612.648
Clinical and electromyographic characteristics of neuromuscular status in preterm children
Clinical and electromyographic criteria were used to characterize neuromuscular status of the preterm children within first 6 weeks of their life. Clinical examination revealed improvement of their neurological status during that time. It was found that in the preterm children interference electromyogram (iEMG) in the first 6 postnatal weeks is highly similar by EMG parameters with the term children right after birth. Namely, it is characterized by “simplified” temporal structure, low amplitude, and frequency, and by retarded dynamics of EMG parameters
Текст научной статьи Клиническая и электромиографическая характеристики нейромышечного статуса у недоношенных детей
Достижения неонатальной медицины в последние десятилетия привели к значительному повышению выживаемости недоношенных детей с очень низкой (ОНМТ) и экстремально низкой массой тела (ЭНМТ). Кроме того, в связи с переходом РФ с 01.01.2012 на новые критерии живорождения, рекомендованные ВОЗ (срок гестации более 22 недель, масса тела ≥ 500 г), количество недоношенных детей будет неуклонно расти [4].
Выхаживание новорожденных, особенно не-доношеных детей, послужило стимулом для развития новых направлений в различных областях медицины (нутрициологии, фармакологии, дальнейшее совершенствование офтальмологии, кардиологии, хирургии, сурдологии и т. д.). С другой стороны, наряду с совершенствованием различных направлений неотложной неонатальной помощи активно развиваются мультидисципли-нарные службы, направленные на реабилитацию и абилитацию недоношенных детей и их семей.
Особенностями недоношенного ребенка являются: диффузная мышечная гипотония («поза лягушки»), быстрая «истощаемость» рефлексов, низкая мышечная масса, малоподвижность и лабильность температуры тела вследствие относительной пойкилотермности [5]. Однако основные показатели моторного развития новорожденного ребенка имеют существенные временные колебания. Очевидно, что имеет место большое различие между морфологическими и физиологическими показателями нервной системы у детей разного гестационного возраста.
Вследствие этого клиницист должен владеть не только различными методиками неврологического осмотра новорожденных детей [8], [10], но и иметь углубленные знания по эволюционной неврологии.
Развитие технологий выхаживания преждевременно родившихся детей позволяет повышать их выживание и улучшать качество жизни. Однако, несмотря на создание для недоношенного ребенка оптимальных условий выхаживания, полностью ограничить его от воздействия внешних факторов невозможно, и поэтому темпы его развития будут, вероятнее всего, быстрее по сравнению с его сверстниками, находящимися еще в утробе матери. Вследствие этого при постнатальной оценке психомоторного и физического развития ребенка, родившегося преждевременно, обычно учитывается не биологический возраст после рождения, как у доношенных детей, а его постконцептуальный (ПКВ), или постменструальный, возраст, то есть возраст с момента зачатия [7], [10], [11].
Настоящая работа посвящена оценке неврологического статуса недоношенного ребенка на различных сроках постконцептуального развития с позиции онтогенетической адаптации.
Из экспериментальных исследований H. F. R. Prechtl известно, что двигательная активность является первичной по отношению к другим формам неврологической деятельности плода и младенца [3], [6]. Таким образом, именно клиническая и нейрофизиологическая оценка моторной функции младенца явилась приоритетной в данном исследовании.
Цель работы – исследовать нейромышечный статус недоношенных детей с помощью схем неврологического осмотра недоношенного ребенка: схема качественной и количественной оценки недоношенных детей в соответствии с их ПКВ (Пальчик А. Б., 2008) и новых параметров иЭМГ.
МЕТОДИКА
В группу недоношенных вошли 10 детей обоего пола низкой степени риска с гестационным возрастом 31/32 недели, средняя масса при рождении составила 1650 ± 105 г, средняя оценка по шкале Апгар – 6/7 баллов. Под низкой степенью риска подразумевается отсутствие серьезных отклонений в соматическом и неврологическом статусе ребенка. Их обследование проводилось в динамике на 2, 4 и 6-й неделе жизни (фактически в 33, 35, 37 недель посконцептуального возраста, то есть количество недель беременности + возраст после рождения в неделях). Группу контроля составили 10 доношенных детей обоего пола, родившихся в срок (38/39 недель гестации) с нормальной оценкой по шкале Апгар (8/9 баллов), средней массой тела 3430 ± 90 г, обследованных также в возрасте 2, 4 и 6 недель после рождения. Общий дизайн исследования представлен на рис. 1.
Доношенные дети (n=10) Р/38-39
0 40 42 44

Недоношенные 0 2 4 6
Постнатальный возраст

0 33 35 37
Р/31-32
Постконцептуальный возраст
Рис. 1. Общий дизайн исследования и группы обследованных детей: Р – срок рождения (гестационный возраст в неделях), черные стрелки указывают соответствие постнатального возраста у доношенных и недоношенных детей;
0 – концепция. Пунктиром обозначен неисследованный возраст у недоношенных детей
Дети обследовались в ГБУЗ «Детская республиканская больница» (Петрозаводск), с информированного согласия мамы ребенка, с разрешения Этического комитета при Минздравсоцразвития РК.
Для объективизации полученных данных клинический неврологический осмотр проводился с помощью схем неврологического осмотра недоношенного ребенка в 33 и 35 недель ПКВ, предложенных А. Б. Пальчиком в 2008 году [3]. Общая сводная схема включает в себя 40 показателей: рефлекторный ответ на прикосновение, вздрагивание (страртл-реакция), генерализованные движения (generalized movements), изолированные движения руки и ноги, ретрофлексия голо- вы, поворот головы, нерегулярные дыхательные движения и т. д. [3]. Оценка детей в 33 недели ПКВ проводилась по 36 показателям, в 35 и 37 недель – по всем 40 показателям (дополнительно проводилась оценка шагового рефлекса, рефлекса опоры, рефлекса Бабинского, асимметричного шейно-тонического рефлекса). Каждому показателю присваивался балл от 0 до 1,0. Интерпретация теста проводилась по сумме баллов: максимальный показатель (100 %) – 35,5 балла в 33 недели ПКВ и 37,5 балла в 35, 37 недель ПКВ, оптимальный показатель (> 90 %) – ≥ 32 балла в 33 недели и ≥ 34 балла в 35, 37 недель ПКВ, нормальный показатель (> 75 %) – ≥ 26,5 балла в 33 недели и ≥ 28 балла в 35, 37 недель ПКВ. Доношенные дети обследовались неврологически по общепринятой в отечественной неонатологической практике схеме [6]. Исследование проводилось стандартизированно с учетом окружающих условий (температурный режим), состояния обследуемого ребенка, времени после кормления.
Для регистрации иЭМГ использовали поверхностные биполярные электроды фирмы «Нейрософт» (Иваново, Россия). Усиление миоэлектрического сигнала проводили с помощью электромиографов Нейро-МВП-4 и Нейро-МВП-Микро (ООО «Нейрософт», Иваново, Россия). Запись электромиограммы производили последовательно с 4 мышц верхних и нижних конечностей (трехглавой мышцы плеча и двуглавой мышцы плеча справа; икроножной мышцы и передней большеберцовой мышцы слева) на жесткий диск для последующей обработки. Частота опроса аналого-цифрового преобразователя (АЦП) – 20 КГц, полоса пропускания сигнала – 2–1000 Гц.
С учетом того что в практику электромиографии включаются нелинейные методы обработки сигнала [9], [12], [14], нами использованы традиционные линейные и новые нелинейные методы обработки иЭМГ.
Нелинейный анализ иЭМГ (FRACTAN 4.4 ©) включал в себя измерение таких параметров, как: 1) фрактальная размерность ( D ), 2) корреляционная размерность ( Dc ), 3) корреляционная энтропия ( K2 ).
В линейном анализе иЭМГ использованы средняя амплитуда (A, мкВ) и средняя частота (MNF, Гц) [2].
Исследование детей проводилось между кормлениями, во время спонтанной двигательной активности и со строгим соблюдением теплового режима. Дети в 33 недели ПКВ обследовались непосредственно в боксе в условиях кувеза (температура воздуха 32 ºС, влажность 40 %). Наложение электродов и регистрация спонтанной или вызванной двигательной активности производились через окошки и дверцы инкубатора. Температура тела контролировалась с помощью накожного датчика сервоконтроля.
В 35 и 37 недель гестационного возраста дети обследовались на пеленальном столике на фоне частичного распеленания, при температуре воздуха 24–25 ºС и низкой постоянной скорости движения воздуха (0,1 м/с). Доношенные новорожденные дети обследованы в кабинете электрофизиологической диагностики на кушетке после предварительного распеленания или раздевания (1–2-минутная адаптация ребенка в развернутом виде), при температуре воздуха 24–25 ºС и постоянной скорости движения воздуха (0.1 м/с).
Статистическая обработка проведена с использованием программы Excel 2003 и SPSS 12.0™ и Statgraphics Centurion 15.0. Для определения межгрупповых различий (возрастных групп и разных групп детей) использовали W-критерий (Крускалла – Уоллиса) и U-критерий (Манна – Уитни).
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Клиническая оценка недоношенных детей по схеме неврологического осмотра выявила следующие особенности. В 33 недели ПКВ оптимальный показатель развития (≥ 32 баллов) был у 2 (20 %) детей, нормальный показатель развития (≥ 26,5 балла) – у 8 (80 %) (рис. 2). Очаговая симптоматика не отмечена. Асимметрия мышечного тонуса верхних конечностей отмечена у одного ребенка (10 %), нижних конечностей – у 3 (30 %) детей.
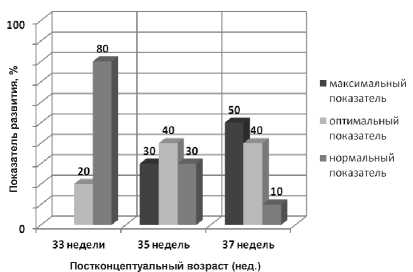
Рис. 2. Показатель неврологического развития у недоношенных детей в 33, 35, 37 недель постконцептуального развития: максимальный показатель – 100 % баллов, оптимальный – > 90 % баллов, нормальный – > 75 % баллов
В 35 недель ПКВ получен максимальный показатель развития у 3 (30 %) детей, оптимальный – у 4 (40 %), нормальный – у 3 (30 %) новорожденных (рис. 2). Очаговая симптоматика отсутствовала. Асимметрия мышечного тонуса в ногах была выявлена у одного ребенка (10 %).
В 37 недель ПКВ максимальный показатель развития был у 5 (50 %) детей, оптимальный – у 4 (40 %), нормальный – у одного (10 %) ребенка (рис. 2). Очаговая симптоматика отсутствовала. Асимметрия мышечного тонуса в ногах была выявлена у одного ребенка (10 %).
Неврологический статус в группе контроля не выявил существенных особенностей в динамике. Необходимо отметить, что в возрасте 2 не- дель у 3 детей (30 %) была отмечена асимметрия мышечного тонуса верхних конечностей, в 4 недели – у 2 (20 %).
Полученные клинические данные у недоношенных детей свидетельствуют об улучшении показателей неврологического развития по мере созревания ребенка. Подобная онтогенетическая динамика очевидна именно у недоношенных детей по сравнению со своими доношенными сверстниками, что свидетельствует о большей уязвимости данной категории детей и потребности в максимально адаптированных к материнской утробе условиях выхаживания постнатально.
Результаты поверхностной ЭМГ были следующими.
У недоношенных детей в возрасте 33 недель фрактальная размерность ( D ) иЭМГ варьировала от 1,5 до 1,64, корреляционная размерность ( Dc ) и корреляционная энтропия ( K2 ) – от 4,0 до 5,0 в мышцах как верхних, так и нижних конечностей (табл. 1). Эти значения были достоверно меньше по сравнению с аналогичными параметрами у доношенных детей, у которых D была в пределах от 1,74 до 1,85, а Dc и K2 достигали значений от 6,4 до 9,9.
Средняя частота спектра иЭМГ составила у 2-недельных недоношенных детей от 166 до 185 Гц, а максимальная средняя амплитуда – от 130 до 173 мкВ (табл. 2). У здоровых доношенных новорожденных данные показатели были значительно выше: от 184 до 238 Гц и от 181 до 230 мкВ (табл. 2).
У недоношенных детей в течение всех 4 недель обследования нелинейные параметры характеризовались медленным увеличением к 37-й неделе гестационного возраста (то есть к 6-й неделе жизни) (табл. 1). У доношенных детей подобной динамики не наблюдалось и значения всех нелинейных параметров оставались высокими на протяжении всего периода обследования (табл. 1).
У недоношенных детей в течение первых 6 недель жизни амплитуда и частота иЭМГ практически не изменялись, за исключением средней максимальной амплитуды в m. triceps brachii dextra , для которой было характерно повышение до 160–300 мкВ (табл. 2).
В нашем исследовании более низкие значения всех нелинейных параметров, которые были отмечены для недоношенных детей, характеризуют их электромиографический сигнал как «менее сложный», «более регулярный» и «более предсказуемый». Это означает, что сигнал иЭМГ генерируется меньшим количеством уравнений, то есть меньшим количеством нейронных ансамблей [5]. Вследствие недостаточной интерференции меньшего количества генераторов на иЭМГ возникают ритмы (кластеризация иЭМГ), которые визуально не всегда заметны. Появление этих ритмов и приводит к упрощению иЭМГ и ее большей предсказуемости.
Таблица 1
Показатели корреляционной размерности ( Dc ), корреляционной энтропии ( K2 ) и фрактальной размерности ( D ) в зависимости от гестационного и постнатального возраста в разных мышцах новорожденного ребенка
|
Мышца |
Недоношенные дети, постконцептуальный возраст (нед.) |
Доношенные дети, постнатальный возраст (нед.) |
||||
|
33 |
35 |
37 |
2 |
4 |
6 |
|
Корреляционная размерность (Dc)
|
m. triceps br. |
4,86 ± 0,51 |
5,12 ± 0,28 |
5,3 ± 0,28* |
6,45 ± 2,52 |
7,46 ± 2,12* |
6,42 ± 1,4 |
|
m. biceps br. |
4,42 ± 0,37 |
5,26 ± 0,56 |
5,27 ± 0,33* |
7,63 ± 1,82*** |
7,08 ± 1,13** |
6,26 ± 2,16** |
|
m. gastrocnemius |
5,09 ± 0,75 |
4,67 ± 0,18 |
4,84 ± 0,23 |
7,52 ± 0,64 |
7,51 ± 2,96*** |
8,37 ± 1,34* |
|
m.tibialis ant. |
4,96 ± 0,33 |
5,08 ± 0,33 |
4,93 ± 0,33* |
7,41 ± 1,86 |
7,03 ± 0,45*** |
7,4 ± 0,61* |
Корреляционная энтропия (К2)
|
m. triceps br. |
4,35 ± 0,21 |
4,26 ± 0,14 |
4,19 ± 0,27 |
9,96 ± 1,04*** |
9,49 ± 0,55 |
9,12 ± 0,19* |
|
m. biceps br. |
4,77 ± 0,33 |
4,5 ± 0,05 |
4,78 ± 1,00 |
9,81 ± 1,02*** |
7,01 ± 0,96 |
7,47 ± 1,65 |
|
m. gastrocnemius |
4,46 ± 0,16 |
4,82 ± 0,65* |
4,71 ± 0,49* |
9,99 ± 1,71*** |
9,03 ± 0,73*** |
9,67 ± 0,38** |
|
m. tibialis ant. |
4,21 ± 0,57 |
3,85 ± 0,3 |
3,87 ± 0,33 |
9,37 ± 1,82** |
9,22 ± 0,61** |
9,01 ± 1,58** |
Фрактальная размерность (D)
|
m. triceps br. |
1,59 ± 0,51 |
1,54 ± 0,09 |
1,66 ± 0,08 |
1,85 ± 0,1 |
1,74 ± 0,09 |
1,81 ± 0,14* |
|
m. biceps br. |
1,64 ± 0,09 |
1,62 ± 0,09 |
1,63 ± 0,09 |
1,74 ± 0,05*** |
1,79 ± 0,03 |
1,80 ± 0,04* |
|
m. gastrocnemius |
1,49 ± 0,07 |
1,49 ± 0,07 |
1,56 ± 0,07*** |
1,74 ± 0,11*** |
1,81 ± 0,07*** |
1,78 ± 0,07* |
|
m. tibialis ant. |
1,49 ± 0,05 |
1,51 ± 0,06 |
1,87 ± 1,09 |
1,81 ± 0,16*** |
1,79 ± 0,03 |
1,72 ± 0,15 |
Примечание. * – р < 0,05, ** – p < 0,01, *** – p < 0,001 при сравнении детей с 33 неделями гестационного возраста с детьми 35, 37 недель постменструального возраста и 2, 4, 6-недельными доношенными детьми.
Таблица 2
Средняя частота спектра и средняя максимальная амплитуда (мкВ) иЭМГ в зависимости от постнатального возраста в разных мышцах ребенка в первые 6 недель жизни (M ± SD, недели)
|
Мышца |
Недоношенные дети (нед.) |
Доношенные дети (нед.) |
||||
|
2 |
4 |
6 |
2 |
4 |
6 |
|
Средняя частота спектра
|
m. biceps br. |
166,35 ± 32,68 |
180,63 ± 45,03 |
163,88 ± 29,63 |
218,4 ± 90,99 |
177,08 ± 48,03 |
202,57 ± 73,71 |
|
m. triceps br. |
185,35 ± 27,29 |
179,74 ± 34,54# |
153,8 ± 41,4# |
226,02 ± 48,47** |
211,24 ± 78,05### |
265,84 ± 73,71### |
|
m. gastrocnem. |
182,32 ± 21,05 |
188,39 ± 48,46 |
183,87 ± 45,82 |
237,55 ± 39,99 |
217,43 ± 28,32*** |
261,21 ± 71,78***# |
|
m. tibialis ant. |
171,12 ± 31,19 |
163,46 ± 47,15 |
150,41 ± 25,27# |
184,39 ± 50,14*** |
195,78 ± 36,51 |
262,9 ± 124,9*** |
Средняя максимальная амплитуда, мкВ
|
m. biceps br. |
153,67 ± 53,1 |
162,0 ± 49,0 |
144,67 ± 11,9 |
180,75 ± 22,49*** |
205,0 ± 23,4*** |
195,25 ± 43,51 |
|
m. triceps br. |
146,67 ± 30 |
169,93 ± 18,0 |
233,0 ± 76,13# |
187,75 ± 35,4*** |
315,67 ± 131,4** |
213,75 ± 51,6*** |
|
m. gastrocnem. |
129,67 ± 29,57 |
133,33 ± 4,04 |
134,0 ± 9,0 |
190,5 ± 42,1*** |
216,0 ± 80,85 |
157,75 ± 16,8***### |
|
m. tibialis ant. |
173,0 ± 96,17 |
179,33 ± 48,0 |
176 ± 19,69 |
230,5 ± 69,59** |
220,33 ± 74,07*** |
226,0 ± 41,53*** |
Примечание. * – р < 0,05, ** – p < 0,01, *** – p < 0,001 при межгрупповом сравнении с детьми 2 недель жизни; # – р < 0,05, ## – p < 0,01, ### – p < 0,001 при внутригрупповом сравнении с детьми 2 недель жизни.
На протяжении 6-недельного постнатального периода иЭМГ недоношенного ребенка имеет сходство с таковой доношенного новорожденного первых дней жизни и характеризуется «упрощенной» временной структурой и низкой амплитудой и частотой спектра. В отличие от доношенного новорожденного, у недоношенного ребенка динамика параметров иЭМГ замедлена. С точки зрения динамики систем это может быть следствием меньшего по сравнению со «сложным» сигналом количества нервных центров или уровней, участвующих в генерации сигнала, а также снижения количества связей между центрами (индекса кластеризации) [13]. Известно, что при увеличении числа генераторов их работа в основном асинхронна, и как следствие этого – система производит более сложный сигнал. Таким образом, у недоношенных детей начиная с 2-недельного возраста, вероятно, меньше связей между элементами нервной системы на уровнях ЦНС и большая синхронизация активности двигательных единиц.
Значения всех нелинейных параметров в группе контроля (доношенные дети) достаточно большие уже к концу 2-й недели ( D ≈ 1,80, Dc и K2 ~ 6,0–9,0) и далее практически не изменяются. Это свидетельствует о том, что у 2-недельного доношенного ребенка формируется иЭМГ, уже вполне «зрелая» с точки зрения временной организации нейронного генератора, сопоставимая с иЭМГ взрослого человека.
Мы предполагаем, что резкое увеличение значений нелинейных параметров иЭМГ у доношенных детей в течение первых 2 недель после рождения является следствием перехода из внутриутробной во внеутробную среду. Основ- ными факторами новой среды являются резкое исчезновение иммерсии, которая, как показано, может являться аналогом микрогравитации [1], и более низкая температура.
Очевидно, что из-за более короткого пребывания во внутриутробном состоянии двигательная система недоношенного ребенка менее зрелая и подготовленная к внеутробной жизни. Поэтому названные выше новые факторы среды для недоношенных детей являются даже более агрессивными. Это свидетельствует о том, что при работе с недоношенными детьми нужно особое внимание уделять именно вопросам выхаживания.
Полученные нами данные могут быть использованы для прогнозирования состояния двигательной системы недоношенного ребенка в будущем, в том числе в отдаленном (через несколько лет), как это делается по методу Prechtle с помощью видеомониторинга движений [3].
ВЫВОДЫ
В настоящей работе апробирована схема неврологического осмотра недоношенного ребенка с разным ПКВ (А. Б. Пальчик, 2008). Полученные клинические данные позволили качественно и количественно оценить психомоторный статус обследуемых детей. Результаты ЭМГ исследования нейромышечного статуса свидетельствуют о чувствительности метода у детей различного гестационного возраста и позволяют объективизировать и дополнить данные клинического осмотра.
Нам представляется перспективным обследовать детей с еще меньшей массой тела при рождении, а также в течение двух недель после рождения.
* Работа выполнена при поддержке Программы стратегического развития (ПСР) ПетрГУ в рамках реализации комплекса мероприятий по развитию научно-исследовательской деятельности на 2012–2016 гг.
Список литературы Клиническая и электромиографическая характеристики нейромышечного статуса у недоношенных детей
- Мейгал А. Ю. Онтогенетическая модель гравитации и невесомости: теоретические и практические аспекты//Физиология человека. 2011. Т. 37. № 6. С. 130-138.
- Меклер А. А. Применение аппарата нелинейного анализа динамических систем для обработки сигналов ЭЭГ//Вестник новых медицинских технологий. 2007. Т. 14. № 1. С. 73.
- Пальчик А. Б., Федорова Л. А., Понятишин А. Е. Неврология недоношенных детей. М.: МЕДпресс-информ, 2010. 352 с.
- Приказ Минздравсоцразвития России № 1687н от 27 декабря 2011 г.
- Федер Е. Фракталы: Пер. с англ. М.: Мир, 1991. 254 с.
- Шабалов Н. П. Неонатология. Т. II. СПб.: Специальная литература, 2004. 608 с.
- Bollard J. L., Kazmaier K., Driver M. A. A simplified assessment of gestational age//Pediatr. Res. 1977. Vol. 11. P. 374.
- Dubowitz L. M. S., Dubowitz V., Mercuri E. The neurological assessment of the pre-term and full-term infant. Clinics in Developmental Medicine, № 148. London: MacKeith Press, 1999. 155 p.
- Farina D., Merletti R., Enoka R. M. The extraction of neural strategies from the surface EMG//J. Appl. Physiol. 2003. Vol. 96. P. 1486-1495.
- Gosselin J., Amiel-Tison C. Evaluation neurologique de la naissance à 6 ans. Presses de l’Hôpital Sainte-Justine. Montréal; Paris: Masson, 2007.
- Grenier A. La motricité libérée du nouveau-né. Paris: Médecine et enfance, 2000.
- Meigal A., Rissanen S., Tarvainen M. et al. Linear and nonlinear tremor acceleration characteristics in patients with Parkinson’s disease//Physiol. Measur. 2012. Vol. 33. P. 395-412.
- Stam C. J. Nonlinear dynamical analysis of EEG and MEG: Review of an emerging field//Clinical Neurophysiology. 2005. Vol. 116. P. 226-2301.
- Sung P. S., Zurcher U., Kaufman M. Comparison of spectral and entropic measures for surface electromyography time series: a pilot study//J. Rehabil. Res. and Dev. 2007. Vol. 44. P. 599-610.


