Клинические, гемодинамические и метаболические эффекты, влияние на микроциркуляцию комбинированной терапии небиволола с индапамидом у больных ишемической дисфункцией сердца, отягощенной сахарным диабетом 2-го типа
Автор: Горюцкий В.Н., Тепляков А.Т., Лукинов А.В., Кузнецова А.В., Улятовский В.А.
Журнал: Сибирский журнал клинической и экспериментальной медицины @cardiotomsk
Рубрика: Клинические исследования
Статья в выпуске: 1 т.24, 2009 года.
Бесплатный доступ
У 38 больных ишемической болезнью сердца (ИБС), ассоциированной с сахарным диабетом (СД) 2-го типа, в течение 12 недель оценивалась клиникогемодинамическая и антиишемическая эффективность комбинированной терапии кардиоселективным β1-блокатором третьего поколения небивололом («БерлинХеми/Менарини Фарма ГмбХ») с NO-модулирующей активностью с нейтральным диуретиком индапамидом (фирма «МАКИЗ-ФАРМА», Москва), а также влияние на состояние углеводного и липидного обменов. По результатам исследования через 12 недель терапии отмечались статистически значимые гипотензивный и антиишемический эффекты комбинации препаратов. Наблюдалось уменьшение уровня постпрандиальной гликемии и атерогенной дислипидемии. Отмечался явный кардио- и вазопротективный эффект. На фоне улучшения показателей микроциркуляции и регресса индекса массы миокарда улучшалась диастолическая функция левого желудочка.
Ибс, сд 2-го типа, небиволол, индапамид, антиишемические эффекты, микроциркуляция
Короткий адрес: https://sciup.org/14918997
IDR: 14918997 | УДК: 615.217.03:616-005.4-06:616.379-008-64
Clinical, hemodynamic and metabolic effects, influence of microcirculation on combined therapy of nebivolol with indapamid in patients having cardiac ischemic dysfunction associated with the 2-nd type diabetes mellitus
Clinical-hemodynamic and anti-ischemic activity of combined therapy of cardioselective ?1-blocker of the third generation nebivolol (Berlin-Chemie/Menarini Pharma GmbH) having NO-modulating activity with neutral diuretics indapamid (Firm ?Makiz-Pharma?, Moscow) and influence of carbohydrate and lipid exchange were assessed in 38 CAD patients associated with the diabetes mellitus of the 2-nd type. Significant hypertensive and anti-ischemic effects of the combined drugs were noted 12 weeks after. Decreased level of postprandial glycemia and atherogenous dislipidaemia was observed. Marked cardiac-and vasoprotective effects were noted. In the setting of improved microcirculation indices and myocardial mass index regress, left ventricular diastolic function was improved.
Текст научной статьи Клинические, гемодинамические и метаболические эффекты, влияние на микроциркуляцию комбинированной терапии небиволола с индапамидом у больных ишемической дисфункцией сердца, отягощенной сахарным диабетом 2-го типа
Сахарный диабет (СД) признан экспертами ВОЗ неинфекционной эпидемией и представляет собой серьезную медико-социальную проблему. Согласно данным И.И. Дедова, 5% населения России (8 млн. человек) страдают СД, из них 90% – СД 2-го типа [1]. Артериальная гипертензия (АГ) встречается примерно у 80% больных СД 2-го типа. Сочетание этих двух взаимосвязанных патологий ассоциируется со значительным увеличением процента преждевременной инвалидизации и смерти больных от сердечно-сосудистых осложнений. При СД 2-го типа без сопутствующей АГ риск развития ишемической болезни сердца (ИБС) и инсульта повышается в 2-3 раза. При присоединении к СД АГ риск этих осложнений возрастает еще в 2-3 раза даже при удовлетворительном контроле метаболических нарушений [2]. Следовательно, коррекция артериального давления (АД) является первостепенной задачей в лечении больных СД. В последние годы при изучении пато-20
генеза ангиопатий при СД и АГ инициирующая роль в нарушении тонуса и развитии последующих атеросклеротических изменений сосудов принадлежит дисфункции эндотелия, а именно дефициту эндоте-лийзависимого вазорелаксирующего фактора (оксида азота). Оксид азота (NO) вследствие своих ауто- и паракринных функций является универсальным ан-гиопротективным веществом, которое регулирует периферическое сопротивление, АД и распределение кровотока в сосудистой сети. Помимо механизма, опосредованного активацией растворимой цГМФ, NO также регулирует базальный тонус системных, коронарных и легочных сосудов за счет ингибирования синтеза эндотелиального констрикторного фактора эндотелина-1 и ограничения высвобождения норадреналина из симпатических нервных окончаний [3-6]. NO оказывает прямое отрицательное инотропное действие на сократимость миокарда, а также регулирует реакцию кардиомиоцитов на адренергические стимулы [7, 8]. NO тормозит пролиферацию гладкомышечных клеток, за счет чего он оказывает антиатеросклеротическое действие, поскольку замедляет образование неоинтимы и утолщение стенок сосудов при гиперхолестеринемии [9]. NO обладает противовоспалительными свойствами, связанными с его способностью ингибировать синтез и экспрессию цитокинов, а также молекул адгезии, которые привлекают моноциты к эндотелиальной поверхности и облегчают их проникновение в сосудистую стенку, инициируя атеросклеротический процесс. NO тормозит агрегацию и адгезию тромбоцитов [10]. Таким образом, лечение и эффективная вторичная профилактика больных ИБС в сочетании с АГ на фоне СД 2-го типа должны быть направлены не только на адекватное снижение АД, но и по возможности на коррекцию дисфункции эндотелия (ангиопротекцию) с целью предотвращения отдаленных сердечно-сосудистых осложнений, улучшения качества жизни и снижения риска летальности.
В то же время монотерапия у данной категории пациентов не всегда позволяет достигнуть целевых значений АД, адекватного антиишемического эф- фекта. Как правило, таким пациентам требуется комбинированная терапия с применением препаратов, являющихся «метаболически нейтральными» [11]. Одним из основных механизмов развития АГ при МС и СД является гиперволемия, возникающая вследствие повышенной реабсорбции натрия и воды в проксимальных отделах почечных канальцев на фоне гиперинсулинемии. Поэтому применение диуретиков нового поколения с нейтральными метаболическими эффектами является патогенетически обоснованным [12]. В этом отношении большой интерес представляет диуретический препарат индапамид.
Целью нашего исследования была оценка клинических, гемодинамических и метаболических эффектов длительного (12 недель) применения нового кар-диоселективного 3 1 -блокатора третьего поколения небиволола с NO-модулирующей активностью в комбинации с индапамидом у больных ИБС, отягощенной СД 2-го типа.
МАТЕРИАЛ И МЕТОДЫ
Проведено открытое клинически контролируемое исследование антиишемической и антигипертензивной эффективности, безопасности суперселективного З 1 -адреноблокатора небиволола (неби-лет, «Берлин-Хеми/Менарини Фарма ГмбХ», Германия) в комбинации с нейтральным диуретиком индапамидом (фирма «МАКИЗ-ФАРМА», Москва) у больных ИБС, отягощенной СД 2-го типа.
В исследование включено 38 пациентов с СД 2-го типа (28 мужчин, 10 женщин) в среднем возрасте 57,6±8,1 лет. К моменту обследования в 9 (23,7%) случаях диагностировалась стабильная стенокардия напряжения II ФК, у 24 (63,2%) – III ФК, у 5 (13,2%) – прогрессирующая стенокардия. В среднем стаж ИБС составил 5,3±2,7 лет. Почти у половины – 18 (47,4%) обследованных регистрировались рубцовые изменения на ЭКГ как следствие перенесенного крупноочагового ИМ давностью более 6 мес. По поводу стенозирующего коронарного атеросклероза в 8 (21,1%) случаях выполнена хирургическая реваскуляризация сердца давностью 27,4±3,2 мес и у 7 (18,4%) больных – эндоваскулярная реваскуляризация давностью 16,3±5,8 мес. У всех больных ИБС регистрировалась АГ I-II степени длительностью 15,3±10,7 года.
Все пациенты, включенные в исследование, имели повышенную массу тела (ИМТ 31,2±4,9 кг/м2). Избыточная масса тела диагностировалась у 17 (44,7%) больных, ожирение I степени – у 12 (31,6%), II степени – у 7 (18,4%), III степени – у 2 (5,3%) больных. Объем талии (ОТ) – 104±13,7 см; ОТ/ОБ у женщин составил 0,87±0,1, у мужчин – 0,97±0,3, что отражало преобладание абдоминального типа ожирения у отобранной группы.
Показатели углеводного обмена (в частности базальная гипергликемия в пределах 6,9±0,4 ммоль/л и постпрандиальная гипергликемия – 10,5±0,8 ммоль/л)
в группе исследованных пациентов свидетельствовали об умеренной декомпенсации СД. Для коррекции гипергликемии пациенты принимали пероральные сахароснижающие препараты (ПССП) из группы сульфаниламидов или комбинации сульфаниламидов и бигуанидов. Дозы ПССП корректировались эндокринологом на старте и оставались неизменными в течение всего исследования при отсутствии гипогликемических реакций.
Показатели артериального давления соответствовали умеренной форме АГ. Средний уровень систолического АД исходно достигал 158,2±8,1 мм рт. ст., диастолического АД – 93,8±3,8 мм рт. ст.
У больных имела место гиперхолестеринемия – исходный уровень общего холестерина (ОХ) составлял 6,2±1,1 ммоль/л, гипертриглицеридемия – 2,9±0,35 ммоль/л. Уровень антиатерогенных липопротеидов высокой плотности (ЛПВП) соответствовал нижней границе нормы 0,96±0,05 ммоль/л. Отмечалось увеличение уровня атерогенных липопротеидов низкой плотности (ЛПНП) 4,05±0,8 ммоль/л.
По результатам стратификации сердечно-сосудистого риска по шкале «SCORE» отобранные в исследование пациенты характеризовались высокой (21% больных) и очень высокой (79% больных) степенью риска развития неблагоприятных сердечнососудистых событий.
В соответствии с протоколом исследования в проспективное наблюдение не включали больных с мозговыми сосудистыми осложнениями (ишемическими атаками, мозговыми инсультами) АГ давностью менее 12 мес или крупноочаговым инфарктом миокарда (ИМ) давностью менее 6 мес, тяжелой ХСН (IV ФК по NYHA), с брадиаритмиями, нарушениями АВ-проводимости более II степени, бронхиальной астмой, периферическим атеросклерозом с синдромом Лериша, а также пациентов, имевших противопоказания к назначению З-адреноблокато-ров и индапамида.
Все пациенты дали свое письменное информированное согласие на участие в исследовании. Клиникодемографическая характеристика пациентов представлена в табл. 1.
Препараты назначались после отмены предшествующего лечения (включавшего З-адреноблокаторы, антиаритмические средства, периферические вазодилататоры, антагонисты кальция, иАПФ) после 5-дневного периода «отмывания». Допускался сублингвальный прием короткодействующих форм нитроглицерина. При подъемах АД допускался прием коринфара в дозе 10 мг.
После выполнения предусмотренных протоколом исследований всем больным путем индивидуального титрования дозы назначался небиволол в сочетании с индапамидом. Начальная суточная доза небиволола составляла 2,5 мг с последующим увеличением до 5 мг и при необходимости (для достижения целевого гипотензивного эффекта) до 10 мг/сут.
Таблица 1
Клинико-демографическая характеристика больных
|
Критерии |
Количество пациентов |
% отношение |
|
Всего больных |
38 |
100 |
|
Пол: – мужчины – женщины |
28 10 |
73,7 26,3 |
|
Возраст, годы |
57,6±8,1 |
|
|
Стаж ИБС, годы |
5,3±2,7 |
|
|
Стенокардия напряжения: II ФК III ФК |
9 24 |
23,7 63,2 |
|
ФК ХСН (по NYHA): I-II ФК III ФК |
33 5 |
86,8 13,2 |
|
Нестабильная стенокардия |
5 |
13,2 |
|
Перенесенный инфаркт миокарда, в т.ч. Q-ИМ |
18 |
47,4 |
|
Перенесенный повторный ИМ |
7 |
18,4 |
|
Постинфарктная аневризма ЛЖ |
3 |
7,9 |
|
Коронарография: Гемодинамически значимые стенозы (≥50% диаметра) КА стеноз 1 КА стеноз 2 КА стеноз 3 КА |
30 8 7 15 |
78,9 21,1 18,4 39,4 |
|
Артериальная гипертензия I-II степени |
38 |
100 |
|
Стаж ГБ, годы |
15,3±10,7 |
|
|
ЖЭС высоких градаций (по Lown B. и Wolff W.) |
8 |
21,1 |
|
Пароксизмальная форма ФП |
5 |
13,2 |
|
Сахарный диабет 2-го типа легкой и средней степени тяжести |
38 |
100 |
|
Стаж СД 2-го типа, годы |
7,4±3,8 |
|
|
Гиперхолестеринемия > 5,6 ммоль/л |
38 |
100 |
|
Курение |
9 |
23,7 |
|
Стаж курения, годы |
27,6±7,3 |
|
|
Абдоминальное ожирение: Избыточная масса тела I степени II степени III степени |
38 17 12 7 2 |
100 44,7 31,6 18,4 5,3 |
|
АКШ+МКШ |
8 |
21,1 |
|
Стентирование КА |
7 |
18,4 |
|
Предшествующая терапия: аспирин пролонгированные нитраты ингибиторы АПФ ^-адреноблокаторы антагонисты кальция |
38 7 16 12 11 |
100 18,4 42,1 31,6 28,9 |
Примечание. ФК – функциональный класс; ХСН – хроническая сердечная недостаточность; ИМ – инфаркт миокарда; КА – коронарные артерии; ФП – фибрилляция предсердий; СД – сахарный диабет; АКШ и МКШ – аорто- и маммарокоронарное шунтирование; АПФ – ангио-тензинпревращающий фермент.
Независимо от дозы небиволола все пациенты получали индапамид в суточной дозе 1,5 мг/сут. Продолжительность курсовой терапии составила 12 недель.
На контрольных визитах (один раз в месяц) проводился комплексный клинический осмотр больных с определением АД, ЧСС, веса, объема талии и бедер, уровня базальной и постпрандиальной гликемии, фиксировались возможные эпизоды гипогликемии, а также любые побочные медицинские события и изменения в сопутствующей медикаментозной терапии. Индивидуальную переносимость препарата оценивали по результатам опроса больного о развитии побочных явлений, их характере и времени возникновения в процессе лечения.
Переносимость препарата расценивали как хорошую при отсутствии побочных эффектов, как удовлетворительную – при возникновении преходящих побочных эффектов, не требовавших отмены препарата, как неудовлетворительную – при появлении побочных эффектов, потребовавших отмены препарата.
Влияние на антиишемические кардио-протективные, гемодинамические и метаболические эффекты, а также на клиническое течение ИБС и безопасность 12недельной курсовой комбинированной терапии небивололом с индапамидом оценивали по динамике клинических проявлений коронарной недостаточности, регрессу суточной частоты и тяжести стенокардии, суточной потребности в нитроглицерине, динамики увеличения физической толерантности (ТФН), тесту 6-минутной ходьбы. Качество жизни оценивали посредством Миннесотского опросника «Жизнь с сердечной недостаточностью» (Minnesota Living Heart Failure Questionnaire – MLHFQ) [13].
Антигипертензивная эффективность проводимой терапии изучалась на основании данных суточного мониторирования АД (аппарат Astrocard, Санкт-Петербург). Суточное мониторирование артериального давления (СМАД) проводили по стандартной методике в течение 24 часов [14]. Анализировали следующие показатели: средние дневные (д) и ночные (н) значения систолического и диастолического артериального давления, их вариабельность (стандартное отклонение от средней величины), суточный индекс САД и ДАД (разница между средним дневным АД и средним ночным АД, отнесенная к среднему дневному АД и выраженная в процентах), индекс времени дневной и ночной систолической и диастолической гипертензии (процент измерения АД, превышавшего 140/90 мм рт. ст. в период бодрствования, и 120/80 мм рт. ст. в период сна). Результаты считали статистически значимыми, если при автоматической обработке было исключено не более 20% измерений. Использовали следующие критерии антигипертензивной эффективности: «очень хорошая» – снижение среднего АД (АДср) более чем на 15% от исходного; «хорошая» – при снижении его более чем на 10%, но менее 15%; «удовлетворительная» – менее чем на 10%, но более чем на 5%; «малоэффективная» – снижение АДср менее чем на 5%.
В зависимости от величины суточного индекса выделяли следующие группы больных: «Dipper» – СИ составляет 10-22%, «Non-dipper» – СИ менее 10%, «Over-dipper» – СИ более 22%, «Night-peakег» – СИ с отрицательными значениями.
Верхними границами нормы вариабельности считали САДд – 15,5 мм рт. ст., ДАДд – 13,3 мм рт. ст., САДн – 14,8 мм рт. ст., ДАДн – 11,3 мм рт. ст. Вариабельность считали повышенной, если она превышала хотя бы одно из указанных значений.
Влияние проводимой курсовой терапии на структуру левого желудочка (ЛЖ) и состояние внутрисердечной гемодинамики оценивали методом эхокардиографии (ЭхоКГ) с допплеровским анализом трансмитрального кровотока на аппарате «Aloka SSD-5500 SV» (Япония), Ultramark. 9 (ATL, США). Определяли следующие морфометрические параметры ЛЖ: конечные диастолический и систолический объемы, ударный объем, толщину задней стенки ЛЖ (ЗС ЛЖ, мм) и межжелудочковой перегородки (МЖП ЛЖ, мм) в диастолу. Оценивалась масса миокарда ЛЖ (ММ ЛЖ, г), индекс ММ ЛЖ (ИММ ЛЖ, г/м2). О гипертрофии левого желудочка (ГЛЖ) судили по критерию ИММ ЛЖ более 120 г/м2.
Диастолическую функцию ЛЖ оценивали по соотношению трансмитральных потоков Е/А, где Е – максимальная скорость раннего диастолического потока, А – максимальная скорость потока предсердной систолы. Диастолическое наполнение считали нормальным при значениях Е/А более 1; диастолической дисфункции по типу нарушения релаксации соответствовало Е/А менее 1; рестриктивному типу – Е/А более 2.
Метаболическую эффективность препарата оценивали по динамике в крови значений липидного спектра, уровня глюкозы натощак и постпрандиаль-ной гликемии.
Физическая толерантность оценивалась исходно в контрольном периоде, затем по окончанию 12-недельной курсовой терапии. Велоэргометрия проводилась на эргометре «Siemens-Elema». Использовалась непрерывно ступенчато возраставшая пороговая нагрузка. Пробу начинали с нагрузки 25 Вт, которую увеличивали на 25 Вт каждые 5 минут.
Микроциркуляция исследовалась посредством лазерной допплеровской флоуметрии (ЛДФ) на аппарате фирмы «Transonic System Inc.» (США). Исследование проводилось в положении сидя с расположением предплечья на уровне сердца. Датчик располагался в области наружной поверхности правого предплечья в точке, находящейся по срединной линии на 3-4 см выше основания шиловидных отростков локтевой и лучевой костей. Температура воздуха в помещении при проведении измерений варьировала в пределах 20-22°С. В исследовании анализировались данные исходной регистрации ЛДФ, показатели окклюзионной и дыхательной проб. При выполнении окклюзионной пробы оценивался показатель микроциркуляции (ПМ) до окклюзии плечевой артерии, показатели максимального постокклюзионного кровотока (МПК), резерва капиллярного кровотока (РКК), прироста капиллярного кровотока (ПКК) и время восстановления (ВВ) значений до исходных значений [15, 16]. По результатам исследования РКК и ПМ распределяли пациентов по гемодинамическим типам микроциркуляции (ГТМ) с выделением нормального, гипере-мического, спастического и застойно-стазического вариантов [17].
Безопасность препаратов оценивали по клиническим признакам проявления побочных эффектов, а также по показателям клинических и биохимических анализов крови с регистрацией степени их выраженности и времени возникновения.
Статистическая обработка данных осуществлялась с помощью пакета прикладных программ Statis-tica 6.0 с представлением данных в виде средней величины и ее стандартной ошибки (M±m). Для сравнения показателей до и после курсового лечения использовался непараметрический критерий Вилкок-сона. Различия считали статистически значимыми при р<0,05.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
В ходе исследования отмечалась хорошая переносимость препарата и высокая приверженность пациентов к лечению, все пациенты закончили лечение (12 недель). Переносимость оцениваемой комбинации препаратов была хорошей и не требовала отмены терапии. Масса тела и ИМТ существенно не изменялись. В ходе исследования не было зафиксировано ни одного случая гипогликемии.
В результате 12-недельной курсовой комбинированной терапии небивололом с индапамидом в индивидуально подобранных дозах частота стенокардии уменьшилась на 52,6% (р<0,01). Недельная потребность в нитроглицерине также статистически значимо (p<0,01) сократилась на 61,1%. При этом физическая толерантность по результатам велоэрго-метрии существенно возросла на 26% (с 60,3±6,1 Вт до 76,0±6,7 Вт). Данные изменения сопровождались уменьшением (р<0,05) объемов транзиторных ише-
Таблица 2
Влияние 12-недельной курсовой комбинированной терапии β1-адреноблокато-ром небивололом в дозе 5,9±0,3 мг/сут с индапамидом в дозе 1,5 мг/сут на регресс симптомов ХСН и качество жизни у больных с ишемической дисфункцией ЛЖ, ассоциированной с СД 2-го типа (М±m)
|
Показатель |
Исход (n=38) |
Курс (n=38) |
А,% |
|
Частота стенокардии, сут |
1,9±0,3 |
0,9±0,1 ** |
-52,6 |
|
Потребность в НТГ, таб/сут |
1,8±0,3 |
0,7±0,1 ** |
-61,1 |
|
Мощность ВЭМ нагрузки, Вт |
60,3±6,1 |
76,0±6,7* |
26,0 |
|
L, м |
361,8±13,1 |
405,7±11,4* |
12,1 |
|
Качество жизни, баллы |
23,5±8,1 |
16,8±4,2* |
-28,5 |
|
Стабильный ДП,% |
21,0±2,6 |
18,6±2,0 |
-11,4 |
|
Преходящий ДП,% |
14,4±5,1 |
12,3±1,6* |
-14,6 |
Примечание. НТГ – табл. нитроглицерина; ВЭМ – вело-эргометрический тест; L – тест 6-минутной ходьбы; КЖ – качество жизни. * – р<0,05; ** – р<0,01, различия с исходными данными.
мических дефектов перфузии миокарда на 14,6% и улучшением качества жизни на 28,5% (табл. 2).
Результаты СМАД при комбинированной терапии небивололом с индапамидом представлены в табл. 3.
Согласно результатам СМАД исходный средний уровень артериального давления у отобранной группы больных соответствовал 2-й степени артериальной гипертензии. Отмечалось повышение таких независимых маркеров сердечно-сосудистых осложнений, как пульсовое АД, нагрузка давлением и вариабельность САД и ДАД в дневные и ночные часы. В зависимости от величины суточного индекса выделены следующие группы больных: «Dipper» – 8 человек, «Non-dipper» – 19 человек, «Over-dipper» – 3 пациентов, «Night-peaker» – 4 человека.
Через 12 недель терапии у большинства больных – 24 (63,2%), включенных в исследование, отмечался «очень хороший» гипотензивный эффект терапии, у 14 (36,8%) – «хороший». Средний уровень САД составил 132,5±3,8 мм рт. ст. (р<0,05), ДАД – 86,7± 2,9 мм рт. ст. (р<0,05). У 3 (8%) больных гипотензивный эффект небиволола проявился на дозе 2,5 мг, у 26 (68,4%) больных – на дозе 5 мг, у 9 (23,6%) больных потребовалось увеличение дозы препарата до 10 мг/сут на фоне фиксированной дозы индапами-да 1,5 мг/сут. Полученные данные свидетельствуют о высокой эффективности комбинированной терапии небиволола с индапамидом.
Таблица 3
Динамика параметров суточного профиля АД у больных ИБС с СД 2-го типа при комбинированной терапии небивололом в средней дозе 5,9±0,3 мг/сут и индапамидом в дозе 1,5 мг/сут (M±m)
|
Показатели |
До лечения (n=34) |
После лечения (n=34) |
А(%) |
|
Среднесуточные |
|||
|
САД, мм рт. ст. |
158,2±8,1 |
132,5±3,8* |
-16,2 |
|
ДАД, мм рт. ст. |
93,8±3,8 |
86,7±2,9* |
-7,6 |
|
Пульсовое АД, мм рт. ст. |
64,4±4,4 |
45,8±3,2** |
-28,8 |
|
ЧСС, в 1 мин |
81,3±3,7 |
65,4±3,6* |
-19,5 |
|
Дневные |
|||
|
САД среднее, мм рт. ст. |
162,4±7,1 |
136,7±5,4* |
-15,8 |
|
ДАД среднее, мм рт. ст. |
97,3±6,7 |
87,3±5,5* |
-10,3 |
|
Пульсовое АД, мм рт. ст. |
65,1±5,2 |
49,4±4,3** |
-24,1 |
|
Вариабельность САД, мм рт. ст. |
19,2±1,6 |
14,8±1,7** |
-22,9 |
|
Вариабельность ДАД, мм рт. ст. |
15,7±1,5 |
10,7±1,6** |
-31,8 |
|
Индекс времени САД, % |
67,5±6,5 |
37,6±5,1** |
-44,3 |
|
Индекс времени ДАД, % |
56,1±7,7 |
35,2±6,6** |
-37,2 |
|
ЧСС, в 1 мин |
85,2±4,6 |
70,4±4,7* |
-17,4 |
|
Ночные |
|||
|
САД среднее, мм рт. ст. |
149,5±4,5 |
126,3±3,9* |
-15,5 |
|
ДАД среднее, мм рт. ст. |
86,4±6,7 |
72,6±2,6* |
-15,9 |
|
Пульсовое АД, мм рт. ст. |
63,1±4,7 |
53,7±2,8* |
-14,9 |
|
Вариабельность САД, мм рт. ст. |
16,4±1,2 |
11,3±1,3** |
-31,1 |
|
Вариабельность ДАД, мм рт. ст. |
13,6±1,9 |
10,9±1,9* |
-19,9 |
|
Индекс времени САД, % |
77,2±5,4 |
46,8±5,4** |
-39,4 |
|
Индекс времени ДАД, % |
52,7±8,9 |
35,7±5,5** |
-32,2 |
|
ЧСС, в 1 мин |
76,7±3,4 |
60,9±3,7** |
-20,6 |
|
Суточный индекс |
|||
|
САД, % |
9,8±1,4 |
12,8±2,9** |
30,6 |
|
ДАД, % |
9,1±1,7 |
13,1±2,5** |
43,9 |
Примечание: САД – систолическое артериальное давление, ДАД – диастолическое артериальное давление, ЧСС – частота сердечных сокращений, * – p<0,05, ** – p<0,01.
По данным СМАД у исследуемой группы пациентов произошла нормализация средних величин САД и ДАД в дневное время. Достижение целевого уровня артериального давления произошло у 30 (78,9%) человек. У 23 (60,5%) больных целевой уровень АД достигался уже на 8-й-9-й неделе терапии. Обращала на себя внимание высокая гипотензивная эффективность комбинации препаратов как в отношении систолического, так и диастолического АД, обусловленная потенцированием адреноблокирующих и прямых вазодилатирующих свойств небиво-лола и диуретика индапамида.
Кроме того, в результате курсового 12-недельного лечения уменьшилась степень нагрузки давлением (табл. 3), которая, по современным представлением, является предиктором раннего развития ИБС [18]. Также отмечалась нормализация вариабельности САД и ДАД как в дневные, так и в ночные часы (р<0,01). В настоящее время высокую вариабельность АД рассматривают как независимый фактор риска поражения органов-мишеней, определяющий неблагоприятный прогноз сердечно-сосудистой патологии.
На фоне курсовой терапии нормализовались показатели пульсового давления в дневные часы – 49,4±4,3 мм рт. ст. (р<0,01) и в ночные часы – 53,7± 2,8 мм рт. ст. (р<0,05). Повышение пульсового АД связано с увеличением жесткости магистральных артерий и является другим важным независимым маркером повышенного риска сердечно-сосудистой смертности [14].
Комбинированная терапия небивололом с инда-памидом благоприятно повлияла и на показатели суточного ритма АД, нарушение которого у больных с СД 2-го типа по данным литературы [19] ассоциируется с более чем 20-кратным увеличением риска сердечно-сосудистой смерти по сравнению с пациентами с сохранным суточным ритмом АД. К концу проспективного наблюдения увеличилось число пациентов в группе «Dipper» – до 23 (67,6%) человек, уменьшилось число пациентов в группе с преимущественно ночным повышением АД – «Night-peaker» – до 2 (5,8%) человек. В группу «Non-dipper» вошло 6 (17,6%) человек. Количество пациентов с чрезмерным снижением АД – «Over-dipper» осталось прежним 3 (8,8%) человека (рис. 1).
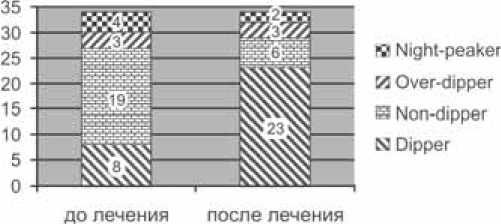
Рис. 1. Динамика распределения больных по показателю суточного индекса АД до и после 12-недельной курсовой комбинированной терапии небивололом с индапамидом
По данным ЭхоКГ гипертрофия миокарда диагностировалась у 32 (84,2%) больных. В среднем по группе толщина ЗС ЛЖ составила 11,1±1,0 мм, МЖП – 12,3±1,7 мм, масса миокарда – 250,9±19,5 г, ИММ ЛЖ – 144,9±25,3 г/м2 (при норме менее 120 г/м2). Выраженная гипертрофия миокарда отмечалась у 4 (10,5%) больных, включенных в исследование. По данным литературы [20], ГЛЖ у больных АГ является независимым фактором повышенного риска негативных сердечно-сосудистых событий. Доказано, что риск развития сердечно-сосудистых осложнений у больных АГ с ГЛЖ по данным эхокардиографии увеличен в 2-6 раз по сравнению с пациентами, имеющими нормальную ММ ЛЖ. Увеличение ИММ ЛЖ на 50 г/м2 сопровождается нарастанием риска развития ИБС на 50%. Относительный риск смерти при увеличении ММ ЛЖ на 100 г возрастает в 2,1 раза, а при увеличении толщины задней стенки ЛЖ на 0,1 см – в 7 раз.
У 100% больных, участвовавших в исследовании, выявлены признаки диастолической дисфункции ЛЖ по I типу, в связи с чем соотношение Е/А составило 0,83±0,05 у.е. Именно диастолические свойства миокарда определяют функциональный резерв сердца и уровень толерантности к физическим нагруз-
Таблица 4
Влияние 12-недельной комбинированной терапии небивололом с индапамидом на ремоделирование сердца у больных с ишемической дисфункцией ЛЖ, ассоциированной с СД 2-го типа (M±m)
|
Показатель |
Исход (n=38) |
Курс (n=38) |
А (%) |
|
ЛП, мм |
45,3±5,2 |
44,5±4,9 |
-1,8 |
|
ФВ(М), % |
61,3±1,8 |
61,7±2,1 |
0,7 |
|
КДО, мл |
133,8±8,4 |
131,3±9,7 |
-1,9 |
|
КСО, мл |
60,7±7,4 |
58,8±9,1 |
-3,1 |
|
ФВ(В), % |
57,8±1,8 |
61,5±2,1 |
6,4 |
|
МЖП, мм |
12,3±2,9 |
10,8±1,9* |
-12,1 |
|
ЗС ЛЖ, мм |
10,7±1,1 |
9,9±1,2* |
-7,2 |
|
ММЛЖ, г |
250,9±19,5 |
225,6±14,4* |
-10,1 |
|
ИММЛЖ, г/м2 |
144,9±25,3 |
131,8±22,2* |
-9,0 |
|
УО, мл |
73,2±2,4 |
76,2±2,7 |
4,1 |
|
СИ, л/мин/м2 |
2,2±0,5 |
2,3±0,6 |
4,5 |
|
Е/А |
0,83±0,05 |
0,99±0,07* |
19,3 |
|
ВИР, с |
130,9±5,4 |
112,9±5,3* |
-13,8 |
Примечание. ЛП – левое предсердие; КСО – конечный систолический объем; ФВ – фракция выброса; ЗСЛЖ – задняя стенка левого желудочка; ИММЛЖ – индекс массы миокарда ЛЖ; Е/А – отношение быстрого наполнения левого желудочка к ускорению трансмитрального кровотока вследствие сокращения левого предсердия; ВИР – время изоволюметрического расслабления; СИ – сердечный индекс; * – р<0,05 – различия с исходными данными.
кам. Диастолическая дисфункция ЛЖ у больных артериальной гипертензией является наиболее ранним маркером миокардиального фиброза, обусловливающего повышенную ригидность стенки ЛЖ и повышенный риск развития сердечной недостаточности [21]. КДО, КСО, УО соответствовали норме. Фракция выброса (ФВ) колебалась в пределах физиологических значений (табл. 4).
К концу 12-недельной курсовой терапии в среднем по группе статистически значимо (р<0,05) уменьшились размер задней стенки ЛЖ – на 7,2%, МЖП – на 12,1%, ММ ЛЖ – на 10,1%, и ИММ ЛЖ – на 9%, причем исходно повышенные показатели МЖП, ММ ЛЖ достигли нормы. У 8 (21%) больных наблюдалась нормализация диастолической функции ЛЖ: Е/А достигло 1,2±0,4 и еще у 7 (18,4%) больных она улучшилась – Е/А составило 0,9±0,06 у.е. Полученные данные свидетельствуют об улучшении структурно-функционального состояния кар-диомиоцитарного и интерстициального компонентов сердца, что отразилось на снижении степени риска прогрессирования сердечной недостаточности и кардиоваскулярных осложнений.
На протяжении многих лет применение 3-блокаторов у больных СД 2-го типа было ограничено вследствие неблагоприятного влияния на углеводный и липидный обмены. Неблагоприятные метаболические последствия применения, главным образом неселективных 3-адреноблокаторов первого поколения, связывали с блокадой 3 2 -адренорецепторов в поджелудочной железе, что приводило к замедлению высвобождения инсулина и усугублению гипергликемии. Поэтому неселективные 3-блокаторы первых поколений не нашли широкого применения у больных СД. За последние годы был создан целый ряд высокоселективных 3 1 -блокаторов третьего поколения (с дополнительными положительными фармакодинамическими свойствами, например, NO-мо-дулирующими эффектами и благоприятной фармакокинетикой – небиволол), способных контролировать в терапевтических дозах только 3 1 -адренорецепторы. Одним из таких прекрасных современных кардиоселективных препаратов и является небиво-лол, у которого соотношение pi к рг активности составляет 293 (в то время как у бисопролола аналогичный показатель составляет 26, метопролола – 25, це-липролола – 48) [3]. Данные нашего исследования продемонстрировали статистически значимое улучшение показателей углеводного и липидного обменов на фоне 12-недельной курсовой терапии небиво-лолом (и совпадают с данными Van Nueten L. и соавт. [22]). Это подтверждает не только метаболическую безопасность, но и хорошую антиишемическую и антигипертензивную эффективность небиволола у больных ИБС, отягощенной СД 2-го типа.
На фоне комбинированной терапии небивололом с индапамидом установлено статистически значимое уменьшение на 25,7% (р<0,05) уровня постпран-26
Таблица 5
Влияние 12-недельной комбинированной терапии небивололом дозе 5,9±0,3 мг/сут и индапамидом в дозе 1,5 мг/сут на постпрандиальную гликемию и липидный спектр крови у больных с ишемической дисфункцией ЛЖ, ассоциированной с СД 2-го типа (М±m)
|
Показатель |
Исход (n=30) |
Курс (n=30) |
А, % |
|
ОХС, ммоль/л |
6,2±1,1 |
5,4±0,9* |
-12,9 |
|
ТГ, ммоль/л |
2,9±0,35 |
2,6±0,2 |
-10,3 |
|
ЛПНП, ммоль/л |
4,05±0,8 |
3,2±0,8* |
-20,9 |
|
ЛПВП, ммоль/л |
0,96±0,05 |
1,06±0,06* |
10,4 |
|
ИА |
4,9±0,5 |
3,1±0,3* |
-36,7 |
|
Глюкоза натощак, ммоль/л |
6,9±0,4 |
6,5±0,3 |
-5,8 |
|
Постпрандиаль-ная гликемия, ммоль/л |
10,5±0,8 |
7,8±0,5* |
-25,7 |
|
Hb А1с,% |
8,1±0,4 |
7,5±0,3 |
-7,4 |
Примечание. ОХС – общий холестерин; ТГ – триглицериды; ЛПНП – липопротеиды низкой плотности; ЛПВП – липопротеиды высокой плотности; ИА – индекс атероген-ности; Hb А1с – гликозилированный гемоглобин; * – р<0,05 – различия с исходными данными.
диальной гликемии с 10,5±0,8 до 7,8±0,5 ммоль/л и значение этого показателя приблизилось к целевому уровню.
Также наблюдалось улучшение показателей липидного обмена. В связи с этим статистически значимо снизился в крови ОХС с 6,2±1,1 до 5,4±0,9 ммоль/л (р<0,05), уровень атерогенного ЛПНП уменьшился с 4,05±0,8 до 3,2±0,8 ммоль/л (р<0,05). Антиатеро-генный холестерин ЛПВП статистически значимо повысился с 0,96±0,05 до 1,06±0,06 ммоль/л, достигнув целевых значений. Следует особо отметить то, что наблюдаемые в ходе нашего исследования изменения липидного спектра сыворотки крови повлекли за собой явное (р<0,05) уменьшение индекса атерогенности, достигнувшего 3,1±0,3 у.е. (табл. 5).
Состояние МЦ, оценивалось методом лазерной допплеровской флоуметрии у 20 практически здоровых лиц (контрольная группа) и у 36 больных ИБС с СД 2-го типа. Анализировались гемодинамические типы микроциркуляции (ГТМ). В группе больных ИБС, отягощенной СД 2-го типа, установлены следующие ГТМ: гиперемический – у 5 (14,3%) пациентов, застойно-стазический – у 11 (28,6%) пациентов и спастический – у 20 (57,1%) пациентов. Особенности МЦ у данной категории проявились соответствующими микроциркуляторными изменениями: увеличением тонуса прекапиллярных сфинктеров, интенсификацией шунтового кровотока и нарастанием замедления венозного кровотока, создававшим
Влияние 12-недельной комбинированной терапии небивололом с индапамидом на состояние микроциркуляции у больных с ишемической дисфункцией ЛЖ, ассоциированной с СД 2-го типа (М±т)
|
Показатель |
Здоровые лица (n=20) |
Исход (n=36) |
Курс (n=36) |
А,% |
|
ПМ, перф. ед. |
3,8±0,3 |
2,6±0,4 |
2,9±0,5* |
11,5 |
|
Окклюзионная проба |
||||
|
МПК, перф. ед. |
10,1±2,8 |
9,4±1,2 |
8,7±1,6 |
-8,1 |
|
РКК, % |
265,8±18,7 |
358,1±34,0 |
322,5±33,2* |
-11,0 |
|
ПКК, перф. ед. |
6,2±0,8 |
6,7±0,8 |
5,8±1,2* |
-15,5 |
|
ВВ, с |
96,4±23,2 |
175,6±36,9 |
141,4±11,4* |
-19,5 |
Примечание. ПМ – показатель микроциркуляции; МПК – максимальный постокклюзионный кровоток; РКК – резерв капиллярного кровотока; ПКК – прирост капиллярного кровотока; ВВ – время восстановления; * – р<0,05.
Таблица 6 снижения активности симпатической нервной системы, обусловленной суперселективной блокадой 3 1 -адренорецепторов с дополнительной NO-модулирующей активностью небиволола у данной категории больных.
В то же время улучшение показателей микроциркуляции с сопутствующим гипотензивным эффектом терапии, возможно, обусловлено не только положительным влиянием 31-адреноблокады небиволо-лом, но и вазодилататорным действием индапамида, а также его непосредственным салуретическим эффектом с устранением избыточного содержания натрия в сосудистой стенке и прямым действием на трансмембранный ток кальция в условия для внутрисосудистых нарушений, на фоне выраженных явлений рарефикации органической природы вследствие микроваскулярного склерозирования. Подобные нарушения функционирования микроциркуляторного русла у больных ИБС описывают и другие исследователи [15, 16, 23].
К окончанию курсовой комбинированной терапии небивололом с индапамидом регистрировалась тенденция прироста на 11,5% показателя МЦ в покое. По данным окклюзионной пробы регистрировалось статистически значимое (р<0,05) снижение РКК на 11% и ПКК на 15,5% (табл. 6). В результате отмечались положительные изменения структуры гемодинамических типов микроцируляции. Так, доля больных с нормальным ГТМ составила 14 (38,8%) пациентов, с гиперемическим – 3 (8,3%) пациента, со спастическим – 13 (36,1%) пациентов, с застой-но-стазическим – у 6 (16,6%) пациентов за счет уменьшения доли больных с гиперемическим и застойно-стазическим типами микроциркуляции (рис. 2).
Время восстановления тканевой гемоперфузии до исходного уровня уменьшилось на 19,5% (р<0,05). Эти изменения были обусловлены улучшением сосудистой реактивности на фоне проводимой курсовой терапии небивололом с индапамидом за счет
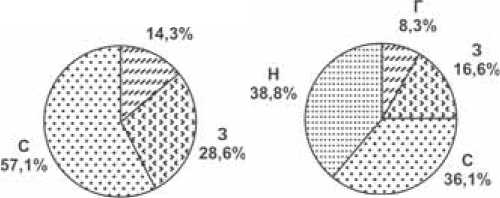
До лечения После лечения
Рис. 2. Структура гемодинамических типов микроциркуляции до и после лечения: Н - нормальный, Г - гиперемический, С - спастический, З - застойно-стазический ГТМ гладкомышечные клетки сосудов [24]. Кроме того, обнаружено, что индапамид способен усиливать синтез простагландина Е2 и простациклина эндотелио-цитами сосудов, ингибируя вазоконстрикторные влияния тромбоксана II [25].
Таким образом, 12-недельная курсовая комбинированная терапия небивололом в дозе 5,9±0,3 мг/сут с индапамидом в дозе 1,5 мг/сут обеспечивает существенные антигипертензивный и антиишемический эффекты, предотвращает процессы ишемического и постинфарктного ремоделирования сердца и сосудов, уменьшает выраженность метаболических нарушений, что значительно снижает степень риска развития коронарной и сердечной недостаточности, улучшая качество жизни пациентов. Положительное влияние такой комбинации обусловлено потенцирующим эффектом обоих препаратов.
ВЫВОДЫ
-
1. Курсовая 12-недельная комбинированная терапия кардиоселективным /3 1 -блокатором третьего поколения с NO-модулирующей активностью небивололом в дозе 5,9±0,3 мг/сут в комбинации с нейтральным диуретиком индапамидом в дозе 1,5 мг/сут у больных ИБС с постинфарктной дисфункцией ЛЖ, отягощенной СД 2-го типа, обеспечивает снижение частоты стенокардии на 52,6%, повышение физической толерантности на 26%, улучшает миокардиальную перфузию на 14,6% и КЖ на 28,5%.
-
2. Курсовая терапия небивололом в индивидуально подобранной дозе у 78,9% пациентов обеспечивает достижение целевых уровней САД и ДАД уже на 8-й-9-й дни проспективного наблюдения.
-
3. Комбинированная терапия небивололом с инда-памидом сопровождалась уменьшением на 25,7% уровня постпрандиальной гликемии, повышением на 10,4% антиатерогенного холестерина
-
4. К концу 12-недельной курсовой терапии небиво-лолом отмечались его кардио- и вазопротектив-ные эффекты, проявившиеся снижением индекса массы миокарда ЛЖ и толщины задней стенки ЛЖ на 9 и 7,2% соответственно. У 39,4% больных наблюдалась явное улучшение диастолической функции ЛЖ, а также регресс нарушений микроциркуляции.
ЛПВП, существенным уменьшением на 20,9% уровня холестерина ЛПНП.
Список литературы Клинические, гемодинамические и метаболические эффекты, влияние на микроциркуляцию комбинированной терапии небиволола с индапамидом у больных ишемической дисфункцией сердца, отягощенной сахарным диабетом 2-го типа
- Мычка В.Б., Чазова И.Е. Бета-блокаторы и сахарный диабет типа 2//Артериальная гипертензия. 2002. № 8 (5). С. 160-164.
- Шестакова М.В. Артериальная гипертония при сахарном диабете: эпидемиология, патогенез и стандарты лечения//Consilium medicum. 2001. № 3 (2). С. 83-86.
- Манухина Е.Б., Лямина Н.П., Долотовская П.В., Машина С.Ю., Лямина СВ., Покидышев Д.А., Малышев И.Ю. Роль оксида азота и кислородных свободных радикалов в патогенезе артериальной гипертензии//Кардиология. 2002. № 11. С. 73-84.
- Lozano G., Pagliaro P., Gatullo D., Marsh N.A. Control of coronary blood flow by endothelial release of nitric oxide//Clin Exp Pharmacol Physiol 1994;21:783-789.
- Levin E.R. Endothelins//N Eng J Med. 1995;323:356-363.
- Schwarz P., Diem R., Dun N.J., Forstermann U. Endogenous and exogenous nitric oxide inhibits norepinephrine release from rat heart sympathetic nerves//Circulat Res. 1995;77:841-848.
- Lewis M.J., Shah A.M. Endothelial modulation of myocardial contraction//Endothelium. 1994;1:237-243.
- Welch G., Loscalzo J. Nitric oxide and cardiovascular system//J Cardiovasc Surg. 1994:9:361-371.
- Jeremy J.Y., Rowe D., Emsley A.M., Newby A.C. Nitric oxide and the proliferation of vascular smooth muscle cells//Cardiovasc Res. 1999;43:580-594.
- Демина Л. Значение окислительного метаболизма лейкоцитов крови. М., 2000.
- Шляхто Е.В., Конради А.О. Комбинированная антигипертензивная терапия -современный взгляд на проблему. Кардиоваск. Тер. и профилакт. 2004; 3 (4): 12-18.
- Чазова И.Е., Мычка В.Б. Обосновано ли назначение диуретиков в качестве антигипертензивной терапии у пациентов с метаболическим синдромом и сахарным диабетом?//Consilium medicum. 2004, № 5.
- Борзова Н.В., Горбаченков А.А. Регресс гипертрофии и улучшение диастолической функции левого желудочка у больных артериальной гипертонией под влиянием антигипертензивной терапии. Кардиология, 6, 2008.
- Кобалава Ж.Д., Терещенко С.Н., Калинкин А.Л. Суточное мониторирование артериального давления: методические аспекты и клиническое значение. М., 1997.
- Крупаткин А.И., Сидоров В.В. Лазерная допплеровская флоуметрия микроциркуляции крови. Москва «Медицина», 2005.
- Тепляков А.Т., Гарганеева А.А. Расстройства микроциркуляции при ишемической болезни сердца. Томск, 2001.
- Маколкин В.И. Микроциркуляция в кардиологии. Москва 2004.
- Cooper RS, Simmons B, Castaner A. Left ventricular hypertrophy is associated with worse survival independence of left ventricular function and coronary arteries severe narrowed//Am J Cardiol. 1990; 65: 441-450.
- UK Prospective Diabetes Study (UKPDS) Group/Tight blood pressure control and risk of macrovascular and microvascular complications in type 2 diabetes: UKPDS 38. BMJ 1998.
- Аbergel E, Tase M, Bohlader J. Which definition for echocardiographic left ventricular hypertrophy?//Am J Cardiol. 1995;75:489-503.
- Калюжин В.В., Тепляков А.Т., Рязанцева Н.В., Вечерский Ю.Ю., Хлапов А.П., Колесников Р.Н. Диастола сердца. Физиология и клиническая патофизиология. Томск. 2007.
- Van Nueten L., Lacourciere Y., Vyssoulis J. et al.//Amer. J. Therapeutics. 1998. Vol. 5. P. 237-243.
- Васильев А.П., Стрельцова Н.Н., Секисова М.А., Савчук Т.Е. Функциональное состояние микроциркуляции у больных артериальной гипертонией в сочетании с метаболическим синдромом и сахарным диабетом. Кардиоваскулярная терапия и профилактика, 2008; 7(5).
- Мironneau J. Indapamide-induced inhibition of calcium movement in smooth muscles. Amer J of Hypertens 1988; 84 (Suppl.1B):P.10-14.
- Delbarre B., Delbarre G. Role of prostaglandins in the antihypertensive mechanism of indapamid. Clin Exp Hypertens 1990; 12: 130.


