Клинический случай дислокации транскатетерного протеза аортального клапана в выходной тракт левого желудочка с успешной эндоваскулярной коррекцией в раннем послеоперационном периоде
Автор: Горовая А.Д., Зубарев Д.Д., Краснов В.С., Чернявский М.А., Прохорихин Алексей Андреевич
Журнал: Патология кровообращения и кардиохирургия @journal-meshalkin
Рубрика: Случаи из клинической практики
Статья в выпуске: 4 т.25, 2021 года.
Бесплатный доступ
Представлен клинический случай успешной эндоваскулярной коррекции дислокации самораскрывающегося протеза аортального клапана в выходной тракт левого желудочка. 72-летний мужчина поступил в ФГБУ «НМИЦ им. В.А. Алмазова» Минздрава России для эндоваскулярной коррекции тяжелого аортального стеноза. При транскатетерном протезировании аортального клапана произошла миграция самораскрывающегося протеза на 10-12 мм в выходной тракт левого желудочка. После оптимизации каркаса баллонным катетером и достижения I-II ст. аортальной регургитации операцию завершили. Однако на 17-е сут. послеоперационного периода возникла острая левожелудочковая недостаточность с эпизодами асистолии вследствие тяжелой парапротезной регургитации. Коррекцию дислокации выполнили путем эндоваскулярной тракции протеза двумя петлевыми катетерами-ловушками. Послеоперационный период прошел без особенностей. Пациента в удовлетворительном состоянии выписали на 31-е сут. Дислокация самораскрывающегося протеза в выходной отдел левого желудочка - осложнение, характерное только для транскатетерной имплантации аортального клапана, которое может привести к стремительному ухудшению состояния пациента, ввиду чего необходимо как можно быстрее произвести коррекцию позиции биопротеза. В клиническом случае успешная эндоваскулярная коррекция дислокации биопротеза с помощью тракции петлевым катетером-ловушкой позволила избежать «открытого» хирургического вмешательства. Описанная техника может помочь эндоваскулярному хирургу в подобной ситуации.
Аортальный стеноз, дислокация самораскрывающегося протеза, клинический случай, транскатетерная имплантация аортального клапана
Короткий адрес: https://sciup.org/142230621
IDR: 142230621 | DOI: 10.21688/1681-3472-2021-4-112-117
Successful delayed endovascular correction of migration of transcatheter aortic valve prosthesis in left ventricle outflow tract: case report
We report the successful endovascular correction of the migration of a transcatheter aortic valve prosthesis in the left ventricle outflow tract (LVOT). A 72-old man was underwent transcatheter aortic valve implantation (TAVI) at Almazov National Medical Research Centre for severe aortic stenosis. During the procedure, the self-expanding prosthesis dislocated 10-12 mm into the LVOT. The frame was optimised with the use of a balloon catheter, and aortic regurgitation I-II degree was achieved. However, on day 17 of hospitalisation, acute heart failure with episodes of asystole occurred as a result of severe paravalvular regurgitation; cardiopulmonary resuscitation was necessary. The prosthesis malpositioning was corrected by traction with endovascular snare devices. The patient was stable during the postprocedural period and discharged on day 31. Dislocation of self-expanding prostheses into the LVOT is a complication specific to TAVI that may quickly aggravate a patient's condition; therefore, correction of valve malpositioning should be performed as soon as possible. The case reported here in an illustration of successful endovascular correction of dislocation performed with the snare traction technique. This bail-out approach can be used by interventional cardiologists in similar situations.
Текст научной статьи Клинический случай дислокации транскатетерного протеза аортального клапана в выходной тракт левого желудочка с успешной эндоваскулярной коррекцией в раннем послеоперационном периоде
А.Д. Горовая,
Д.Д. Зубарев,
В.С. Краснов,
М.А. Чернявский, А.А. Прохорихин,
Транскатетерная имплантация аортального клапана — метод выбора лечения пожилых пациентов с критическим аортальным стенозом высокого и среднего хирургического риска [1–3]. С первого протезирования в 2002 г. [4] зарегистрировано около 500 тыс. имплантаций в более чем 70 странах мира [5]. В связи с распространением техники эндоваскулярного протезирования клапана возросло количество выявляемых осложнений. Дислокация самораскрывающегося протеза в выходной тракт левого желудочка и связанная с этим аортальная регургитация — пример жизнеугрожающего осложнения, ассоциированного с транскатетерной имплантацией аортального клапана. Зачастую в таких случаях производят экстренную конверсию в «открытое» вмешательство, что повышает риск интраоперационной летальности. Рекомендации по ведению таких пациентов основаны на малом количестве описанных клинических случаев [6]. Практический интерес представляет клинический случай успешной эндоваскулярной коррекции дислокации транскатетерного биопротеза аортального клапана, проведенной в раннем послеоперационном периоде.
Клинический случай
По данным эхокардиографического исследования, фракция выброса левого желудочка 50 %. Пиковая скорость аортального стеноза 4,5 м/с, максимальный / средний градиент давления 81 / 49 мм рт. ст., аортальная регургитация II ст., расчетная площадь аортального клапана 0,79 см2.
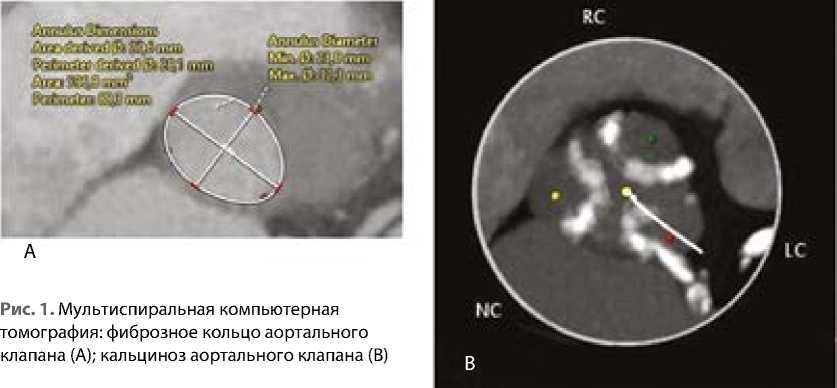
На мультиспиральной компьютерной томографии аортальный клапан трехстворчатый, умеренно кальцинирован. С учетом диаметра / периметра фиброзного кольца аортального клапана 28,1 / 88,3 мм и диаметра восходящего отдела аорты 36,3 мм (рис. 1) пациенту рекомендовали имплантацию самораскры-вающегося протеза Evolut R 34 мм (Medtronic, Миннеаполис, США). Из-за выраженного кальциноза бедренных артерий решили произвести хирургическое выделение правой общей бедренной артерии.
Степень тяжести и симптомное течение аортального стеноза определили показания к оперативному вмешательству. Учитывая высокий интраоперационный риск, аортокоронарное шунтирование
ACT .......
A
Рис. 1. Мультиспиральная компьютерная томография: фиброзное кольцо аортального клапана (A); кальциноз аортального клапана (B)
^ШПл
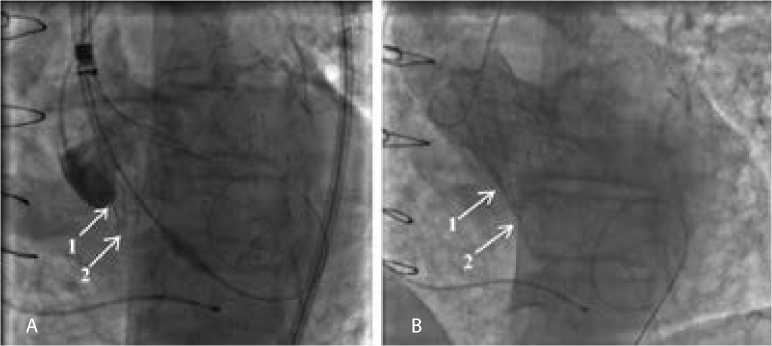
Рис. 2. Аортография после имплантации протеза: позиция протеза перед раскрытием дистальной короны (A) и после постдилатации (B)
Примечание. 1 — уровень фиброзного кольца аортального клапана; 2 — глубина имплантации протеза.
в анамнезе и отказ пациента от повторной «открытой» операции, решили протезировать аортальный клапан эндоваскулярным способом.
Предоперационная селективная коронарошун-тография показала: рестеноз передней межжелудочковой артерии до 70 % в проксимальной трети, периферия заполняется по функционирующему маммарокоронарному шунту, рестеноз до субокклюзии в проксимальной трети огибающей артерии и стеноз до субокклюзии в средней трети, периферия заполняется по функционирующему аутовенозному шунту, диаметр правой коронарной артерии менее 2 мм, окклюзия в дистальной трети. Одномоментно выполнили стентирование огибающей артерии с переходом на маргинальную ветвь.
Транскатетерную имплантацию аортального клапана осуществляли по стандартной методике, принятой в ФГБУ «НМИЦ им. В.А. Алмазова» Минздрава России. Однако многократные попытки позиционировать клапан в условиях высокочастотной кардиостимуляции привели к резкому падению гемодинамических показателей с эпизодом фибрилляции желудочков. После электроимпульсной терапии возник длительный период электрической активности без пульса, потребовавшей сердечно-легочной реанимации и подключения к аппарату непрямого массажа сердца Lucas (JOLIFE, Лунд, Швеция) в течение 30 мин. После восстановления сердечной деятельности выполнили финальное позиционирование и имплантацию протеза аортального клапана. После раскрытия дистальной короны произошла дислокация протеза в левый желудочек на
10–12 мм. На интраоперационной трансторакальной эхокардиографии определили регургитацию II ст. Интраоперационно приняли решение о постдилатации аортального протеза баллонным катетером NuCLEUS 28 × 40 мм (BVM Medical Ltd., Хинкли, Великобритания) (рис. 2). После постдилатации на контрольной эхокардиографии определяли аортальную регургитацию I–II ст., прямое артериальное давление 170 / 70 мм рт. ст. С учетом риска новой остановки кровообращения и удовлетворительных гемодинамических показателей решили завершить вмешательство.
Послеоперационный период осложнился инфарктом миокарда в 1-е сут. с повышением тропонина I в динамике до 51,67 нг/мл (референсные значения 0,00–0,03 нг/мл) и острым нарушением мозгового кровообращения распространенного кардиоэмболического генеза с проявлением умеренного правостороннего гемипареза, которые не оказали жизнеугрожающего влияния на клинический статус пациента. Однако на 17–18-е сут. после вмешательства значительно ухудшилась гемодинамика, что привело к нескольким эпизодам асистолии. Провели сердечно-легочную реанимацию. На экстренной транспищеводной эхокардиографии выявили протрузию биопротеза до 12 мм от плоскости фиброзного кольца аортального клапана в выходной тракт левого желудочка с тяжелой парапротезной регургитацией.
С учетом тяжелого состояния пациента, прогрессирования явлений острой левожелудочковой недостаточности, неоднократных остановок
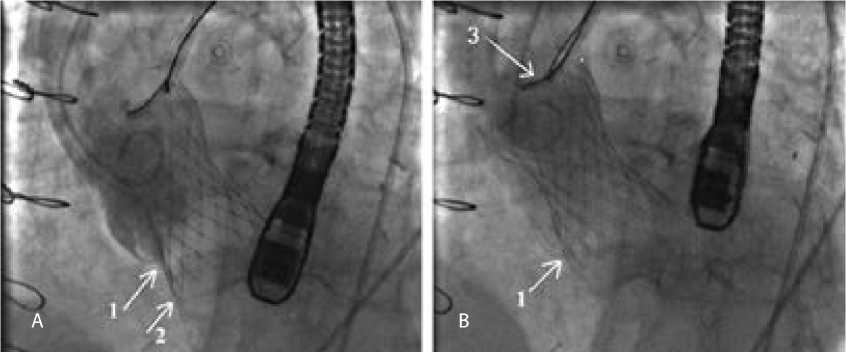
Рис. 3. Аортография перед тракцией и после тракции петлевыми катетерами-ловушками: исходная позиция протеза (А); результат после тракции (B)
Список литературы Клинический случай дислокации транскатетерного протеза аортального клапана в выходной тракт левого желудочка с успешной эндоваскулярной коррекцией в раннем послеоперационном периоде
- Otto C.M., Nishimura R.A., Bonow R.O., Carabello B.A., Erwin J.P. 3rd, Gentile F., Jneid H., Krieger E.V., Mack M., McLeod C., O'Gara P.T., Rigolin V.H., Sundt T.M. 3rd, Thompson A., Toly C. 2020 ACC / AHA guideline for the management of patients with valvular heart disease: a report of the American College of Cardiology / American Heart Association Joint Committee on Clinical Practice Guidelines. Circulation. 2021;(5):e72-e227. DOI: 10.1161/CIR.0000000000000923 PMID: 33332150
- Baumgartner H., FalkV., Bax J.J., De Bonis M., Hamm C., Holm PJ., Iung B., Lancellotti P., Lansac E., Munoz D.R., Rosenhek R., Sjogren J., Mas P.T., Vahanian A., Walther T., Wendler O., Windecker S., Zamorano J.L., ESC Scientific Document Group. 2017 ESC / EACTS Guidelines for the management of valvular heart disease. Eur Heart J. 2017;(36):2739-2791. DOI: 10.1093/eurheartj/ehx391 PMID: 28886619
- Kamenskaya O., Loginova I., Kretov E., Prokhorikhin A., Tarkova A., Lomivorotov V.V., Karaskov A. Effect of transcatheter aortic valve implantation on health-related quality of life in older adults with multimorbidity. Arch Gerontol Geriatr. 2019;80:76-81. DOI: 10.1016/j.archger.2018.10.007 PMID: 30390428
- Cribier A., Eltchaninoff H., Bash A., Borenstein N., Tron C., Bauer F., Derumeaux G., Anselme F., Laborde F., Leon M.B. Percutaneous transcatheter implantation of an aortic valve prosthesis for calcific aortic stenosis: first human case description. Circulation. 2002;106(24):3006-3008. DOI: 10.1161/01.cir.0000047200.36165.b8 PMID: 12473543
- Costa G., Barbanti M., Tamburino C. Trends in European TAVI Practice. Cardiac Interventions Today. 2018;12(2):51-54.
- Ibebuogu U.N., Giri S., Bolorunduro O., Tartara P., Kar S., Holmes D., All O. Review of reported causes of device embolization following trans-catheter aortic valve implantation. Am J Cardiol. 2015;115(12):1767-1772. DOI: 10.1016/j.amjcard.2015.03.024 PMID: 25882773
- Geisbusch S., Bleiziffer S., Mazzitelli D., Ruge H., Bauernschmitt R., Lange R. Incidence and management of CoreValve dislocation during transcatheter aortic valve implantation. Circ Cardiovasc Interv. 2010;3(6):531-536. DOI: 10.1161/circinterventions.110.944983 PMID: 21063000
- Laborde J.-C., Brecker S.J.D., Roy D., Jahangiri M. Complications at the time of transcatheter aortic valve implantation. Methodist Debakey Cardiovasc J. 2012;8(2):38-41. PMCID: PMC3405794. DOI: 10.14797/mdcj-8-2-38 PMID: 22891127


