Клинический случай гибридного лечения пациента с критическим стенозом аортального клапана, поражением ствола левой коронарной артерии и кровоточащим раком желудка
Автор: Б.Г. Алекян, Д.В. Ручкин, Н.Г. Карапетян, Н.Л. Иродова, Н.Н. Мелешенко, Л.Г. Гёлецян, А.Ш. Ревишвили
Журнал: Патология кровообращения и кардиохирургия @journal-meshalkin
Рубрика: Случаи из клинической практики
Статья в выпуске: 2 т.26, 2022 года.
Бесплатный доступ
Стеноз аортального клапана и кровоточащий рак желудка — грозные заболевания с высокой летальностью. Длительное время «золотым стандартом» лечения больных аортальным стенозом было «открытое» вмешательство — протезирование аортального клапана. Применяемая с 2002 г. эндоваскулярная операция транскатетерной имплантации аортального клапана стала стандартом в группе пациентов высокого хирургического риска. Рак желудка — одно из основных тяжелых онкологических заболеваний, единственный способ лечения которых — хирургический. Сочетание этих двух патологий значительно ухудшает прогноз и затрудняет выбор оптимальной врачебной тактики. Поскольку стандарты лечения мультиморбидных пациентов не разработаны, стратегию определяет междисциплинарный консилиум. Цель — представить клиническое наблюдение пациента с критическим аортальным стенозом, сопутствующим тяжелым поражением коронарных артерий и кровоточащим раком желудка, которому по решению мультидисциплинарной команды выполнили успешную одномоментную операцию: чрескожное коронарное вмешательство, транскатетерную имплантацию аортального клапана и «открытую» гастрэктомию с реконструкцией на петле по Ру, — при одном анестезиологическом пособии. Пациента выписали в удовлетворительном состоянии. В отдаленном периоде наблюдения из-за возврата стенокардии и рестеноза стента в передней межжелудочковой ветви провели повторное вмешательство в виде рестентирования с положительным клиническим результатом. Гибридный подход в лечении пациентов с критическим стенозом аортального клапана в сочетании с ишемической болезнью сердца и кровоточащим раком желудка может быть принят как одна из возможных стратегий, но необходимо накапливать клинический материал и проводить дальнейшие исследования в этом направлении.
Аортальный стеноз, гибридная хирургия, клинический случай, рак желудка, сердечная команда, транскатетерная имплантация аортального клапана, чрескожное коронарное вмешательство
Короткий адрес: https://sciup.org/142232024
IDR: 142232024 | DOI: 10.21688/1681-3472-2022-2-58-65
Case report of a multidisciplinary approach to one-time treatment of a patient with critical aortic valve stenosis, lesion of the left main coronary artery and bleeding stomach cancer
Aortic valve stenosis and bleeding gastric cancer are formidable diseases characterized by high mortality. For a long time, the gold standard for treating patients with aortic stenosis has been open-heart surgery — aortic valve replacement. However, the endovascular operation that appeared in 2002 — transcatheter aortic valve implantation (TAVI) has become the standard of care for patients with high surgical risk. Gastric cancer is one of the major severe oncological diseases in which surgery is the only way to cure. The combination of these two diseases signicantly worsens the prognosis and is a dicult clinical task for choosing the optimal tactics for treating a patient. Given the lack of developed standards for the treatment of multimorbid patients, the treatment plan is determined by an interdisciplinary consultation. But with a combination of these diseases, there is no generally accepted approach in the known recommendations. The purpose of this report is to present a clinical case of a patient with critical aortic stenosis, concomitant severe coronary artery disease, and bleeding stomach cancer, who underwent a successful one-stage operation — percutaneous coronary intervention, TAVI and open gastrectomy with Roux-loop reconstruction with one anesthetic aid by the decision of a multidisciplinary team. The patient was discharged in a satisfactory condition. In the late follow-up period, angina pectoris returned with restenosis of the stent in the anterior interventricular branch (LAD), which required repeated intervention in the form of LAD restenting with a good clinical result. A hybrid approach in the treatment of patients with critical aortic valve stenosis in combination with coronary artery disease and bleeding gastric cancer can be accepted as one of the possible strategies, but further research is needed in this direction.
Текст научной статьи Клинический случай гибридного лечения пациента с критическим стенозом аортального клапана, поражением ствола левой коронарной артерии и кровоточащим раком желудка
Цитировать: Алекян Б.Г., Ручкин Д.В., Карапетян Н.Г., Иродова Н.Л., Мелешенко Н.Н., Гёлецян Л.Г., Ревишвили А.Ш. Клинический случай гибридного лечения пациента с критическим стенозом аортального клапана, поражением ствола левой коронарной артерии и кровоточащим раком желудка. Патология кровообращения и кардиохирургия. 2022;26(2):58-65. 10.21688/1681-3472-2022-2-58-65
Клинический случай
У пациентки В. 73 лет с длительным анамнезом артериальной гипертензии и инсулинпотребно-го сахарного диабета при обследовании по месту жительства диагностировали критический стеноз АК. В одном из федеральных центров г. Москвы выполнили коронарографию, выявили многососудистое поражение артерий со стенозом устья ствола ЛКА 70 %, стенозом п/3 передней межжелудочковой ветви (ПМЖВ) 70 %, стенозом п/3 огибающей ветви 80 %, стенозом с/3 ветви тупого края 60 %. Планировали выполнить сочетанное «открытое» оперативное вмешательство: аортокоронарное шунтирование и протезирование АК. Однако в ходе комплексного обследования перед операцией по
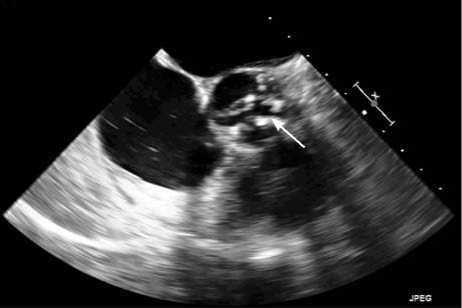
На основании жалоб и данных обследования поставили диагноз: дегенеративный критический аортальный стеноз, аортальная недостаточность 1–2-й ст. Стенокардия 3-го функционального класса по классификации Канадского сердечно-
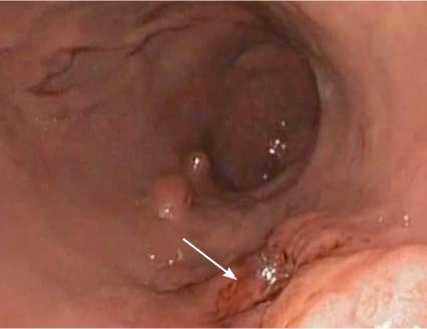
В день хирургического вмешательства (в июне 2018 г.) для минимизации риска желудочно-кишечного кровотечения за 60 мин до ЧКВ и ТИАК начали двойную антиагрегантную терапию (300 мг аспирина и 600 мг клопидогреля). Трансрадиальным доступом выполнили ЧКВ: стентирование огибающей ветви стентом Promus Element Plus 2,5 × 38,0 мм
(Boston Scientific, Мальборо, США), стентирование ствола ЛКА с переходом в с/3 ПМЖВ стентом Xience Xpedition 3,5 × 48,0 мм (Abbott, Эбботт-Парк, США) под контролем внутрисосудистого ультразвукового исследования (рис. 3). Выбор стента был обусловлен диаметром проксимальной ПМЖВ по данным измерения: около 2,5 мм. Диаметр стента более 2,5 мм, по нашему мнению, мог привести к осложнениям после имплантации. Через феморальный артериальный доступ имплантировали клапан CoreValve 26 (Medtronic, Миннеаполис, США) в проекцию АК. При контрольной чреспищеводной ЭхоКГ и ангиографии положение клапана корректное, данных о значимой паравальвулярной регургитации не получили, компрометации устьев коронарных артерий не выявили (рис. 4). С помощью системы Рerclose Proglide (Abbott, Эбботт-Парк, США) выполнили чрескожное ушивание отверстий бедренных артерий.
По данным послеоперационной ЭхоКГ, пиковый градиент давления на аортальном протезе 10 мм рт. ст. Транспротезная регургитация 1-й ст. (гемодинамически незначимая). Митральная регургитация 1–2-й ст. Из катетеризационной лаборатории пациентку перевели в хирургическую операционную, где выполнили «открытую» гастрэктомию, холецистэктомию, лимфодиссекцию D2 с последующей реконструкцией на петле по Ру. Больную экстубировали на операционном столе и перевели в отделение реанимации.
Ранний послеоперационный период осложнился острым повреждением почек, вероятно, контраст-индуцированным на фоне смешанной нефропатии (диабетической, гипертонической), что потребовало заместительной почечной терапии в течение 7 дней. К моменту выписки явления острого по-
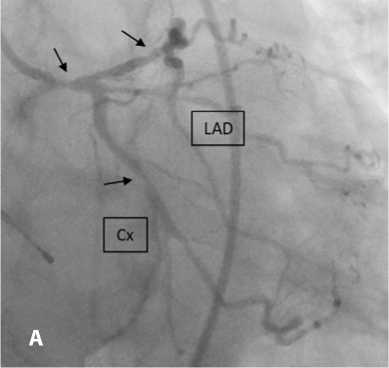
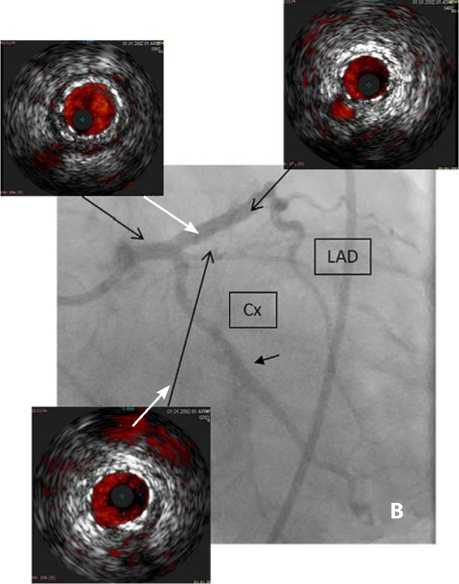
Рис . 3. Коронарография до (A) и после (B) чрескожного коронарного вмешательства
Примечание. LAD (англ. left anterior descending artery) — передняя межжелудочковая ветвь; Cx (англ. circumflex artery) — огибающая ветвь левой коронарной артерии.
чечного повреждения разрешились, восстановились темпы диуреза, в анализах крови креатинин 95–105 мкмоль/л, скорость клубочковой фильтрации по формуле CKD-EPI 50–44 мл/мин/1,73 м2).
По данным ЭхоКГ в раннем послеоперационном периоде и при выписке, функция протеза АК не нарушена, градиент давления на протезе 11 мм рт. ст., регургитация 2-й ст. Левый желудочек не увеличен (конечный диастолический размер 44 мм), фракция выброса 58 %. В раннем послеоперационном периоде развилась высокая легочная гипертензия: систолическое давление в легочной артерии 80 мм рт. ст. со снижением до 60 мм рт. ст. на фоне терапии к моменту выписки.
Повышение давления в легочной артерии носило, видимо, смешанный характер (дыхательная недостаточность на фоне множественных дистелектазов легких, явления декомпенсации сердечной недостаточности на фоне острого повреждения почек, выраженной диастолической дисфункции левого желудочка вследствие его гипертрофии; убедительных данных о тромбоэмболии легочной артерии не получили). По данным компьютерной томографии к моменту выписки, эзофагоеюноанастомоз состоятелен, проходим. На фоне проведенной терапии состояние больной с положительной динамикой. Восстановлен пероральный прием пищи.
На 15-й день после операции пациентку выписали в удовлетворительном состоянии. Назначили стандартную комплексную терапию, включающую двойную антиагрегантную терапию (кишечнорастворимую форму аспирина и клопидогрель) сроком не менее 6 мес. согласно рекомендациям Европейского общества кардиологов (англ. European Society of Cardiology), статины, бета-адреноблокаторы, антагонисты рецепторов ангиотензина II, диуретики, сахароснижающую терапию.
В течение 16 мес. после гибридного хирургического вмешательства самочувствие было удовлетворительным, пациентка хорошо переносила физические нагрузки, наблюдалась по месту жительства. За этот период не отметили кардиальных событий, в том числе эпизодов декомпенсации сердечной недостаточности, клиники нестабильной стенокардии, инфаркта миокарда, потребовавших госпитализации.
При контрольном обследовании в НМИЦ хирургии им. А.В. Вишневского при ЭхоКГ функция протеза АК удовлетворительная: средний градиент 9 мм рт. ст., недостаточность 1–2-й ст.; фракция выброса левого желудочка 58 %, систолическое давление в легочной артерии 45–50 мм рт. ст. Основные лабораторные показатели в пределах нормы, сохранялось снижение функции почек (хроническая
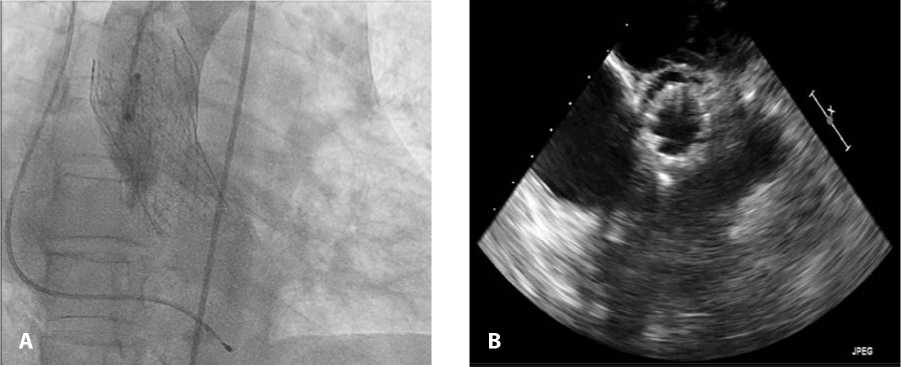
Рис. 4. Имплантация аортального клапана CoreValve 26 (Medtronic, Миннеаполис, США): ангиограмма после имплантации (A); контрольная интраоперационная эхокардиография (B)
болезнь почек стадии 3А, креатинин 100 мкмоль/л, скорость клубочковой фильтрации по формуле CKD-EPI 46 мл/мин/1,73 м2), неудовлетворительная компенсация сахарного диабета (гликированный гемоглобин 8,1–8,8 %). Рекомендовали нагрузочный тест в плановом порядке и при показаниях коронарографию, однако в связи с эпидемиологической обстановкой по COVID-19 пациентка исследование не проходила. Данных о рецидиве онкопатологии нет.
Через 20 мес. после гибридного хирургического вмешательства состояние ухудшилось: появилась и прогрессировала одышка, постепенно снизилась толерантность к нагрузкам, возникли эпизоды жжения за грудиной. Однако для проведения коронарографии пациентка обратилась в НМИЦ хирургии им. А.В. Вишневского лишь спустя год после появления жалоб (через 34 мес. после операции).
При госпитализации на фоне прогрессирования почечной недостаточности (хроническая болезнь почек 4-й стадии, креатинин 168 мкмоль/л, скорость клубочковой фильтрации 28 мл/мин/1,73 м2), декомпенсированного сахарного диабета (гликированный гемоглобин 8,8 %) ведущей являлась клиника ИБС и выраженной застойной сердечной недостаточности: двусторонний гидроторакс; уровень N-концевого мозгового натрийуретического пептида (NT-proBNP) 21 400 пг/мл. По данным ЭхоКГ, функция протеза АК не нарушена (пиковый градиент на протезе 5,5 мм рт. ст., недостаточность на протезе 2–3-й ст.), митральная недостаточность 1–2-й ст.; признаки выраженной легочной гипертензии с повышением расчетного давления в правом желудочке до 60–70 мм рт. ст. и снижение сократительной способности миокарда левого желудочка с фракцией выброса около 40 %. Данных о рецидиве онкопатологии нет.
Перед коронарографией провели подготовку: медикаментозную коррекцию сердечной и почечной недостаточности. Отметили положительную динамику: уменьшение клинических проявлений застойной сердечной недостаточности, снижение уровня N-концевого мозгового натрийуретического пептида с 21 400 до 18 600 пг/мл.
На фоне мер по профилактике контраст-индуци-рованной нефропатии выполнили коронарографию: ранее имплантированный стент в стволе ЛКА с переходом в с/3 ПМЖВ проходим, однако в п/3 ПМЖВ рестеноз до 90 %, ранее имплантированный стент в огибающей ветви проходим. Приняли решение о рестентировании ПМЖВ. Через правый трансрадиальный доступ с предилатацией (баллонным катетером Maverick 2,5 × 20,0 мм (Boston Scientific, Мальборо, США) с однократным раздуванием до 12 атм.) выполнили рестентирование ПМЖВ стентом с лекарственным покрытием Resolute Integrity 2,75 × 30,00 мм (Medtronic, Миннеаполис, США) с постдилатацией баллонным катетером Maverick 3,0 × 20,0 мм (Boston Scientific, Мальборо, США) (рис. 5).
В раннем послеоперационном периоде признаки контраст-индуцированной нефропатии с повышением креатинина до 320 мкмоль/л (калий 4,2–4,8 ммоль/л) и снижением темпов диуреза. На фоне проводимой терапии снижение уровня креатинина до 257–300 мкмоль/л, восстановление темпов диуреза, уменьшение выраженности явлений
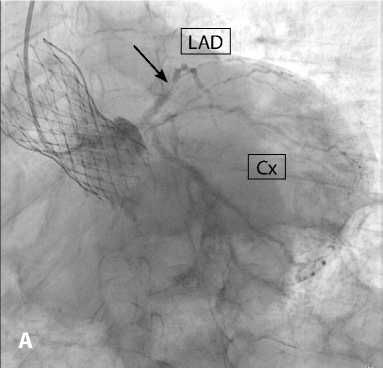
Рис. 5. Коронарография до (A) и после (B) чрескожного коронарного вмешательства
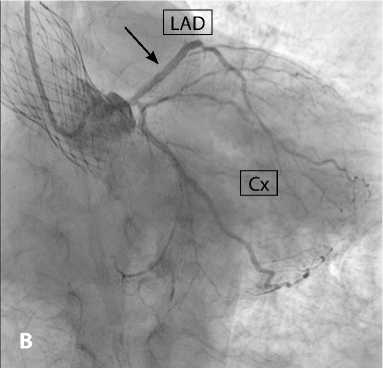
Примечание. LAD (англ. left anterior descending artery) — передняя межжелудочковая ветвь; Cx (англ. circumflex artery) — огибающая ветвь левой коронарной артерии.
застойной сердечной недостаточности (фракция выброса левого желудочка 43–45 %, систолическое давление в легочной артерии 50 мм рт. ст.). Пациентку выписали в удовлетворительном состоянии.
Через 38 мес. после гибридного хирургического вмешательства самочувствие удовлетворительное, хорошая переносимость нагрузок, стабилизировались показатели азотовыделительной функции почек и гликемии; по ЭхоКГ функция протеза АК не нарушена. Пациентка продолжает амбулаторное наблюдение по месту жительства у кардиолога, нефролога, эндокринолога, онколога.
Обсуждение
По мере старения населения ежегодно увеличивается количество ассоциированных с возрастом заболеваний, таких как кальцинированный порок АК и онкопатология [9]. Стеноз АК имеют 4–6 % лиц старше 65 лет, это наиболее распространенный порок сердца взрослого населения, который требует оперативного вмешательства [10]. У 40 % пациентов со стенозом АК диагностируют сопутствующую ишемическую болезнь сердца [11].
Рак желудка встречается у 5,6 % пациентов с онкологическими заболеваниями и занимает 4-е место в структуре онкологических патологий . Частота встречаемости у больного одновременно приобретенного порока сердца, ИБС и рака желудка неизвестна, однако ко- личество пациентов с несколькими конкурирующими заболеваниями в клинической практике возрастает. Четких клинических рекомендаций для этой группы больных не существует. Имеются публикации об удачных этапных или «открытых» симуль-тантных вмешательствах при ИБС и онкопатологии [5; 6] или аортальном стенозе и сопутствующей онкопатологии [7; 8].
Заключение
Список литературы Клинический случай гибридного лечения пациента с критическим стенозом аортального клапана, поражением ствола левой коронарной артерии и кровоточащим раком желудка
- Cribier A., Eltchaninoff H., Bash A., Borenstein N., Tron C., Bauer F., Derumeaux G., Anselme F., Laborde F., Leon M.B. Percutaneous transcatheter implantation of an aortic valve prosthesis for calcific aortic stenosis: first human case description. Circulation. 2002;106(24):3006-3008. PMID: 12473543. https://doi.org/10.1161/01.CIR.0000047200.36165.B8
- Cribier A., Savin T., Saoudi N., Rocha P., Berland J., Letac B. Percutaneous transluminal valvuloplasty of acquired aortic stenosis in elderly patients: an alternative to valve replacement? Lancet. 1986;1(8472):63-67. PMID: 2867315. https://doi.org/10.1016/S0140-6736(86)90716-6
- Алекян Б.Г., Григорьян А.М., Стаферов А.В., Карапетян Н.Г. Рентгенэндоваскулярная диагностика и лечение заболеваний сердца и сосудов в Российской Федерации – 2019 год. Эндоваскулярная хирургия. 2020;7(2, спец. вып.):S5-S230. https://doi.org/10.24183/2409-4080-2020-7-2S-S5-S230
- Alekyan B.G., Grigoryan A.M., Staferov A.V., Karapetyan N.G. Endovascular diagnostics and treatment of diseases of the heart and blood vessels in the Russian Federation – 2019. Endovaskulyarnaya Khirurgiya = Russian Journal of Endovascular Surgery. 2020;7(2, Special Iss.):S5-S230. (In Russ.) https://doi.org/10.24183/2409-4080-2020-7-2S-S5-S230
- Алекян Б.Г., Григорьян А.М., Стаферов А.В., Карапетян Н.Г. Рентгенэндоваскулярная диагностика и лечение заболеваний сердца и сосудов в Российской Федерации – 2017 год. Эндоваскулярная хирургия. 2018;5(2, спец. вып.):93-240. https://doi.org/10.24183/2409-4080-2018-5-2-93-240
- Alekyan B.G., Grigoryan A.M., Staferov A.V., Karapetyan N.G. Endovascular diagnostics and treatment in the Russian Federation (2017). Endovaskulyarnaya Khirurgiya = Russian Journal of Endovascular Surgery. 2018;5(2, Special Iss.):93-240. (In Russ.) https://doi.org/10.24183/2409-4080-2018-5-2-93-240
- D'Ascenzo F., Verardi R., Visconti M., Conrotto F., Scacciatella P., Dziewierz A., Stefanini G.G., Paradis J.-M., Omedè P., Kodali S., D'Amico M., Rinaldi M., Salizzoni S. Independent impact of extent of coronary artery disease and percutaneous revascularization on 30-day and 1-year mortality after TAVI: a meta-analysis of adjusted observational results. EuroIntervention. 2018;14(11):e1169-e1177. PMID: 30082258. https://doi.org/10.4244/eij-d-18-00098
- Cao D., Chiarito M., Pagnotta P., Reimers B., Stefanini G.G. Coronary revascularisation in transcatheter aortic valve implantation candidates: Why, who, when? Interv Cardiol. 2018;13(2):69-76. PMID: 29928311; PMCID: PMC5980648. https://doi.org/10.15420/icr.2018:2:2
- Sakai T., Yahagi K., Miura S., Hoshino T., Yokota T., Tanabe K., Ikeda S. Transcatheter aortic valve implantation for patients with lung cancer and aortic valve stenosis. J Thorac Dis. 2018;10(5):E387-E390. PMID: 29998000; PMCID: PMC6006067. https://doi.org/10.21037/jtd.2018.04.83
- Nagata H., Kanzaki R., Kanou T., Ose N., Funaki S., Shintani Y., Minami M., Mizote I., Sakata Y., Maeda K., Kuratani T., Sawa Y., Okumura M. Two cases of lobectomy for lung cancer after transcatheter aortic valve implantation. Surg Case Rep. 2018;4(1):139. PMID: 30511270; PMCID: PMC6277400. https://doi.org/10.1186/s40792-018-0548-7
- Iung B., Delgado V., Rosenhek R., Price S., Prendergast B., Wendler O., De Bonis M., Tribouilloy C., Evangelista A., Bogachev-Prokophiev A., Apor A., Ince H., Laroche C., Popescu B.A., Piérard L., Haude M., Hindricks G., Ruschitzka F., Windecker S., Bax J.J., Maggioni A., Vahanian A., EORP VHD II Investigators. Contemporary presentation and management of valvular heart disease: The EURObservational Research Programme Valvular Heart Disease II Survey. Circulation. 2019;140(14):1156-1169. PMID: 31510787. https://doi.org/10.1161/CIRCULATIONAHA.119.041080
- Iung B., Baron G., Butchart E.G., Delahaye F., Gohlke-Bärwolf C., Levang O.W., Tornos P., Vanoverschelde J.-L., Vermeer F., Boersma E., Ravaud P., Vahanian A. A prospective survey of patients with valvular heart disease in Europe: the Euro Heart Survey on Valvular Heart Disease. Eur Heart J. 2003;24(13):1231-1243. PMID: 12831818. https://doi.org/10.1016/s0195-668x(03)00201-x
- Faggiano P., Frattini S., Zilioli V., Rossi A., Nistri S., Dini F.L., Lorusso R., Tomasi C., Cas L.D. Prevalence of comorbidities and associated cardiac diseases in patients with valve aortic stenosis. Potential implications for the decision-making process. Int J Cardiol. 2012;159(2):94-99. PMID: 21376407. https://doi.org/10.1016/j.ijcard.2011.02.026


