Клинический случай комплексного лечения метастатического рака мочевого пузыря
Автор: Лыков Александр Валерьевич, Знобищев Вячеслав Геннадьевич, Попов Иван Борисович, Кельн Артм Александрович
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Случай из клинической практики
Статья в выпуске: 6 т.18, 2019 года.
Бесплатный доступ
Актуальность. Мышечно-неинвазивный рак мочевого пузыря (РМП) отличается высоким риском рецидивирования после радикального лечения (до 50-60 %), тогда как мышечно-инвазивные формы РМП склонны к метастазированию в 30 % случаев. Первично метастатический рак мочевого пузыря выявляется в 10-15 % случаев. Основным методом лечения локализованного мышечно-неинвазивного РМП является трансуретральная резекция мочевого пузыря, мышечно-инвазивного - радикальная цистэктомия. При лечении метастатического РМП применяется лекарственная терапия, при данной распространенности процесса роль хирургического вмешательства пока не определена. В литературе мы встретили единичные сообщения о метастазэктомии при РМП на этапах комбинированного лечения. Описание клинического случая. Представлен случай успешного лечения метастатического РМП, когда применялись хирургические, лучевые, химиотерапевтические методы лечения. В настоящее время наблюдается ремиссия заболевания. Заключение. Данные зарубежной литературы и наш пример показывают, что удаление метастазов у пациентов с распространенным уротелиальным раком технически осуществимо и может быть безопасно выполнено. Метастазэктомия может положительно влиять на выживаемость. Однако она остается предметом клинических исследований и должна предлагаться только при ограниченной распространенности процесса и хорошем ответе на системную терапию.
Рак мочевого пузыря, уротелиальный рак, хирургическое лечение, метастазэктомия, циторедукция
Короткий адрес: https://sciup.org/140254299
IDR: 140254299 | УДК: 616.62-006.6-033.2-08 | DOI: 10.21294/1814-4861-2019-18-6-140-144
Clinical case of multimodality treatment of metastatic bladder cancer
Background. Bladder cancer is one of the most common cancers. Non-muscle-invasive bladder cancer is characterized by the high frequency of recurrence after radical treatment (up to 50-60 %), and muscle-invasive bladder cancer has a lower recurrence rate (30 %). Primary metastatic bladder cancer (BC) is detected in 10-15 % of cases. Transurethral resection of the bladder is the main treatment modality for non-muscle-invasive BC. For muscle-invasive BC, radical cystectomy is the curative treatment of choice. Chemotherapy is used for the treatment of metastatic BC. The role of surgery for metastatic BC has not yet been determined. There are only a few reports regarding multimodality treatment including metastasectomy for metastatic BC. Case description. We present a clinical case of successful treatment of metastatic BC, we used surgery, radiotherapy, chemotherapy and X-ray endovascular technologies. The patient is alive with no evidence of disease. Conclusion. Our findings are consistent with other reports which indicate that the removal of metastases in patients with advanced urothelial carcinoma is technically feasible and can be safely performed. Metastasectomy can have a positive effect on survival. However, metastasectomy remains the subject of clinical studies, and should be recommended only for patients a good response to systemic therapy.
Текст научной статьи Клинический случай комплексного лечения метастатического рака мочевого пузыря
Рак мочевого пузыря (РМП) – тяжелое ин-валидизирующее заболевание, для которого не разработано системы активного выявления, имеет большую склонность к рецидивированию и прогрессированию [1]. Для локального контроля поверхностных опухолей применяются трансуретральные резекции мочевого пузыря, при мышечно-инвазивном РМП выполняется радикальная цистэктомия с различными вариантами деривации мочи [2, 3]. Примерно у половины пациентов, несмотря на радикальное лечение, заболевание прогрессирует. Местные рецидивы составляют порядка 30 %, в остальных случаях наблюдаются отдаленные метастазы. Около 10–15 % пациентов на момент установки диагноза уже имеют отдаленные метастазы [4].
Основным методом лечения метастатического РМП являются химиотерапевтические комбинации MVAC (метотрексат, винбластин, доксорубицин, карбоплатин) и GC (гемцитабин, цисплатин), которые способствуют увеличению медианы общей выживаемости больных до 14,8 и 13,8 мес соответственно, при частоте ответа опухоли – 46–49 % [1, 5, 6]. Во второй линии терапии применяется препарат группы винкалкалоидов Винфлунин, показавший увеличение общей выживаемости в сравнении с поддерживающей терапией, – 6,9 и 4,3 мес соответственно [7]. Для лечения диссеминированного РМП перспективной выглядит иммунотерапия, показавшая значительную противоопухолевую активность, допустимые профили безопасности и длительный ответ [8–11].
Несмотря на значительный прогресс в лекарственной терапии, у большинства пациентов заболевание в дальнейшем будет прогрессировать. Стоит также отметить, что данные группы препаратов дороги и не всегда доступны. При этом ряд авторов сообщают о допустимости удаления отдаленных очагов в комбинации с системной терапией и возможном влиянии данной стратегии на выживаемость [12–20]. Представленный клинический случай показывает возможные способы контроля прогрессирующего метастатического РМП.
Описание клинического случая
Пациент Ш., 1960 г.р., наблюдается в Многопрофильном клиническом медицинском центре «Медицинский город» (ранее Тюменский областной онкологический диспансер) и Областном урологическом центре АО МСЧ «Нефтяник» с
2010 г. с диагнозом рак мочевого пузыря II стадия (pT2aNxM0).
В марте 2006 г. впервые заметил примесь крови в моче, которая самостоятельно купировалась. За медицинской помощью не обращался. В 2009 г., в связи с периодической макрогематурией направлен в Тюменский областной онкологический диспансер, где выполнена цистоскопия, обнаружена опухоль мочевого пузыря. Тогда от оперативного лечения больной отказался.
Спустя год обратился повторно. 16.08.10 выполнена трансуретральная резекция (ТУР) мочевого пузыря, при которой на правой стенке мочевого пузыря, в зоне устья имелась экзофитная опухоль до 4–5 см в диаметре, рядом отсев до 1 см. Гистологическое заключение: низкодифференцированный веретенообразный вариант переходно-клеточного рака. При обследовании установлен диагноз; рак мочевого пузыря II (pT2aNxM0) стадии. Учитывая низкую степень дифференцировки и большой объем опухоли, на консилиуме решено провести 2 курса адъювантной полихимиотерапии (АПХТ) по схеме MVAC с последующей цистоскопической оценкой. Лечение перенес удовлетворительно. При контрольной цистоскопии, ТУР-биопсии мочевого пузыря признаков злокачественного роста не выявлено. Далее динамически наблюдался.
В августе 2011 г. и августе 2013 г. ТУР мочевого пузыря по поводу поверхностного рецидива. На контроле отметил жалобы на появление образования в правой паховой области, уплотнение правой ягодичной мышцы. На компьютерной томографии органов малого таза (КТ ОМТ) от 27.08.13 обнаружено образование ягодичной области справа, лимфаденопатия паховых лимфоузлов справа. 6.09.13 под внутривенным наркозом выполнена паховая лимфаденэктомия справа (лимфоузел до 3 см, черного цвета, плотный). Вторым этапом выполнена трепанобиопсия образования ягодичной области. Гистологическое заключение: метастаз переходно-клеточного рака. 18.09.13 обсужден на консилиуме, учитывая прогрессирование заболевания, рекомендовано и проведено 4 курса ПХТ по схеме MVAC. При ПЭТ-КТ с 18F-фтордезоксиглюкозой (3.02.14) участков патологического гиперметаболизма в органах и тканях за пределами мочевого пузыря, в пределах диапазона сканирования не отмечено. КТ ОМТ (3.02.14): состояние после ТУР мочевого пузыря, образование ягодичной области (организующаяся гематома). При КТ ОМТ (17.10.14) в мягких
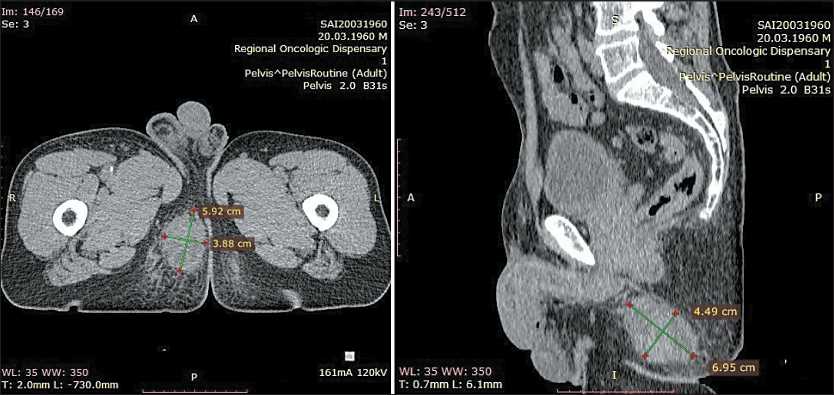
Рис. 1. КТ органов малого таза. Мягкотканное образование до 6 см в ягодичной области справа
тканях ягодичной области справа образование не визуализируется.
В декабре 2014 г. выполнена ТУР мочевого пузыря по поводу поверхностного рецидива. Пациент обсужден на консилиуме, учитывая данные обследования, поражение паховых лимфоузлов справа и рецидивирующую форму рака мочевого пузыря, решено провести лучевое лечение. С марта по май 2015 г. проведена дистанционная гамма-терапия на мочевой пузырь, регионарные и паховые лимфоузлы, СОД 55,7 Гр в 2 этапа. Лечение перенес удовлетворительно.
В декабре 2016 г. на контрольном осмотре отметил уплотнение в правой ягодичной области. При КТ ОМТ в ягодичной области справа ближе к промежности определяется мягкотканное образование до 6 см с неровными контурами, неоднородное, окружающая клетчатка уплотнена, инфильтрирована (рис. 1). При обследовании дополнительных очагов не выявлено. 12.01.17 под эндотрахеальным наркозом выполнено иссечение образования. Опухоль до 6 см в диаметре бурого цвета с участками жидкостных включений плотно прилежит к седалищной кости и сращена с ягодичными мышцами, собственной капсулы не имеет. Гистологическое заключение: морфологическая картина может соответствовать метастазу уротелиального рака, образование удалено в пределах здоровых тканей.
Консилиумом в составе уролога, химиотерапевта и радиолога решено возобновить курсы системной терапии. С июня 2017 г. получил 1 курс интенсивной ПХТ и 4 курса химиотерапии с редукцией дозы цитостатика на 15 % по схеме M-VAC. Последний курс осложнился лейкопенией IV степени (лейкоциты – 0,4×109/л), тромбоцитопенией IV степени (тромбоциты – 23×109/л), стоматитом. В сентябре 2017 г. с интервалом в 3 нед проведено 2 курса внутриартериальной ПХТ под рентген-эндоваскулярным контролем по схеме M-VAC с редукцией дозы цитостатика на 30 %. Достигнута стабилизация опухолевого процесса.
При контрольной цистоскопии (20.08.18) выявлена рецидивная опухоль в мочевом пузыре, выполнена ТУР мочевого пузыря (экзофитная опухоль на узком основании до 2 см). Гистологическое заключение: морфологическая картина папиллярной уротелиальной опухоли низкой степени злокачественности. Достоверных признаков злокачественного роста нет. При обследовании по остальным системам без признаков прогрессирования. В настоящее время пациент продолжает динамическое наблюдение. Жалоб, в том числе со стороны органов мочеполовой системы, не предъявляет.
Обсуждение
Впервые о результатах хирургического удаления одиночных метастазов уротелиального рака в легкие у 6 пациентов сообщили Cowles et al. [17]. Медиана общей выживаемости составила 5 лет, при медиане среди всех пациентов с метастазами РМП – 3 мес. Авторы подчеркивают важность индивидуального подхода в лечении данной группы пациентов.
В клинике MD Anderson проследили результаты лечения 31 пациента c диссеминированным РМП, которым были удалены очаги в легких в 24 (77 %), отдаленные лимфатические узлы – в 4 (13 %), в головном мозге – в 2 (7 %), в подкожной жировой клетчатке – в 1 (3 %) случае [18]. Полная циторедукция была достигнута у 30 (97 %) пациентов. Медиана выживаемости от времени выявления метастазов и от даты резекции составила 31 и 23 мес соответственно. Общая выживаемость в течение 5 лет после метастазэктомии составила 33 %.
J. Lehmann et al. представили ретроспективный анализ наблюдения 44 пациентов с метастатическим уротелиальным раком, которые прошли полную резекцию всех обнаруживаемых метастазов. Метастатические очаги по локализации: забрю- шинные лимфатические узлы (56,8 %), отдаленные лимфатические узлы (11,3 %), легкие (18,2 %), кости (4,5 %), надпочечники (2,3 %), мозг (2,3 %), тонкая кишка (2,3 %) и кожа (2,3 %). Медиана выживаемости от времени выявления метастазов и от даты резекции составила 35 и 27 мес соответственно. Общая выживаемость в течение 5 лет после метастазэктомии для всей когорты больных составила 28 % [19].
T. Nakagawa et al. [20] сообщали об опыте лечения 37 подобных больных, которым чаще удалялись легочные метастазы и лимфатические узлы. Медиана выживаемости составила 35,4 мес от времени обнаружения метастазов и 34,3 мес от даты паллиативной операции. Пятилетняя раково-специфическая выживаемость составила 39,7 %. Авторы делают вывод, что оперативное
Список литературы Клинический случай комплексного лечения метастатического рака мочевого пузыря
- Рак мочевого пузыря. Клинические рекомендации. 2018. [Интернет]. URL: https://oncology-association.ru/files/clinical-guidelines_adults%C2%A0-%20projects2018/rak-mochevogo-puzyrya_pr2018.pdf (дата обращения: 5.02.2019).
- Лыков А.В., Кельн А.А., Зырянов А.В., Пономарев А.В. Проблемы хирургических осложнений радикальной цистэктомии: опыт одной клиники. Уральский медицинский журнал. 2017; (2): 109-113.
- Кельн А.А. Анализ результатов радикального лечения пациентов с мышечно-инвазивным раком мочевого пузыря. Университетская медицина Урала. 2016; 2(5): 27-29.
- Rosenberg J.E., Carroll P.R., Small E.J. Update on chemotherapy for advanced bladder cancer. J Urol. 2005 Jul; 174(1): 14-20. DOI: 10.1097/01.ju.0000162039.38023.5f
- Muscle-invasive and Metastatic Bladder Cancer" EAU Guidelines, 2018 [Internet]. URL: https://uroweb.org/guideline/bladder-cancer-muscleinvasive-and-metastatic (cited 5.02.2019).


