Клинический случай лечения пациента с перипротезной инфекцией после артропластики коленного сустава с использованием оригинального способа изготовления артикулирующего спейсера
Автор: Ефремов И.М., Мидленко В.И.
Журнал: Ульяновский медико-биологический журнал @medbio-ulsu
Рубрика: Клиническая медицина
Статья в выпуске: 1, 2024 года.
Бесплатный доступ
Перипротезная инфекция (ППИ) является одним из самых тяжелых осложнений тотального эндопротезирования коленного сустава. В лечении пациентов с хронической глубокой ППИ после артропластики коленного сустава используют двухэтапное ревизионное эндопротезирование с промежуточной установкой антимикробного спейсера коленного сустава. Преимуществом артикулирующего спейсера является возможность сохранения двигательной активности до реимплантации постоянного эндопротеза. Однако использование для изготовления фабричных форм, в т.ч. созданных с помощью 3D-печати, в рутинной клинической практике не всегда возможно, учитывая высокую стоимость и ограниченную доступность оборудования. Представлен клинический случай пациента с хронической глубокой ППИ после тотального эндопротезирования левого коленного сустава, в лечении которого использовался оригинальный способ интраоперационного изготовления тибиального компонента артикулирующего спейсера. Методика включает изготовление в стерильных условиях при помощи примерочного пластикового вкладыша и пластичной полимерной массы формы, в которую укладывают костный цемент, импрегнированный антибактериальными препаратами. После застывания костного цемента из формы извлекают готовый тибиальный компонент спейсера. Простерилизованный бедренный и изготовленный тибиальный компоненты спейсера имплантируют при помощи костного цемента, импрегнированного антибиотиками. При отсутствии технической возможности использования примерочных вкладышей может применяться ранее удаленный пластиковый вкладыш от эндопротеза. Разработанный оригинальный метод имеет ряд преимуществ, в т.ч. возможность индивидуального подбора размеров спейсера, самостоятельного добавления необходимого количества и вида антибактериальных препаратов, а также экономическую целесообразность. Успешное купирование инфекции у пациента позволило провести в дальнейшем ревизионное эндопротезирование с установкой постоянного эндопротеза.
Перипротезная инфекция, артикулирующий спейсер, артропластика, костный цемент
Короткий адрес: https://sciup.org/14129940
IDR: 14129940 | УДК: 617-089.844 | DOI: 10.34014/2227-1848-2024-1-73-81
Management of a periprosthetic infection after total left knee replacement using an original method for articulating spacer manufacturing: case study
Periprosthetic infection (PPI) is one of the most severe complications after total knee replacement. While managing patients with chronic deep PPI after total knee replacement, two-stage revision arthroplasty with intermediate installation of an antimicrobial knee joint spacer is used. The advantage of an articulating spacer is the ability to maintain motor activity until reimplantation of a permanent endoprosthesis. However, factory moulds including 3D-printed are not always available in routine clinical practice, given the high cost and limited equipment accessibility. We present a case study of a patient with chronic deep PPI after total left knee replacement. An original method of intraoperative manufacturing of the tibial component of the articulating spacer was used in the course of treatment. The technique involves sterile mould making using a fitting plastic liner and soft polymer mass. Bone cement impregnated with antibacterial drugs is placed into the mould. When the bone cement hardens, a tibial spacer component is ready. The sterilized femoral and fabricated tibial spacer components are implanted using antibiotic-impregnated bone cement. If it is not technically possible to use fitting inserts, a previously removed plastic insert from the endoprosthesis can be used. The developed original method has a number of advantages: individual selection of spacer sizes, independent addition of the required quantity and type of antibacterial drugs, and economic efficiency. Successful infection relief in the patient allowed further revision endoprosthetics with installation of a permanent endoprosthesis.
Текст научной статьи Клинический случай лечения пациента с перипротезной инфекцией после артропластики коленного сустава с использованием оригинального способа изготовления артикулирующего спейсера
Введение. Перипротезная инфекция (ППИ) является одним из самых тяжелых осложнений тотального эндопротезирования коленного сустава (ТЭКС) [1]. Частота развития ППИ, по данным различных авторов, достигает 2 % [2]. Золотым стандартом лечения пациентов с хронической глубокой ППИ после артропластики коленного сустава является двухэтапное ревизионное эндопротезирование с промежуточной установкой антимикробного спейсера коленного сустава [3–5].
В настоящее время используются блоковидные или артикулирующие варианты анти- микробных спейсеров. Основным преимуществом артикулирующего спейсера коленного сустава является возможность осуществления движений в коленном суставе в период ожидания реимплантации постоянного эндопротеза [6, 7]. Однако использование фабрично изготовленных артикулирующих спейсеров в условиях рутинной клинической практики не всегда возможно из-за ограниченной доступности и высокой стоимости оборудования.
Приводим клинический случай лечения пациента с использованием оригинальной методики интраоперационного изготовления тибиального компонента артикулирующего спейсера.
Пациент М., 61 г., поступил в клинику в марте 2022 г. с диагнозом «хроническая глубокая перипротезная инфекция после ТЭКС».
Анамнез. Пациенту в связи с болевым синдромом, обусловленным гонартрозом, в августе 2021 г. выполнено первичное цементное ТЭКС слева. В послеоперационном периоде получал базисную терапию, включавшую антикоагулянты, инфузионную терапию перевязки, лечебную физкультуру. Выписан из стационара через 8 дней. В раннем послеоперационном периоде обращался за консультацией в связи с болевым синдромом. Пациенту назначено обследование с целью исключения ППИ, однако пациент на повторный прием не явился.
Через 20 дней пациент был госпитализирован в связи с развитием внебольничной пневмонии, обусловленной COVID-19. Во время стационарного лечения в ковидном госпитале у пациента развилась ППИ, по поводу которой была проведена телемедицинская консультация со специалистом федеральной клиники. Пациенту было назначено динамическое наблюдение и комбинированная пероральная антибиотикотерапия (АБТ), включавшая (по результатам бактериологических анализов) ципрофлоксацин 500 мг 2 раза в сутки внутрь 2 нед. и ко-тримоксазол 960 мг 2 раза в сутки внутрь 4 нед. Однако согласно рекомендациям пациенту на тот момент была показана ревизионная артропластика коленного сустава с полным удалением компонентов эндопротеза [8]. Несмотря на проводимую терапию улучшения не наблюдалось, болевой синдром не купировался в связи с чем пациент обращался за врачебной помощью. В феврале 2022 г. пациент повторно перенес COVID-19 (лечился амбулаторно). Настоящая госпитализация (март 2022 г.) в клинику травматологии и ортопедии была обусловлена необходимостью проведения ревизионного эндопротезирования коленного сустава.
Жалобы. При осмотре пациент предъявлял жалобы на постоянные боли в левом коленном суставе, усиливающиеся при физической нагрузке, ограничение объема движений в оперированном суставе, длительное (в течение нескольких недель) повышение температуры тела до субфебрильных значений, отек области коленного сустава, нарушение функции.
Ортопедический статус. Пациент передвигался самостоятельно при помощи трости. Осевая нагрузка на левую ногу была болезненная. Визуально отмечался отек левого коленного сустава и болезненность при пальпации левого коленного сустава. Активные и пассивные движения в суставе резко ограничены из-за болевого синдрома: разгибание 170°, сгибание 70–75°. Отмечалась небольшая гиперемия и гипертермия кожи над левым коленным суставом. Симптом баллотирования надколенника отрицательный. Чувствительность на периферии левой нижней конечности сохранена. Кожа левой стопы теплая на ощупь. Пульс на артерии тыла стопы и задней большеберцовой артерии сохранен. Послеоперационный рубец по передней поверхности левого коленного сустава без патологических изменений. Свищей и ран в области левого коленного сустава нет.
Бактериологическое исследование. При микробиологическом исследовании пунктата левого коленного сустава первично выделен Staphylococcus capitis . При повторном микробиологическом исследовании пунктата левого коленного сустава выделен Staphylococcus ep-idermidis менее 104 КОЕ/мл, устойчивый к стафилококковому бактериофагу, ампициллину, оксациллину, эритромицину, амоксициллину + клавуланату.
Лабораторная диагностика. СОЭ 73 мм/ч, С-реактивный белок 13,8 мг/л.
Рентгенологические данные. По данным рентгенографии и мультиспиральной компьютерной томографии: тотальный эндопротез левого коленного сустава NexGen® LPS (производитель Zimmer Biomet, США); локальных очагов деструкции костной ткани не выявлено; ось конечности сохранена; четких признаков септической нестабильности компонентов эндопротеза левого коленного сустава не выявлено.
Предоперационное планирование. Учитывая наличие хронической ППИ после
ТЭКС, согласно критериям Второй Международной согласительной конференции по скелетно-мышечной инфекции (ICM – The International Consensus Meeting on Musculoskeletal Infection, 2018) [8], в соответствии с которыми диагноз ППИ подтверждается при наличии одного из двух «больших» диагностических критериев или трех из пяти «малых» критериев, было принято решение о проведении у пациента двухэтапного ревизионного эндопротезирования левого коленного сустава с промежуточной установкой артикулирующего спейсера и длительной АБТ.
18.03.2022 под регионарной спинномозговой анестезией произведена стандартная артротомия левого коленного сустава медиальным парапателлярным доступом. При помощи ревизионного инструментария компоненты эндопротеза удалены с экономной потерей костной ткани бедра и большеберцовой кости (тип F1/Т1 по классификации AORI (Anderson Orthopaedic Research Institute, США)) (рис. 1).
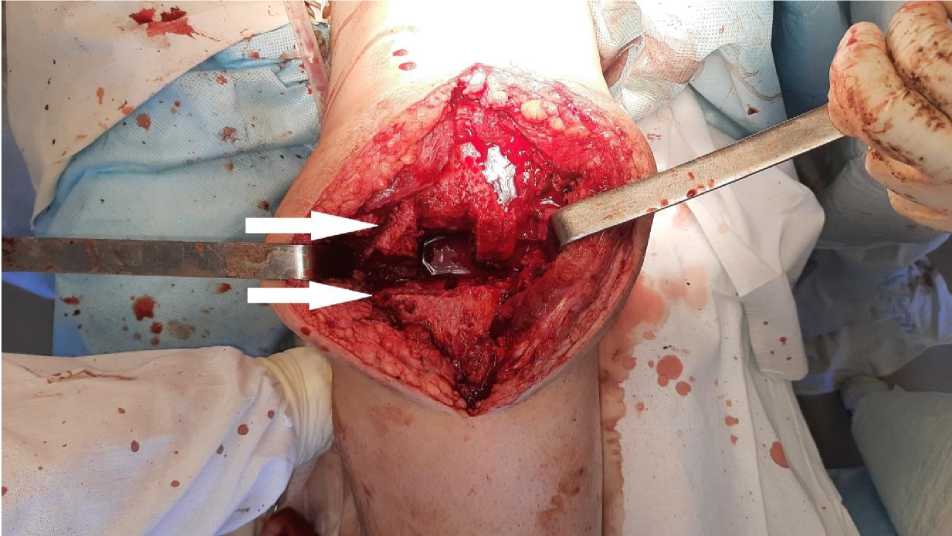
Рис. 1. Дефекты костной ткани бедра и большеберцовой кости F1/T1 по AORI (дефекты указаны стрелками)
Fig. 1. F1/T1 AORI bone defects of the femur and tibia (arrows indicate bone defects)
Бедренный компонент протеза обработан от остатков костного цемента и стерилизован путем автоклавирования. Выполнены радикальный дебридмент, ультразвуковая кавитация раны и пульс-лаваж раны системой Pulsavac® Plus Wound Debridement System (Zimmer Biomet, США) 4000 мл 0,9 % физического раствора с активным вакуумированием.
Оригинальным способом из дозы костного цемента Refobacin Revision 1×40 (BIOMET, Франция) был изготовлен тибиаль-ный компонент артикулирующего спейсера, соответствующий форме и размеру вкладыша E-F/5-6/12 мм LPS (Zimmer Biomet, США), который армирован титановым винтом (рис. 2).
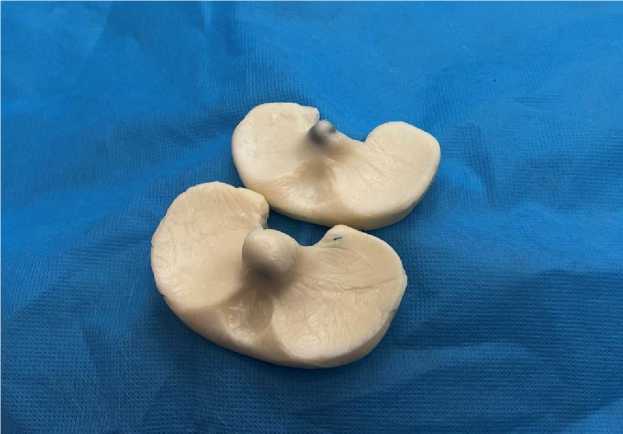
Рис. 2. Внешний вид тибиального компонента спейсера
Fig. 2. Tibial component of the spacer
Компоненты артикулирующего спейсера имплантированы при помощи дозы костного цемента 1×40 Synicem 1 (Synimed, Франция), импрегнированного порошком антибактери- ального препарата ванкомицин 4000 мг (рис. 3, 4). Рана послойно ушита и дренирована по Редону. Дренажи удалены на следующий день после операции.
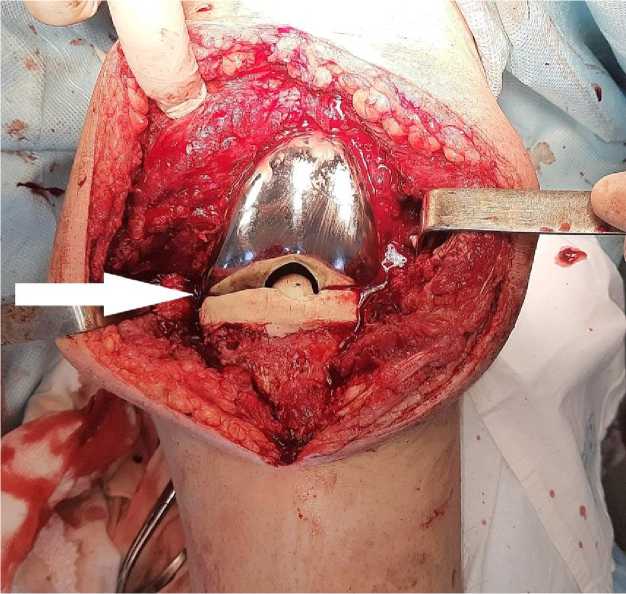
Рис. 3. Внешний вид имплантированного артикулирующего спейсера (указан стрелками) левого коленного сустава
Fig. 3. Implanted articulating spacer of the left knee joint (the arrow indicates the articulating spacer)
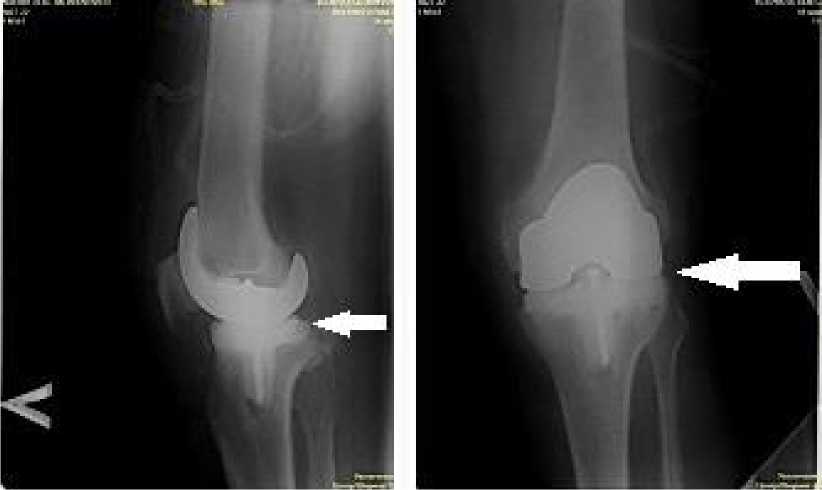
Рис. 4. Рентгенограммы левого коленного сустава после имплантации артикулирующего спейсера (указан стрелками)
Fig. 4. Radiographs of the left knee joint after implantation of the articulating spacer (arrows indicate the articulating spacer)
По согласованию с клиническим фармакологом в послеоперационном периоде пациенту назначена комбинированная парентеральная антибактериальная терапия: ванкомицин 1500 мг 2 раза в сутки в/в капельно и левофлоксацин 500 мг 2 раза в сутки в/в капельно 10 дней с переходом на пероральную АБТ на амбулаторный период лечения (левофлоксацин 500 мг 2 раза в сутки и ко-тримок-сазол 960 мг 2 раза в сутки внутрь на 21 день). Антикоагулянтная терапия: эноксапарин натрия 40 мг 2 раза в сутки п/к на период стационарного лечения, переход на прием дабигат-рана этексилата 220 мг 1 раз в сутки внутрь 30 дней.
Рана зажила первичным натяжением. ППИ купирована, что позволило провести пациенту ревизионное эндопротезирование с установкой постоянного эндопротеза по программе высокотехнологичной медицинской помощи в федеральной клинике.
Обсуждение. Известны различные типы артикулирующих спейсеров коленного сустава: фабрично изготовленные (преформированные) или изготовленные интраоперационно.
Преформированные спейсеры выпускаются различными зарубежными производителями [10]. Основными недостатками префор-мированных спейсеров являются ограниченный модельный размерный ряд компонентов артикулирующего спейсера, низкое содержание антибактериальных препаратов в составе спейсера, ограниченный выбор антибактериальных препаратов, входящих в состав компонентов спейсера, высокая стоимость изделий.
В то же время известны различные типы спейсеров, изготовленных интраоперационно: при помощи фабрично изготовленных литьевых форм, при помощи форм, индивидуально произведенных 3D-печатью, по методу Hoffman или изготовленные вручную.
Недостатками спейсеров, сделанных на основе литьевых форм, являются сложность изготовления формообразующих изделий, необходимость наличия в операционной обширной модельной линейки для изготовления спейсера.
Спейсеры, изготовленные при помощи фабричных литьевых форм, обладают высокой стоимостью, в ряде случаев требуют ис- пользования дорогостоящих одноразовых расходных материалов (миксер и пистолет для смешивания и введения костного цемента), а также наличия в операционной обширной мо-дельнойлинейкизаливочных форм [7].
Недостатками спейсеров, изготовленных при помощи индивидуальных форм по технологии 3D-печати, являются сложность и дороговизна процесса изготовления формообразующих элементов.
Необходимо отметить экономическую составляющую применения промышленно изготовленных компонентов спейсера или форм для их изготовления. Ввиду высокой стоимости их использование в рамках оказания медицинской помощи по программе обязательного медицинского страхования или программе высокотехнологичной медицинской помощи становится невозможным и/или нецелесообразным.
Недостатком спейсеров, изготовленных интраоперационно вручную, является снижение артикулирующих свойств спейсера за счет повышенной силы трения ввиду наличия неровностей в узле трения.
В представленном клиническом случае использовался оригинальный способ интраоперационного изготовления артикулирующего спейсера. Предлагаемый способ заключается в следующем. В процессе ревизионной операции, после удаления компонентов инфицированного эндопротеза и проведения радикального дебридмента, определяют необходимый размер и высоту тибиального компонента спейсера (с целью установления баланса сгибательного и разгибательного промежутков, сохранения высоты суставной линии). Удаленный бедренный компонент эндопротеза тщательно очищают от остатков костного цемента и подвергают стерилизации путем авто- клавирования. В стерильных условиях при помощи примерочного пластикового вкладыша необходимого размера и пластичной полимерной массы, покрытой стерильной пленкой, изготавливают форму, в которую укладывают костный цемент, импрегнированный антибактериальными препаратами. После застывания костного цемента из формы извлекают готовый тибиальный компонент спейсера. При отсутствии технической возможности использования примерочных вкладышей применяют ранее удаленный пластиковый вкладыш от эндопротеза, но при отсутствии грубых макроскопических дефектов. Простерилизованный бедренный и изготовленный тибиальный компоненты спейсера имплантируют при помощи костного цемента, импрегнированного антибиотиками (в представленном клиническом случае – ванкомицином).
Преимуществами данного способа являются:
– интраоперационное изготовление спей-сера коленного сустава;
– возможность индивидуального подбора размеров спейсера;
– возможность самостоятельного добавления необходимого количества и вида антибактериального препарата;
– простота и быстрота изготовления спей-сера;
– низкая стоимость спейсера.
Заключение. Представленный клинический случай является демонстрацией успешного купирования перипротезной инфекции при комплексном лечении с использованием оригинального метода интраоперационного изготовления артикулирующего спейсера без применения дорогостоящих технологий и комплектующих.
Список литературы Клинический случай лечения пациента с перипротезной инфекцией после артропластики коленного сустава с использованием оригинального способа изготовления артикулирующего спейсера
- Иванов П.П., Корнилов Н.Н., Куляба Т.А. Ревизионные хирургические вмешательства при пери-протезной инфекции коленного сустава (обзор литературы). Кафедра травматологии и ортопедии. 2017; 1: 35-43.
- Джакофски Д.Дж., Хедли Э.К. Ревизионное эндопротезирование коленного сустава: руководство для врачей. Москва: ГЭОТАР-Медиа; 2015. 320. ISBN 978-5-9704-3186-3.
- Клюшин Н.М., Абабков Ю.В., Ермаков А.М. Наш опыт лечения перипротезной инфекции коленного сустава. Гений ортопедии. 2019; 2: 162-171. DOI: 10.18019/1028-4427-2019-25-2-162-171.
- Кюн Клаус-Дитер. Перипротезная инфекция. Перспективы диагностики, особенности лечения, стратегии профилактики и их экономические издержки. Москва; 2022. 328. ISBN 978-5-9704-2966-2.
- Signore A., Sconfienza L.M., Borens O. Consensus document for the diagnosis of prosthetic joint infections: a joint paper by the EANM, EBJIS, and ESR (with ESCMID endorsement). Eur J Nucl Med Mol Imaging. 2019; 46 (4): 971-988. DOI: 10.1007/s00259-019-4263-9.
- Преображенский П.М., Божкова С.А., Пантелеев А.Н. Свищевая и несвищевая формы перипро-тезной инфекции коленного сустава: исходы лечения. Травматология и ортопедия России. 2020; 4: 21-31. URL: https://journal.rniito.org/jour/artide/view/1541/1011 (дата обращения: 18.06.2023). DOI: 10.21823/2311 -2905-2020-26-4-21-31.
- Куляба Т.А., Корнилов Н.Н. Ревизионная артропластика коленного сустава. Санкт-Петербург: РНИИТО им. Р.Р. Вредена; 2016. 192.
- Карманный справочник диагностики и лечения перипротезной инфекции суставов (ПИС) (версия 8: ноябрь 2018). URL: www.pro-implant-foundation.org (дата обращения: 08.06.2023).
- Тихилов Р.М., Божкова С.А., Шубняков И.И., ред. Материалы Второй Международной согласительной конференции по скелетно-мышечной инфекции. Санкт-Петербург: РНИИТО им. Р.Р. Вредена; 2019. 314.
- Silvestre A., Almeida F., Renovell P. Revision of infected total knee arthroplasty: two-stage reimplantation using an antibiotic-impregnated static spacer. Clin. Orthop. Surg. 2013; 5 (3): 180-187. DOI: 10.4055/cios.2013.5.3.18.
- Бо Лю, Тихилов Р.М., Шубников И.И. Анализ эффективности санирующих операций при параэн-допротезной инфекции. Травматология и ортопедия России. 2014; 2: 22-29.


