Клинический случай ранней диагностики холангиокарциномына фоне хронического псевдотуморозного панкреатита с помощью метода
Автор: Сазонов Дмитрий Валерьевич, Иванов Юрий Викторович, Шабловский Олег Радомирович, Данилевская Олеся Васильевна, Забозлаев Федор Георгиевич, Лебедев Дмитрий Петрович, Сорокина Анастасия Викторовна, Сафронова Татьяна Сергеевна
Журнал: Клиническая практика @clinpractice
Рубрика: Случай из практики
Статья в выпуске: 3 (15), 2013 года.
Бесплатный доступ
Приведено клиническое наблюдение редкого заболевания – холангиокарциномы общего желчного протока, развившейся на фоне хронического псевдотуморозного панкреатита. Отражены сложности диагностики на ранней стадии заболевания. Впервые при данной патологии с диагностической целью применен метод кофокальной лазерной эндомикроскопии, позволивший уточнить и верифицировать диагноз. Авторы предполагают, что при заболеваниях панкреато-билиарной зоны метод кофокальной лазерной эндомикроскопии может иметь решающее значение при неэффективности или малоинформативности других методов.
Холангиокарцинома, конфокальная лазерная эндомикроскопия, хронический псевдотуморозный панкреатит, стент
Короткий адрес: https://sciup.org/14338460
IDR: 14338460
Case history of early diagnostic of cholangiocarcinoma in patient with chronic pseudotumor-like pancreatitis using the confocal laser endomicroscopy
It is described the clinical case of a rare disease – cholangiocarcinoma of the common bile duct, which developed in patient with chronic pseudotumor-like pancreatitis. It is reflected the complexity of diagnosis at an early stage of the disease. The method of confocal laser endomicroscopy was for the first time applied for the given pathology for diagnostic purposes that allowed to clarify and verify the diagnosis. The authors suggest that in diseases of the pancreato-biliary zone the method of confocal laser endomicroscopy can be crucial in cases of inefficiency or uninformativeness of other methods.
Текст научной статьи Клинический случай ранней диагностики холангиокарциномына фоне хронического псевдотуморозного панкреатита с помощью метода
Введение . Холангиокарцинома (карцинома желчных протоков) – относительно редкая злокачественная опухоль, исходящая из мутировавших эпителиальных клеток желчных протоков, которая по своей гистологической структуре относится к аденокарциноме.
В странах Европы и Северной Америки заболеваемость холангиокарциномой составляет
1-2 случая на 100 000 населения в год, но её уровень растет в течение последних десятилетий [1]. Опухоль поражает преимущественно внепеченочные желчные протоки: 60-80 % – в воротах печени (опухоль Клацкина) и 10-30 % – в дистальных отделах протока. В большинстве случаев холангиокарцинома развивается на фоне первичного склерозирующего холангита
(ПСХ), сопровождающегося язвенным колитом. Считается, что риск развития холангио-карциномы повышается при следующих врожденных кистозных заболеваниях: фиброз печени, кистозные расширения внутрнпеченочных протоков (синдром Кароли), кисты холедоха, поликистоз печени, микрогамартомы (комплексы фон Мейенберга), а также при билиарном циррозе [2]. В то же время, у большинства пациентов с холангиокарциномой специфические факторы риска в анамнезе отсутствуют.
Некоторые авторы отмечают и тот факт, что риск развития карциномы внепеченочных желчных протоков через 10 лет и более после холецистэктомии значительно снижается, что, возможно, свидетельствует о связи опухоли с желчными камнями [1, 3].
Своевременная диагностика холангиокар-циномы, когда еще возможно выполнение радикальной операции, представляет определенные трудности и зависит как от возможностей имеющейся диагностической аппаратуры, так и от квалификации врачей диагностов. Затрудняет диагностику и тот факт, что при ранней стадии заболевания характерно отсутствие какой-либо симптоматики, и его обнаружение является случайной находкой при обследовании по поводу другого заболевания.
В тех случаях, когда у пациентов уже имеется сопутствующая патология панкреатобили-арной зоны, ранняя диагностика холангиокар-циномы значительно затруднена вследствие наличия морфо-функциональных изменений данной области, а также ориентированности врача на установленную ранее патологию.
Особенно сложна диагностика холангиокар-циномы у больных, страдающих хроническим псевдотуморозным панкреатитом, холангитом, рубцовыми стриктурами внепеченочных желчных протоков, так как в большинстве случаев одной из составляющих частей комплексного лечения является эндоскопическое протезирование или стентирование желчных протоков. Находящийся в просвете протока стент делает невозможным взятие биопсийного материала для цито- или гистологического исследования без предварительного его удаления. Кроме того, длительное нахождение стента в желчном протоке неизбежно вызывает визуальные и морфологические изменения эпителия, что затрудняет своевременную диагностику холан-гиокарциномы [4].
Некоторые авторы считают, что длительное течение хронического индуративного панкреатита или склерозирующего холангита, превышающее 10 лет, может сопровождаться развитием рака поджелудочной железы или холанги-окарциномы [2, 3]. Хирургическое лечение хо-лангиокарциномы малоэффективно, в основном вследствие малой доступности опухоли и поздней ее диагностики. Большинство пациентов обращается за медицинской помощью на этапе, когда опухоль уже является неоперабельной, так как на ранних стадиях заболевание течет малосимптомно. В этом случае основными методами лечения являются адъювантная химиотерапия и лучевая терапия, паллиативная помощь. При неоперабельной опухоли аргументом в пользу рентгенохирургических и эндоскопических вмешательств служит устранение желтухи и зуда у умирающих больных.
Имеющиеся в настоящее время методы и способы диагностики данной патологии, включающие спиральную компьютерную томографию (СКТ), магниторезонансную холангиопанкреатографию (МРХПГ), эндоскопическое ультразвуковое исследование (ЭУЗИ), эндоскопическую ретроградную холангиопанкреатографию (ЭРХПГ), бывают не всегда информативны, оставляя проблему ранней диагностики холангиокарциномы актуальной и не до конца решенной. В связи с этим растет спрос на новые технологии, позволяющие с высокой достоверностью выявить рак поджелудочной железы или холангиокарциному у пациентов с хроническим псевдотуморозным панкреатитом, рубцовым стенозом общего желчного протока и механической желтухой, перенесших эндопротезирование желчных протоков.
В последние годы в качестве одного из таких методов рассматривается конфокальная лазерная эндомикроскопия (КЛЭМ), оборудование (Cellvizio) для которой разработано компанией "Maunakea tech, France" [5, 6].
В качестве примера, показывающего высокую диагностическую возможность метода КЛЭМ в ранней диагностике холангиокарцино-мы на фоне длительно существующего хронического псевдотуморозного панкреатита, приводим собственное клиническое наблюдение.
Клиническое наблюдение . Пациент Г., 1960 г.р., наблюдался в ФГБУ ФНКЦ ФМБА России с 2005 г., проходя курсы стационарного лечения в отделениях гастроэнтерологии и хирургии с клиническим диагнозом: хронический псевдотуморозный панкреатит.
Из анамнеза известно, что в начале 2005 г. перенес панкреонекроз. В июле 2005 г. в связи с развившимся после перенесенного панкрео-некроза стенозом двенадцатиперстной кишки выполнена операция: лапаротомия, гастро-эн-теростомия на длинной петле с межкишечным соустьем по Брауну. 30 июня 2006 г. по поводу механической желтухи производится ЭРХПГ, выявляются признаки псевдотуморозного панкреатита, сдавление интрапанкреатической части общего желчного протока воспалительным инфильтратом головки поджелудочной железы, расширение общего желчного и панкреатического протоков. Было произведено би-лиодигестивное эндопротезирование с эффектом, желтуха разрешилась.
В течении 2007 - 2010 гг. пациенту выполнялись плановые рентгеноэндоскопические вмешательства по замене стентов, назо-билиарные дренирования с целью декомпрессии билиарной системы. Следует отметить, что в периоды между госпитализациями в стационар пациент не соблюдал диету, злоупотреблял алкоголем, не принимал назначенные препараты и в то же время отказывался от возможной радикальной операции (гастропанкреатодуоденальная резекция). В октябре 2010 г. возник рецидив механической желтухи, в связи с чем в стационаре по месту жительства больному была выполнена операция: лапаротомия, наружнее дренирование общего желчного протока, желтуха купирована.
В 2010 - 2011 гг. проходил неоднократное стационарное лечение по поводу хронического псевдотуморозного панкреатита, острого гнойного холангита, проводилась комплексная консервативная терапия с эффектом. В марте 2011 г. при контрольном обследовании, учитывая категоричный отказ пациента от радикальной операции, короткий срок службы пластиковых эдопротезов в связи с их постоянной обтурацией билиарным сладжем и большие потери желчи по наружнему дренажу, больному был установлен нитиноловый саморасправляющийся стент непокрытого типа с одновременным удалением наружнего дренажа из общего желчного протока (рис. 1). В мае 2012 г. в связи с рецидивом механической желтухи, обусловленной обтурацией стента гиперплазированной слизистой оболочкой общего желчного протока, пациенту выполнено чрескожно-чреспеченочное наружне-внутреннее дренирование общего желчного протока (рис. 2, 3).
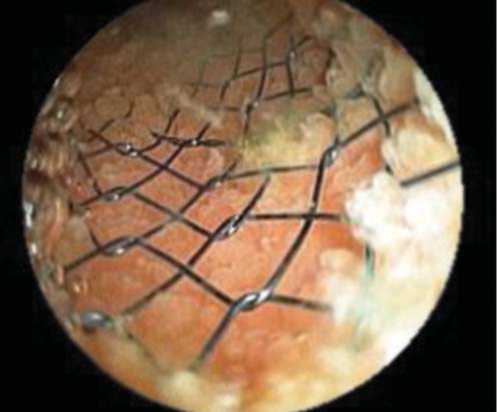
Рис. 1. Эндофото. Общий вид имплантированного саморасправ-ляющегося нитинолового стента в общий желчный проток.
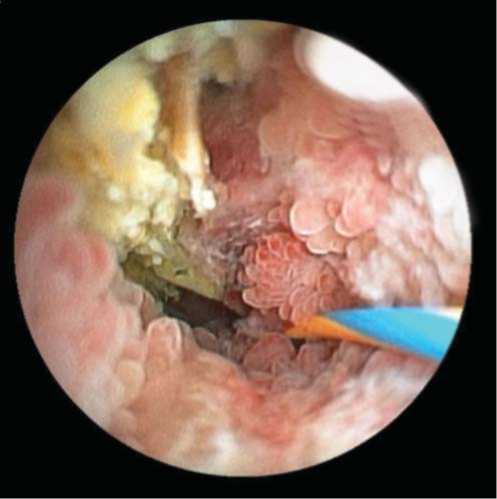
Рис. 2. Эндофото. Общий вид гиперплазии слизистого слоя общего желчного протока с обтурацией нитинолового стента.
При выполнении фистулографии и ЭГДС с осмотром большого дуоденального сосочка возникли подозрения на возможное опухолевое поражение дистальной части общего желчного протока. Была выполнена щеточная биопсия, однако убедительных данных за онкологический процесс получено не было.
С целью уточнения и возможной верификации диагноза впервые в ФНКЦ ФМБА России был использован новый метод – КЛЭМ,
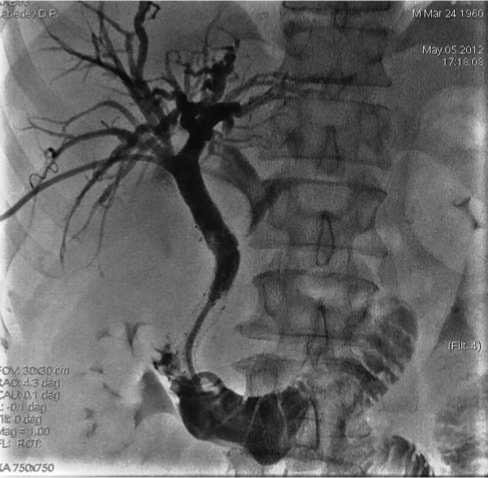
Рис. 3. Чрескожно-чреспеченочная холангиограмма. Общий вид наружне-внутреннего дренирования общего желчного протока.
который был освоен и внедрен эндоскопической службой Центра в 2011 г. с целью дифференциальной диагностики заболеваний легких. Через сформированный канал гепатикохо-лангиостомы проведен гибкий эндоскоп EB-
530T. Через инструментальный канал эндоскопа с помощью минизонда "Cholangioflex" выполнена КЛЭМ (рис. 4).
Микроэндоскопическая картина позволила выявить наличие регулярных крипт и капил-
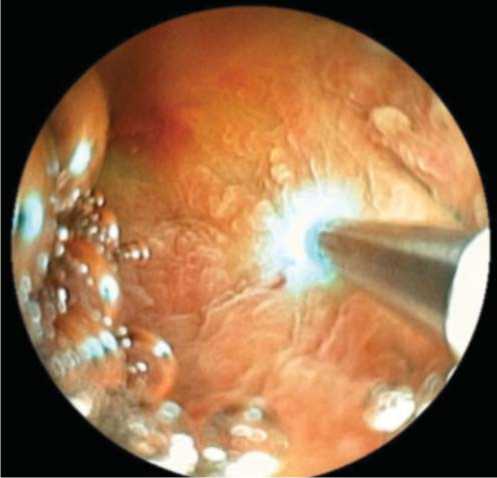
Рис. 4. Эндофото. Сеанс КЛЭМ слизистого слоя общего желчного протока.
ляров в зоне гиперплазии слизистой оболочки холедоха. На этом фоне при последовательном сканировании мы обнаружили фокус нерегулярных, расширенных сосудов с подтеканием контраста, широкие черные извитые полосы, толщиной более 20 µm, нерегулярные скопления черных округлых элементов. Это было расценено как предиктор холангиокарциномы, что подтверждено результатами планового гистологического исследования после выполненной биопсии (рис. 5 - 9).

Рис. 5. Микроскопическая картина неизмененного слизистого слоя общего желчного протока при КЛЭМ.
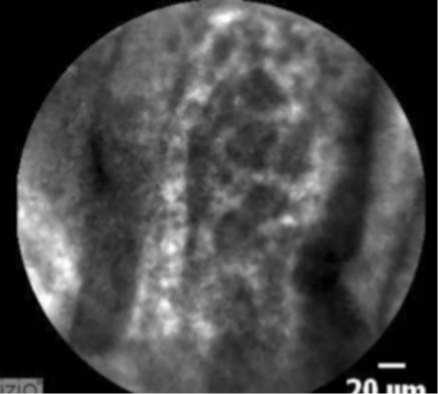
Рис. 6. Микроскопическая картина гиперплазии кубического эпителия общего желчного протока при КЛЭМ.
Пациент консультирован онкологом, назначена адьювантная химиолучевая терапия.
Обсуждение . Гиперпластический (псевдо-туморозный) хронический панкреатит встречается у 4-6% стационарных больных хрони-

Рис. 7. Микроскопическая картина фокуса холангиокарциномы общего желчного протока при КЛЭМ.
ческим панкреатитом. Осложнения при заболевании такой формы бывают у 30% больных и развиваются примерно через 7-15 лет [2]. Склеротические процессы в головке поджелудочной железы приводят к клинической картине, напоминающей сдавление протоков желчевыводящих путей и протока поджелудочной железы (Вирсунгова протока). Нарушение оттока желчи в таких случаях вызывает механи- ческую желтуху. При алкогольном и наследственном хроническом панкреатите наблюдается реакция преципитации кальция и белков внутри панкреатических протоков. В норме преципитация предотвращается ПСП-белками, которые секретируются ацинальными клетками. Уровень данного вида белков у больных хроническим панкреатитом заметно снижен, что способствует повышению кальция в панкреатическом соке, его микрокристаллизации. В просвете протока образуются кальцина-ты, закупоривающие протоки, происходит повышение давления в них. В конечном счете развивается фиброз.
В последние годы эндопротезирование желчных протоков широко используется для лечения хронического панкреатита, осложненного развитием стеноза общего желчного протока, механической желтухой. Впервые эндопротезирование общего желчного протока произвел Soehendra и Reynders-Frederix в 1979 г. [3]. В руках опытного эндоскописта эта методика не кажется столь сложной, а низкая травматичность и эффективность делают ее привлекательной в клинической практике. В настоящее время используются различные эндопротезы – нитиноловые саморасширяющиеся стенты и пластиковые стенты (рис. 10). Основным недостатком последних является высокая вероятность обтурации протеза через 2-6 меся-
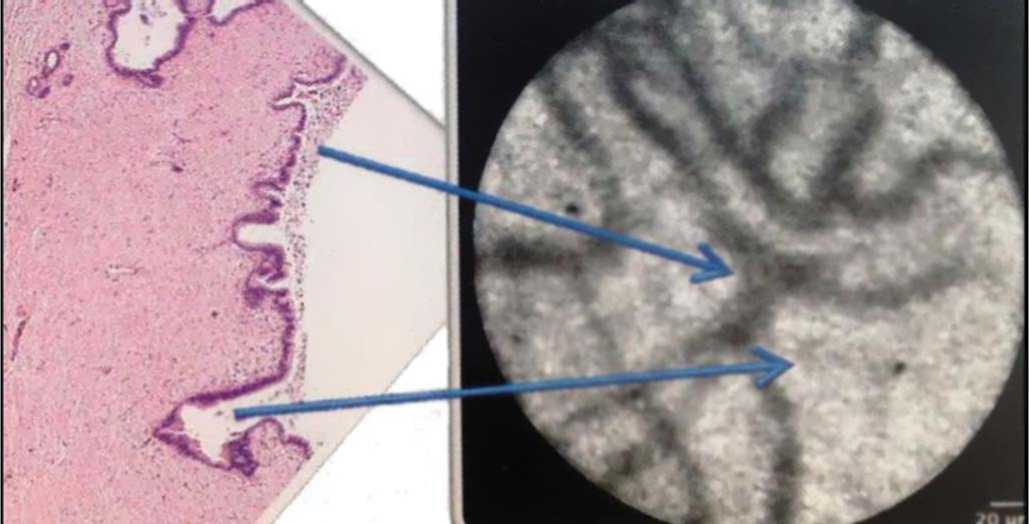
Рис. 8. Сопоставление гистологических и КЛЭМ образцов неизмененной слизистой оболочки общего желчного протока. Клетки и межклеточные пространства показаны стрелками.
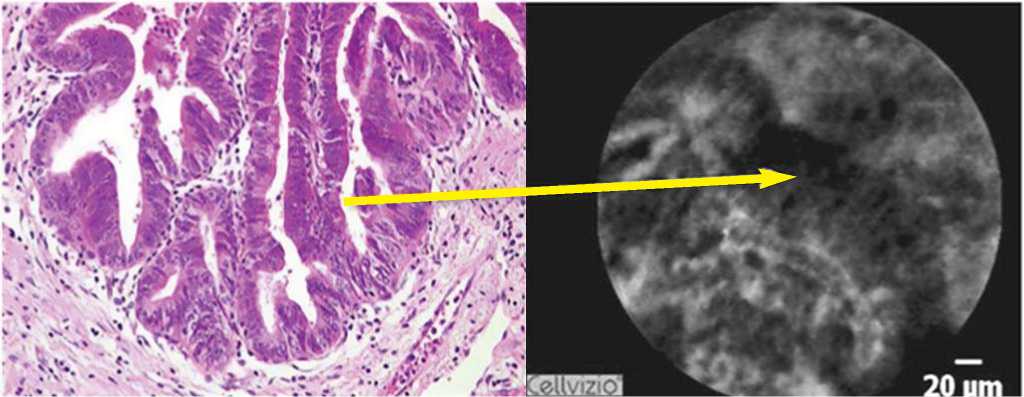
Рис. 9. Сопоставление гистологических и КЛЭМ образцов слизистой оболочки общего желчного протока с фокусом холангиокарциномы (показана стрелкой).
цев после постановки в результате отложения на нем солей желчных кислот и бактериальных пленок. Для поддержания их просвета свободным необходимо проводить регулярные санационные эндоскопические промывания просвета протеза, что в итоге не увеличивает срок их действия, а только позволяет сохранить на короткое время дренажную функцию [4].
Металлические саморасправляющиеся стенты сохраняют проходимость дольше, чем пластиковые – около 6 месяцев и более. Использование металлических стентов ассоциируется с риском прорастания гиперплазированной ткани эпителия протоков или опухоли, что требует последующей реканализации. Со временем стояние саморасправляющего билиарного стента непокрытого типа может осложняться гиперплазией кубического эпителия общего желчного протока, что приводит к обтурации стента. С целью устранения указанного эффекта используют покрытые нитиноловые стенты, в которых между ячейками впаяна пластиковая мембрана, препятствующая его прорастанию. На этом фоне, независимо от типа стентирования, диагностика холангиокарцином запаздывает в связи с имеющимися изменениями данной зоны, техническими сложностями при взятии биопсии и ориентированностью врачей на другую, ранее установленную патологию.
Подозрение на холангиокарциному возникает при необъяснимой этиологии билиарной обструкции. Лабораторные исследования отра-
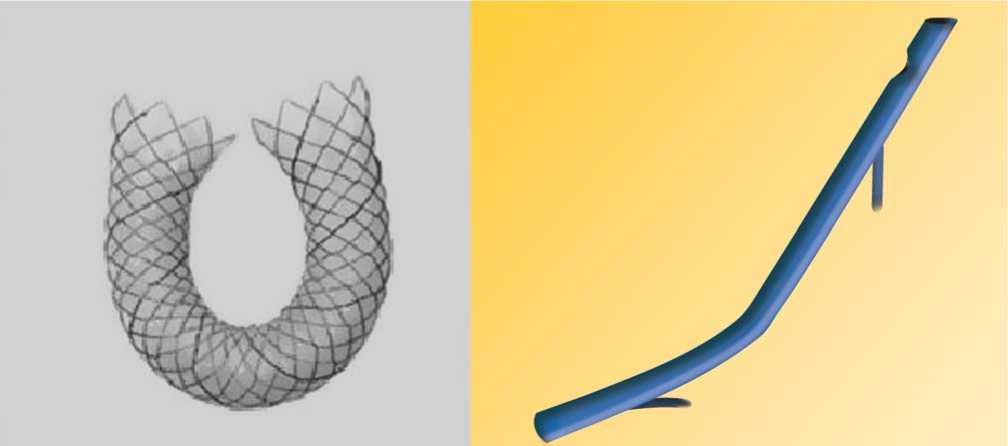
Рис. 10. Общий вид металлического и пластикового билиарного стента.
жают лишь степень холестаза. Диагностика основана на УЗИ или КТ. Если эти методы не позволяют верифицировать диагноз, необходимо проводить МРХПГ или ЭРХПГ с чрескожной чреспеченочной холангиографией. В некоторых случаях ЭРХПГ не только диагностирует опухоль, но также позволяет выполнить биопсию ткани щеточкой, что обеспечивает гистологическую диагностику без тонкоигольной биопсии под контролем УЗИ или КТ. Для верификации диагноза необходимо выполнение биопсии с последующим гистологическим исследованием полученного материала [2].
Примененный в нашем клиническом наблюдении метод КЛЭМ позволил не только уточ- нить, но и верифицировать диагноз, когда другие современные методы диагностики оказались малоинформативны. Метод КЛЭМ основан на принципе конфокальной флюоресцентной микроскопии (рис. 11). Лазерный луч с длиной волны 488 нм, расположенный в рабочей станции, передается с помощью систем зеркал на фиброоптический зонд и попадает на поверхность исследуемой ткани. Часть света поглощается, а индуцируемый лазером эффект флюоресценции вызывает свечение тканей, которое попадает через тот же самый зонд на конфокальный микроскоп, обрабатывается компьютером, позволяя получить динамическое монохромное изображение на мониторе.
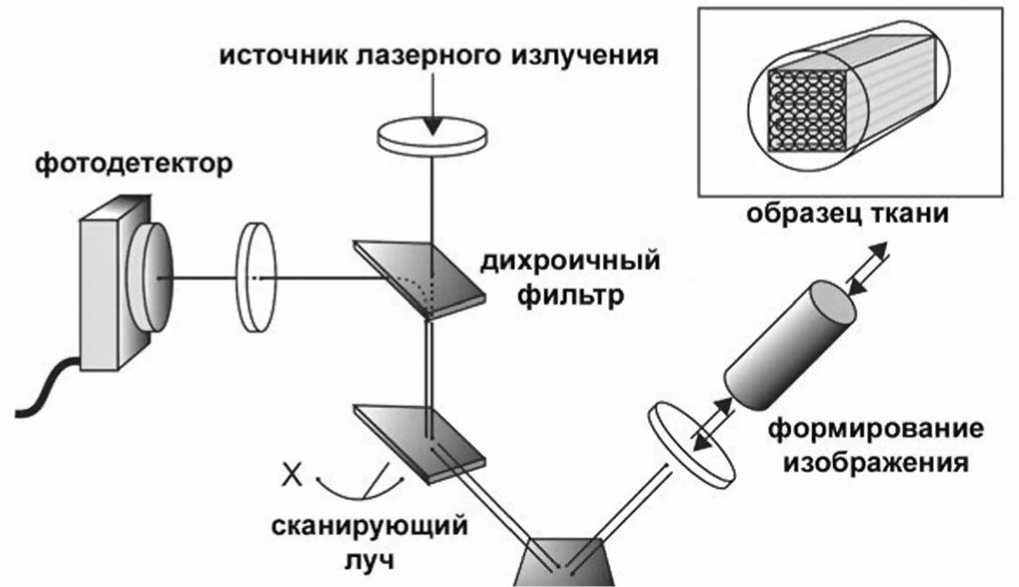
Рис. 11. Схематичное изображение системы "Cellvizio", используемой при КЛЭМ (Mauna Kea Technologies, France).
Для исследования желудочно-кишечного тракта применяются зонды "Gastroflex", "Colonoflex", "Cholangioflex". Их разрешающая способность достигает 3,5 мкм, диаметр оптического поля составляет 600 мкм, а глубина исследования – 0-50 мкм. Минизонд проводится через инструментальный канал эндоскопа, при этом минимальный требуемый диаметр инструментального канала должен быть не менее 2,2 мм, что позволяет использовать подавляюще большинство гибких эндоскопов.
К настоящему времени имеются лишь единичные зарубежные работы, посвященные методу КЛЭМ при патологии гепатопанкреато-дуоденальной зоны. Три мультицентрических исследования, проведенных в Европе и США продемонстрировали высокую специфичность – 73-88% и чувствительность – 83-97% внутрипротоковой КЛЭМ при стриктурах желчных протоков неясной этиологии [7]. Некоторые зарубежные авторы считают, что на современном этапе развития диагностики КЛЭМ при заболеваниях желчных протоков может иметь решающее значение при неэффективности других методов [5, 6].
Заключение. Диагностика холангиокарци-ном на ранней стадии заболевания даже с помощью современных методов исследования сложна и не всегда возможна. Наибольшие трудности возникают при развитии опухоли на фоне уже имеющейся панкреатобилиарной патологии: хронического псевдотуморозного панкреатита, гнойного холангита и т.д. Для своевременной диагностики целесообразно проведение КЛЭМ и прицельной биопсии из зоны наиболее выраженных изменений. Данное клиническое наблюдение показывает необходимость дальнейшего проведения контролируемых исследований с целью определения специфичности и чувствительности метода КЛЭМ при различной патологии желчных и панкреатических протоков.
Список литературы Клинический случай ранней диагностики холангиокарциномына фоне хронического псевдотуморозного панкреатита с помощью метода
- Nordback I.H., Pitt H.A., Coleman J. et al. Unresectable hilar cholangiocarcinoma: percutaneous versus operative palliation//Surgery. 1994. Vol.115. Р. 597-603.
- Гальперин Э.И., Тюжева Т.Г. Лекции по гепато-панкреатобилиарной хирургии с CD. М.:Видар, 2011. 536 с.
- Soehendra N., Reynders-Frederix V. Palliative gallengangdrainage//Dtsch. Med. Wochenschr. 1979. Vol.104. Р.206-209.
- Сhan C.H., Telford J.J. Endoscopic management of benign biliary strictures//Gastrointest Endosc Clin N Am. 2012;22(3):511-537.
- Caillol F., Filoche B., Gaidhane M., Kahaleh M. Refined probe-based confocal laser endomicroscopy classification for biliary strictures: the Paris Classification//Dig. Dis. Sci. 2013. Vol.58(6). Р. 1784-89.
- Giovannini M., Bories E., Monges G., Pesenti C., Caillol F., Delpero J.R. Results of a phase I-II study on intraductal confocal microscopy (IDCM) in patients with common bile duct (CBD) stenosis//Surg. Endosc. 2011;25(7):2247-53.
- Davids P.H., Goren A.K., Rauws E.A. et al. Randomized trial of self-expanding metal stents versus polyethylene stents for malignant bile duct obstruction//Lancet. 1992. Vol.340 Р.1488-92.


