Клинический случай торакоскопически видеоассистированной повторной стернотомии при первичной дисфункции гомографта корня аорты
Автор: Малышенко Егор Сергеевич, Петко С.А., Попов В.А., Гасангусенов М.Г., Ревишвили А.Ш.
Журнал: Патология кровообращения и кардиохирургия @journal-meshalkin
Рубрика: Случаи из клинической практики
Статья в выпуске: 3 т.26, 2022 года.
Бесплатный доступ
Спаечный процесс в переднем средостении после ранее перенесенных оперативных вмешательств на сердце является предиктором фатальной травматизации камер сердца, крупных магистральных сосудов и легких при повторных кардиохирургических операциях. Используемые для профилактики подобных осложнений подходы за прошедшие десятилетия эволюционировали, но необходимость их улучшения сохраняется. Ежегодное увеличение количества операций на сердце, старение населения экономически развитых стран и активное использование имплантов биологического происхождения (например, биопротезов клапанов сердца) предопределяют рост количества повторных кардиохирургических вмешательств и актуализируют поиск новых технологий безопасной рестернотомии. Представлен случай репротезирования у пациента с первичной дегенерацией гомографта в позиции корня аорты, имплантированного 13 лет назад по поводу аортального стеноза по методике full root. Применяемая оригинальная методика (патент РФ RU 2726605 C1: «Способ эндоскопической профилактики травматизации сердца, легких и крупных сосудов переднего средостения при повторных кардиохирургических операциях») предусматривает сочетание минимально инвазивных и классических хирургических подходов. Торакоскопически выполнили тотальный адгезиолиз переднего средостения: заднюю поверхность грудины и хрящевую часть ребер полностью освободили от сращений с правым желудочком, аортой, легкими и безымянной веной. Рестернотомию выполнили стандартным электрическим стернотомом под прямым визуальным контролем с защитой правого желудочка при помощи эндоскопических ретракторов. При этом удалось полностью исключить риск хирургической травмы органов переднего средостения и сделать объем интраоперационной кровопотери сопоставимым со стандартной (первичной) стернотомией.
Кардиохирургическая операция, клинический случай, репротезирование, рестернотомия, спаечный процесс
Короткий адрес: https://sciup.org/142235613
IDR: 142235613 | DOI: 10.21688/1681-3472-2022-3-91-96
Video-assisted thoracoscopic redo sternotomy for primary dysfunction of the aortic root homograft: a case report
Adhesion in the anterior mediastinum following previous heart surgeries is a predictor of fatal trauma of the heart chambers, large vessels and lungs during redo cardiac procedures. The approaches used to prevent such complications have evolved over the past decades, but the need for their improvement remains. Annual increase in heart surgeries, coupled with the phenomenon of "aging population" in economically developed countries, predetermines the growth of redo cardiac surgical procedures. An important role in this process is also played by the recent more active use of various biological implants (for example, bioprosthetic heart valves), which makes the search for new technologies for safe redo sternotomy even more urgent. The publication presents a case of redo surgery in a patient with primary degeneration of the homograft in the aortic root position implanted 13 years ago for aortic stenosis using the Full Root technique. The original technique applied (Method for endoscopic prevention of traumatisation of cardiac, lung and major vessels of anterior mediastenum accompanying repeated cardiosurgical operations. Patent No. RU 2726605 C1) provides for a combination of minimally invasive and classic surgical approaches. Total adhesiolysis of the anterior mediastinum was performed thoracoscopically: the posterior surface of the sternum and the cartilaginous part of the ribs were completely freed from adhesions with the right ventricle, the aorta, lungs and innominate vein. The redo sternotomy was made using a standard electric saw under direct visual control and protection of the right ventricle and the ascending aorta with endoscopic retractors. The risk of surgical trauma of the anterior mediastinum organs was fully eliminated and the intraoperative blood loss was comparable to a traditional sternotomy approach.
Текст научной статьи Клинический случай торакоскопически видеоассистированной повторной стернотомии при первичной дисфункции гомографта корня аорты
Цитировать: Малышенко Е.С., Петко С.А., Попов В.А., Гасангусенов М.Г., Ревишвили А.Ш. Клинический случай торакоскопически видеоассистированной повторной стернотомии при первичной дисфункции гомографта корня аорты. Патология кровообращения и кардиохирургия. 2022;26(3):91-96. https:// org/10.21688/1681-3472-2022-3-91-96
Е.С. Малышенко, С.А. Петко, В.А. Попов, М.Г. Гасангусенов,
А.Ш. Ревишвили,
Проблема безопасной рестернотомии при кардиохирургических вмешательствах наращивает актуальность [1; 2]. Хотя абсолютное количество повторных «открытых» операций на сердце невелико по сравнению с числом первичных аналогичных вмешательств [3–5], из-за ежегодного увеличения частоты протезных эндокардитов и количества клапанных коррекций (в том числе пластики клапанов, биопротезирования) [6–9] необходимость повторных «открытых» вмешательств на сердце растет [10; 11]. Кроме того, с повышением средней продолжительности жизни населения планеты закономерно увеличивается продолжительность жизни среднестатистического кардиохирургического пациента, что в будущем обещает еще больший прирост рассматриваемых операций. Трудности при рестернотомии обусловлены адгезией различных отделов сердца, магистральных сосудов, легких к задней поверхности грудины [12]. Фатальные кровотечения при рестернотомии связаны с повреждением правого желудочка (39 %), коронарных шунтов (20 %), аорты (15 %), магистральных вен (12 %) [13]. Лучевые компьютерные методики диагностики помогают оценивать риск осложнений и планировать стратегию хирургической протекции органов переднего средостения при рестернотомии [14–16]. Разработка и усовершенствование хирургических методик, позволяющих уменьшить риск значимой травматизации перечисленных структур переднего средостения, представляют значительный интерес. Цель — демонстрация клинического случая репротезирования гомографта корня аорты в связи с его дисфункцией с акцентом внимания на профилактику хирургических осложнений, ассоциированных с повторной срединной стернотомией.
Клинический случай
Пациент П. 56 лет (рост 175 см, вес 90 кг, индекс массы тела 29 кг/см²) обратился в НМИЦ хирургии им. А.В. Вишневского с жалобами на одышку, снижение толерантности к физической нагрузке, слабость, утомляемость. Из анамнеза известно, что в 1983 г. диагностирован врожденный порок сердца: двустворчатый аортальный клапан. В 2008 г. ввиду прогрессирования дегенеративных изменений аортального клапана и увеличения размера корня аорты выполнено плановое хирургическое вмешательство в объеме протезирования корня аорты гомографтом 26 мм по методике full root. Отказ от применения механического протеза аорталь-
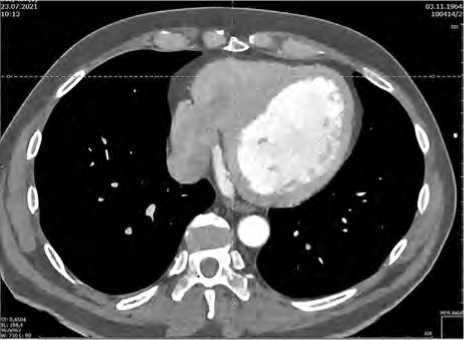
Рис. 1. Мультиспиральная компьютерная томография органов грудной клетки. Плотные сращения правых камер сердца с грудиной и хрящевыми частями ребер ного клапана обусловлен информированным выбором пациента.
По данным трансторакальной эхокардиографии отмечался выраженный кальциноз тубулярной части и створок гомографта, что гемодинамически проявлялось регургитацией 4-й степени и умеренным стенозом биопротеза. Градиент давления: максимальный 52 мм рт. ст., средний 30 мм рт. ст., конечный диастолический объем левого желудочка 263 мл, конечный систолический объем левого желудочка 134 мл, ударный объем 126 мл. Фракция выброса по Симпсону 42 %, минутный объем кровообращения 7,3 л/мин. Коронарография: неровности контуров коронарных артерий, сбалансированный тип коронарного кровообращения. При мультиспи-ральной компьютерной томографии органов грудной клетки с контрастным усилением выявили массивный кальциноз гомографта в позиции корня аорты. При оценке переднего средостения определили массивные сращения между правым желудочком и ретростернальной поверхностью (рис. 1).
Протокол оперативного вмешательства. Положение пациента на операционном столе на спине. После раздельной интубации трахеи, однопросветной вентиляции левого легкого сформировали доступ через правую плевральную полость к переднему средостению. В IV межреберном промежутке по передней подмышечной линии установили оптический эндоскопический порт диаметром 5 мм, плевральную полость осмотрели при помощи эндоскопической камеры (диаметр 5 мм, 0°). Два порта 5 мм для рабочих инструментов установили в III и V межреберных промежутках между среднеключичной и передней подмышечной линиями. Визуализирова-
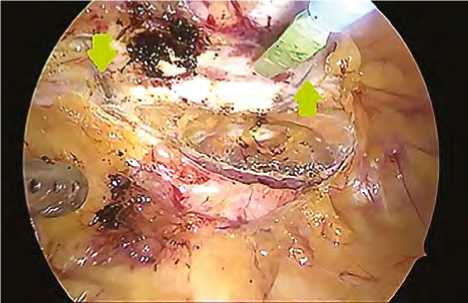
Рис. 2. Визуализация двух проволочных швов. Зелеными стрелками указаны лигатуры из нержавеющей стали ли ретростернальную клетчатку. Все анатомические структуры переднего средостения спаяны с ретро-стернальной поверхностью. Имеются спайки между правым желудочком и задней поверхностью грудины. При помощи лопатки для электрокоагуляции, эндоскопического ретрактора и эндоскопического ирригатора-аспиратора выполнили адгезиолиз по направлению от мечевидного отростка к яремной вырезке. Поочередно отсепарировали переднюю поверхность правого желудочка и магистральных сосудов (аорты, безымянной вены). Визуализировали лигатуры из нержавеющей стали (рис. 2).
Выполнили разрез кожи на грудной стенке с иссечением рубца, удалили проволочные швы. Под прямым визуальным эндоскопическим контролем выполнили срединную стернотомию (рис. 3).
Полость перикарда после ранее выполненных оперативных вмешательств не ушивали. Провели основной этап операции в объеме репротезирова- ния корня аорты клапаносодержащим кондуитом диаметром 25 мм (операция Карболя в модификации Свенсона).
Объем интраоперационной кровопотери 580 мл, время искусственного кровообращения 170 мин, время пережатия аорты 110 мин. Дренажные потери за 1-е и 2-е сутки работы активных ретростерналь-ных дренажей 250 и 80 мл соответственно. Время искусственной вентиляции легких 720 мин. Длительность нахождения в отделении интенсивной терапии 68 ч.
Провели контрольную трансторакальную эхокардиографию: максимальный градиент давления на протезе аортального клапана 15 мм рт. ст., средний 8 мм рт. ст., конечный диастолический объем левого желудочка 221 мл, конечный систолический объем левого желудочка 117 мл, ударный объем 104 мл, фракция выброса по Симпсону 47 %.
Пациента перевели из реанимационного отделения на 3-е сутки послеоперационного периода. Выписали на 12-е сутки в удовлетворительном состоянии.
Обсуждение
Проблема безопасной рестернотомии существует с момента зарождения кардиохирургии. Первые попытки повторных вмешательств на сердце с целью репротезирования клапанов сердца без применения специальных подходов к рестернотомии были сопряжены с крайне высокой интраоперационной летальностью и существенно сдерживали развитие направления. Первым подходом к решению проблемы было применение осциляторных стер-нотомов, которые позволили уменьшить частоту
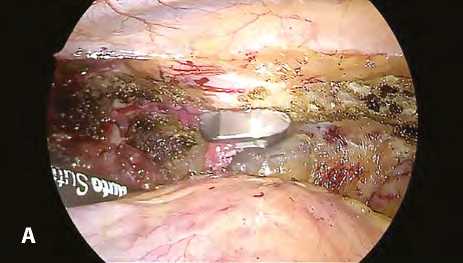
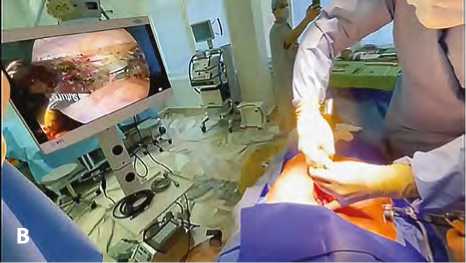
Рис. 3. Стернотомия под прямым визуальным контролем: грудная аорта и правый желудочек оттеснены эндоскопическими ретракторами во время работы электрического стернотома (А); общий вид операционной и операционного поля: хирург выполняет рестернотомию, ассистент при помощи эндоскопических ретракторов под контролем эндоскопической камеры оттесняет освобожденную от спаек восходящую аорту (B)
повреждения правого желудочка не менее чем на 40 %. Однако количество осложнений оставалось неприемлемо высоким, поэтому ряд клиник кардинально пересмотрели концепцию хирургической протекции сердца и магистральных сосудов при рестернотомии [17]. Подключение аппарата искусственного кровообращения непосредственно перед рестернотомией позволяет разгрузить камеры сердца (в особенности правый желудочек), что уменьшает вероятность летальной кровопотери в случае, если травматизация все же произошла [13; 18]. Однако эта технология имеет существенные недостатки: а) необходимо выполнять рестернотомию и адгезиолиз в условиях тотальной гепаринизации; б) существенно увеличиваются продолжительность искусственного кровообращения и, как следствие, значимость его неблагоприятных системных эффектов; в) периферическая канюляция сопряжена с риском специфических осложнений и не всегда выполнима у пациентов с мультифокальным атеросклерозом.
Оригинальная методика безопасной рестернотомии (патент РФ RU 2726605 C1: «Способ эндоскопической профилактики травматизации сердца, легких и крупных сосудов переднего средостения при повторных кардиохирургических операциях»), применяемая в НМИЦ хирургии им. А.В. Вишневского, не исключает периферическое подключение искусственного кровообращения, однако в нашей клинической практике не было ситуаций, когда технически не удавалось выполнить тотальный адгезиолиз переднего средостения. Обе протективные стратегии имеют все предпосылки для конвергенции. Использование описанной методики в клинической практике можно рекомендовать кардиохирургическим центрам, которые обеспечены соответствующими технологиями и уже выполняют торакоскопические (кардиоэндоскопические) вмешательства.
Заключение
Использованная в клиническом случае протек-тивная эндоскопическая стратегия обеспечила безопасное выполнение хирургического доступа, что снизило риск травматизации правого желудочка и магистральных сосудов. Описанный подход может быть востребован в кардиохирургических клиниках, выполняющих повторные операции на сердце, во всех ситуациях, когда в качестве хирургического доступа планируется повторная срединная стернотомия.
Список литературы Клинический случай торакоскопически видеоассистированной повторной стернотомии при первичной дисфункции гомографта корня аорты
- Kindzelski B.A., Bakaeen F.G., Tong M.Z., Roselli E.E., Soltesz E.G., Johnston D.R., Wierup P., Pettersson G.B., Houghtaling P.L., Blackstone E.H., Gillinov A.M., Svensson L.G.; Cleveland Clinic Collaboration on Cardiac Reoperations Working Group Collaborators. Modern practice and outcomes of reoperative cardiac surgery. J Thorac Cardiovasc Surg. 2021;S0022-5223(21)00125-2. PMID: 33757681. https://doi.org/10.1016/i. jtcvs.2021.01.028 [Online ahead of print]
- Machiraju V.R. Problems related to redo cardiac surgery. In: Machiraju V., Schaff H., Svensson L., editors. Redo cardiac surgery in adults. New York: Springer; 2012. pp. 1-6. https://doi. org/10.1007/978-1-4614-1326-4 1
- Temeck B.K., Katz N.M., Wallace R.B. An approach to reoperative median sternotomy. J Card Surg. 1990;5(1):14-25. PMID: 2133819. https://doi.org/10.11117i.1540-8191.1990. tb00732.x
- Agarwal S., Choi S.W., Fletcher S.N., Klein A.A., Gill R.; Contributors. The incidence and effect of resternotomy following cardiac surgery on morbidity and mortality: a 1-year national audit on behalf of the Association of Cardiothoracic Anaesthesia and Critical Care. Anaesthesia. 2021;76(1):19-26. PMID: 32406071. https://doi.org/10.1111/anae.15070
- Керен М.А., Казарян А.В. Рецидив ишемии после открытой реваскуляризации миокарда: современное состояние проблемы, факторы риска, прогноз, тактика и результаты повторных вмешательств. Анналы хирургии. 2017;22(5):257-264. Keren M.A., Kazaryan A.V. Recurrent ischemia after open myocardial revascularization: current state of the problem, risk factors, prognosis, tactics and results of repeated interventions. Annals of Surgery. 2017;22(5):257-264. (In Russ.)
- Скопин И.И., Кахкцян П.В., Латышев М.С., Мурысова Д.В., Куприй Т.А., Жангериев И.А., Хасигова Э.В., Енокян Л.Ж. Повторные операции на корне аорты при позднем протезном эндокардите (серия клинических случаев). Патология кровообращения и кардиохирургия. 2019;23(4):73-82. https://dx.doi.org/10.21688/1681-3472-2019-4-73-82 Skopin I.I., Kakhktsyan P.V., Latyshev M.S., Murysova D.V., Kupriy T.A., Zhangeriev I.A., Khasigova E.V., Enokyan L.Zh. Redo aortic root operations in late prosthetic endocarditis: clinical case series. Patologiya krovoobrashcheniya i kardiokhirurgiya = Circulation Pathology and Cardiac Surgery. 2019;23(4):73-83. (In Russ.) https://dx.doi.org/10.21688/1681-3472-2019-4-73-82
- Awad W.I., De Souza A.C., Magee P.G., Walesby R.K., Wright J.E., Uppal R. Re-do cardiac surgery in patients over 70 years old. Eur J Cardiothorac Surg. 1997;12(1):40-46. PMID: 9262079. https://doi.org/10.1016/S1010-7940(97)00147-4
- François K., De Backer L., Martens T., Philipsen T., Van Belleghem Y., Bové T. Repeat aortic valve surgery: contemporary outcomes and risk stratification. Interact Cardiovasc Thorac Surg. 2021;32(2):213-221. PMID: 33279996; PMCID: PMC8906689. https://doi.org/10.1093/icvts/ivaa257
- Greason K.L., Schaff H.V. Reoperation for prosthetic mitral valve endocarditis. In: Machiraju V., Schaff H., Svensson L., editors. Redo cardiac surgery in adults. New York: Springer; 2012. pp. 99108. https://doi.org/10.1007/978-1-4614-1326-4 12
- Ismail I., Zhang R., Ringe K., Fischer S., Haverich A. Retrosternal adhesiolysis through an anterior minithoracotomy: a novel approach facilitating complete median redo sternotomy with a patent internal thoracic artery graft. J Thorac Cardiovasc Surg. 2009;137(4):1034-1035. PMID: 19327540. https://doi. org/10.1016/i.itcvs.2008.03.028
- Гордеев М.Л., Гребенник В.К., Исмаил-заде И.К., Иш-мухаметов Г.И., Иванов И.Ю., Абуталимова Н.Р., За-варзина Д.Г. Анализ непосредственных результатов повторного коронарного шунтирования. Патология кровообращения и кардиохирургия. 2021;25(1):85-96. https:// dx.doi.org/10.21688/1681-3472-2021-1-85-96 Gordeev M.L., Grebennik V.K., Ismail-zade I.K., Ishmu-khametov G.I., Ivanov I.Yu., Abutalimova N.R., Zavarzina D.G. Analysis of direct results of reoperative coronary artery bypass surgery. Patologiya krovoobrashcheniya i kardiokhirurgiya = Circulation Pathology and Cardiac Surgery. 2021;25(1):85-96. (In Russ.) https://dx.doi.org/10.21688/1681-3472-2021-1-85-96
- Сигаев И.Ю., Казарян А.В. Оперативные доступы при повторных операциях коронарного шунтирования. Бюллетень НЦССХ им. А.Н. Бакулева РАМН. 2021 ;2(22):130-138. https://doi.org/10.24022/1810-0694-2021-22-2-130-138 Sigaev I.Yu., Kazaryan A.V. Operational access during redo coronary artery bypass grafting. The Bulletin of Bakoulev Center. Cardiovascular Diseases. 2021;2(22):130-138. (In Russ.) https://doi.org/10.24022/1810-0694-2021-22-2-130-138
- Luciani N., Anselmi A., De Geest R., Martinelli L., Perisano M., Possati G. Extracorporeal circulation by peripheral cannulation before redo sternotomy: indications and results. J Thorac Cardiovasc Surg. 2008;136(3):572-577. PMID: 18805254. https://doi.org/10.1016/i.itcvs.2008.02.071
- Valente T., Bocchini G., Rossi G., Sica G., Davison H., Scaglione M. MDCT prior to median re-sternotomy in cardiovascular surgery: our experiences, infrequent findings and the crucial role of radiological report. Br J Radiol. 2019;92(1101 ):20170980. PMID: 31199672; PMCID: PMC6732917. https://doi.org/10.1259/bjr.20170980
- Kirmani B.H., Brazier A., Sriskandarajah S., Azzam R., Keenan D.J. A meta-analysis of computerized tomography scan for reducing complications following repeat sternotomy for cardiac surgery. Interact Cardiovasc Thorac Surg. 2016;22(4):472-479. PMID: 26740589. https://doi. org/10.1093/icvts/ivv367
- Morishita K., Kawaharada N., Fukada J., Yamada A., Masaru T., Kuwaki K., Abe T. Three or more median sternotomies for patients with valve disease: role of computed tomography. Ann Thorac Surg. 2003;75(5):1476-1480; discussion 1481. PMID: 12735565. https://doi.org/10.1016/S0003-4975(02)04821-X
- Yin C.-H., Yan J., Li Sh.-J., Li D.-Y., Wang Q., Wang E.-S. Effect analysis of repeat sternotomy in pediatric cardiac operations. J Cardiothorac Surg. 2015;10:179. PMID: 26621353; PMCID: PMC4666069. https://doi.org/10.1186/s13019-015-0381-z
- Esper S.A., Subramaniam K., Tanaka K.A. Pathophysiology of cardiopulmonary bypass: current strategies for the prevention and treatment of anemia, coagulopathy, and organ dysfunction. Semin Cardiothorac Vasc Anesth. 2014;18(2):161 -176. PMID: 24876231. https://doi. org/10.1177/1089253214532375


