Клинический случай успешного лечения гигантского серозного рака эндометрия
Автор: Беришвили Александр Ильич, Иванов Юрий Викторович, Лебедев Дмитрий Петрович, Забозлаев Федор Георгиевич, Кравченко Эдуард Васильевич, Клыпа Татьяна Валерьевна, Кедрова Анна Генриховна
Журнал: Клиническая практика @clinpractice
Рубрика: Клинический случай
Статья в выпуске: 4 т.12, 2021 года.
Бесплатный доступ
Обоснование. Гигантские опухоли брюшной полости возникают, как правило, у возрастных пациентов с характерологическими особенностями и представляют серьезную проблему в плане выбора радикального метода терапии. Особую сложность составляют случаи гигантского серозного рака эндометрия, требующие дифференциальной диагностики с раком яичников. Описание клинического случая. Представлен клинический случай гигантского серозного рака эндометрия, имитирующего рак яичников у женщины в возрасте 55 лет. Пациентка обратилась в онкологическое отделение с жалобами на увеличение живота, затруднение дыхания и кровянистые выделения из половых путей. При обследовании были выявлены гигантское образование (40×65 см), занимающее весь малый таз и всю брюшную полость, асцит, поражение забрюшинных лимфатических узлов и большого сальника, пупочная грыжа, при компьютерной томографии (КТ) органов грудной клетки - множественные метастазы до 3-13 мм, накапливающие контраст. По решению консилиума, после предварительной химиоэмболизации обеих маточных и яичниковых артерий были выполнены надвлагалищная ампутация матки с придатками, резекция большого сальника, удаление пупочной грыжи с пластикой сетчатым имплантатом и иссечением избыточного кожного лоскута. При морфологическом исследовании операционного материала верифицирована серозная карцинома эндометрия с субтотальным некрозом опухоли, инвазией миометрия более 1/2 толщины, участками опухолевого роста в периметрии, метастатическим поражением обоих яичников, большого сальника, передней брюшной стенки. Стадия T3b (FIGO IIIB). В послеоперационном периоде проведено 6 курсов химиотерапии комбинацией паклитаксела/карбоплатина (AUC4-5) с хорошим клиническим эффектом. Пациентка выписана в удовлетворительном состоянии. После 6-го курса химиотерапии при контрольной позитронно-эмиссионной томографии с одновременной КТ патологии в грудной клетке не обнаружено, в брюшной полости - без признаков прогрессирования процесса. В настоящий момент ремиссия заболевания составляет 9 мес. Заключение. Представлен алгоритм диагностических мероприятий, направленных на постановку правильного диагноза, описана тактика успешного лечения больной с гигантским серозным раком эндометрия.
Серозный рак эндометрия, гигантская опухоль, хирургия, химиотерапия
Короткий адрес: https://sciup.org/143178093
IDR: 143178093 | DOI: 10.17816/clinpract90662
A clinical case of successful treatment of a giant serous endometrial carcinoma imitating ovarian cancer
Background: Giant tumors of the abdominal cavity, as a rule, occur in elderly patients with characteristic features and represent a serious problem in terms of choosing a radical method of therapy. Of particular difficulty are cases of giant serous endometrial cancer, requiring a differential diagnosis with ovarian cancer. Clinical case description: A clinical case of giant serous endometrial cancer mimicking ovarian cancer in a 55-year-old woman is presented. The patient came to the oncology department with complaints of abdominal enlargement, difficulty breathing and bloody discharge from the genital tract. The examination revealed the following: a giant formation (40×65 cm), occupying the entire pelvic and the entire abdominal cavities, ascites, lesions of the retroperitoneal lymph nodes, and the greater omentum, an umbilical hernia. A chest CT showed multiple contrast-accumulating circular shadows of 3-13 mm (metastases). By the decision of the council, after the preliminary chemoembolization of both the uterine and ovarian arteries, a supravaginal amputation of the uterus with appendages was performed, along with the resection of the greater omentum, removal of the umbilical hernia with positioning a plastic mesh implant and excision of an excess skin flap. The histological examination of the intraoperative material made it possible to verify the diagnosis of a serous endometrial carcinoma with subtotal tumor necrosis, the myometrium invasion of more than a half of its thickness, with the egress to the perimetrium, metastatic lesions of both ovaries, the greater omentum, anterior abdominal wall. Stage T3b (FIGO IIIB). In the postoperative period, 6 courses of Paclitaxel / Carboplatin (AUC4-5) chemotherapy were carried out with a pronounced clinical effect. The patient was discharged in a satisfactory condition. The control PET-CT scan after the 6th chemotherapy course showed no pathology in the thoracic cavity, and no process progress in the abdominal cavity. Currently, the remission of the disease is 9 months. Conclusion: An algorithm for the diagnostic measures aimed at making the correct diagnosis is presented, and the tactics of treating a patient with giant serous endometrial cancer is described.
Текст научной статьи Клинический случай успешного лечения гигантского серозного рака эндометрия
Submitted 24.09.2021 Revised 16.12.2021 Published 21.12.2021
на клиническую результативность терапии, а именно на количество дней с головной болью, частоту, длительность и интенсивность приступов; снижать степень влияния головной боли на повседневную активность и этим повышать качество жизни.
Клиническая картина болезни пациента с болью зависит от использования им различных приемов совладения со стрессовой ситуацией — копинг-стратегий, которые описываются как попытка человека использовать когнитивные и поведенческие стратегии для управления эмоциями в ответ на стресс [6]. Стойкость к дезадаптивным стратегиям преодоления является фактором риска рецидивов ХМ [7]. Согласно литературным данным, выявлена связь между рецидивами эпизодов мигренозной головной боли и дезадаптивными копинг-стратеги-ями [8]. M.K. Gunel и F.Y. Akkaya [9] сообщили, что пациенты с мигренью меньше обращаются к социальной поддержке, чем пациенты, не страдающие мигренью. D. D’Amico и соавт. [10] выявили умеренную взаимосвязь между уровнем инвалидизации и качества жизни и психологическими факторами у пациентов с ХМ и сопутствующей абузусной головной болью.
Лучшее понимание связи между качеством жизни и личностным профилем пациентов может привести к повышению эффективности лечения ХМ. Более высокий уровень приверженности к активным копинг-стратегиям пациентов, страдающих ХМ, связан с большим комплаенсом [11]. Пассивные копинг-стратегии являются прогностическим индикатором неблагоприятного исхода при лечении ХМ [11]. Ранее копинг-стратегии личности у пациентов с ХМ изучались в небольшом количестве исследований, однако этот психологический аспект является клинически важным для лечения головной боли [10–12].
До сих пор не сообщалось о клинических особенностях пациентов, страдающих ХМ, в зависимости от профиля их личности.
Цель исследования — оценить клинические особенности пациентов, страдающих ХМ, в зависимости от преобладающей копинг-стратегии личности.
МЕТОДЫ
Обследовано 104 человека с ХМ. Диагноз ХМ установлен в соответствии с критериями Международной классификации головной боли, 3-й версии (2018).
Исследование проводилось на базе Клиники головной боли и вегетативных расстройств имени академика Александра Вейна.
Всем пациентам были проведены клинико-неврологическое обследование, анализ дневников головной боли и анкетное тестирование с помощью

кт ГА
следующих инструментов: MIDAS (Migraine Disability Assessment — опросник оценки влияния мигрени на повседневную активность пациента ), HIT-6 (Headche Impact Test — индекс влияния головной боли на повседневную активность ), HALT (Headche Attributed Lost Time — индекс времени, потерянного из-за головной боли ), шкалы депрессии Бека (Beck Depression Inventory), шкалы Спилбергера по оценке тревожности (State-Trait Anxiety Inventory, STAI), индикатор копинг-стратегий (Д. Амир-хан) [13], и Гиссенский опросник соматических жалоб (Giesener Beschwerdebogen, GBB).
Статистический анализ проводился при помощи программы Statistica 12 (StatSoft Inc.). Статистически значимыми считались различия p <0,05.
РЕЗУЛЬТАТЫ
Нами проведен анализ социодемографических показателей, частоты головной боли и оценка качества жизни, выраженности психоэмоциональных нарушений, степени выраженности соматических проявлений у пациентов, страдающих ХМ, с различными личностными копинг-стратегиями (табл. 1).
В нашей группе из 104 пациентов, страдающих ХМ, наиболее распространенной копинг-страте-гией личности, по опроснику Д. Амирхан, была стратегия разрешения проблемы (47,1%), реже выявлялась стратегия поиска социальной поддержки (36,5%), наиболее редкой была стратегия избегания (16,3%).
Распределение по полу было представлено следующим образом: среди пациентов со стратегией разрешения проблемы женщин было 75,5%, мужчин — 24,5%; среди пациентов, имеющих стратегию поиска социальной поддержки, преобладали женщины — 86,8% против 13,2% мужчин. В группе пациентов со стратегией избегания выявлен достоверно ( p =0,025) больший процент женщин (52,9%) и меньший — мужчин (47,1%).
По уровню образования достоверной разницы между пациентами с различными копинг-стратеги-ями не выявлено ( p =0,298).
Пациенты со стратегией разрешения проблемы имели достоверно ( p <0,001) более низкий возраст (Me 37,0 лет; Q1–Q3 34,0–46,0) по сравнению с пациентами со стратегией поиска социальной поддержки (Me 49,5 лет; Q1–Q3 43,0–56,0) и пациентами группы стратегии избегания (Me 45,0 лет; Q1–Q3 42,0–56,0).
Пациенты со стратегией поиска социальной поддержки имели достоверно ( p <0,001) более высокую длительность анамнеза хронической мигрени (Me 11,0 лет; Q1–Q3 7,0–15,0) по сравнению
Таблица 1 / Table 1
Клинические показатели пациентов, страдающих хронической мигренью, в зависимости от копинг-стратегии личности /
Clinical indices of CM patients, depending on their coping strategies
|
Показатель |
Категории |
p |
||||||||
|
Стратегия разрешения проблемы |
Стратегия поиска социальной поддержки |
Стратегия избегания |
||||||||
|
Me |
Q1–Q3 |
n |
Me |
Q1–Q3 |
n |
Me |
Q1–Q3 |
n |
||
|
Возраст, полных лет |
37 |
34,0–46,0 |
49 |
49,5 |
43,0–56,0 |
38 |
45 |
42,0–51,0 |
17 |
<0,001* |
|
Анамнез ХМ, лет |
5 |
3,0–7,0 |
49 |
11 |
7,0–15,0 |
38 |
4 |
3,0–17,0 |
17 |
<0,001* |
|
Частота головной боли, день |
18 |
16,0–22,0 |
49 |
18 |
15,5–24,0 |
38 |
22 |
16,0–25,0 |
17 |
0,138 |
|
Опросник MIDAS, балл |
42 |
37,0–80,0 |
49 |
45 |
38,0–50,0 |
38 |
56 |
26,0–56,0 |
17 |
0,393 |
|
Индекс HIT-6, балл |
63 |
60,0–67,0 |
49 |
63 |
60,0–65,0 |
38 |
50 |
30,0–54,0 |
17 |
<0,001* |
|
Шкала депрессии Бека, балл |
12 |
6,0–18,0 |
49 |
18 |
16,0–22,0 |
38 |
25 |
9,0–32,0 |
17 |
<0,001* |
|
Шкала Спилбергера (личностная), балл |
54 |
49,0–59,0 |
49 |
55 |
55,0–63,0 |
38 |
63 |
51,0–63,0 |
17 |
0,005* |
|
Гиссенский опросник, балл |
36 |
22,0–68,0 |
49 |
80 |
68,0–91,0 |
38 |
86 |
29,0–90,0 |
17 |
<0,001* |
Примечание. * Различия показателей статистически значимы ( p <0,05).
Note. * — differences are statistically significant ( p <0.05)
с пациентами со стратегией разрешения проблемы (Me 5,0 лет; Q1–Q3 3,0–7,0) и пациентами группы стратегии избегания (Me 4,0 года; Q1–Q3 3,0–17,0).
Частота головной боли ( p =0,138) и степень влияния мигрени на повседневную активность по опроснику MIDAS ( p =0,393) достоверно не различались у пациентов с различными личностными стратегиями.
Пациенты, имеющие стратегию разрешения проблемы (Me 63,0 балл; Q1–Q3 60,0–67,0), и пациенты со стратегией поиска социальной поддержки (Me 63,0 балл; Q1–Q3 60,0–65,0) имели значительно (<0,001) более высокий уровень влияния ГБ головной боли на повседневную активность по индексу HIT-6 в сравнении с пациентами, имеющими стратегию избегания (Me 50,0 балл; Q1–Q3 30,0–54,0).
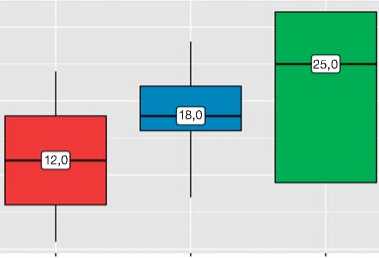
Самый высокий уровень депрессии по шкале депрессии Бека ( p =0,004) имели пациенты с преобладающей личностной стратегией избегания (Me 25,0 баллов; Q1–Q3 9,0–32,0) в сравнении с пациентами со стратегией разрешения проблемы (Me 12,0 баллов; Q1–Q3 6,0–18,0) и стратегией поиска социальной поддержки (Me 18,0 баллов; Q1–Q3 16,0–22,00); рис. 1.
Самый высокий уровень личной тревоги по шкале личной тревожности Спилбергера был отмечен у пациентов со стратегией избегания (Me 63,0 балл; Q1–Q3 51,0–63,0), однако эти отличия не были статистически значимы. У пациентов со стратегией поиска социальной поддержки уровень был достоверно (p=0,004) выше (Me 55,0 балл; (Q1–Q3 55,0–63,0), чем у пациентов со стратегией разрешения проблемы (Me 54,0 балл; Q1–Q3 49,0–59,0); рис. 2.
Пациенты со стратегией разрешения проблемы существенно отличались от пациентов со стратегией поиска социальной поддержки ( p <0,001) и пациентов со стратегией избегания ( p =0,049) по уровню соматических жалоб по Гиссенскому тесту. Группа пациентов со стратегией разрешения проблемы имела достоверно меньший уровень соматических жалоб по Гиссенскому опроснику (Me 36,0 баллов; Q1–Q3 22,0–68,0) в сравнении с пациентами со стратегией поиска социальной поддержки (Me 80,0 баллов; Q1–Q3 68,0–91,0) и стратегией избегания (Me 86,0 баллов; Q1–Q3 29,0–90,0).
ОБСУЖДЕНИЕ
У обследованных нами пациентов преобладали активные копинг-стратегии личности, намного реже выявлялись пассивные копинг-стратегии. Полученные результаты отличаются от данных исследования T. Wieser и соавт. [14], которые сообщили, что у пациентов с головной болью часто используется дисфункциональный копинг, характеризующийся избеганием. В исследовании V. Donisi и соавт. [15] также сообщается о более широком использовании стратегий избегания у пациентов, страдающих ХМ. Отличие, вероятно, связано с тем, что наше исследование проводилось в условиях специализированной клиники по лечению головной боли, где пациенты имеют более высокий уровень комплаентности, чем в целом в популяции. Однако
Индикатор копинг-стратегий (Д. Амирхан)
е Стратегия разрешения проблемы е Стратегия поиска социальной поддержки
Стратегия избегания
S 70,0
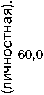
Индикатор копинг-стратегий (Д. Амирхан)
Стратегия разрешения проблемы е Стратегия поиска социальной поддержки в Стратегия избегания
Рис. 1. Уровень депрессии по шкале депрессии Бека в зависимости от копинг-стратегий личности у пациентов, страдающих хронической мигренью.
-
Fig. 1. The levels of depression of CM patients by the Beck Depression Inventory, depending on their coping strategies.
Рис. 2. Уровень личностной тревоги по шкале Спилбер-гера в зависимости от копинг-стратегий личности у пациентов с хронической мигренью.
-
Fig. 2. The level of personal anxiety of CM patients by Spielberger’s STAI, depending on their coping strategies.
КТ ГА
в исследовании M. Gandolfi и соавт. [3] было показано, что копинг-стратегии, используемые пациентами с ХМ, сопоставимы с общей популяцией.
В нашем исследовании пациенты со стратегией избегания имели наименьшую длительность анамнеза заболевания, наименьшую выраженность влияния мигрени на повседневную активность, но были сопоставимы по частоте головной боли и времени, потерянному из-за головной боли, с пациентами с активными копинг-стратегиями. У пациентов с дисфункциональным копингом, включенных в нашу работу, выявлялся наиболее высокий уровень психоэмоциональных коморбидных нарушений. Подобных литературных данных в доступных нам источниках не выявлено.
Наиболее благоприятной для курации является группа пациентов с активными копинг-стратегия-ми, так как они имеют наиболее высокий уровень комплаентности. Нами впервые получены данные, что пациенты, страдающие ХМ, с активными поведенческими копинг-стратегиями имеют более низкий уровень коморбидных психоэмоциональных нарушений.
Пациенты с копинг-стратегией избегания наиболее трудны в лечении, так как имеют низкую приверженность к терапии. Они требуют при лечении особую настороженность в отношении наличия коморбидной депрессии и тревоги. Наивысших результатов в лечении данной группы пациентов возможно добиться только при мультидисциплинарном подходе к терапии. Необходимо привлечение к те- рапии клинических психологов и психотерапевтов для улучшения функционирования копинг-страте-гий у пациентов с ХМ. Обоснованным является назначение комплексных профилактических методов лечения, которые сочетают в себе фармакологическую и нефармакологическую терапию с элементами психотерапии, что было подтверждено в работе G. Castelnuovo и соавт. [16]. Психотерапевтические методы имеют различия, но все они положительно влияют на дезадаптивные копинг-стратегии и образ мышления пациентов с ХМ [16–18].
ЗАКЛЮЧЕНИЕ
Понимание особенностей личности пациентов, страдающих ХМ, позволяет использовать индивидуализированный подход к их реабилитационному лечению. Врачи-неврологи при выявлении пассивных копинг-стратегий должны быть ориентированы на активное выявление комор-бидных психоэмоциональных нарушений у дан- ной категории пациентов с потенциально низким уровнем терапевтического ответа и комплентно-сти. В их реабилитационном лечении уместно сочетанное использование фармакологических и психотерапевтических методов, которые позволяют производить коррекцию копинг-стра-тегий и тем самым повышать результативность терапии в целом.
ДОПОЛНИТЕЛЬНАЯ ИНФОРМАЦИЯ
Вклад авторов . Автор подтверждает соответствие своего авторства международным критериям ICMJE.
Author contribution. The author made a substantial contribution to the conception of the work, acquisition, analysis, interpretation of data for the work, drafting and revising the work, final approval of the version to be published and agree to be accountable for all aspects of the work.
Источник финансирования. Исследование и публикации статьи осуществлены на личные средства автора.
Funding source. The study had no sponsorship.
Список литературы Клинический случай успешного лечения гигантского серозного рака эндометрия
- Charo LM, Plaxe SC. Recent advances in endometrial cancer: a review of key clinical trials from 2015 to 2019. F1000Res. 2019;8:F1000. Faculty Rev-849. doi: 10.12688/f1000research.17408.1
- Siegel RL, Miller KD, Jemal A. Cancer statistics, 2019. CA Cancer J Clin. 2019;69(1):7-34. doi: 10.3322/caac.21551
- Miller D, Filiaci V, Fleming G, et al. Late-breaking abstract 1: Randomized phase III noninferiority trial of first line chemotherapy for metastatic or recurrent endometrial carcinoma: A Gynecologic Oncology Group study. Gynecol Oncol. 2012;125(3):771. doi: 10.1016/j.ygyno.2012.03.034
- Hamilton CA, Cheung MK, Osann K, et al. Uterine papillary serous and clear cell carcinomas predict for poorer survival compared to grade 3 endometrioid corpus cancers. Br J Cancer 2006;94(5):642-646. doi: 10.1038/sj.bjc.6603012
- Rungruang B, Olawaiye AB. Comprehensive surgical staging for endometrial cancer. Rev Obstet Gynecol. 2012; 5(1):28-34.
- Bestvina CM, Fleming GF. Chemotherapy for endometrial cancer in adjuvant and advanced disease settings. Oncologist. 2016;21(10):1250-1259. doi: 10.1634/theoncologist.2016-0062
- Fader AN, Roque DM, Siegel E, et al. Randomized phase II trial of carboplatin-paclitaxel versus carboplatin-paclitaxel-trastu-zumab in uterine serous carcinomas that overexpress human epidermal growth factor receptor 2/neu. J Clin Oncol. 2018;36(20): 2044-2051. doi: 10.1200/JC0.2017.76.5966
- Shaeffer DT, Randall ME. Adjuvant radiotherapy in endometrial carcinoma. Oncologist. 2005;10(8):623-631. doi: 10.1634/theoncologist.10-8-623
- Le Gallo M, Bell DW. The emerging genomic landscape of endometrial cancer. Clin Chem. 2014;60(1):98-110. doi: 10.1373/clinchem.2013.205740
- Lokich E, Kole M, Raker C, et al. Molecular markers in uterine serous cancer: Correlation between endometrial biopsy and hysterectomy specimens. Gynecol Oncol Rep. 2019;29:98-101. doi: 10.1016/j.gore.2019.04.005
- Schwab CL, Santin AD. Targeted therapy in the treatment of uterine serous carcinoma. Pharmacogenomics. 2015;16(2):97-99. doi: 10.2217/pgs.14.176
- Meng X, Laidler LL, Kosmacek EA, et al. Induction of mitotic cell death by overriding G2/M checkpoint in endometrial cancer cells with non-functional p53. Gynecol Oncol. 2013; 128(3):461-469. doi: 10.1016/j.ygyno.2012.11.004
- Houghton PJ. Everolimus. Clin Cancer Res. 2010;16: 1368-1372. doi: 10.1158/1078-0432.CCR-09-1314
- Barrington DA, Dilley SE, Smith HJ, Straughn JM. Pem-brolizumab in advanced recurrent endometrial cancer: A cost-effectiveness analysis. Gynecol. Oncol. 2019;153(2):381-384. doi: 10.1016/j.ygyno.2019.02.013


