Клинический случай успешной эндоваскулярной коррекции артерио-мочеточниковой фистулы
Автор: Чернявский Михаил Александрович, Мосоян М.С., Ванюркин А.Г., Сусанин Н.В., Казанцев А.Н.
Журнал: Патология кровообращения и кардиохирургия @journal-meshalkin
Рубрика: Случаи из клинической практики
Статья в выпуске: 3 т.25, 2021 года.
Бесплатный доступ
Артерио-мочеточниковая фистула - относительно редкое патологическое состояние, которое характеризуется дефектом между кровеносными сосудами и прилегающими к ним дистальными сегментами мочеточника. Ввиду высокого риска геморрагического шока на фоне рецидивирующей массивной гематурии является жизнеугрожающим. Цель публикации - продемонстрировать успешное эндоваскулярное лечение пациентки 51 года с артерио-мочеточниковыми фистулами. Из анамнеза: эвисцерация органов малого таза с формированием уретерокутанеостомы и колостомы. Для улучшения оттока мочи и профилактики стенозов мочеточников установлены мочеточниковые стенты. После удаления стентов эпизоды рецидивирующих профузных кровотечений из уретерокутанеостомы. При поступлении выполнили мультиспиральную компьютерную томографию с ангиографией подвздошных артерий, экстравазаций контрастного вещества не выявили, однако определили сдавление левой общей подвздошной артерии извне левым мочеточником. После дообследования имплантировали баллонорасширяемый стент-графт в левую общую подвздошную артерию. В послеоперационном периоде кровотечения не рецидивировали. Клинический случай демонстрирует высокую эффективность эндоваскулярного лечения артерио-уретеральных фистул, а также необходимость комплексного и мультидисциплинар-ного подхода при ведении таких больных. Малоинвазивная методика позволяет снизить хирургическую травму и в короткие сроки изолировать патологический сброс крови из артерии в мочеточник. Обсуждены преимущества и недостатки эндоваскулярных технологий при лечении представленной патологии.
Артерио-мочеточниковая фистула, артерио-уретеральная фистула, массивная гематурия, мочеточниковый стент, стент-графт, эвисцерация органов
Короткий адрес: https://sciup.org/142230791
IDR: 142230791 | DOI: 10.21688/1681-3472-2021-3-100-105
Clinical case of successful endovascular correction of an arterio-ureteral fistula
Arterio-ureteral fistulas are a pathological condition characterised by the appearance of a defect between the blood vessels and adjacent distal segments of the ureter. Arterio-ureteral fistulas are relatively rare and potentially life-threatening, since they are associated with a high risk of developing haemorrhagic shock against the background of recurrent massive haematuria. This study describes the successful endovascular treatment of arterio-ureteral fistulas in a 51-year-old female patient. Evisceration of the pelvic organs was performed, followed by uretero-cutaneostomy and colostomy. Ureteral stents were installed to improve the outflow of urine and prevent ureteral stenosis. After stent removal, episodes of recurrent profuse bleeding from uretero-cutaneostomy occurred. On admission, multi-spiral computed tomography with angiography of the iliac arteries was performed. Extravasation of the contrast agent was not detected; however, external compression of the left common iliac artery by the left ureter was identified. After further examination, a balloon-expandable stent-graft was implanted into the left common iliac artery. The postoperative period thereafter was uneventful. This clinical case demonstrates the highly efficient endovascular treatment of the presented pathology and exemplifies the need for an integrated and multidisciplinary approach in the diagnosis and treatment of arterio-ureteral fistulas. Minimally invasive techniques can reduce surgical trauma and quickly isolate pathological blood discharge from the artery into the ureter. The advantages and disadvantages of endovascular technologies in the treatment of the presented pathology are also discussed.
Текст научной статьи Клинический случай успешной эндоваскулярной коррекции артерио-мочеточниковой фистулы
М.А. Чернявский,
М.С. Мосоян,
А.Г. Ванюркин,
Н.В. Сусанин,
А.Н. Казанцев,
Артерио-мочеточниковая фистула (АМФ) — относительно редкое и потенциально опасное для жизни состояние, характеризующееся высокой смертностью из-за рецидивирующих спонтанных кровотечений [1; 2]. Клиническая картина включает в себя задержку мочи, лихорадку, боль в животе, однако наиболее частый признак — гематурия различной интенсивности [3; 4]. Среди пациентов женского и мужского пола АМФ распространены в соотношении 3 : 2 [3–5]. Основные факторы риска — постоянный мочеточниковый стент в мочеточниках, злокачественное новообразование в анамнезе, хирургическое вмешательство на органах брюшной полости и малого таза [5–7].
Первичное диагностическое обследование включает ангиографию, компьютерную томографию, уретерографию. Симптомы патологии неспецифические и на момент обследования могут отсутствовать [1–5]. Есть данные о проведении провокационных тестов при цистоскопии, инициирующих гематурию из фистулы, однако метод может вызвать неконтролируемое кровотечение и геморрагический шок [3–7].
15 % известных случаев АМФ связаны с первичным ослаблением артериальной и мочеточниковой стенок при артериовенозных мальформациях, аневризмах аорты и подвздошных артерий [8; 9]. Воспаление или хронические дегенеративные процессы приводят к эрозии стенки мочеточника в прилегающую сосудистую сеть или магистральные артерии [1; 5; 7; 9]. Пульсирующий кровоток в артериях создает механическое трение, вызывая раздражение и структурное ослабление стенок с последующим прорывом крови в просвет мочеточника [2; 3; 6]. 85 % АМФ вторичные, возникающие после хирургических вмешательств по поводу рака органов брюшной полости и малого таза, а также из-за размещения артериальных трансплантатов вблизи от мочеточников, установки постоянных мочеточниковых стентов для отвода мочи [8–11]. Патогенез вторичных АМФ схож с первичными: пульсация артерии и ее непосредственная близость с мочеточником создают механическое трение и приводят к эрозии их стенок.
Дефицит исследований, обусловленный редкостью патологии, создает неопределенность в лечении изучаемой когорты больных. Опубликованы единичные клинические случаи по «открытым» и эндоваскулярным техникам. В настоящей работе продемонстрирован эндоваскулярный способ коррекции АМФ у пациента с макрогематурией и оперативным лечением органов малого таза в анамнезе.
Клинический случай
Пациентка К., 51 год, поступила в отделение сердечно-сосудистой хирургии № 2 ФГБУ «НМИЦ им. В.А. Алмазова» Минздрава России в экстренном порядке. Из анамнеза: состояние после комплексной терапии и хирургического лечения по поводу рака шейки матки — экстирпации матки с придатками в феврале 2020 г. В мае 2020 г. ввиду рецидива злокачественного новообразования выполнена эвисцерация органов малого таза с резекцией подвздошной кишки, аппендэктомией и последующим наложением колостомы и уретерокутанеостомы. После оперативного вмешательства в обоих мочеточниках установлены мочеточниковые стенты для улучшения оттока мочи и профилактики стенозирования. Периодическую замену стентов осуществлял уролог по месту жительства. В ноябре 2020 г. во время планового удаления стентов возникло обильное кровотечение из кутанеосто-мы. Гематурию купировали повторной установкой левого мочеточникового стента. Пациентку обследовали в хирургическом стационаре по месту жительства, на селективной ангиографии признаков экстравазации не выявили, выполнили масляную окклюзию левой мочеточниковой артерии. Проводили гемостатическую и гемотрансфузионную коррекцию с целью восполнения объема циркулирующей крови. На второй день после выписки из стационара возник рецидив массивного кровотечения из кутанеостомы. Пациентку экстренно госпитализировали в хирургический стационар по месту жительства, провели консультацию уролога по поводу гематурии, по жизненным показаниям выполнили левостороннюю нефрэктомию. На 3-й и 6-й дни после операции — повторные эпизоды кровотечения. Провели телемедицинскую консультацию с сосудистым хирургом ФГБУ «НМИЦ им. В.А. Алмазова» Минздрава России, 08.01.2021 г. сан-транспортом доставили больную в отделение сердечно-сосудистой хирургии № 2.
На момент поступления состояние гемодинамически стабильное, эпизода кровотечения не было. Моча по уретерокутанеостоме соломенно-желтого цвета. Пульсация на магистральных артериях сохранена. Общий анализ крови: гемоглобин 87,6 г/л, эритроциты 3,1 × 1012/л, гематокрит 33,9 %. Общий
Рис. 1. Мультиспиральная компьютерная томография – ангиография аортоподвздошного сегмента, 3D-реконструкция Примечание. 1 — гемодинамически незначимое сужение левой общей подвздошной артерии.
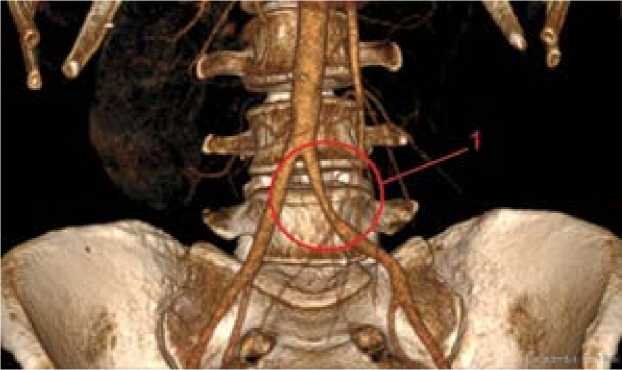
анализ мочи: эритроциты 75 × 106/л, лейкоциты 103 × 106/л.
С целью верификации локализации АМФ выполнили мультиспиральную компьютерную томографию – ангиографию артерий аорто-подвздошного сегмента, по данным которой экстравазации контрастного вещества в брюшном отделе аорты, ее висцеральных ветвях и подвздошных артериях не обнаружили. Выявили гемодинамически незначимое сужение левой общей подвздошной артерии (рис. 1).
Пациентка предоставила результаты мультиспи-ральной компьютерной томографии – ангиографии органов брюшной полости после установки мочеточниковых стентов, по которым левый мочеточник пересекает левую общую подвздошную артерию, вызывая ее сдавление (рис. 2).
Диагноз по результатам обследования — ар-терио-уретеральная фистула между левым мочеточником и левой общей подвздошной артерией. Осложнение — рецидивирующее наружное кровотечение. Острая постгеморрагическая анемия средней степени тяжести. Сопутствующий рак шейки матки рT2bNxM0 после комплексной терапии в 2019 г., оперативного лечения в 2020 г. Эвисце-рация органов малого таза по поводу рака шейки матки в 2020 г. Нефрэктомия слева в 2020 г. Коло-стома слева, двухсторонняя уретерокутанеостома.
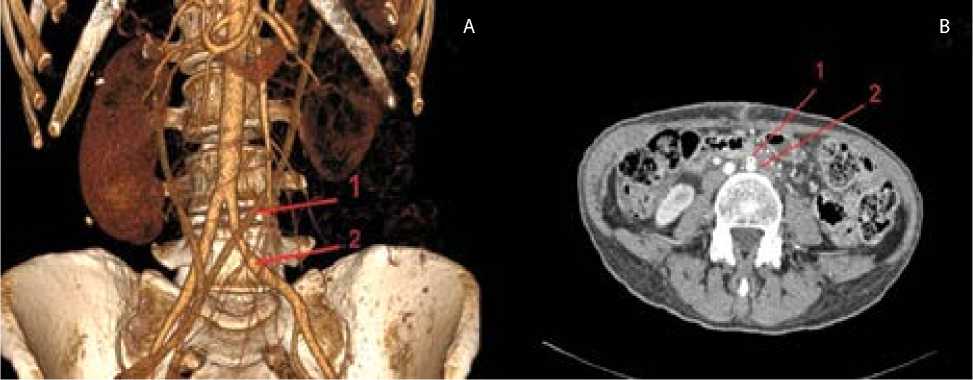
Рис. 2. Мультиспиральная компьютерная томография – ангиография аортоподвздошного сегмента после установки мочеточниковых стентов: 3D-реконструкция (A); поперечный срез на уровне общих подвздошных артерий (B) Примечание . 1 — левый мочеточниковый стент; 2 — левая общая подвздошная артерия.
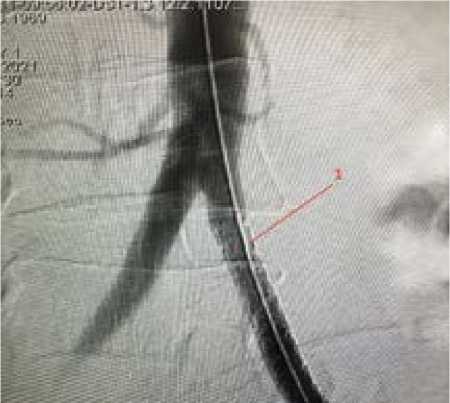
Рис. 3. Ангиография аорто-подвздошного сегмента после установки стента
Примечание. 1 — стент-графт LifeStream, имплантированный в левую общую подвздошную артерию.
Поскольку активное кровотечение из АМФ во время обследования отсутствовало, решили основываться на предоставленных результатах муль-тиспиральной компьютерной томографии – ангиографии и на анамнезе заболевания: эпизоды кровотечения были спровоцированы удалением левого мочеточникового стента и купированы его обратной установкой. Мультидисциплинарный консилиум из сердечно-сосудистого хирурга, уролога, кардиолога, анестезиолога-реаниматолога принял решение об эндоваскулярной установке стент-графта в левую подвздошную артерию в месте ее сдавления левым мочеточником.
Ход операции
После обработки операционного поля под местной анестезией 10,0 мл 0,1% раствора лидокаина выполнили пункцию левой общей бедренной артерии, установили интродьюсер 7F. На ангиографии определили гемодинамически незначимый стеноз левой общей подвздошной артерии на границе верхней и средней третей. В зону дефекта стенки сосуда завели и имплантировали баллонорасширяемый стент-графт LifeStream (Becton, Dickinson and Company, Франклин Лейкс, США) 8 × 58 мм. Выполнили постдилатацию баллонным катетером Mustang (Boston Scientific, Мальборо, США)
7 × 20 мм. Контрольная ангиография показала область стентирования без гемодинамически значимых остаточных стенозов, диссекций, экстраваза-ций (рис. 3). Удалили инструменты из сосудистого русла, ушили пункционное отверстие устройством Angio-Seal (Terumo Medical Corporation, Сомерсет, США), наложили асептическую повязку.
Послеоперационный период протекал без особенностей, болевой синдром, кровотечение и макрогематурия отсутствовали, пульсация на магистральных артериях сохранялась удовлетворительной. Общий анализ крови: гемоглобин 94,2 г/л, эритроциты 3,2 × 1012/л, гематокрит 33,8 %. Общий анализ мочи: эритроциты 0, лейкоциты 34 × 106/л. Пациентку выписали для амбулаторного наблюдения в удовлетворительном состоянии на 3-е сут. после вмешательства.
Обсуждение
Для коррекции АМФ используют хирургические и эндоваскулярные методы. Поскольку у большинства пациентов в анамнезе хирургические вмешательства на органах брюшной полости и малого таза, операция сопряжена с техническими сложностями из-за повторного доступа и высоким риском летального исхода. Имеется информация об эмболизации АМФ спиралью, однако данный метод повышает риск дистальной эмболизации магистральных артерий, что может привести к острой ишемии нижних конечностей [1; 5; 7; 9]. При локализации фистулы на общей или наружной подвздошных артериях эндоваскулярная имплантация стент-графта оптимальна, безопасна и сопряжена с наименьшим риском осложнений [2; 5; 7]. Основные преимущества — малотравматичность и возможность в короткие сроки изолировать патологическое сообщение на момент кровотечения. Недостатком является необходимость назначения антиагрегантной терапии для профилактики тромбоза стент-графта, которая ограничивает применение эндоваскулярного подхода при высоком риске кровотечения [3; 5; 7; 9]. Также у пациентов с хроническим воспалительным процессом в мочевыводящих путях после имплантации стент-графта существует угроза его инфицирования в послеоперационном периоде, что может потребовать профилактического назначения антибиотикоте-рапии в периоперационном периоде [3; 7–9; 11]. Конкретные рекомендации по лечению АМФ отсутствуют, а выбор тактики определяется опытом ангиохирургов, возможностью выполнять как «открытое», так и эндоваскулярное вмешательство [1; 2; 4; 5; 10]. Представленный клинический случай демонстрирует, что для диагностики и определения оптимального и наименее травматичного подхода к лечению артерио-уретеральных фистул необходим мультидисциплинарный подход.
Ограничения
Клинический случай реализован с опорой на опыт эндоваскулярных хирургов и урологов. Отсутствие данных в действующих рекомендациях о лечении данной патологии создавало неопределенность в выборе стратегии. Единственный правильный вариант коррекции дифференцировал мультидисциплинарный консилиум.
Заключение
Установка стент-графта в область АМФ эффективна и безопасна в лечении сложного для курации пациента. При множественных полостных вмешательствах на органах малого таза эта методика коррекции оптимальна. Стратегию лечения данной когорты больных должен определять мультидис-циплинарный консилиум персонифицированно, с учетом всех факторов риска пациента.
Список литературы Клинический случай успешной эндоваскулярной коррекции артерио-мочеточниковой фистулы
- Yoshioka N., Takagi K., Morita Y., Kawase M., Morishima I. Endovascular treatment of arterio-ureteral fistula with new-generation balloon-expandable stent graft using a 7-French system. SAGE Open Med Case Rep. 2020;8:2050313X20959219. PMID: 33062280; PMCID: PMC7534066. https://doi. org/10.1177/2050313X20959219
- Kaneko T., Sakamoto A., Yamada Y., Yamamoto M., Kondo H., Nakagawa T. Uretero-arterial fistula treated with endovascular stent graft following multiple interventions. IJU Case Rep. 2020;3(6):275-277. PMID: 33163924; PMCID: PMC7609180. https://doi.org/10.1002/iiu5.12216
- Malgor R.D., Oderich G.S., Andrews J.C., McKusick M., Kalra M., Misra S., Gloviczki P., Bower T.C. Evolution from open surgical to endovascular treatment of ureteral-iliac artery fistula. J Vasc Surg. 2012;55(4):1072-1080. PMID: 22326578; PMCID: PMC4476467. https://doi.org/10.1016/uvs.2011.11.043
- Guntau M., Hegele A., Rheinheimer S., Hofmann R., Mahnken A.H. Balloon-expandable stent graft for treating uretero-iliac artery fistula. Cardiovasc Intervent Radiol. 2017;40(6):831-835. PMID: 28150018. https://doi.org/10.1007/ s00270-017-1586-4
- Horie K., Fujiwara T., Satoyoshi K., Munehisa M., Inoue N. Endovascular treatment of ureteroarterial fistula using a covered stent, evaluated by intravascular ultrasound: a case report. CVIR Endovasc. 2019;2(1):16. PMID: 32026230; PMCID: PMC6966421. https://doi.org/10.1186/s42155-019-0060-6
- Gallo F., Gastaldi E., Spirito G., Barile A., Kosir C., Giberti C. A case of iliac-artery-ureteral fistula managed with a combined endoscopic approach. Nat Clin Pract Urol. 2008;5(4):225-228. PMID: 18334976. https://doi.org/10.1038/ncpuro1059
- Kuramoto T., Muraoka S., Nishikawa T., Matsumoto Y., Uokawa K. A Case of ureteroarterial fistula successfully treated with endovascular stent graft. Hinyokika Kiyo. 2019;65(7):299-303. PMID: 31501396. https://doi.org/10.14989/ ActaUrolJap 65 7 299
- Araki T., Nagata M., Araki T., Takihana Y., Takeda M. Endovascular treatment of ureteroarterial fistulas with stent-grafts. Radiat Med. 2008;26(6):372-375. PMID: 18677613. https://doi.org/10.1007/s11604-008-0235-x
- Krenzien J., Wagner R. Iliac artery-ureteral fistula and its treatment. Zentralbl Chir. 2003;128(9):768-773. PMID: 14533048. https://doi.org/10.1055/s-2003-42757
- Mahlknecht A., Bizzotto L., Gamper C., Wieser A. A rare complication of ureteral stenting: Case report of a uretero-arterial fistula and revision of the literature. Arch Ital Urol Androl. 2018;90(3):215-217. PMID: 30362691. https://doi. org/10.4081/aiua.2018.3.215
- Madonia M., Russo G.I., Trignano E., Paliogiannis P., Cimino S., Corbu C., Morgia G. A case of gross haematuria due to an ureteric-iliac artery fistula. Ann Ital Chir. 2013;84(ePub):S2239 253X13021750. PMID: 24395028.


