Клиническое значение суточного мониторирования артериального давления в прогнозировании развития артериальной гипертензии у больных подагрой
Автор: Губанова М.В., Кушнаренко Н.Н., Караваева Т.М.
Журнал: Сибирский журнал клинической и экспериментальной медицины @cardiotomsk
Рубрика: Клинические исследования
Статья в выпуске: 3 т.36, 2021 года.
Бесплатный доступ
Цель исследования: разработать модель ранней диагностики артериальной гипертензии (АГ) у больных подагрой, основанную на данных суточного мониторирования артериального давления (СМАД).Материал и методы. Проведено одномоментное поперечное проспективное исследование 69 пациентов с подагрой. Было выделено 3 исследуемые группы: 1-я группа (основная) - 41 мужчина с подагрой и АГ, 2-я группа (группа сравнения) - 28 мужчин с подагрой с нормальным уровнем АД, 3-я группа (контрольная) включала 30 относительно здоровых мужчин. СМАД проводили в амбулаторных условиях прибором BPLab («Петр Телегин», Россия).Результаты. Были выявлены статистически значимые межгрупповые различия по показателям минимального, среднего, максимального суточного систолического артериального давления (САД) у пациентов основной группы и группы сравнения (р
Подагра, артериальная гипертензия, суточное мониторирование артериального давления
Короткий адрес: https://sciup.org/149139340
IDR: 149139340 | УДК: 616-002.78-06-037:616.12-008.331.1-07 | DOI: 10.29001/2073-8552-2021-36-3-104-110
Clinical significance of 24-hour blood pressure monitoring in prediction of hypertension development in patients with gout
Aim. The aim of the study was to develop the model for establishing early diagnosis of hypertension in patients with gout. The model was based on data of 24-hour blood pressure monitoring.Material and Methods. A total of 69 patients with gout were enrolled in a single-stage cross-sectional prospective study. Three study groups were assigned as follows: group 1 (main group) comprised hypertensive men with gout (n = 41); group 2 (comparison group) comprised normotensive men with gout (n = 28); group 3 (control) included relatively healthy men (n = 30). Daily blood pressure monitoring was performed on an outpatient basis using a BPLab device (Peter Telegin, Russia).Results. The significant intergroup differences were found in the following parameters: lowest, mean, and highest 24-hour systolic blood pressure (SBP) values in patients of main and comparison groups (p
Текст научной статьи Клиническое значение суточного мониторирования артериального давления в прогнозировании развития артериальной гипертензии у больных подагрой
Подагра является самой распространенной формой воспалительного артрита, обусловленной отложением кристаллов моноурата натрия (МУН), образующихся в результате длительной гиперурикемии [1]. Помимо «классических» суставных проявлений подагра характе- ризуется высокой частотой сопутствующих заболеваний, прежде всего, почек и сердечно-сосудистых патологий, а также высокой смертностью, превышающей популяционную [2]. Особый вклад в развитие и прогрессирование сердечно-сосудистых осложнений при подагре вносит артериальная гипертензия (АГ) [3, 4]. Последние два десятилетия посвящены исследованию сложных клинико-патогенетических взаимодействий повышенного уровня мочевой кислоты и АГ [5, 6]. Действительно, повышение уровня мочевой кислоты сыворотки крови в результате воздействия внешнесредовых и генетических факторов способствует инициации иммуновоспалитель-ных нарушений, окислительного стресса, циклооксигеназы-2, пролиферации эндотелия, гломерулотубулярного повреждения, формированию тубулоинтерстициального фиброза, нейрогуморальной активации, индуцирующих повышение артериального давления (АД) [7, 8]. В свою очередь наличие АГ способствует утяжелению некоторых сопутствующих состояний – инсулинорезистентности, дислипидемии, хронической болезни почек, создавая порочный круг причинно-следственных взаимосвязей повышенного уровня уратов и развития подагры в будущем [5, 9]. Таким образом, ранняя диагностика и лечение АГ у больных подагрой является важным в плане контроля связанных с АГ сопутствующих состояний [3].
Цель исследования: разработать модель ранней диагностики АГ у больных подагрой, основанную на данных суточного мониторирования АД (СМАД).
Материал и методы
В течение 2011–2016 гг. проведено одномоментное поперечное исследование с участием 69 пациентов
Критерии включения: пациенты мужского пола с подтвержденным диагнозом подагры, установленным в соответствии с рекомендациями ACR/EULAR (2015) [10] или имеющие один или несколько критериев S.L Wallace (1977) [11].
Критерии исключения: наличие ишемической болезни сердца, сахарного диабета, дебют АГ до возникновения вспышки подагрического артрита, наличие острых воспалительных и хронических заболеваний в стадию обострения, алиментарно-конституциональное ожирение.
Были выделено 3 исследуемые параллельные группы: 1-я группа (основная) - 41 мужчина с подагрой и АГ, 2-я группа (группа сравнения) - 28 мужчин с подагрой с нормальным уровнем АД, 3-я группа (контрольная) включала 30 относительно здоровых мужчин.
Исследование одобрено этическим комитетом Читинской государственной медицинской академии Министерства здравоохранения Российской Федерации (протокол № 64 от 23.06.2014 г.). Перед проведением комплекса необходимых исследований получено информированное добровольное согласие пациентов, работа выполнена в соответствии с требованиями Хельсинкской декларации Всемирной медицинской организации (2013).
Всем пациентам проведено общеклиническое и лабораторное (определение концентрации мочевой кислоты сыворотки крови) обследование. СМАД проводили в амбулаторных условиях прибором BPLab («Петр Телегин», Россия), позволяющим анализировать показатели периферического и центрального аортального давления. Интервал измерений составлял 15 мин днем (06:00– 22:00) и 30 мин ночью (22:00– 06:00). Изучали общепринятые параметры СМАД: средние значения АД, вариабельность АД, индексы гипер- и гипотензии, степень ночного снижения АД.
Статистическая обработка результатов исследования осуществлялась с помощью пакета программ IBM SPSS STATISTICS, Version 25.0 (IBM, США). При проведении статистического анализа авторы руководствовались принципами Международного комитета редакторов медицинских журналов (ICMJE) и рекомендациями
«Статистический анализ и методы в публикуемой литературе» (SAMPL) [12]. Учитывая численность исследуемых групп (менее 50), оценка нормальности распределения признаков проводилась с помощью W-критерия Шапиро - Уилка, который в данной ситуации является наиболее эффективным, так как обладает большей мощностью по сравнению с альтернативными критериями проверки нормальности. В отсутствие нормальности распределения признаков данные представлены в виде медианы, первого и третьего квартилей ( Me [ Q1, Q3 ]). Различия количественных показателей в трех независимых группах пациентов выявлялись по критерию Краскела – Уоллиса. Апостериорные попарные сравнения количественных показателей в группах проводились по критерию Манна - Уитни с поправкой Бонфер-рони. Для определения степени линейных взаимосвязей между возможными предикторами АГ у больных подагрой использовали коэффициент корреляции Спирмена. Силу связи между исследуемыми параметрами оценивали по шкале Чеддока [13]. Методом логистической регрессии была создана модель, позволяющая прогнозировать развитие АГ у больных подагрой [13]. Для анализа качества предлагаемой прогностической модели был выполнен ее ROC-анализ [13].
Результаты во всех случаях считали статистически значимыми при р < 0,05.
Результаты и обсуждение
В исследование были включены 69 мужчин в возрасте 52,0 [41,3; 57,8] лет с диагнозом «подагра» с различным клиническим течением заболевания (интермиттирующим и хроническим), одинаково сопоставимым по дозе ингибитора ксантиноксидазы (аллопуринола). Медиана возраста дебютa подагры составила 43,0 [36,0; 47,0] года. У преобладающего большинства пациентов (58 человек, 84%) отмечалось классическое начало заболевания (интенсивные боли в I плюснефаланговом суставе большого пальца стопы). У 11 (16%) мужчин начало болезни имело атипичную картину, что послужило причиной поздней диагностики подагры (табл. 1).
Нами были изучены основные показатели периферической гемодинамики методом СМАД с оценкой суточных показателей (минимального, среднего и максимального) систолического (САД), диастолического (ДАД) и пульсового давления (ПД), таблица 2.
Установлено, что у больных подагрой, страдающих АГ, медиана среднесуточного САД была на 10,5% выше значений медианы среднесуточного САД у пациентов с подагрой с нормальным уровнем АД и на 14% выше медианы среднесуточного САД у здоровых лиц.
Кроме того, у пациентов 1-й группы медиана среднесуточного ДАД увеличивалась в среднем на 11,5% по сравнению со 2-й группой и на 8,5% – по сравнению с 3-й группой.
При анализе параметров ПД установлено, что медиана среднесуточного ПД у больных подагрой с АГ превышала медиану данного показателя в контрольной группе в 1,31 раза и в группе сравнения – в 1,21 раза.
Обращает на себя внимание тот факт, что медианные показатели среднесуточного ПД у пациентов 2-й группы увеличивались относительно контрольной группы в 1,16 раза, что может указывать на повышение жесткости крупных артерий у мужчин, страдающих подагрой с нормальными цифрами АД.
Таблица 1. Клиническая характеристика больных подагрой в исследуемых группах, df = 2
Table 1. Clinical characteristics of patients with gout in the study groups, df = 2
|
Показатели Parameters |
Исследуемые группы Study groups |
|
|
1-я группа, n = 41 Group 1, n = 41 |
2-я группа, n = 28 Group 2, n = 28 |
|
|
Длительность заболевания, лет Duration of disease, years |
7,5 [3,0; 13,5]* |
2,0 [1,0; 3,0] |
|
Частота рецидивов артрита в год Frequency of arthritis relapses per year |
4,0 [2,0; 7,0]* |
2,0 [0,5; 2,0] |
|
Количество пораженных суставов Number of affected joints |
5,0 [2,0; 7,0]* |
2,0 [1,0; 2,0] |
|
Длительность артрита, дни Duration of arthritis, days |
6,0 [5,0; 15,0]* |
3,0 [2,0; 4,0] |
|
Уровень мочевой кислоты, мкмоль/л Uric acid level, mmol/L |
614,4 [509,2; 680,8]* |
507,66 [472,28; 578,4] |
|
Холестерин липопротеинов высокой плотности, ммоль/л High-density lipoproteins, mmol/L |
0,98 [0,93; 1,3] |
1,2 [1,15; 1,25] |
|
Холестерин липопротеинов низкой плотности, ммоль/л Low-density lipoproteins, mmol/L |
2,5 [1,5; 3,3]* |
3,6 [3,5; 3,7] |
|
Триглицериды, ммоль/л Тriglycerides, mmol/L |
2,4 [1,7; 5,4]* |
2,1 [1,7; 3,8] |
|
Холестерин, ммоль/л Cholesterol, mmol/l |
5,16 [4,6; 5,6] |
5,5 [5,3; 5,8] |
|
Индекс атерогенности, ммоль/л Atherogenic index, mmol/L |
4,3 [3,4; 4,8]* |
3,75 [3,5; 3,8] |
|
Индекс массы тела, кг/м2 Body mass index, kg/m2 |
30,6 [28,2; 33,1] |
29,9 [26,7; 32,1] |
Примечание: * – р < 0,01 – статистическая значимость различий пациентов с подагрой и пациентов контрольной группы.
Note: *– р < 0.01 – significant differences between patients with gout and patients of control group.
Таблица 2. Показатели периферической гемодинамики в исследуемых группах, df = 2
Table 2. Parameters of peripheral hemodynamics in the study groups, df = 2
|
Клинические параметры Clinical parameters |
Исследуемые группы Study groups |
||
|
1-я группа, n = 41 Group 1, n = 41 |
2-я группа, n = 28 Group 2, n = 28 |
3-я группа, n = 30 Group 3, n = 30 |
|
|
Суточное САД min, мм рт. ст. Lowest 24-hour SBP, mm Hg |
104,2 [102,0; 106,4] *,*** |
95,7 [94,5; 97,0] |
89,9 [88,4; 91,5] |
|
Суточное САД mean, мм рт. ст. Mean 24-hour SBP, mm Hg |
134,6 [132,8; 136,4] *,*** |
119,6 [118,5; 120,6] |
114,9 [113,3; 116,4] |
|
Суточное САД max, мм рт. ст. Highest 24-hour SBP, mm Hg |
167,1 [164,4; 169,7] *,*** |
148,4 [146,5; 150,2] |
142,8 [140,3; 145,3] |
|
Суточное ДАД mean, мм рт. ст. Mean 24-hour DBP, mm Hg |
78,9 [77,1; 80,7] *, *** |
70,2 [69,1; 71,3] |
72,4 [71,1; 73,7] |
|
Суточное ДАД max, мм рт. ст. Highest 24-hour DBP, mm Hg |
109,0 [106,7; 111,3] *,*** |
96,0 [93,6; 98,2] |
98,8 [96,3; 101,2] |
|
Суточное ПД min, мм рт. ст. Lowest 24-hour PBP, mm Hg |
35,1 [33,6; 36,6] *,*** |
31,8 [30,8; 32,9] ** |
28,3 [27,4; 29,3] |
|
Суточное ПД mean, мм рт. ст. Mean 24-hour PBP, mm Hg |
55,8 [54,3; 57,3] *, *** |
49,9 [48,8; 51,1] ** |
42,6 [41,7; 43,4] |
|
Суточное ПД max, мм рт. ст. Highest 24-hour PBP, mm Hg |
81,8 [79,3; 84,2] *,*** |
70,6 [68,3; 72,9] ** |
59,5 [57,8; 61,2] |
Примечание: * – р < 0,001 – статистическая значимость различий основной группы и группы сравнения, ** – р < 0,05 – статистическая значимость различий группы сравнения с контрольной группой, *** – р < 0,001 – статистическая значимость различий основной группы с контрольной группой. Note: * – р < 0.001 – significant differences between main group and comparison group. ** – р < 0.05 – significant differences between comparison group and control group, *** – р < 0.001 significant differences between main group and control group.
Согласно современным представлениям, среднесуточная величина пульсового АД > 53 мм рт. ст. ассоциируется с высокой частотой сердечно-сосудистых осложнений и неблагоприятным прогнозом у больных АГ [14].
Важным критерием, определяющим безопасный уровень АД, является индекс времени (ИВ). Данный показатель определяет процент времени, в течение которого величины АД превышают критический («безопасный») уровень, т. е. демонстрирует, в каком проценте времени от общей длительности мониторирования АД было выше
(ниже) нормального, причем условной границей нормы для дневного времени считается 140/90, а для ночного – 125–130/80 мм рт. ст. ИВ у большинства здоровых лиц колеблется от 10 до 20% и не превышает 25%. Значение ИВ для САД более 25% считается патологическим, что дает основание для постановки диагноза лабильной АГ. Стабильная АГ диагностируется при ИВ не менее чем у 50% пациентов в дневное и ночное время [15]. На основании анализа этого показателя у пациентов основной группы диагностирована систоло-диастолическая (лабильная и стабильная) АГ. В данную группу были внесены пациенты с ИВ, превышающим 25% (табл. 3).
Установлено, что у больных подагрой, страдающих АГ, медианные значения ИВ САД днем, ИВ САД ночью, ИВ ДАД днем увеличивались относительно группы сравнения более чем в 7 раз ( р < 0,001), величины ИВ ДАД ночью – в 4,4 раза ( р < 0,001).
Медианные показатели ИВ САД днем и ИВ САД ночью у больных подагрой с АГ превышали аналогичные показатели контрольной группы более чем в 8,43 раза (р < 0,001). Медианы ИВ ДАД днем и ИВ ДАД ночью у больных 1-й группы превышали таковые 3-й группы более чем в 3,25 раза (р < 0,001).
Были определены значимые независимые предикторы развития АГ у больных подагрой - показатели СМАД, построена модель бинарной логистической регрессии, на основе которой был получен алгоритм для ранней диагностики АГ у больных подагрой (табл. 4).
Таблица 3. Показатели индекса времени в исследуемых группах, df = 2
Table 3. Time index values in the study groups, df = 2
|
Клинические параметры Clinical parameters |
Исследуемые группы Study groups |
Уровень статистической значимости различий Statistical significance |
||
|
1-я группа, n = 41 Group 1 n = 41 |
2-я группа, n = 28 Group 2 n = 28 |
3-я группа, n = 30 Group 3 n = 30 |
||
|
ИВ САДд SBP TI, day |
47,7 [42,2; 53,2] |
6,4 [5,1; 7,8] |
4,4 [3,0; 5,7] |
< 0,001 |
|
ИВ САДн SBP TI, night |
49,7 [43,3; 56,2] |
6,4 [5,3; 7,6] |
8,2 [6,2; 10,2] |
< 0,001 |
|
ИВ ДАДд DBP TI, day |
29,2 [24,0; 34,4] |
4,0 [2,7; 5,3] |
7,7 [5,5; 9,8] |
< 0,001 |
|
ИВ ДАДн DBP TI, night |
41,5 [34,8; 48,1] |
9,4 [6,9; 11,8] |
15,3 [12,5; 18,2] |
< 0,001 |
Таблица 4. Коэффициенты регрессии в разработанной модели
Table 4. Regression coefficients in the developed model
|
Модель Мodel |
B |
Среднеквадратичная ошибка Root-mean-square error |
Вальд Wald |
Число степеней свободы Degree of freedom |
Значимость Significance |
Exp (B) |
|
Константа Constant |
51,93 |
13,52 |
14,75 |
1 |
0,001 |
0,001 |
|
САД min Lowest SBP |
–0,14 |
0,08 |
3,02 |
1 |
0,082 |
0,869 |
|
САД mean Mean SBP |
0,39 |
0,11 |
12,41 |
1 |
0,001 |
1,477 |
|
САД мах Highest SBP |
0,11 |
0,06 |
3,73 |
1 |
0,053 |
1,111 |
Согласно построенному прогностическому алгоритму для каждого пациента вычислялась величина К, определяемая формулой:
K =___________________________________________ , 1 + e51,93 + 0,14 x CAД min – САД mean – 0,11 x САД max где e – математическая константа, равная приблизительно 2,72; САД min – минимальное суточное САД (мм рт. ст.); САД mean – среднесуточное САД (мм рт. ст.); САД max – максимальное суточное САД (мм рт. ст.). Вычисленное значение К сравнивалось с пороговым значением 0,54, определенным в модели логистической регрессии. При значении К > 0,54 прогнозируется развитие АГ у больных подагрой. Чувствительность разработанной прогностической модели составляет 0,84, специфичность – 0,95; площадь под ROC-кривой – 0,95 (95% ДИ = 0,91–0,99), рисунок 1.
Учитывая сложность необходимых расчетов, для упрощения использования способа в повседневной клинической практике создано приложение для Android в среде разработки Delphi (Delphi 10.3.3 Rio, Embarcadero Technologies, License No. 2UHK-Z9NG5B-DYPETV-3J8D, США), которое позволяет подтвердить факт развития АГ у больных подагрой. Использование данного алгоритма позволит не только выявить наличие АГ, но и своевременно назначить антигипертензивную терапию.
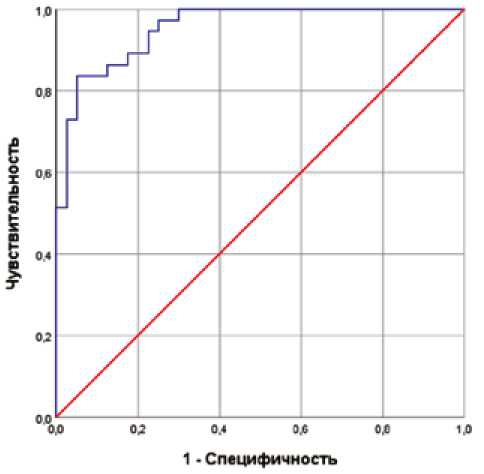
Рис. 1. Площадь под ROC-кривой для разработанной модели
Fig. 1. The area under the ROC curve for the developed model
Заключение
При изучении параметров СМАД установлено превышение значений среднесуточного минимального, среднего и максимального САД, среднего и максимального ДАД, минимального, среднего и максимального ПД у больных подагрой и АГ по сравнению с мужчинами, страдающими подагрой, с нормальными цифрами АД и здоровыми лицами. Однако при анализе ПД в группе больных подагрой с нормотонией выявлено значимое различие параметров минимального, среднего и максимального среднесуточ- ного ПД по сравнению с контрольной группой, что указывает на повышение риска развития АГ у данной категории больных. При оценке величин индексов нагрузки выявлено увеличение ИВ для САД и ДАД днем и ночью у пациентов, страдающих подагрой и АГ, по сравнению с больными подагрой с нормальными цифрами АД и здоровыми лицами. Модель, основанная на определении среднесуточных САД min, САД mean, САД max, позволяет с точностью в 90% проводить раннюю диагностику АГ у больных подагрой.
Список литературы Клиническое значение суточного мониторирования артериального давления в прогнозировании развития артериальной гипертензии у больных подагрой
- Richette P., Bardin T. Gout. Lancet. 2010;375(9711):318-328. DOI: 10.1016/S0140-6736 (09) 60883-7.
- Kuo C.F., Luo S.F. Gout: Risk of premature death in gout unchanged for years. Nat. Rev. Rheumatol. 2017;13(4):200-201. DOI: 10.1038/nr-rheum.2017.27.
- Richette P., Clerson P., Perissin L. Revisiting comorbidities in gout: A cluster analysis. Ann. Rheum. Dis. 2015;74(1):142-147. DOI: 10.1136/ annrheumdis-2013-203779.
- Цыганкова Д.П., Федорова Н.В., Кривошапова К.Е., Максимов С.А., Индукаева Е.В., Шаповалова Э.Б. и др. Социально-экономические факторы риска артериальной гипертензии у пожилых лиц. Сибирский журнал клинической и экспериментальной медицины. 2020;35(4):111-118. DOI: 10.29001/2073-8552-2020- 35-4111-118.
- Елисеев М.С., Новикова А.М. Коморбидность при подагре и гипер-урикемии: распространенность, причины, перспективы уратснижаю-щей терапии. Терапевтический архив. 2019;91(5):120-128. DOI: 10. 26442/00403660.2019.05.000232.
- Полянская А.В., Тузкова Т.С., Паторская О.А. Клиническая характеристика, особенности коморбидности и кардиальных нарушений у пациентов с подагрой и артериальной гипертензией. Военная медицина. 2018;2:57-60.
- Feig D.I., Kang D.H., Johnson R.J. Uric acid and cardiovascular risk. N. Engl. J. Med. 2008;359:1811-1821. DOI: 10.1056/NEJMra 0800885.
- Кушнаренко Н.Н., Мишко М.Ю., Медведева Т.А. Полиморфизм генов фолатного цикла у больных подагрой в популяции русских Забайкальского края. Сибирский журнал клинической и экспериментальной медицины. 2020;35(1):142-150. DOI: 10.29001/2073-8552-202035-1-142-150.
- Кошельская О.А., Журавлева О.А., Карпов РС. Маркеры хронической болезни почек у пациентов с артериальной гипертензией высокого риска: связь с нарушением суточного профиля артериального давления и уровнем внутрипочечного сосудистого сопротивления. Артериальная гипертензия. 2018;24(4):478-489. DOI: 10.18705/1607-419X-2018-24-4-478-489.
- Елисеев М.С. Классификационные критерии подагры (рекомендации ACR/ EULARJ. Научно-практическая ревматология. 2015;53(6):581-585.
- Wallace S.L., Robinson H., Masi A.T., Decker J.L., McCarty D.J., Yu T.F. Preliminary criteria for the classification of the acute arthritis of gout. Arthritis Rheum. 1977;20(3):895-900. DOI: 10.1002/art.1780200320.
- Lang T.A., Altman D.G. Statistical analyses and method sinthepublished literature: The SAMPL guidelines. Medical Writing. 2016;25(3):31-36. DOI: 10.18243/eon/2016.9.7.4.
- Мудров В.А. Алгоритмы корреляционного анализа данных в биомедицинских исследованиях с помощью пакета программ SPSS. Забайкальский медицинский вестник. 2020;2:169-176. URL: http:// zabmedvestnik.ru/arhiv-nomerov/nomer-2-za-2020-god/algoritmy-korreljacionnogo-analiza-dannyh-v-biomedicinskih-issledovanijah-s-pomoshhju-paketa-programm-spss (дата обращения: 9.07.2021).
- Islam M.S. Ambulatory blood pressure monitoring in the diagnosis and treatment of hypertension. Adv. Exp. Med. Biol. 2017;956:109-116. DOI: 10.1007/5584_2016_177.
- Рогоза А.Н. Современные неинвазивные методы измерения артериального давления для диагностики артериальной гипертонии и оценки эффективности антигипертензивной терапии: пособие для врачей. М.: Медика; 2007:72.


