Клиническое значение вариантов внутрисердечных анатомических структур и малых аномалий (обзор литературы)
Автор: Трисветова Е.Л.
Журнал: Сибирский журнал клинической и экспериментальной медицины @cardiotomsk
Рубрика: Обзоры и лекции
Статья в выпуске: 1 т.41, 2026 года.
Бесплатный доступ
Широкое применение в клинической практике прижизненных методов визуализации внутренних структур сердца позволяет выявлять анатомические особенности строения органа и патологические внутрисердечные образования. Из-за неоднородности и вариативности внутрисердечных образований, встречающихся в нормальном сердце, появляются трудности для дифференциальной диагностики с патологическими образованиями (тромб, опухоль) и решения вопроса о дальнейшей тактике. Нормальные внутрисердечные структуры обычно не сопровождаются патологическими клиническими проявлениями, их обнаруживают прижизненно случайно или при аутопсии. Вместе с тем изредка их топографические и морфологические варианты вызывают появление аритмий сердца или тромбоэмболии. Для предотвращения ошибочных диагнозов при развитии патологических симптомов исключаются другие структурные заболевания сердца (ишемическая болезнь сердца, кардиомиопатия, миокардит и т. п.). Основным доступным методом исследования внутрисердечных структур и малых аномалий сердца является трансторакальная эхокардиография (ЭхоКГ), результаты которой дополняют чреспищеводным исследованием, при необходимости – компьютерной томографией (КТ) и магнитно-резонансной томографией (МРТ). При аритмическом синдроме для установления причин аритмии выполняют электрофизиологическое исследование. Мультимодальная визуализация с применением современных методов исследования, электрофизиологическое исследование и знание топографии анатомических вариантов внутренних структур и малых аномалий сердца позволят своевременно выполнить дифференциальную диагностику и планировать дальнейшую тактику лечения или наблюдения.
Внутрисердечные анатомические структуры, малые аномалии сердца, диагностика, визуализирующие методы исследования сердца
Короткий адрес: https://sciup.org/149150633
IDR: 149150633 | УДК: 616.12-018.2(048.8) | DOI: 10.29001/2073-8552-2026-41-1-30-39
Clinical significance of intracardiac anatomical variations structures and minor anomalies (literature review)
Wide application of intravital methods of visualization of internal cardiac structures in clinical practice allows identifying anatomical features of the organ structure and pathological intracardiac formations. Due to heterogeneity and variability of intracardiac formations found in a normal heart, difficulties arise in differential diagnostics with pathological formations (thrombus, tumor) and decision on further tactics. Normal intracardiac structures are usually not accompanied by pathological clinical manifestations, they are discovered during life by chance or during autopsy, however, occasionally their topographic and morphological variants cause cardiac arrhythmias or thromboembolism. To prevent false diagnoses in the development of pathological symptoms, other structural heart diseases (ischemic heart disease, cardiomyopathy, myocarditis, etc.) are excluded. The main available method for studying intracardiac structures and minor cardiac anomalies is transthoracic echocardiography, the results of which are supplemented by transesophageal examination, if necessary – computed tomography and magnetic resonance imaging. In case of arrhythmic syndrome, an electrophysiological study is performed to establish the causes of arrhythmia. Multimodal visualization using modern research methods, electrophysiological study and knowledge of the topography of anatomical variants of internal structures and minor anomalies of the heart will allow timely differential diagnostics and planning of further treatment or observation tactics.
Текст научной статьи Клиническое значение вариантов внутрисердечных анатомических структур и малых аномалий (обзор литературы)
Распространенной проблемой в клинической практике остается дифференциальная диагностика внутрисердечных образований при исследованиях визуализирующими методами. В камерах сердца выявляют различные структуры, которые являются вариантом нормы или патологическими образованиями. Среди вариантов нормального развития сердца встречаются такие образования, как сеть Chiari, евстахиев клапан, левый боковой гребень, модераторный тяж и т. п., а также малые аномалии сердца (аномально расположенные хорды сердца, аномалии папиллярных мышц). Морфологические особенности анатомических образований, их форма, размер, количество, топография могут обусловливать появление таких патологических симптомов, как обструкция выходного тракта левого желудочка, наджелудочковые и желудочковые аритмии, тромбоэмболии [1].
Внутрисердечные образования часто протекают бессимптомно, в редких случаях выслушивается систолический шум на верхушке сердца, из-за которого проводят обследование визуализирующими методами, как правило, наиболее доступными – эхокардиографией (ЭхоКГ). При визуализации внутрисердечного анатомического образования, изменчивость которого велика, его нередко принимают за патологическую структуру (доброкачественную или злокачественную опухоль, метастаз, тромб), требующую медикаментозного лечения или хи- рургического вмешательства. Применение компьютерной томографии (КТ), магнитно-резонансной томографии (МРТ) расширяет диагностические возможности в диагностике нормального анатомического или патологического внутрисердечного образования и для принятия решения о медикаментозной или хирургической тактике лечения либо наблюдения. В случае появления патологических симптомов в виде аритмии сердца, при отсутствии признаков других сердечно-сосудистых заболеваний, причины и источник аритмии выявляют методом электрофизиологического исследования.
Методология исследования
Поиск литературных источников проводился в научных базах Pubmed, eLIBRARY.ru, Embase, Web of Science, КиберЛенинка преимущественно за истекшие 10 лет по ключевым словам и словосочетаниям: евстахиев клапан (Eustachian valve), сеть Киари (Chiari network), гребенчатые мышцы (pectineal muscles;), фиброзномышечный гребень (fibromuscular ridge), модераторный тяж (moderator band), избыточная трабекулярность левого желудочка (left ventricular hypertrabeculation), аномально расположенные хорды (false band), аномалии папиллярных мышц (papillary muscle abnormalities), внутрисердечные образования (Cardiac Masses). Цитируются источники, наиболее соответствующие целям обзора.
Внутрисердечные образования и малые аномалии сердца
В камерах сердца визуализируют известные анатомические структуры сердца, не ассоциированные с патологическими симптомами. Но в случае изменений размеров, формы, протяженности, топографии в эмбриональном периоде под влиянием многих факторов анатомические структуры инициируют развитие патологических симптомов: в правом предсердии – евстахиев клапан, сеть Chiari, пограничный гребень, гребенчатые мышцы; в правом желудочке – наджелудочковый гребень, модераторный пучок; в левом предсердии – левый боковой гребень, аномальный тяж; в левом желудочке – избыточная тра-бекулярность. Малые аномалии сердца – аномалии папиллярных мышц в виде изменения количества, размера, формы, топографии и аномально расположенные хорды встречаются в левом и правом желудочках сердца [2].
Правое предсердие
Евстахиев клапан (заслонка нижней полой вены, евстахиева заслонка или евстахиев клапан) является остатком эмбрионального клапана нижней полой вены и представляет собой складку эндокарда в виде полумесяца, расположенную между устьем нижней полой вены и межпредсердной перегородкой (рис. 1). Во время эмбриогенеза клапан направляет струю крови из нижней полой вены к открытому овальному окну, а при его закрытии после рождения ребенка утрачивает свое функциональное значение. Евстахиев клапан не препятствует обратному току крови в нижнюю полую вену, таким образом, он не функционирует как истинный клапан. По положению, форме, размерам и толщине обнаруживают значительную вариативность евстахиева клапана [1, 3]. Его средняя длина составляет 3,6 мм. У большинства пациентов клинические симптомы отсутствуют, и при ЭхоКГ или при оперативном вмешательстве клапан рассматривают как вариант нормы.
Вместе с тем при изменении размера, протяженности или влиянии неблагоприятных факторов евстахиев клапан является причиной осложнений. Изредка возникает обструкция нижней полой вены, тромбоз, эмболия легочной артерии.
Удлиненный клапан евстахиева канала флотирует в кровотоке в полости правого предсердия, и его необходимо дифференцировать с вегетациями при инфекционном эндокардите, опухолью на ножке или тромбом [4]. Изредка на евстахиевом клапане фиксируются тромбы, при бактериемии появляются вегетации, обусловливающие тромбоэмболию в малый круг кровообращения, а в случае открытого овального окна возрастает риск парадоксальной эмболии в сосуды большого круга кровообращения [4]. При удлиненном евстахиевом клапане создается препятствие для манипуляций при проведении интродьюсера и установки окклюдера.
Рефлекторное раздражение пейсмекерных образований правого предсердия удлиненным евстахиевом клапаном, а также сам клапан с наличием мышечных волокон с клетками проводящей системы инициируют появление аритмий сердца (фибрилляция / трепетание предсердий, наджелудочковая тахикардия) [3–5]. Больших размеров евстахиев клапан вызывает обструкцию потока крови из нижней полой вены и расширение просвета вены. В литературе описаны редкие случаи формирования кисты евстахиевого клапана и миксомы [3–5]. Евстахиев клапан значительных размеров делит полость правого предсердия на две камеры. При этом, как правило, имеется дефект межпредсердной перегородки или открытое овальное окно. В большинстве случаев на гемодинамику евстахиев клапан не влияет, поскольку не полностью делит правое предсердие на две камеры [6]. Клинические проявления в этом случае зависят от наличия сопутствующих аномалий сердца и анатомических характеристик евстахиева клапана.
Сеть Chiari – подвижное сетчатое образование в правом предсердии, которое встречается у 3% населения при аутопсии и сочетается с открытым овальным окном (80%), аневризмой межпредсердной перегородки (20%), евстахиевым клапаном (79%) [7]. Сеть Chiari является остатком правого клапана венозного синуса в случае неполной его резорбции, расположение которого вариативно. Начинается сеть Chiari от области впадения нижней полой вены в правом предсердии и заканчивается вблизи места впадения коронарного синуса (рис.1А). Изредка при значительных размерах сеть Chiari достигает отверстия трикуспидального клапана. При ЭхоКГ сеть Chiari выглядит как фенестрированная тонкая, подвижная структура, которая смещается в систолу и диастолу (рис. 2). При визуализации (ЭхоКГ, МРТ) ее дифференцируют с тромбом, опухолью на ножке, вегетациями и отрывом створочной хорды [8].
Несмотря на то, что сеть Chiari относится к нормальным анатомическим вариантам и у большинства пациентов не сопровождается патологическими симптомами, возможны осложнения, которые будут определять клинические проявления. Подвижность сети Chiari способствует образованию тромбов, попадающих в правый желудочек и малый круг кровообращения, а через открытое овальное окно тромбы проникают в левое предсердие и вызывают парадоксальную эмболию в большом круге кровообращения [9].
M.Q. Al-Sabbagh и соавт. анализировали исследования, выполненные с участием пациентов с кардиоэмболическим инсультом, у которых выявили сеть Chiari / евстахиев клапан и открытое овальное окно. Среди 883 пациентов (средний возраст – 44,6 ± 13,8 года) распространенность сети Chiari / евстахиева клапана и открытого овального окна составила 50% (95% ДИ, 31–68). У 18% (95% ДИ, 12–25) пациентов выявили изолированную сеть Chiari, у 43% (95% ДИ, 25–63) – изолированный евстахиев клапан [10]. У пациентов с кардиоэмболическим инсультом сеть Chiari / евстахиев клапан встречался чаще по сравнению с контрольной группой (ОШ = 2,45; 95% ДИ, 1,2–5; р < 0,01).
К редким клиническим случаям относится выявление папиллярной фиброэластомы на сети Chiari. При ЭхоКГ у 54-летнего мужчины в правом предсердии в области коронарного синуса обнаружили образование, подобное папиллярной фиброэластоме. Резекция опухоли при оперативном вмешательстве и последующее гистологическое исследование подтвердили диагноз папиллярной фиброэластомы, возникшей из сети Chiari [11]. Авторы выявили всего две печатные работы с подобной локализацией папиллярной фиброэластомы.
Пограничный гребень (crista terminalis) , или фиброзномышечный гребень, образован в эмбриональном периоде в результате неполной резорбции клапана правого венозного синуса. Пограничный гребень – это анатомическое образование в нормальном сердце, гладкое, чет-
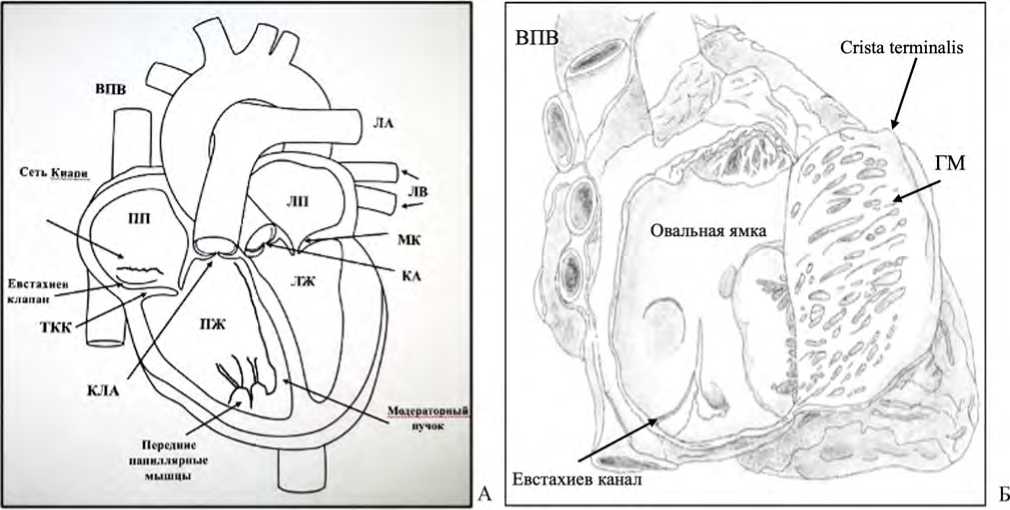
Рис. 1. А – схема строения сердца и положения евстахиева клапана, сети Киари в правом предсердии, модераторного пучка правого желудочка. ВПВ – верхняя полая вена, ПП – правое предсердие, ТКК – трикуспидальный клапан, КЛА – клапан легочной артерии, ПЖ – правый желудочек, ЛА – легочная артерия, ЛП – левое предсердие, ЛВ – легочные вены, МК – митральный клапан, КА – клапан аорты, ЛЖ – левый желудочек; Б – схема топографии евстахиева канала, гребенчатых мышц (ГМ) и crista terminalis в правом предсердии
Fig. 1. А – Scheme of heart anatomy and the location of the Eustachian valve, Chiari network in the right atrium, moderator bundle of the right ventricle. ВПВ – superior vena cava, ПП – right atrium, ТКК – tricuspid valve, КЛА – pulmonary artery valve, ПЖ – right ventricle, ЛА – pulmonary artery, ЛП – left atrium, ЛВ – pulmonary veins, МК – mitral valve, КА – aortic valve, ЛЖ – left ventricle; Б – diagram of the topography of the Eustachian canal, pectineal muscles (ГМ) and crista terminalis in the right atrium
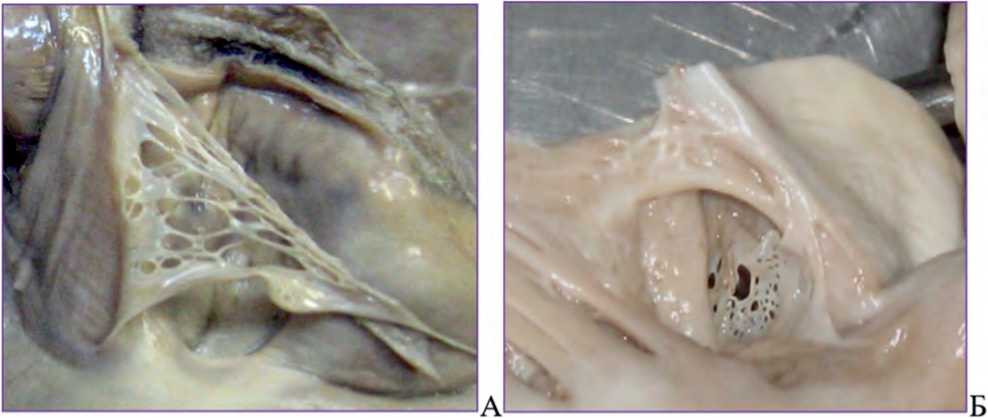
Рис. 2. А, Б. Макроскопическая картина вариантов строения сети Киари в правом предсердии [2]
Fig. 2. A, Б. Macroscopic view of anatomical variants of the Chiari network in the right atrium [2]
ко выраженное, С-образное, отделяющее гладкую венозную часть правого предсердия от неровной стенки его ушка, представленной гребенчатыми мышцами (см. рис. 1Б). Гребень начинается от переднелатеральной стенки правого предсердия от межпредсердной перегородки и тянется по направлению к устью нижней полой вены (см. рис. 1Б). Размеры и форма пограничного гребня различные: длина – 42–51 мм, толщина – от 3–6 до 15 мм [12]. При трансторакальной ЭхоКГ невыраженный гребень обычно не определяется, однако в случае выступающего гребня при чреспищеводной ЭхоКГ его обнаруживают как дополнительное образование или патологическую внутрисердечную массу (тромб, опухоль?) в правом предсердии [13].
Избежать диагностической ошибки позволяет мультимодальное исследование (чреспищеводная ЭхоКГ, КТ и МРТ). При ЭхоКГ пограничный гребень изменяет размер во время сокращений предсердия, а эхогенность его подобна таковой миокарда. Результаты КТ свидетельствуют о контрастном усилении в области пограничного гребня, аналогичном миокарду. При МРТ выявляемость выступающего пограничного гребня достигает 40%, он обнаружи- вается как изоинтенсивное образование [13, 14]. Близкое расположение гребня к артерии синусового узла обусловливает его участие в развитии аритмий (часто трепетания предсердий), зависящее от формы и размеров пограничного гребня [13].
Гребенчатые мышцы правого предсердия представляют собой мышечные гребни, которые отходят от пограничного гребня и располагаются на внутренней поверхности ушка правого предсердия по переднелатеральной стенке (см. рис. 1Б). При ЭхоКГ исследовании гребенчатые мышцы нередко выглядят как тромб или опухоль правого предсердия. Самый большой и наиболее выступающий мышечный гребень, образующий на наружной поверхности предсердия пограничную борозду (sulcus terminalis), называется taenia sagittalis [12]. Область соединения гребенчатых мышц и пограничного гребня является аритмогенной, в ней нередко инициируются пароксизмы тахикардии, получившие название «cristal tachycardias» [15]. К развитию предсердных аритмий также предрасполагает трабекулярность гребенчатых мышц, способствующая неравномерному распространению электрического импульса по миокарду и формированию кругов re-entry [16].
Правый желудочек
В отличие от левого желудочка в апикальной части правого желудочка выявляют выраженную трабекуляр-ность. Трабекулы поперечно ориентированы и протягиваются от атриовентрикулярного соединения до верхушки желудочка.
Наджелудочковый гребень представляет собой мышечный вал, прикрепляющийся к верхней части межжелудочковой перегородки, сливающийся с ней, образующий заднюю стенку подлегочного инфундибулума (выходного тракта правого желудочка), таким образом соединяет передне-верхнюю часть межжелудочковой перегородки с базальной частью правого желудочка. Наджелудочковый гребень отграничивает атриовентрикулярное отверстие и отверстие легочного ствола, таким образом отделяет входную и выходную части правого желудочка и играет важную роль в механике сокращений правого желудочка. В составе наджелудочкового гребня встречаются две ветви: одна ветвь пристеночная, распространяется по свободной стенке правого желудочка, вторая – перегородочная или перегородочно-краевая трабекула, протягивается по правой стороне межжелудочковой перегородки до основания передней сосочковой мышцы [17]. От основания передней сосочковой мышцы часто отходит межмышечная трабекула, которая перекидывается через полость правого желудочка к основанию задней сосочковой мышцы. Перегородочную ветвь наджелудочкового гребня и межмышечную трабекулу называют модераторным пучком или септомаргинальной трабекулой [18].
Модераторный пучок относится к наиболее выраженному мышечному гребню правого желудочка и простирается от межжелудочковой перегородки до свободной стенки правого желудочка к основанию передней папиллярной мышцы, крайне редко к стенке правого желудочка (см. рис. 1А). Результаты исследований показали значительную вариативность размера, положения модераторного пучка [18, 19]. По форме выделяют три типа модераторного пучка: цилиндрический, длинный и тонкий, широкий и плоский, его средняя толщина – 4,5 ± 1,8 мм, средняя длина – 16 ± 2 мм. Большинство волокон моде- раторного пучка находится в апикальной части правого желудочка. В 5–15% случаев при аутопсии модераторный пучок невыраженный, и его не обнаруживают в сердце [19]. В составе модераторного пучка находятся специализированные волокна Пуркинье, окруженные кардиомиоцитами, которые быстро активируют свободную стенку правого желудочка. Физиологическая роль модераторного тяжа заключается в предотвращении чрезмерной дилатации верхней части правого желудочка, поддержке передней папиллярной мышцы. Благодаря положению правой ножки пучка Гиса, находящейся в модераторном пучке, он является частью проводящей системы сердца, обеспечивая быструю активацию свободной стенки правого желудочка и перегородки [17].
При ЭхоКГ выраженного модераторного пучка он выглядит как эхо-плотная структура, подобная по плотности миокарду. Нередко его дифференцируют с тромбом или опухолью правого желудочка, используя чреспищеводную ЭхоКГ и МРТ. При исключении структурных заболеваний сердца, инициирующих развитие желудочковых аритмий (желудочковой экстрасистолии, рецидивирующей желудочковой тахикардии, фибрилляции желудочков), исследуют проаритмический потенциал модераторного пучка, формирующийся при растяжении, развитии фиброза или каналопатии [20].
Аномально расположенные (ложные) хорды – это тонкие фиброзные или фиброзно-мышечные тяжи, не связанные со створками атриовентрикулярного клапана, пересекающие полость правого желудочка [2, 21]. Происхождение аномально расположенных хорд точно не установлено. Вероятно, они представляют остаток внутреннего мышечного слоя примитивного сердца, возникающего в эмбриональном периоде при отшнуровке сосочковых мышц. Другая гипотеза рассматривает аномальные хорды как мышечные трабекулы, втягивающиеся в полость желудочка, в случае его дилатации или образования аневризм [21].
M. Loukas и соавт. представили пять типов соединений структур желудочков аномальными хордами и их частоту при аутопсии: I (37,1%) – между заднемедиальной папиллярной мышцей и межжелудочковой перегородкой, II (22,1%) – между двумя папиллярными мышцами, III (16,5%) – между переднебоковой папиллярной мышцей и межжелудочковой перегородкой, IV (12,5%) – между межжелудочковой перегородкой и свободной стенкой желудочка, V (11,6%) – образующие сети с тремя и более точками прикрепления [2].
Исследователи обращают внимание на значительное расхождение результатов диагностики прижизненных аномально расположенных хорд методом ЭхоКГ и при аутопсии. При аутопсии и эндоскопии 90 сердец в 62,2% выявили аномально расположенные хорды желудочков, в то же время у тех же пациентов прижизненно при ЭхоКГ аномально расположенные хорды определили лишь в 27,7%. В 30% случаев в аномально расположенных хордах обнаружили клетки проводящей системы [22]. Толщина аномально расположенных хорд составляет 1,4 ± 0,5 мм, длина – 18 ± 7 мм [21]. В клинической практике применяется классификация J. Beauttie и соавт., согласно которой выделяют поперечные, базальные и продольные аномально расположенные хорды, располагающиеся в верхушечном, средне-желудочковом и базальном отделах желудочка.
Клиническое значение аномально расположенных
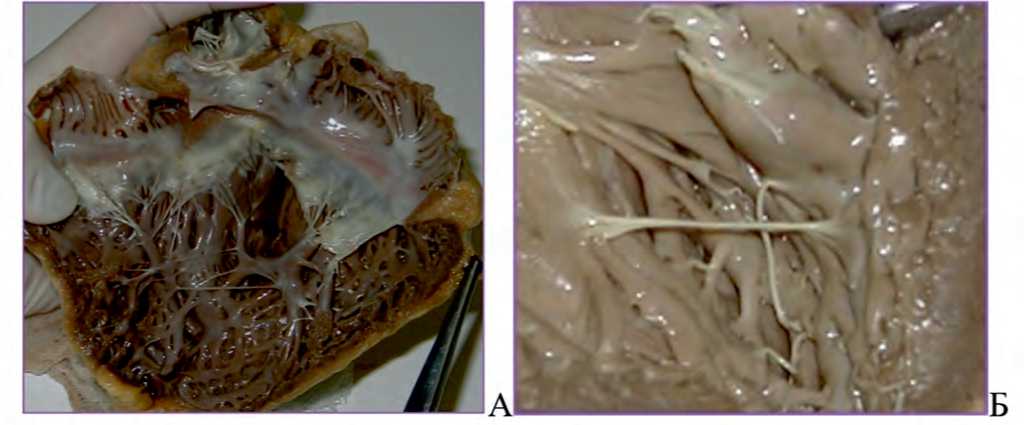
Рис. 3. А – Поперечная аномальная хорда правого желудочка, Б – две аномально расположенных хорды левого желудочка
Fig. 3. A – Transverse anomalous chord of the right ventricle, Б – two anomalously located chords of the left ventricle
хорд рассматривается неоднозначно, поскольку их топография, места крепления и морфология различные [2, 21]. В большинстве случаев аномально расположенные хорды являются «случайной находкой» при ЭхоКГ или аутопсии (рис. 3А, Б). Вместе с тем поперечное положение аномальной хорды в камере сердца служит препятствием кровотоку, подвергается травматическому повреждению и служит причиной шума в сердце. Нередко на поврежденной аномальной хорде образуются вегетации, тромбы, определяются признаки миксоматоза, приводящие к разрыву тяжа. Наличие клеток проводящей системы в аномальной хорде предрасполагает к развитию экстрасистолии, синдрому ранней реполяризации. Короткие фиброзные аномальные хорды способствуют нарушению расслабления желудочков и развитию диастолической дисфункции миокарда [21, 22]. К тому же в местах крепления аномальной хорды при постоянном натяжении появляются участки воспаления, фиброза, обусловливающие нарушения сократительной функции миокарда [2, 23].
L. Wang и соавт. описали случай аномально расположенной хорды между межжелудочковой перегородкой и свободной стенкой правого желудочка у пациента как причину желудочковых экстрасистол, желудочковой тахикардии и эпизода фибрилляции желудочков. Исключив другие возможные причины аритмии сердца и не получив эффекта от медикаментозной антиаритмической терапии, авторы выполнили трехмерное картирование, внутрисердечную ЭхоКГ и электрокардиограмму и определили участок активности на свободной стенке правого желудочка в области прикрепления аномальной хорды. Аритмии сердца не повторялись после радиочастотной аблации этого участка [24]. Исследование L. Wang и со-авт. подтвердило аритмогенность аномальных хорд правого желудочка и важность обследования для выявления истинной причины аритмии сердца.
Папиллярные мышцы правого желудочка располагаются по передней стенке от 1 до 3, на задней стенке – от 1 до 4. На медиальной стенке располагаются перегородочные папиллярные мышцы от 1 до 5. Вариабельность морфологии, топографии и количества папиллярных мышц влияет на количество и функционирование ство- рочных хорд, которые, в свою очередь, вызывают дисфункцию правого атриовентрикулярного клапана [21]. Удлинение и гипертрофия папиллярной мышцы, от которой начинаются створочные хорды, является основанием для появления пролабирования трехстворчатого клапана. Изредка гипертрофированную или атипично расположенную папиллярную мышцу ошибочно рассматривают при ЭхоКГ как патологическое внутрисердечное образование (тромб, опухоль?). Диагностику проводят с использованием чреспищеводной ЭхоКГ и МРТ [25].
Левое предсердие
Анатомические особенности левого предсердия представляют особый интерес, поскольку в этой камере сердца выполняются многие лечебные манипуляции: изоляция легочной вены, катетерная аблация, оперативные малоинвазивные вмешательства на митральном клапане, окклюзия ушка левого предсердия. Изменчивость внутренних структур левого предсердия может оказать негативное влияние на продолжительность и безопасность манипуляций, а внутрисердечные образования, не диагностированные или ошибочно рассмотренные как патологические структуры (тромб, опухоль) повлекут ненужные лечебные мероприятия.
Аномальный тяж (аномально расположенная хорда, аберрантная полоса левого предсердия) левого предсердия относится к редкой врожденной аномалии, частота которой при аутопсии составляет 2% [26]. Аномальный тяж, состоящий из фиброзной и мышечной ткани, протягивается от левой стороны овальной ямки к свободным стенкам левого предсердия, изредка к створке митрального клапана, вызывая митральную регургитацию [27]. Клинические проявления при наличии аномального тяжа в левом предсердии у большинства пациентов отсутствуют, вместе с тем описаны наджелудочковые аритмии чаще по сравнению с людьми, у которых тяж не обнаруживали (41 против 11%, р > 0,01) [28, 29]. Аномальный тяж левого предсердия встречался нередко в сочетании с сетью Chiari (27 против 8%, р > 0,01) и открытым овальным окном (23 против 8%, р > 0,05) [26].
-
H. Tian и соавт. выполнили крупное исследование по аномальным тяжам левого предсердия. Авторы ана-
- лизировали клинические данные и результаты КТ с ангиографией 10 796 пациентов, из которых у 35 (0,32%) обнаружены аномальные тяжи левого предсердия. После исключения из исследования одного пациента, у которого не получили клинические данные, сравнивали результаты двух подгрупп, основанием для разделения которых послужили точки прикрепления аномальных тяжей (18 мужчин, 16 женщин, средний возраст – 57 лет). В 1-й подгруппе аномальные тяжи протягивались между свободными стенками предсердия, во 2-й – между межпредсердной перегородкой и свободной стенкой левого предсердия. Длина аномального тяжа в подгруппах составила 2,64 ± 0,99 см и 3,39 ± 0,68 см соответственно, в 55,88% случаев аномальные тяжи локализовались вблизи от устья левой нижней легочной вены. Аритмии сердца (фибрилляция предсердий, наджелудочковая экстрасистолия) чаще встречались в группе с аномальными тяжами по сравнению с контрольной группой (р = 0,009), но не зависели от зон прикрепления тяжей. Транзиторная ишемическая атака отмечена у 3 пациентов с аномальными тяжами, что достоверно отличалось от контрольной группы (р = 0,035) [30]. Сравнительное исследование результатов диагностики показало, что при ЭхоКГ аномальный тяж выявлен у одного пациента, все остальные случаи диагностированы при КТ.
Таким образом, редкую аномалию в виде дополнительного тяжа в левом предсердии следует рассматривать как находку, возможно связанную с наджелудочковой аритмией и транзиторной ишемической атакой.
Другое анатомическое образование, которое выявляют в левом предсердии при ЭхоКГ – левый боковой гребень (кумадиновый гребень, варфариновый гребень). Он представляет собой лентовидную складку ткани, иногда узловатую, на стенке предсердия между левой верхней легочной веной и ушком левого предсердия, оставшуюся от эмбрионального периода. В гребне проходит связка Маршалла, вегетативный нервный пучок и небольшая артерия предсердия или синоатриального узла. Название «кумадиновый или варфариновый» гребень получил из-за того, что его ошибочно диагностировали как тромб и назначали варфарин или кумадин [31]. К другим образованиям, ошибочно диагностированным при наличии левого бокового гребня, относятся опухоли сердца (миксомы). Левый боковой гребень является потенциальным источником аритмий и представляет собой препятствие при выполнении аблации. К. Platek-Koziej и соавт., исследовав 200 сердец, в 59,5% случаев обнаружили левый боковой гребень, средняя длина которого составила 22,4 ± 5,1 мм, ширина в нижнем отделе гребня преобладала над шириной в верхнем отделе (6,2 ± 3,5 против 4,3 ± 1,8 мм, р > 0,001) [32]. Ширина гребня (узкий или широкий) влияет на рецидив фибрилляции предсердий после катетерной аблации. При узком гребне по сравнению с широким чаще возникают рецидивы фибрилляции предсердий после радиочастотной аблации (ОШ 2,58; 95% ДИ, 1,48–4,51; p = 0,001). При ЭхоКГ левый боковой гребень выглядит как линейное или узловатое образование с тонкой проксимальной частью и выпуклой дистальной (симптом «ватной палочки»), волнообразно колеблющееся при сокращениях сердца. Эхогенность гребня подобна эхогенности окружающих структур сердца, при КТ и МРТ интенсивность сигнала не отличается от сигнала тканей сердца [33]. Левый боковой гребень имеет мышечное соединение с левой легочной веной, являющееся триггером фокальной фибрилляции предсердий [34].
Изредка в области левого бокового гребня обнаруживают миксому или папиллярную фиброэластому. Папиллярная фиброэластома – доброкачественная опухоль сердца, часто локализующаяся на клапанах сердца, преимущественно на створках аортального клапана, неклапанное расположение опухоли в левом предсердии встречается крайне редко. H.M. Lac и соавт. описали случай гистологически подтвержденной папиллярной фиброэластомы, которая локализовалась на левом боковом гребне в левом предсердии. Течение папиллярной фиброэластомы осложнилось кардиоэмболическим инсультом и пароксизмами фибрилляции предсердий у 70-летней пациентки с открытым овальным окном [35].
Левый желудочек
Помимо створочных хорд, протягивающихся от папиллярных мышц к створкам митрального клапана, в полости левого желудочка часто по сравнению с правым желудочком обнаруживают аномально расположенные хорды (см. рис. 3Б). Аномально расположенные хорды левого желудочка встречаются в 0,4–83% случаев и часто соединяют межжелудочковую перегородку и свободную стенку левого желудочка или сосочковую мышцу [36, 37]. Классифицируют аномально расположенные хорды левого желудочка так же, как аномальные хорды правого желудочка. Наличие аномально расположенной хорды левого желудочка, как правило, сопровождается выслушиваемым систолическим шумом над областью сердца. На ЭКГ при аномально расположенных хордах левого желудочка обнаруживают синдром ранней реполяризации, отрицательные симметричные, двухфазные зубцы Т (в отведениях V1–V3), которые становятся положительными при физической нагрузке (повышение частоты сердечных сокращений) [37].
Аномально расположенные хорды как правого, так и левого желудочка, обусловливают развитие желудочковых аритмий сердца, диастолической и систолической дисфункции миокарда [36, 38]. Развитие желудочковых аритмий (желудочковая экстрасистолия, желудочковая тахикардия) связывают с наличием клеток Пуркинье в некоторых аномально расположенных хордах как левого, так и правого желудочка. Из-за механического растяжения левого желудочка повышается автоматизм клеток проводящей системы, что инициирует развитие желудочковых аритмий с комплексами QRS с морфологией блокады правой ножки пучка Гиса и отклонением электрической оси сердца влево у пациентов без структурных изменений сердца [39].
Папиллярные мышцы левого желудочка располагаются на передней и задней стенке желудочка и являются непосредственным продолжением миокарда. В норме рассматривают две папиллярных мышцы: переднелатеральную и заднемедиальную, от которых начинаются створочные хорды. Вместе с тем результаты аутопсии свидетельствуют о том, что типичные структуры характерны для 3,5–30% людей, а в большинстве случаев встречается от 2 до 16 головок папиллярных мышц [40]. Вариабельность топографии, количества и морфологии папиллярных мышц свидетельствует об относительности нормы и различном функциональном значении.
Морфологические особенности папиллярных мышц протекают бессимптомно либо при значительной длине мышцы обусловливают признаки обструкции путей оттока из левого желудочка. Количественные и топографические изменения папиллярных мышц при ЭхоКГ необходимо дифференцировать с патологическими образованиями в полости левого желудочка. Участие папиллярных мышц в развитии патологических симптомов необходимо рассматривать с применением мультимодальной визуализации [41]. Прижизненно и при аутопсии представлено разнообразное количество папиллярных мышц: на общем основании – много головок, на одном основании – одна головка, на нескольких основаниях – одна головка. По морфологии также описана значительная изменчивость папиллярных мышц, к наиболее распространенным относятся конические, усеченные, пирамидальные и веерообразные, различного диаметра и длины. Диаметр более 1,1 см рассматривается как признак гипертрофии папиллярной мышцы, длина – от 1 до 3,5 см [41].
Аномалии папиллярных мышц встречаются при аномалиях створочных хорд и створок митрального клапана. Створочные хорды, тянущиеся из единственной папиллярной мышцы к передней и задней створкам митрального клапана, приводят к появлению «парашютообразного» митрального клапана. Короткие створочные хорды вызывают значительную тракцию папиллярной мышцы и прилежащего миокарда. В этом случае в области папиллярной мышцы и прилежащем к ней миокарде методом МРТ обнаруживают кровоизлияния, фиброз и кальцификацию.
Морфологические изменения папиллярных мышц левого желудочка обусловливают появление желудочковых нарушений ритма, в том числе жизнеугрожающих (фибрилляция желудочков, желудочковая тахикардия) [42, 43].
Аномально удлиненная папиллярная мышца с обструкцией выходного тракта левого желудочка описана K. Oe и соавт. У 65-летнего мужчины с синкопе с молодого возраста, систолическим шумом на верхушке сердца и удлинением передней створки митрального клапана при ЭхоКГ выявили множественные папиллярные мышцы левого желудочка и удлинение передней папиллярной мышцы, которая вызывала персистирующую обструкцию выходного тракта левого желудочка [44]. Поскольку от хирургического лечения пациент отказался, градиент давления в выходном тракте левого желудочка немного снизили, применяя перорально бисопролол.
Аномалия митрального клапана с увеличенными и удлиненными, изредка соединенными между собой папиллярными мышцами, с короткими фиброзными тяжами, прикрепляющимися к свободному краю передней створки митрального клапана, встречается редко, ее диагностируют преимущественно у детей в возрасте до 3 лет при кардиохирургическом вмешательстве. Вследствие отсутствия створочных хорд ограничивается движение створки, препятствующее смыканию передней и задней створок, появляются признаки митральной недостаточности и / или стеноза. Задняя створка часто не изменена и соединяется с папиллярными мышцами обычными по длине сухожильными хордами [2, 44]. Митральный клапан в этом случае приобретает форму аркады (или гамака, А. Carpentier, 1976). Поскольку створки клапана нормальной или увеличенной толщины, возникают неправильные предположения о ревматической природе порока сердца.
Избыточная трабекулярность левого желудоч- ка встречается не только при некомпактном миокарде, рассматриваемом как генетически детерминированная форма неклассифицируемой кардиомиопатии (наличие ее обсуждается), но выявляется у здоровых людей при ЭхоКГ обследовании по поводу беременности, занятий спортом или заболеваний сердца. Избыточная или чрезмерная трабекулярность характеризуется аномальными трабекулами и глубокими межтрабекулярными углублениями. Несколько авторов разработали критерии для диагностики избыточной трабекулярности [45–47].
R. Jenni и соавт. предложили количественное определение некомпактного миокарда, включающего наличие двухслойного миокарда (тонкий уплотненный миокард и толстый неуплотненный–трабекулярный) с отношением трабекулярного слоя к компактному, измеренное в конце систолы по короткой оси, как < 2 : 1. Предполагалось типичное расположение выраженной трабекулярности в среднелатеральном, апикальном и среднем нижнем сегментах и отсутствие сопутствующих структурных аномалий сердца [46]. С. Stöllberger и соавт. считали, что необходимо наличие по крайней мере трех трабекул с подтвержденным межтрабекулярным кровотоком в области папиллярных мышц и верхушки сердца. К тому же конечно-диастолическое отношение некомпактного слоя к компактному должно составлять ≥ 2 [47].
При МРТ диагностические критерии включают отношение в диастолу некомпактного слоя к компактному > 2,3 или > 2 в конце систолы либо при массе трабекул > 20% [45, 48, 49]. В настоящее время отсутствует четкое представление, какие критерии следует выбрать для диагностики патологического состояния. В клинической практике наиболее доступным является метод ЭхоКГ, а более надежным, с дополнительной информацией о структуре миокарда – МРТ. При визуализации методом ЭхоКГ и МРТ трабекулы по плотности соответствуют плотности миокарда и при сокращении и расслаблении левого желудочка движутся синхронно с миокардом. Для некомпактной кардиомиопатии с избыточной трабекулярностью левого желудочка характерны типичные осложнения в виде аритмии, сердечной недостаточности и тромбоэмболии [50]. В диагностике учитывают наследственность и семейный анамнез заболеваний сердца. Нередко избыточную трабекулярность обнаруживают в сочетании с гипертрофической или дилатационной кардиомиопатией. Изолированная избыточная трабекулярность не сопровождается патологическими симптомами и структурными изменениями сердца.
При обнаружении избыточной трабекулярности левого желудочка у детей необходимо наблюдение для своевременной диагностики гипертрофической или дилатационной кардиомиопатии либо эндомиокардиального фиброэластоза. У взрослых людей не доказано влияние изолированной избыточной трабекулярности на качество и прогноз жизни.
Заключение
Образования в камерах сердца, обнаруженные при ЭхоКГ, могут оказаться нормальной анатомической структурой или тромбом, доброкачественной или злокачественной опухолью, метастазом. Семейный анамнез, клинические симптомы и признаки, исследования другими методами визуализации (КТ, МРТ) являются обязательными для дифференциальной диагностики обнаруженных анатомических образований. При нали- чии симптомов в виде аритмии сердца, тромбоэмболии, сердечной недостаточности доступными методами выявляют заболевания сердечно-сосудистой системы. При отсутствии заболеваний и патологических структурных нарушений сердца следует изучить влияние на развитие аритмии или тромбоэмболии внутрисердечных анатомических образований, являющихся вариантом нормы.


