Клинико-гемодинамические результаты имплантации бесшовных биопротезов PERCEVAL s в аортальной позиции из мини-доступа у пожилых пациентов
Автор: Молчанов Андрей Николаевич, Идов Э.М., Кондрашов К.В., Чаплюк П.Ю., Шахмаева Н.Б.
Журнал: Патология кровообращения и кардиохирургия @journal-meshalkin
Рубрика: Приобретенные пороки сердца
Статья в выпуске: 3 т.21, 2017 года.
Бесплатный доступ
Обоснование В перечне сердечно-сосудистых заболеваний аортальные пороки по частоте встречаемости входят в первую тройку. Так, стеноз аортального клапана выявляется в 70% случаев клапанных пороков. Сегодня операция протезирования аортального клапана является наиболее эффективным методом лечения аортального порока. Однако традиционная шовная методика замены аортального порока у пожилых пациентов ассоциирована с высоким риском осложнений, чаще всего обусловленных временем ишемии миокарда на период имплантации клапанного протеза, а также сопутствующими заболеваниями. В качестве альтернативного метода лечения была предложена имплантация бесшовного протеза Perceval S в аортальную позицию у пациентов, входящих в критерии отбора. Цель Исследование динамики клинических и гемодинамических показателей на различных этапах послеоперационного периода у больных после имплантации бесшовного биопротеза аортального клапана Perceval S (n = 32), оценка его интраоперационных преимуществ, а также уровня послеоперационных осложнений. Методы В данном проспективном когортном исследовании выполнена оценка клинических и функциональных результатов хирургического лечения результатов имплантации бесшовных биопротезов Perceval S в аортальной позиции из J-министернотомии (n = 22) и срединной стернотомии (n = 10) в ближайшем и среднеотдаленном послеоперационных периодах. Результаты Отмечено уменьшение трансаортального градиента: в раннем послеоперационном периоде пиковый градиент - 21,6±4,2 мм рт. ст. (p = 0,1), средний - 11,3±2,8 (p = 0,58); в среднеотдаленном периоде пиковый градиент - 15,8±5,5 мм рт. ст. (p = 0,342), средний - 8,8±1,9 (p = 0,54). За весь период наблюдения прослеживается снижение индекса массы миокарда (p = 0,01). Случаев деформации и нарушений функции протеза, биодеградации не выявлено. Летальных осложнений в послеоперационном периоде не было. Выживаемость к 36-му мес. наблюдения составила 93,75%. Выводы Ксеноперикардиальные бесшовные биопротезы аортального клапана Perceval S адекватно корригируют внутрисердечную гемодинамику, обеспечивая нормализацию функциональных показателей левого желудочка в ближайшем и среднеотдаленном периодах и могут быть рекомендованы для пациентов пожилого возраста. Имплантация бесшовного протеза из мини-доступа не увеличивает техническую сложность операции и способствует более гладкому раннему послеоперационному периоду.
Хирургическое лечение аортальных пороков, аортальный стеноз, бесшовный аортальный биологический клапан perceval s
Короткий адрес: https://sciup.org/142140804
IDR: 142140804 | DOI: 10.21688/1681-3472-2017-3-32-39
Clinical and hemodynamic outcomes of PERCEVAL'S sutureless bioprostheses implanted through a mini-approach in the aortic position
Aim. Aortic valve disease is one of three most common cardiovascular problems. Aortic stenosis is responsible for 70% of valve disease. Aortic valve replacement is the most effective treatment for aortic stenosis nowadays. A traditional suture technique of aortic valve replacement is associated with a high risk of complications. Most of these complications occur due to ischemic aortic cross-clamp time and comorbidities. Perceval S sutureless aortic valves to be implanted in selected patients are supposed to meet the challenge. The study was aimed at assessing Perceval S sutureless aortic valve hemodynamic and clinical parameters, its intraoperative advantages and postoperative complication rates. Methods. A prospective cohort study of Perceval S sutureless aortic valve implanted via J-sternotomy (n = 22) and median sternotomy (n = 10) was conducted. Early and medium postoperative clinical and functional outcomes were obtained and evaluated. Results. A decrease in the transaortic gradient was observed in early (peak gradient 21.6±4.2 (p = 0.1), mean gradient 11.3±2.8 (p = 0.58)) and medium (peak gradient 15.8±5.5 (p = 0.342), mean gradient 8.8±1.9 (p = 0.54)) follow-up. The myocardial mass index tended to be reduced throughout the entire follow-up (p = 0.01). There were no prosthesis dysfunctions or biodegradation. No patient died in the postoperative period. Survival at 36 months of follow-up was 93.75%. Conclusion. Perceval S xenopericardial sutureless aortic bioprostheses adequately resolve hemodynamic problems and improve left ventricle functional parameters in early and median follow-up. They may be recommended for elderly patients. Sutureless aortic valve implantation is technically feasible through J-sternotomy and contributes to an eventless follow-up.
Текст научной статьи Клинико-гемодинамические результаты имплантации бесшовных биопротезов PERCEVAL s в аортальной позиции из мини-доступа у пожилых пациентов
Для быстро стареющего населения развитых стран замена клапана аорты стала самой частой операцией при клапанной болезни сердца [1]. Развитие и совершенствование хирургических методов за последние 10 лет привели к пониманию того, что минимально инвазивные доступы при операциях на клапане аорты по результатам, безопасности, эффективности, числу осложнений не уступают традиционной стернотомии, а в ряде случаев существенно облегчают течение послеоперационного периода [2]. Ксеноперикардиальные бесшовные биопротезы аортального клапана (АК) Perceval S, созданные на основе инновационных технологий и материалов (Sorin Group Italia S.r.L., Италия) как альтернатива традиционным протезам, были внедрены в клиническую практику в конце 2007 г. [3, 4]. В России биопротез Perceval S получил одобрение на использование в кардиохирургии только в 2013 г. В результате бесшовной процедуры имплантации получено преимущество в сокращении времени пережатия аорты, уменьшении времени хирургического вмешательства [5, 6], снижении риска операции и вероятности таких осложнений, как прорезывание кольца аорты [2], стенки аорты, аортальной связки, а также кальциевой эмболии по большому кругу кровообращения [7].
Начиная с первой имплантации клапана Perceval S в 2007 г. в более 95 публикациях показаны многообещающие результаты послеоперационных гемодинамических характеристик, отсутствие дисфункции клапана и повторной операции во время одно- [8, 9] и двухлетних [10] исследований. Ряд авторов в резюме трех последовательных пятилетних европейских многоцентровых исследований (Pilot, Pivotal, Сavalier) пожилой когорты пациентов (средний возраст 78,5 года) сообщили о благоприятных клинических и гемодинамических результатах, включая низкие ранние и отсроченные показатели смертности (1,9 и 1,4 %), низкую частоту ранних параклапанных фистул (1,4%) [5, 11–15]. М. Eusanio [16] и К. Phan [4] описали бесшовное протезирование аортального клапана не только как многообещающую альтернативу обычному протезированию, но также отметили хорошие функциональные гемодинамические результаты с меньшим количеством осложнений. Положительные результаты безопасности и эффективности до настоящего времени делают Perceval S альтернативой стандартному биологическому клапану и открывают потенциально новый стандарт для минимально инвазивной хирургии на клапане аорты [17].
По данным мировой статистики, на конец 2016 г. в мире имплантировано более 30 тыс. протезов Perceval S, в России — менее 130. Данная работа представляет собой одно из первых отечественных исследований по оценке непосредственных клинических и функциональных результатов протезирования бесшовного биопротеза Perceval S в ближайшем и среднеотдаленном послеоперационных периодах.
Целью работы явилось исследование динамики клинических и гемодинамических показателей на различных этапах послеоперационного периода у больных после имплантации бесшовного биопротеза аортального клапана Perceval S, оценка его интраоперационных преимуществ, а также уровня послеоперационных осложнений.
Методы
За 2014–2017 г. в ГБУЗ СО «СОКБ № 1» Центра сердца и сосудов им. М.С. Савичевского протезирование АК с использованием бесшовного каркасного биопротеза из бычьего перикарда Perceval S было выполнено 32 больным. Исследование одобрено Комитетом по этике научных исследований ГБУЗ СО «СОКБ № 1» от 13.12.2012 г. (выписка из протокола № 99). Клиническая характеристика больных представлена ниже.
|
Показатель |
Пациенты |
|
Мужчины / женщины, n (%) |
20 (62,5) /12 (37,5) |
|
Средний возраст (min – max), лет Этиология порока, n (%): |
75,9±7,04 |
|
дегенеративный |
14 (43) |
|
ревматическая болезнь |
7 (21) |
|
двухстворчатый аортальный клапан |
11 (36) |
|
Морфология порока, n (%): |
|
|
стеноз |
22 (68,8) |
|
стеноз – недостаточность |
10 (31,2) |
|
Функциональный класс по NYHA, n (%): |
|
|
III |
22 (68,5) |
|
IV |
10 (31,5) |
|
Недостаточность кровообращения по Стражеско – Василенко, n (%): |
|
|
2А |
27 (84,3) |
|
2Б |
5 (15,7) |
|
Сопутствующие заболевания, n (%): артериальная гипертензия |
32 (100) |
|
фибрилляция предсердий |
11 (34,4) |
|
сахарный диабет |
23 (71,8) |
|
ишемическая болезнь сердца |
8 (25) |
|
хроническая обструктивная болезнь легких |
12 (37,5) |
|
хроническая почечная недостаточность |
14 (43,7) |
|
цереброваскулярная болезнь, инсульт в анамнезе |
7 (21) |
|
прочее |
15 (46,8) |
|
Средний показатель по EuroSCORE II |
13,4±2,5 |
|
Средний показатель по STS |
7,6±1,5 |
Примечание. NYHA — классификация Нью-Йоркской ассоциации сердца (англ. New York Heart Association)
Критерии отбора пациентов: возраст более 60 лет, исходная тяжесть состояния пациентов, изолированный стеноз или комбинированный порок аортального клапана с кальцинозом 2 или 3 ст., размер фиброзного кольца аортального клапана от 19 до 25 мм, отсутствие дилатации восходящей аорты.
Среди пороков аортального клапана преобладали пороки дегенеративной этиологии, что обусловило превалирование изолированного стеноза АК (68,8%). О тяжести состояния больных до операции свидетельствовали наличие сопутствующих заболеваний, функциональный класс, недостаточность кровообращения у всех пациентов, высокие показатели EuroSCORE II и STS.
Всем больным перед операцией, выпиской из стационара (в среднем через 10 дней после операции) и через 6, 12 и 36 мес. выполняли эхокардиографическое исследование функции аортального протеза и левого желудочка (ЛЖ). Функцию левого желудочка пациентов оценивали по линейным и объемным размерам в систолу и диастолу. О сократительной функции ЛЖ судили по значениям фракции выброса, фракции укорочения, сердечному индексу. Степень гипертрофии миокарда характеризовалась размерами задней стенки левого желудочка, межжелудочковой перегородки. Оценивались масса миокарда, индексированная масса миокарда. Для оценки функции клапанного протеза использовали показатели эффективной площади отверстия (ЭПО), трансаортального градиента на протезе.
Отличительными особенностями клапана Perceval S являются уникальная система стента из супермягкого сплава, эксклюзивное сочетание двойной «юбки»
и анатомической формы, клиновидная форма синотубулярного кольца, уникальное антитромботическое покрытие, химическая стерилизация клапана при производстве (Propylparaben – Methylparaben). На данный момент это единственный зарегистрированный в нашей стране (от 11 декабря 2012 г.) каркасный бесшовный протез для имплантации в аортальную позицию.
Этапы операции имплантации бесшовного протеза Perceval S
Срединную мини-J-стернотомию до 4-го межреберья [11] либо срединную стернотомию (n = 10) выполняли на этапе внедрения технологии. Подключение аппарата искусственного кровообращения по обычной методике с двустадийной канюлей, антеградной кровяной кардиоплегией, с постоянной инсуфляцией СО2 в рану. После асистолии и поперечного рассечения аорты на уровне аортальной складки (на 4 см выше фиброзного кольца АК) иссекаются створки АК до фиброзного кольца. Особенностью имплантации бесшовного клапана Perceval S является отсутствие необходимости полного удаления кальция с фиброзного кольца АК. Измеряется размер фиброзного кольца АК, и накладываются три одиночных направляющих шва на область соответствующей самой нижней точке фиброзных полулуний из желудочка в аорту на расстоянии 120° друг от друга. Далее при помощи сжимающего устройства (collapser), в соответствии с размером, протез обжимается на держателе (holder), а затем по ранее наложенным направляющим швам опускается к фиброзному кольцу АК с последующим снятием с держателя и удалением направляющих швов [18].
После установки протеза в фиброзном кольце АК выполняется баллонная дилатация протеза под давлением до 3,5–4 атм. в течение 30 сек. с постоянным орошением протеза теплым физиологическим раствором (37,0 °С). Размер баллона должен соответствовать размеру клапана для имплантации.
Баллонная дилатация обеспечивает оптимальную герметизацию протеза с фиброзным кольцом АК, во время которой баллон должен быть абсолютно устойчивым, чтобы избежать неравномерного прижатия протеза к фиброзному кольцу или повреждения протеза [18]. Удаление баллона проводится в спущенном состоянии, что предотвращает смещение протеза.
Следует визуально контролировать расположение опорной манжеты имплантированного протеза к фиброзному кольцу АК. Верхняя «юбка» Perceval S должна располагаться выше фиброзного кольца, а «юбка» при- тока — интрааннулярно. Если фиброзное кольцо видно сверху над верхней «юбкой», протез расположен слишком низко. Если кольцо видно с желудочковой стороны, протез помещен слишком высоко. При неправильном расположении протеза относительно фиброзного кольца АК протез следует удалить и повторить процедуру имплантации. После отключения искусственного кровообращения выполняется контроль функции протеза при помощи транспищеводного ЭхоКГ. Далее операция проводится по стандартной методике.
Средняя длительность операции составила 108,5±17,8 мин, время искусственного кровообращения — 37,3±5,8 мин; среднее время пережатия аорты 23,6±4,9 мин. Средний койко-день после операции у данной группы пациентов составил 8,4±1,6 сут.
Статистический анализ
Ведение баз данных и математическое преобразование результатов экспериментальных измерений выполнялось в программе Microsoft® Office Excel 2007 (12.0.4518.1014) MSO (12.0.4518.1014), включенной в Microsoft Office Enterprise 2007. © 2006 Microsoft Corporation. Статистическая обработка проводилась в SPSS Statistics 17.0.
Критическим уровнем значимости ( α ) в исследовании принят α = 0,05. Для нивелирования проблемы множественных сравнений в случаях сравнения трех и более групп между собой выполнялся перерасчет критического уровня значимости по формуле: α * = 1 – 0,951 / n, где n — количество сравнений. Суждения о статистической значимости полученных результатов выполнялись при сопоставлении достигнутого уровня значимости р с уточненным критическим уровнем значимости α *.
Исходя из относительно малой выборки для проверки статистической гипотезы применены непараметрические критерии сравнения связанных групп: для сравнения двух групп критерий Уилкоксона, для сравнения трех групп критерий Фридмана.
Для построения прогностической модели функции выживания использован непараметрический метод составления таблиц Каплана – Майера.
Таблица 1 Внутрисердечные гемодинамические показатели в дооперационном, раннем и среднеотдаленном послеоперационных периодах
|
p2 |
p3 |
||||||
|
Показатель |
До операции |
рации |
6 мес. |
36 мес. |
p1 |
||
|
ЭПО, см2 |
0,4±0,12 |
1,7±0,09 |
1,78±0,06 |
2,1±0,05 |
0,045 |
0,065 |
0,012 |
|
ИЭПО, см2/м2 |
0,25±0,04 |
1,3±0,14 |
1,4±0,07 |
1,5±0,06 |
0,080 |
0,005 |
0,011 |
|
PG, мм рт. ст. |
62,1±8,9 |
21,6±4,2 |
18,4±2,7 |
15,8±5,5 |
0,100 |
0,061 |
0,342 |
|
MG, мм рт. ст. |
38,7±4,6 |
11,3±2,8 |
10,1±3,5 |
8,8±1,9 |
0,580 |
0,120 |
0,540 |
|
КДО, мл |
174,3±11,4 |
171,6±18,5 |
145,4±9,4 |
136,3±8,2 |
0,150 |
0,400 |
0,095 |
|
КСО, мл |
61,35±11,4 |
57,6±4,17 |
53,43±3,25 |
58,38±4,1 |
0,330 |
0,680 |
0,500 |
|
КДР, мм |
51,6±0,79 |
48,32±0,6 |
53,43±3,25 |
45,76±4,7 |
0,055 |
0,090 |
0,200 |
|
КСР, мм |
36,41±0,85 |
34,9±0,55 |
33,51±1,37 |
31,97±3,8 |
0,012 |
0,032 |
0,008 |
|
ФВ ЛЖ % |
51,2±13,6 |
46,4±8,1 |
52,3±4,8 |
63,6±3,1 |
0,002 |
0,060 |
0,005 |
|
ФУ ЛЖ % |
24,37±3,5 |
21,8±1,17 |
26,6±2,5 |
31,5±3,21 |
0,034 |
0,150 |
0,007 |
|
ЗСЛЖ, см |
1,67±0,12 |
1,74±0,3 |
1,42±0,08 |
1,32±0,1 |
0,070 |
0,024 |
0,002 |
|
МЖП, см |
1,7±0,2 |
1,75±0,5 |
1,58±0,3 |
1,24±0,1 |
0,285 |
0,315 |
0,400 |
|
СИ, л/мин/м2 |
4,17±0,8 |
3,27±0,75 |
3,89±0,88 |
4,29±0,34 |
0,060 |
0,008 |
0,012 |
|
ММ ЛЖ, г |
415,3±25,7 |
398,5±41,2 |
345,7±11,5 |
286,3±23,2 |
0,007 |
0,030 |
0,287 |
|
ИИ ММ ЛЖ, г/л2 |
220,2±27,9 |
186,2±13,6 |
175,5±16,2 |
152,2±9,8 |
0,036 |
0,014 |
0,010 |
Примечание. ЭПО — эффективная площадь открытия; ИЭПО — индексированная эффективная площадь открытия; PG — пиковый градиент; MG — средний градиент; КДО — конечный диастолический объем; КСО — конечный систолический объем; КДР — конечный диастолический размер; КСР — конечный систолический размер; ФВ — фракция выброса; ЛЖ — левый желудочек; ФУ — фракция укорочения; ЗС — задняя стенка; МЖП — межжелудочковая перегородка; СИ — сердечный индекс; ММ — масса миокарда; ИИ ММ — индексированный индекс массы миокарда; р1 — уровень статистической значимости показателей дооперационного и ближайшего послеоперационного периодов; р2 — уровень статистической значимости показателей дооперационного периода и через 6 мес. после операции; р3 — уровень статистической значимости показателей дооперационного периода и через 36 мес. после операции pihsrovivrus evitalumuC / еитижод еонвитялуму
1,0
0,8
0,6
0,4
0,2
0,0
Функция дожития / Survivorship function
Функция дожития
Survivorship function х Цензурированные Censored
20 30 40
Срок наблюдения, мес. / Follow-up (months)
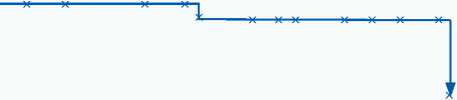
Кумулятивная функция дожития в линейном масштабе. Крестиками отмечены цензурированные (не достигшие прогнозируемого события) наблюдения (n = 32)
Linear cumulative survivorship function. Censored (failed to run up an anticipated event) follow-ups (n = 32) are marked with “x”.
Результаты
Эхокардиографическое исследование, выполненное перед выпиской, в среднеотдаленном послеоперационном периоде позволило установить, что бесшовные биопротезы Perceval S обладают хорошими гемодинамическими характеристиками. Эффективная площадь открытия пораженного аортального клапана не превышала, как правило, 1,0 см2 и в среднем составила 0,4 см2. Показатели ЭПО независимо от размера протеза не имели статистически значимых различий при разных диаметрах Perceval S. Следует отметить, что значение ЭПО после операции составило 1,7–2,1 см2 за все время наблюдения, что позволяет говорить об адекватной коррекции порока аортального клапана (табл. 2).
До операции пиковый трансаортальный градиент давления был повышен в среднем до 62,1±8,9 мм рт. ст., средний трансаортальный — до 38,7±4,6 мм рт. ст.
Средние значения трансаортального градиента как пикового, так и среднего имели тенденцию к уменьшению в раннем послеоперационном (21,6±4,2 / 11,3±2,8 мм рт. ст.) и среднеотдаленном (15,8±5,5 / 8,8±1,9 мм рт. ст.) периодах.
Показатели трансаортального градиента при использовании биопротезов различного размера представлены в табл. 3.
При анализе получено, что объемные и линейные показатели ЛЖ (конечные диастолические объем и размер, конечные систолические объем и размер) увеличивались в раннем послеоперационном периоде, а затем имели тенденцию к уменьшению в долгосрочном периоде и свидетельствовали о восстановлении диастолической функции и геометрии левого желудочка [19]. Отмечено постепенное снижение размеров задней стенки левого желудочка и межжелудочковой перегородки, массы миокарда, что может говорить об умень-
Таблица 2 Значения трансаортального градиента для протезов Perceval S различного размера
|
Размер протеза |
Пиковый трансаортальный градиент, мм рт. ст. |
p |
|||
|
до операции |
после операции |
6 мес. |
36 мес. |
||
|
21 мм |
74,1±5,8 |
21,7±2,17 |
18,7±1,89 |
13,2±0,5 |
0,009 |
|
23 мм |
68,9±6,3 |
17,2±1,63 |
15,4±0,98 |
11,6±1,75 |
0,012 |
|
25 мм |
66,5±8,6 |
15,4±2,2 |
11,6±1,24 |
10,5±2,89 |
0,028 |
Примечание. р — уровень статистической значимости показателей дооперационного периода и ближайшего послеоперационного периода
шении степени гипертрофии миокарда к 3 годам после операции. Таким образом, все эхокардиографические показатели, отражающие функцию ЛЖ, имели в динамике тенденцию к улучшению (табл. 2).
В течение трехлетнего периода наблюдения не выявлено случаев биодеградации, кальцинации, деформации и нарушений функции протеза.
После операции в среднеотдаленном периоде изменился функциональный класс (NYHA) у всех пациентов: 29 больных перешли в I функциональный класс, 3 во II (до операции находились в III–IV функциональном классе).
Послеоперационный период протекал без осложнений у 84,4% пациентов. Среди нелетальных осложнений у 3 пациентов (9,36%) наблюдали сердечную недостаточность, у 2 пациентов (6,24%) нарушения ритма сердца (желудочковая экстрасистолия — у 1, пароксизм желудочковой тахикардии — у 1), которые были купированы медикаментозно. Предсердно-желудочковых нарушений проводимости после имплантации протеза не наблюдалось. Отсутствие параклапанных фистул в послеоперационном периоде свидетельствует о эффективно подобранном размере и технически правильной имплантации протеза Perceval S. Летальных осложнений в послеоперационном периоде не было. В среднеотдаленном периоде умерли два пациента, причина летальности не связана с функцией протеза. Выживаемость к 36 мес. наблюдений составила 93,75%.
Согласно анализу выживаемости по методу Каплана – Майера (малая выборка), вероятность того, что пациент проживет более 15 мес. после процедуры, составляет 0,95±0,049 (95%), вероятность, что переживет 34 мес., — 0,712±0,209 с возможной накопленной ошибкой (0,209) на данном сроке наблюдения ( рисунок ).
Обсуждение
Клапанные пороки сердца встречаются относительно часто, составляя от 20 до 25% всех органических заболеваний сердца у взрослых. Распространенность аортального стеноза (АС) колеблется от 3–4 до 7% среди аортального порока дегенеративной этиологии у пациентов старше 60 лет. С возрастом частота выявления данного порока возрастает, составляя 15–20% у лиц старше 80 лет.
В последние годы в России неуклонно увеличивается количество хирургических вмешательств на аортальном клапане. В 2015 г. выполнено 3 575 операций, в том чис- ле 997 (27,9%) имплантаций биопротезов [20]. В структуре клапанных заменителей появились бесшовные имплантируемые протезы (менее 130 протезирований в России в 2016 г.). Бесшовные биопротезы Perceval S подходят пациентам группы отбора: как правило, это больные старше 60 лет с неблагоприятным коморбид-ным фоном [21, 22]. Преимущество использования мини-доступа у этих пациентов, по сравнению с традиционной стернотомией, заключается в том, что позволяет частично сохранить целостность каркаса грудной клетки и уменьшить проявления дыхательной недостаточности в послеоперационном периоде, обеспечивают более раннюю активизацию больных [23]. Имплантация бесшовного биопротеза Perceval S не вызывает технических сложностей. Длительность искусственного кровообращения и пережатия аорты меньше, по сравнению с имплантацией стандартных механических и биологических протезов, при этом среднее время имплантации составляет всего 10–15 мин [17]. Отсутствие необходимости в наложении швов на фиброзное кольцо аортального клапана, в свою очередь, ведет к отсутствию риска их прорезывания при выраженном кальцинозе с последующим возможным формированием парапротезной фистулы [12]. Несомненным плюсом является также сокращение времени нахождения пациента в отделении реанимации и хирургическом отделении [24].
В сравнении с транскатетерной имплантацией АК, преимуществами метода бесшовного биопротезирования протезом Perceval S являются возможность проведения частичной декальцинации [25], имплантации протеза под прямым визуальным и мануальным контролем, репозиционирования протеза, низкий риск обструкции коронарных артерий, а также меньшая стоимость бесшовного клапана [26]. В связи с этим очевидна потребность в увеличении числа имплантаций бесшовного протеза Perceval S.
Как правило, нормализации функциональных показателей ЛЖ после имплантации бесшовных биопротезов следует ожидать в раннем послеоперационном периоде, но оно продолжается и через 36 мес. после операции. Наиболее выраженный эффект — улучшение гемодинамических показателей — наблюдается через 6–9 мес. Уменьшение дилатации и гипертрофии миокарда ЛЖ предопределяет отдаленную выживаемость оперированных больных и в свою очередь непосредственно связано с такими характеристиками протеза, как индекс ЭПО и транспротезный градиент.
Заключение
Ксеноперикардиальные бесшовные биопротезы аортального клапана Perceval S адекватно корригируют внутрисердечную гемодинамику, обеспечивая нормализацию функциональных показателей ЛЖ в ближайшем и среднеотдаленном периодах и могут быть рекомендованы пациентам пожилого возраста. Имплантация бесшовного протеза из мини-доступа не увеличивает техническую сложность операции и способствует более гладкому раннему послеоперационному периоду.
Финансирование
Исследование не имело спонсорской поддержки.
Список литературы Клинико-гемодинамические результаты имплантации бесшовных биопротезов PERCEVAL s в аортальной позиции из мини-доступа у пожилых пациентов
- Кузнецов А.Н., Андреев Д.Б., Бондарь В.Ю., Семченко А.Н., Явный В.Я., Щава С.П., Внукова Т.Б. Опыт применения бесшовных самофиксирующихся биологических клапанных систем Perceval S как альтернатива традиционному протезированию аортального клапана. Бюллетень НЦССХ им. А.Н. Бакулева РАМН. Сердечно-сосудистые заболевания. 2014;15(S3):146.
- Miceli A., Santarpino G., Pfeiffer S., Murzi M., Gilmanov D., Concistre G., Quaini E., Solinas M., Fischlein T., Glauber M. Minimally invasive aortic valve replacement with Perceval S sutureless valve: early outcomes and one-year survival from two European centers. J Thorac Cardiovasc Surg. 2014;148(6):2838-43. PMID: 24698558. http://dx.doi.o DOI: rg/10.1016/j.jtcvs.2014.02.085
- Chandola R., Teoh K., Elhenawy A., Christakis G. Perceval Sutureless valve -are Sutureless valves here. Curr Cardiol Rev. 2015;11(3):220-8. PMID: 25394851. http://dx.doi.o 3403X11666141113155744 DOI: rg/10.2174/157
- Phan K., Tsai Y.-C., Niranjan N., Bouchard D., Carrel T.P., Dapunt O.E., Eichstaedt H.C., Fischlein T., Gersak B., Glauber M., Haverich A., Misfeld M., Oberwalder P.J., Santarpino G., Shrestha M.L., Solinas M., Vola M., Yan T.D., Eusanio M.D. Sutureless aortic valve replacement: a systematic review and meta-analysis. Ann Cardiothorac Surg. 2014;4(2):100-11. PMID: 25870805. http://dx.doi.o DOI: rg/10.3978/j.issn.2225-319X.2014.06.01
- Flameng W., Herregods M.C., Hermans H., Van der Mieren G., Vercalsteren M., Poortmans G., Van Hemelrijck J., Meuris B. Effect of sutureless implantation of the Perceval S aortic valve bioprosthesis on intraoperative and early postoperative outcomes. J Thorac Cardiovasc Surg. 2011;142:1453-7. PMID: 21474151. http://dx.doi.o DOI: rg/10.1016/j.jtcvs.2011.02.021
- Santarpino G., Pfeiffer S., Concistre G., Grossmann I., Hinzmann M., Fischlein T. The Perceval S aortic valve has the potential of shortening surgical time: does it also result in improved outcome? Ann Thorac Surg. 2013;96(1):77-81. PMID: 23673064. http://dx.doi. org/10.1016/j.athoracsur.2013.03.083
- Gilmanov D., Miceli A., Bevilacqua S., Farneti P., Solinas M., Ferrarini M., Glauber M. Sutureless implantation of the Perceval S aortic valve prosthesis through right anterior minithoracotomy. Ann Thorac Surg. 2013;96(6):2101-8. PMID: 24054468. http://dx.doi.o DOI: rg/10.1016/j.athoracsur.2013.07.007
- Dalen M., Biancari F., Rubino A.S., Santarpino G., De Praetere H., Kasama K., Juvonen T., Deste W., Pollari F., Meuris B., Fischlein T., Mignosa C., Gatti G., Pappalardo A., Sartipy U., Svenarud P. Ministernotomy versus full sternotomy aortic valve replacement with a sutureless bioprosthesis: a multicenter study. Ann Thorac Surg. 2015;99(2):524-30. PMID: 25483001. http://dx.doi. org/10.1016/j.athoracsur.2014.08.028
- Villa E., Messina A., Laborde F., Shrestha M., Troise G., Zannis K., Haverich A., Elfarra M., Folliguet T. Challenge for perceval: aortic valve replacement with small sutureless valves -a multicenter study. Ann Thorac Surg. 2015;99(4):1248-54. PMID: 25661579. http://dx.doi.o DOI: rg/10.1016/j.athoracsur.2014.09.090
- Fischlein T., Pfeiffer S., Pollari F., Sirch J., Vogt F., Santarpino G. Sutureless Valve implantation via mini J-sternotomy: a single center experience with 2 years mean follow-up. PMID: 26177222. Thorac Cardiovasc Surg. 2015;63(6):467-71. http://dx.doi. org/10.1055/s-0035-1554043
- Cerillo A.G., Bevilacqua S., Farneti P.A., Concistre G., Glauber M. Sutureless aortic valve replacement through a right minithoracotomy. J Heart Valve Dis. 2012;21(2):168-71. PMID: 22645850.
- Concistre G., Miceli A., Chiaramonti F., Glauber M. Delayed dislocation of a sutureless aortic bioprosthesis: the first case. Interact Cardiovasc Thorac Surg. 2012;14(6):892-93. PMID: 22388999. http://dx.doi.o DOI: rg/10.1093/icvts/ivr015
- Folliguet T.A., Laborde F., Zannis K., Ghorayeb G., Haverich A., Shrestha M. Sutureless perceval aortic valve replacement: results of two European centers. Ann Thorac Surg. 2012;93(5):1483-8. PMID: 22541180. http://dx.doi.o DOI: rg/10.1016/j.athoracsur.2012.01.071
- Laborde F., Fischlein T., Hakim-Meibodi K., Misfeld M., Carrel T., Zembala M., Madonna F., Meuris B., Haverich A., Shrestha M.; Cavalier Trial Investigators. Clinical and haemodynamic outcomes in 658 patients receiving the Perceval sutureless aortic valve: early results from a prospective European multicentre study (the Cavalier Trial). Eur J Cardiothorac Surg. 2016;49(3):978-86. PMID: 26245628. http://dx.doi.o DOI: rg/10.1093/ejcts/ezv257
- Shrestha M., Folliguet T., Meuris B., Dibie A., Bara C., Herregods M.C., Khaladj N., Hagl C., Flameng W., Laborde F., Haverich A. Sutureless Perceval S aortic valve replacement: a multicenter, prospective pilot trial. J Heart Valve Dis. 2009;18:698-702. PMID: 20099720.
- Di Eusanio M., Phan K. Sutureless aortic valve replacement. Ann Cardiothorac Surg. 2015;4(2):123-30. PMID: 25870807. http://dx.doi.o DOI: rg/10.3978/j.issn.2225-319X.2015.02.06
- Pradelli L., Zaniolo O. Perceval sutureless valves in isolated and concomitant AVR procedures: an economic model shows overall decrease of costs for isolated or combined operations. Patologiya krovoobrashcheniya i kardiokhirurgiya. 2017;21 (3):32-39
- Della Barbera M., Basso C., Valente M., Thiene G. Pre-implantation collapse in the Sorin Perceval S sutureless prosthesis does not affect pericardial graft structure. Cardiovascular pathology. 2013;22(3):e43. http://dx.doi.o DOI: rg/10.1016/j.carpath.2013.01.052
- Овчаренко Е.А., Клышников К.Ю., Влад А.Р., Сизова И.Н., Журавлева И.Ю. Анатомическое обоснование трехмерных моделей корня аорты человека. Клиническая физиология кровообращения. 2013;(2):12-20. https://cfc-journal.com/catalog/web/viewer.php
- Бокерия Л.А., Гудкова Р.Г. Сердечно-сосудистая хирургия. М.: Научный центр сердечно-сосудистой хирургии им. А.Н. Бакулева, 2015. 226 с.
- Крайнюков П.Е., Далинин В.В., Борисов И.А., Афонасков О.В. Первый опыт применения бесшовного протеза Perceval S. Военно-медицинский журнал. 2016;337(8):28-34. http://sc.mil.ru/files/morf/military/archive/N_08.pdf
- Gersak B., Fischlein T., Folliguet T.A., Meuris B., Teoh K.H., Moten S.C., Solinas M., Miceli A., Oberwalder P.J., Rambaldini M., Bhatnagar G., Borger M.A., Bouchard D., Bouchot O., Clark S.C., Dapunt O.E., Ferrarini M., Laufer G., Mignosa C., Millner R., Noirhomme P., Pfeiffer S., Ruyra-Baliarda X., Shrestha M., Suri R.M., Troise G., Diegeler A., Laborde F., Laskar M., Najm H.K., Glauber M. Sutureless, rapid deployment valves and stented bioprosthesis in aortic valve replacement: recommendations of an International Expert Consensus Panel. Eur J Cardiothorac Surg. 2015;49(3):709-18. PMID: 26516193. http://dx.doi.o DOI: rg/10.1093/ejcts/ezv369
- Glauber M., Miceli A. Minimally invasive aortic valve replacement with sutureless valve is the appropriate treatment option for high-risk patients and the ‘‘real alternative’’ to transcatheter aortic valve implantation. J Thorac Cardiovasc Surg. 2016;151:610-3. PMID: 26602264. http://dx.doi.o DOI: rg/10.1016/j.jtcvs.2015.10.028
- Miceli A., Gilmanov D., Murzi M., Marchi F., Ferrarini M., Cerillo A.G., Quaini E., Solinas M., Berti S., Glauber M. Minimally invasive aortic valve replacement with a sutureless valve through a right anterior minithoracotomy versus transcatheter aortic valve implantation in high-risk patients. Eur J Cardiothorac Surg. 2016;49(3):960-5. PMID: 26113005. http://dx.doi.o DOI: rg/10.1093/ejcts/ezv210
- Хубулава Г.Г., Шихвердиев Н.Н., Гавриленков В.Н., Кучеренко В.С. Бескаркасные биопротезы в хирургии пороков клапана аорты. СПб.: Наука, 2009. 187 c.
- Santarpino G., Pietsch L.E., Jessl J., Pfeiffer S., Pollari F., Pauschinger M., Fischlein T. Transcatheter valve-in-valve implantation and sutureless valve replacement: two strategies for one goal in REDO patients. Minerva Cardioangiol. 2016;64(6):581-5. PMID: 26859231.


