Клинико-неврологические особенности у больных с венозной церебральной дисфункцией
Автор: Гафуров Б.Г., Назарова Ж.А.
Журнал: Саратовский научно-медицинский журнал @ssmj
Рубрика: Нервные болезни
Статья в выпуске: 2 т.15, 2019 года.
Бесплатный доступ
Цель: изучить клинико-неврологические особенности у больных с хронической ишемией головного мозга (ХИГМ) в зависимости от наличия венозной церебральной дисфункции (ВЦД). Материал и методы. В исследовании приняли участие 168 пациентов, страдающих ХИГМ (средний возраст 61,2±3,8 года; 45,2 % - мужчины). Контрольная группа включила 20 здоровых людей, сопоставимых по полу и возрасту. Всем пациентам с ХИГМ выполнена реоэнцефалография (РЭГ) для выявления ВЦД, проведено стандартное клинико-неврологическое обследование (жалобы, анамнез, оценка неврологического статуса), изучены клинические особенности головной боли с помощью оригинальной анкеты, определялась интенсивность боли с помощью десятибалльной визуально-аналоговой шкалы (ВАШ). Когнитивный статус оценивался во всех группах исследования методом вызванных потенциалов с использованием методики Р300. Результаты. У больных с ХИГМ в 46,4 % случаев выявлена венозная церебральная симптоматика. У таких пациентов наиболее выражен синдром головной боли, как по клиническим критериям, так и по балльной оценке ВАШ: 6,8 балла против 5,1 балла у больных с ХИГМ без ВЦД (р
Венозная церебральная дисфункция, головная боль, хроническая ишемия головного мозга
Короткий адрес: https://sciup.org/149135281
IDR: 149135281 | УДК: 612.824.4
Clinical and neurological features in patients with venous cerebral dysfunction
Objective: to study the clinical and neurological features in patients with chronic cerebral ischemia, depending on the presence of venous cerebral dysfunction. Material and Methods. 168 patients sufering from chronic cerebral ischemia took part in the study (mean age 61.2±3.8 yrs; 45.2 % - men). The control group comprised 20 healthy subjects comparable in age and sex distribution. All patients with chronic cerebral ischemia underwent rheoencephalographya for detection of cerebral venous dysfunction, as well as standard clinical and neurological examination (patient»s complaints, past history, neurological status assessment). Clinical features of headache were evaluated using the original questionnaire. The intensity of headache were determined using a ten-point visual-analog scale. Cognitive function was assessed in all study groups by means of evoked potential method with using P300 technique. Results. In patients with chronic cerebral ischemia in 46.4 % of cases revealed venous cerebral symptoms. In such patients, headache syndrome is most pronounced, both by clinical criteria and by visual-analog scale score: 6.8 points against 5.1 points in patients with chronic cerebral ischemia without venous cerebral dysfunction (p function show_eabstract() { $('#eabstract1').hide(); $('#eabstract2').show(); $('#eabstract_expand').hide(); }
Текст научной статьи Клинико-неврологические особенности у больных с венозной церебральной дисфункцией
1 Введение. Сосудистые заболевания головного мозга представляют собой актуальную медико-социальную проблему, занимающую ведущее место в структуре заболеваемости и смертности в экономически развитых странах.
В последние годы структура цереброваскулярных заболеваний меняется за счет нарастания ишемических форм. Это обусловлено повышением удельного веса артериальной гипертензии и атеросклероза как основной причины сосудистой патологии мозга [1, 2].
Хроническая ишемия головного мозга (ХИГМ) представляет собой единый патологический процесс, охватывающий многообразные механизмы, которые возникают в результате несоответствия мозгового кровотока метаболическим потребностям мозговой ткани. Ведущую роль в этиологии данной патологии отводят артериальной гипертензии и атеросклерозу церебральных сосудов [3, 4].
В настоящее время уже доказано, что при ХИГМ важное патогенетическое значение, наряду с нарушением притока крови к головному мозгу в бассейне пораженной артерии, имеет затруднение венозного оттока от головного мозга [5–7]. Очевидна необходимость изучения состояния магистральных артерий головы. Проводимые исследования головного мозга свидетельствуют о том, что примерно 85% объема сосудистого русла этого органа приходится на венозные сосуды, 10% на артерии, около 5% на капилляры.
Степень компенсации венозной дисгемии зависит от коллатерального кровообращения и скорости развития венозного застоя внутри черепа. Недооценка роли церебрального венозного кровообращения в формировании сосудистой церебральной патологии мешает правильному пониманию патокинетиче-ских механизмов развития хронической ишемии головного мозга [8, 9].
Изучение венозного компонента мозгового кровообращения значительно отстает от исследований артериальной гемодинамики, несмотря на тесные взаимоотношения артериального звена и венозного русла головного мозга.
Цель: изучить клинико-неврологические особенности у больных с ХИГМ в зависимости от наличия венозной церебральной дисфункции.
Материал и методы. Обследованы 168 пациентов с ХИГМ 2-й стадии, из них 76 мужчин (45,2%) и 92 женщины (54,8%). Возраст обследуемых больных варьировался от 50 до 73 лет, в среднем 61,2±3,8 года. У каждого обследуемого было получено письменное согласие на проведение обследования. Контрольная группа включила 20 здоровых людей, сопоставимых по полу и возрасту.
При проведении РЭГ-исследования у 78 (46,4%) больных выявлена венозная церебральная дисфункция (ВЦД). В зависимости от наличия ВЦД все больные были разделены на группы: 1-ю группу составили 78 больных с ХИГМ и ВЦД; во 2-ю группу вошли 90 больных с ХИГМ без ВЦД.
Всем больным проведено стандартное неврологическое обследование (анализ жалоб пациентов, объективный осмотр, в том числе изучение неврологического статуса), изучение клинических особенностей головной боли (ГБ) с помощью оригинальной анкеты,
определение интенсивности ГБ с помощью десятибалльной визуально-аналоговой шкалы (ВАШ).
Когнитивный статус исследовался методом вызванных потенциалов. Регистрация когнитивных вызванных потенциалов (КВП) проводилась на 16-канальном электроэнцефалографе «Нейрон-Спектр 4/ВП» с использованием электродов С3 и С4, масто-идных электродов А1 и А2 и заземляющего электрода Fpz. Серии стимулов подавались бинаурально с частотой тона для значимого 2000 Гц, для незначимого 1000 Гц. Соотношение количества незначимых стимулов к значимым 70/30. Использовалась методика Р300 — выделение вызванных потенциалов на значимые опознаваемые события. При методике Р300 дается инструкция, согласно которой один из стимулов считается значимым и его нужно опознать и подсчитать.
Стимулы подавались в псевдослучайном порядке в соотношении 3:7, для значимых и незначимых соответственно с интервалом между стимулами в 1 сек через наушники на оба уха одновременно. Длительность подаваемого стимула 50 мс, интенсивность 80 дБ.
Компонент Р300 записывали с постоянного времени 0,3 сек и полосой частот 0,2–75 Гц, эпоха анализа 750 мс. Количество усреднений для значимого стимула составляло 20. Автоматически проводилось усреднение на предъявляемые значимые и незначимые стимулы. Полученные ответы подвергались фильтрации в диапазоне частот от 0,5 до 30 Гц. Выделялись основные пики когнитивного вызванного потенциала: Р1, N1, P2, N2, P3, N3. Вычислялся латентный период компонента Р300 как латентный период пика Р3 в мс, амплитуда Р300 как межпиковая амплитуда N2-P3 в мкВ [10].
Для анализа полученных данных использовался пакет программ Statistica с использованием прикладных программ Statistica 8.0 и Excel. Производилась оценка распределения признаков на нормальность с использованием критерия Колмогорова — Смирнова (распределение нормальное). Для выявления различий между показателями у сравниваемых групп использовали t-критерий Стьюдента. Критический уровень значимости (р) при проверке статистических гипотез в исследовании принимали равным 0,05. При описании результатов исследования количественные данные представлены в виде М (±σ), где М — среднее арифметическое, σ — стандартное отклонение, качественные данные представлены в виде абсолютных значений, процентов и долей.
Результаты. Неврологическое обследование у больных 1-й группы регистрировало мелкоочаговую рассеянную симптоматику. Наиболее частый симптом: болезненность точек выхода V пары черепных нервов. У большинства таких пациентов обнаруживали вегетососудистый и неврозоподобный синдромы. Утренняя отечность лица после ночного сна беспокоила 68,2% пациентов 1-й группы (чаще женщин). При осмотре пациентов с ВЦД была заметна выраженная бледность кожных покровов в сочетании с цианотичной окраской лица. В некоторых случаях наблюдался локальный цианоз губ. Пастозность лица и век по утрам определялась у подавляющего числа пациентов (71,2%). При физической активности отечность к вечеру уменьшалась.
Во 2-й группе больных не прослеживалось «венозных симптомов». Клинико-неврологическая симптоматика у больных в этой группе была менее выражена по сравнению с больными 1-й группы.
1 группа (78)
Группы больных
-
■ Ааешпк-скийсшцром
-
■ Цефапический синдром
-
■ Вегетоахулктынапиром
Пиралпцная недоспио» шоаъ
-
■ Вестпот.тя1)но-атакпп1акий синдром
-
■ Алпюсгатичепошпщдром
-
■ Псевдофльофньшсинщюм
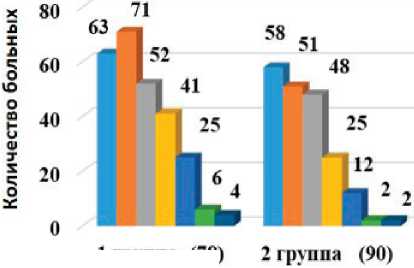
Клинико-неврологическая симптоматика у больных с ХИГМ в зависимости от наличия ВЦД
Все обследуемые больные имели достаточно отчетливую очаговую симптоматику. У большинства больных она была представлена синдромом пирамидной недостаточности, часто в сочетании с начальными проявлениями вестибулярно-атактического и цефалгического синдромов. Наряду с признаками очагового поражения отмечались достаточно выраженные эмоционально-аффективные расстройства и мнестические нарушения. У больных 1-й группы по сравнению со 2-й группой достоверно чаще (р<0,05) встречались такие неврологические синдромы, как астенический, цефалгический, вестибулярно-атактический и пирамидной недостаточности: в 80,7, 91,0, 32,0 и 52,5% случаев соответственно (рисунок).
Цефалгический синдром имел отличительные особенности. Так, у больных 1-й группы головная боль чаще носила двусторонний характер, локализовалась в теменно-затылочной (45,3%) или лобновисочной (48,1 %) областях. В 35,9% случаев локальная ГБ переходила в диффузную. У большинства была постоянной, люди сетовали на чувство тяжести в голове. В 28,5% случаев возникала приступообразная интенсивная боль, которую характеризовали как сжимающую, распирающую, давящую, пульсирующую. Она усиливалась на фоне психоэмоционального или физического напряжения, при работе в наклонном положении (36,2%). Количественная выраженность ГБ у обследуемых больных в среднем определялась в баллах по ВАШ. Имелись межгрупповые различия в характере ГБ.
Так, в 1-й группе ГБ имела степень выраженности 5,1 балла, что достоверно выше по сравнению с таким же показателем во 2-й группе. У всех больных 1-й группы наблюдалась головная боль, возникающая утром при пробуждении, она уменьшалась после подъема с постели и исчезала к середине дня. Больных 1-й группы ГБ в 27,4% случаев беспокоила ночью.
У больных 2-й группы ГБ чаще была приступообразной (53,2%), двухсторонней (41,8%), с проекцией в затылочно-теменной области (42,2%). Усиливалась ГБ на фоне психоэмоционального или физического напряжения, при работе в наклонном положении (39,8%). По ВАШ такая ГБ определялась как умеренная — 4,3 балла. Утренняя ГБ была редкой и наблюдалась в 18,4% случаев.
Оценка коморбидного фона пациентов двух групп представлена в табл. 1. Согласно представленным данным, все пациенты имели сопутствующую патологию, но среди пациентов 1-й группы в большинстве случаев (74,4%) выявлены: метаболический синдром, остеохондроз шейного отдела позвоночника (94,9%), варикозная болезнь нижних конечностей (57,7%), хроническая обструктивная болезнь легких (41,0%), хроническая сердечная недостаточность (ХСН) (29,5%), что достоверно выше аналогичных показателей пациентов 2-й группы.
Таблица 1
Структура коморбидности у больных ХИГМ в зависимости от наличия ВЦД
|
Коморбидные заболевания |
1-я группа (n=78) |
2-я группа (n=90) |
||
|
n |
% |
n |
% |
|
|
Метаболический синдром |
58 |
74,3** |
24 |
26,6 |
|
Остеохондроз шейного отдела позвоночника |
74 |
94,8* |
45 |
50,0 |
|
Хроническая обструктивная болезнь легких |
32 |
41,0** |
6 |
6,6 |
|
Варикозная болезнь нижних конечностей |
45 |
57,6* |
28 |
31,1 |
|
ХСН |
23 |
29,4 |
9 |
10,0 |
П р и м еч а н и е : * — различия между группами статистически значимы, р<0,05; ** — различия между группами статистически значимы, р<0,001.
Таблица 2
Латентности пика РЗ и межпикового интервала N2/P3 слуховых когнитивных вызванных потенциалов у больных с ХИГМ в зависимости от наличия ВЦД по сравнению с контролем
|
Полушарие |
Параметры латентности |
1-я группа |
2-я группа |
Контрольная группа |
|
М±σ |
М±σ |
М±σ |
||
|
Левое |
Латентный период P3 (мс) Межпиковая латентность N2/P3, ампл, мкВт |
358,4±15,2* 8,6±2,8 * |
347,3±17,6^ # 10,7±5,1^ |
336,8±14,6 16,3±4,6 |
|
Правое |
Латентный период P3 (мс) Межпиковая латентность N2/P3, ампл, мкВт |
361,4±11,6* 9,1±1,7* |
348,3±14,3^# 11,2 ± 4,3 ^ |
332,9±12,3 15,9±5,1 |
П р и м еч а н и е : * — значимость различий параметров 1-й и контрольной групп, р<0,05; # — значимость различий параметров 1-й и 2-й групп, р<0,05; ^ — значимость различий параметров 2-й и контрольной групп, р<0,05.
Показатели КВП больных 1-й и 2-й групп по сравнению с контролем представлены в табл. 2.
Анализируя полученные результаты, обнаружили следующие особенности. Выявлено удлинение значений латентности пиков P3 в обоих полушариях у больных 1-й группы по сравнению со 2-й группой и группой контроля. Более значимые изменения отмечались у больных с ВЦД по сравнению с контролем. У больных 2-й группы значимо различались показатели латентного параметра амплитуды N2/P3 в правом полушарии по сравнению с контролем. Так, этот показатель у больных 2-й группы составил 11,2±4,3 мкВт, а в контрольной группе 15,9±5,1 мкВт. Кроме того, наблюдались достоверные межгрупповые различия по показателям Р3 в обоих полушариях (см. табл. 2).
Обсуждение. «Венозные жалобы и симптомы» достаточно часто встречаются среди больных с хронической ишемией мозга. Это обусловлено избыточным кровенаполнением венозных сосудов (вен и венозных синусов) и затруднением венозного оттока. В настоящее время большинство авторов признают важное значение венозного фактора в патогенезе разных форм цереброваскулярной патологии.
Напряжение мышц приводит к сужению артериальных сосудов, что сопровождается ишемией, спазмом капилляров, нарушением питания мышцы и венозного оттока, венозным застоем. Кроме этого, изменения нейрогенной регуляции обусловливают появление расширения артериовенозных шунтов, «обкрадывание» капиллярной сети, что приводит к ишемической гипоксии, затруднению венозного оттока, переполнению венозных сосудов кровью, их избыточному растяжению — дополнительному фактору в генезе цефалгии. Вовлечение венозной системы способствует учащению эпизодов боли и хронизации процесса [11, 12].
Венозная дисгемия способна усугубляться при наличии многих сопутствующих заболеваний. По нашим данным, у больных с ХИГМ 2-й стадии венозная церебральная дисгемия наиболее часто выявлялась у больных с метаболическим синдромом, остеохондрозом шейного отдела позвоночника и хронической обструктивной болезнью легких.
При регистрации когнитивных вызванных потенциалов можно получить дополнительную информацию о состоянии когнитивной сферы у больных с ХИГМ с имеющейся венозной церебральной дисфункцией. Р300 характеризует процессы дифференцировки, запоминания и принятия решения. За гене- рацию Р300 ответственны лобная доля, теменная область, подкорковые структуры и гиппокамп [10]. Увеличение латентности Р300 свидетельствует о нарушении описанных когнитивных процессов и о вероятной дисфункции зон мозга, влияющих на формирование пика Р300. Наличие сопутствующей ВЦД приводит к более выраженному проявлению когнитивного дефицита.
Заключение . При диагностике ХИГМ следует учитывать наличие венозной дисциркуляции головного мозга. Необходимо оценивать «венозные» жалобы больных, особенности неврологического и когнитивного статуса у больных с хронической ишемией мозга, обусловленные венозной церебральной дисфункцией. Следует предположить, что наличие венозной дисциркуляции головного мозга отягощает течение церебральной ишемии.
Список литературы Клинико-неврологические особенности у больных с венозной церебральной дисфункцией
- Гусев Е. И., Скворцова В. И. Ишемия головного мозга. М., 2001; 328 c.
- Котов С. В., Исакова Е. В., Козяйкин В. В. и др. К вопросу о профилактике церебрального инсульта. Русский медицинский журнал 2014; 22 (22): 1582-5
- Суслина З. А., Варакин Ю. Я., Верещагин Н. В. Сосудистые заболевания головного мозга. М.: МЕДпресс-информ, 2015; 356 c.
- Белова Л. А. Венозная церебральная дисциркуляция при хронической ишемии мозга: клиника, диагностика, лечение. Неврологический вестник 2010; 42 (2): 62-7
- Манвелов Л. С., Кадыков А. В. Венозная недостаточность мозгового кровообращения. Атмосфера. Нервные болезни 2007; 2: 18-21
- Иванов А. Ю., Панунцев А. Н., Кондратьев А. Н. и др. Особенности венозного оттока от головного мозга. Неврологический вестник 2010; 42 (2): 5-10
- Гачечиладзе Д. Г., Берулава Д. В., Антия Т. А. Особенности церебральной венозной гемодинамики при хронических нарушениях мозгового кровообращения. Медицинская визуализация 2012; 4: 104-12
- Henry-Feugeas MC, Koskas P. Cerebral vascular aging extending the concept of pulse wave encephalopathy through capillaries to the cerebral veins. Chinese Medical Journal 2012; 125 (7): 1303-9
- Гордеев С. А. Применение метода эндогенных связанных с событиями потенциалов мозга Р300 для исследования когнитивных функций в норме и клинической практике. Физиология человека 2007; 2: 121-33
- Морозова О. Г. Патогенетический подход к лечению головной боли у пациентов с венозной дистензией при начальной хронической церебральной ишемии. Семейная медицина 2008; 3: 83-5
- Bendtsen L, Ashina S, Moore A, et al. Muscles and their role in episodic tension-type headache: implications for treatment. Eur J Pain 2016; 20 (2): 166-75.


