Клиникохморфогенетические варианты атрофического поражения слизистой оболочки желудка
Автор: Наумова Л.А., Пушкарев С.В., Чичагова Е.Е., Саблина О.Ф.
Журнал: Сибирский журнал клинической и экспериментальной медицины @cardiotomsk
Рубрика: Клинические исследования
Статья в выпуске: 4-1 т.26, 2011 года.
Бесплатный доступ
Цель исследования: изучить особенности морфогенеза атрофического процесса в слизистой оболочке желудка. Проведено клинико-морфологическое (световая микроскопия гастробиоптатов, иммуногистохимия) исследование у 117 пациентов с атрофией слизистой оболочки желудка (СОЖ) при отсутствии (1-я группа) и наличии Helicobacter (Н.) pylori-инфекции (2-я группа), изучены особенности экспрессии трансформирующего фактора роста бета (TGF-?) и рецепторов к нему 1-го типа (TGF-?R1) в железистом и стромальном компартментах СОЖ. Выделены два варианта морфогенеза атрофического процесса (АП) в СОЖ. Первый развивается при отсутствии H. pylori#инфекции, ассоциируется с сочетанным влиянием нескольких эндогенных факторов риска развития хронического гастрита, преобладанием дисрегенераторных изменений в теле желудка с выраженной тенденцией к атрофии желез. Клинически он отличается высокой частотой системности атрофического поражения слизистых оболочек желудочно-кишечного тракта, преобладанием среди жалоб дистензионных болей. Второй вариант ассоциируется с сочетанным влиянием эндо- и экзогенных факторов, в частности, наличием H. pylori-инфекции, патогенетических механизмов "химического" гастрита, преобладанием дисрегенераторных и склеротических изменений в антральном отделе желудка. При исследовании эпителио-стромальных отношений по состоянию системы TGF-? - TGF-?R1 отмечены как общие, так и различные для каждого из вариантов проявления ее дисбаланса, отражающие особенности их морфогенеза. Полиэтиологичность АП в целом и наличие его различных морфогенетических вариантов требуют особого диагностического алгоритма и патогенетически обоснованной терапии в каждом конкретном случае. Определение баланса в системе TGF-? - TGF-?R1 может стать важным маркером нарушения эпителио-стромальных отношений при формировании групп риска по развитию рака желудка среди пациентов с АП в СОЖ.
Атрофия слизистой желудка, варианты морфогенеза, трансформирующий фактор роста бета
Короткий адрес: https://sciup.org/14919615
IDR: 14919615 | УДК: 616.33-002.27
Сliniсoxmorfogenetical variants of gastric mucosal atrophy
Aim: to study the features of morphogenesis of atrophic process (AP) in a gastric mucosa. The clinical and pathomorphological research (light microscopy of gastrobiopsies, immunohistochemistry) has been performed to 117 patients with gastric mucosa (GM) atrophy non-associated (group 1) and associated with Helicobacter (H.) pylori-infection (group 2), features of an expression of transforming growth factor beta (TGF-?) and its receptors (TGF-?R1) in glandular and stromal compartments of GM have been studied. According to the results of comparative clinical and morphological analysis, two variants of morphogenesis of AP in GM were defined. The first variant develops in the absence of the H. pylori infection and associates with the combined influence of several endogenous risk factors of chronic gastritis and the primordial predominance of dysregenerative changes in corpus of the stomach with a pronounced tendency to atrophy of the glands. Clinically it is distinguished by a higher rate of systematic atrophic injury of gastro-intestinal tract mucosa with predominance of distending pains. The second variant is associated with a combined influence of endo- and exogenouse factors, in particular, with the presence of H. pylori-infection, pathogenetic mechanisms of "chemical" gastritis (duodeno-gastral reflux, long time defects in diet), predominance of dysregenerative and sclerotic changes in antrum. During the research of epithelio-stromal interactions according to the state of TGF-?-TGF-?R1 system we determined both common and distinct manifestations of dysbalance reflecting the peculiarities of morphogenesis of every variant. Polyaetiology of AP on the whole and the presence of its various morphological variants in GM demands both: individual diagnostic algorithm and pathogenetically based therapy in every concrete case. Determination of balance in TGF-?- TGF-?R1 system can become the important marker of violations of epithelio-stromal interactions at formation of groups of cancer development risk among patients with GM atrophy.
Текст научной статьи Клиникохморфогенетические варианты атрофического поражения слизистой оболочки желудка
Атрофия относится к ярким проявлениям несостоятельности процессов регенерации и на тканевом уровне характеризуется как выраженный дисрегенераторный процесс с формированием двух противоположных тенденций в поведении эпителия – к атрофии и очаговой гипер-, мета- и дисплазии на фоне прогрессирующих склеротических изменений, отражающих нарушения эпителио-стромальных отношений [1, 8, 11].
К одной из важных характеристик эпителио-стро-мальных отношений относится состояние системы транс-формирущего фактора роста в (TGF- β ) и рецепторов к нему, в частности 1-го типа – TGF- β R1. Являясь полипеп-тидным клеточным регулятором, TGF- β участвует в регуляции пролиферации и дифференцировки клеток, процессах репарации, апоптоза, клеточной миграции и адгезии, продукции экстрацеллюлярного матрикса. Усиление экспрессии TGF- β ассоциируется со многими заболеваниями: склерозом, алиментарным ожирением и даже артериальной гипертензией через участие в регуляции экспрессии эндотелина-1 и высвобождении ренина. Дисбаланс в системе TGF- β – TGF- β R1 может ассоциироваться с прогрессированием атрофических изменений и играть ключевую роль в возникновении многих форм рака [13, 16, 17].
Характер эпителио-стромальных отношений во многом, на наш взгляд, определяет дальнейшие морфогене- тические потенции АП, а понимание морфогенетических вариантов последнего – особенности лечения.
Материал и методы
Обследованы 117 пациентов (42 мужчины и 75 женщин) в возрасте от 18 до 58 лет с эндоскопически диагностированной атрофией СОЖ и клиническим диагнозом ХАГ. Первую группу составили 65 больных (средний возраст – 37,0±4,4 лет) без сопутствующей H. pylori-инфекции в анамнезе и на момент обследования, вторую – 52 человека (средний возраст – 32,8±7,0 лет) с H. pylori-позитивным процессом.
Иммуногистохимическое исследование выполнялось стрептавидин-биотиновым иммунопероксидазным методом на серийных парафиновых срезах с использованием моноклональных антител к TGF β и TGF β R1, в обоих случаях в разведении 1 : 40 (Novocastra, Великобритания). Для отрицательного контроля первичные антитела заменяли неиммунной сывороткой. Оценку результатов исследования проводили по условной 6-балльной шкале.
Для описания количественных признаков использовали среднее значение, стандартную ошибку среднего значения, для качественных – долю, стандартную ошибку; дисперсионный анализ (выявление межгрупповых различий) проводили с использованием t-критерия Стъю-дента и χ 2 критерия Пирсона при уровне значимости p<0,05. Статистическая обработка данных проводилась с использованием программного пакета Excel 2002 (Microsoft, США).
Результаты
При сопоставимости рассматриваемых групп по возрасту пациентов, длительности заболевания (10,3±2,1 и 5,9±1,4 лет) и общности ряда проявлений АП сравнительный анализ позволил выделить два его различных клинико-морфогенетических варианта, обозначенных соответственно группам как первый и второй (табл. 1).
Оба варианта ассоциировались с сочетанным влиянием нескольких эндогенных факторов риска хронического гастрита [11]. Это высокая частота висцеральных признаков дисплазии СТ; сопутствующих эндокринопа-тий, среди которых преобладали дисфункции половых желез с клиническими маркерами дис- и гиперэстроге-немии [10]; сопутствующей патологии ГПДЗ, в частности хронической описторхозной инвазии (12,3 и 11,5%), ассоциирующейся, как известно, с увеличением частоты атрофического поражения СОЖ.
Второй морфогенетический вариант АП отличали сочетанное влияние эндо- и экзогенных факторов риска хронического гастрита [11], в частности наличие H. pylori-инфекции, патогенетических звеньев “химического гастрита” (дуоденогастральный рефлюкс, продолжительные погрешности в питании), скудная клиническая симптоматика.
Сравнительный анализ морфогенетических вариантов в возрастном аспекте (табл. 2) показал, что с возрастом увеличивается частота сопутствующих эндокрино-патий преимущественно за счет дисфункции половых желез. Признаки дисплазии СТ практически с одинаковой частотой встречаются во всех возрастных подгруппах. С возрастом нарастает также частота системных проявлений АП и сопутствующих заболеваний ГПДЗ.
Таблица 1
Клинические особенности морфогенетических вариантов АП
|
Особенности анамнеза и проявлений АП |
1-я группа, n=65 |
2-я группа, n=52 |
||
|
абс. |
% |
абс. |
% |
|
|
Признаки дисплазии СТ |
49 |
75,4±5,3 |
43 |
82,7±5,2 |
|
Сопутствующие эндокринопатии, |
||||
|
в том числе дисфункции: |
45 |
69,2±5,7 |
27 |
51,9±6,9 |
|
– половых желез |
36 |
55,4±6,2 |
25 |
48,1±6,9 |
|
– щитовидной железы |
22 |
33,8±5,9* |
9 |
17,3±5,2 |
|
Сопутствующая патология ГПДЗ |
54 |
83,1±4,7 |
37 |
71,2±6,3 |
|
Системность атрофического поражения СО ЖКТ |
38 |
58,5±6,1** |
18 |
34,6±6,6 |
|
Симптомы желудочной диспепсии: |
51 |
78,5±5,1 |
36 |
69,2±6,4 |
|
– дистензионные боли |
36 |
55,4±6,2** |
18 |
34,6±6,6 |
|
– спастические боли |
12 |
18,5±4,8 |
17 |
32,7±6,5 |
|
Астено-невротический синдром |
39 |
60,0±6,1* |
21 |
40,4±6,8 |
|
Эпизоды ↓ массы тела |
13 |
20,0±5,0** |
3 |
5,8±3,2 |
|
Продолжительные погрешности в питании |
21 |
32,3±5,8 |
30 |
57,7±6,9# |
Примечание: ↓ – уменьшение; СО ЖКТ – слизистые оболочки желудочно-кишечного тракта; ГПДЗ – гепато-панкреато-дуоденальная зона; различия между группами значимы: * – р<0,05; ** – р<0,025; # – р<0,01.
Таблица 2
Клинические особенности морфогенетических вариантов АП в возрастном аспекте (%)
|
Клинические особенности |
1-я группа |
2-я группа |
||||
|
18–29 лет |
30–44 лет |
45 и старше |
18–29 лет |
30–44 лет |
45 и старше |
|
|
Сопутствующие эндокринопатии, в том числе дисфункции: |
53,6* |
85,7# |
94,4 |
22,2 |
66,7# |
83,3 |
|
– половых желез |
32,1 |
78,6 |
77,8 |
22,2 |
53,3# |
58,3 |
|
– щитовидной железы |
10,7 |
57,1* |
55,6 |
3,7 |
20,0 |
58,3^ |
|
Сопутствующая патология ГПДЗ |
71,4 |
100,0# |
100,0 |
70,4 |
100,0# |
91,7 |
|
Признаки дисплазии СТ |
89,3 |
78,6^ |
44,4 |
77,8 |
73.3 |
66,7 |
|
Системность АП |
46,4 |
78,6# |
100,0 |
44,4 |
66,7 |
91,7 |
Примечание: р<0,05 при сравнении: * – соответствующих возрастных подгрупп 1 и 2-й группы; # – подгруппы 15–29 лет и 30–44 лет внутри своей группы; ^ – возрастной подгруппы 30–44 и 45 лет и старше внутри своей группы.
двенадцатиперстной кишки (7,7%).
Таблица 3
Частота основных патогистологических изменений в СОЖ по передней стенке и малой кривизне (%)
|
Патогистологические изменения |
1-я группа |
2-я группа |
||||||
|
передняя стенка |
малая кривизна |
передняя стенка |
малая кривизна |
|||||
|
ПЯЭ |
ЖЭ |
ПЯЭ |
ЖЭ |
ПЯЭ |
ЖЭ |
ПЯЭ |
ЖЭ |
|
|
Выраженная гиперплазия |
30,6 |
32,7 |
27,6 |
22,4 |
22,7 |
43,2# |
33,3 |
50,0** |
|
Дисплазия |
18,4 |
20,4 |
25,9** |
31,0 |
13,6 |
25,0 |
10,4 |
31,3# |
|
ПКГ |
24,5* |
6,9 |
15,9 |
8,3 |
||||
|
Признаки мукоидизации желез |
55,1 |
60,3 |
84,1* |
* |
70,8 |
|||
|
Признаки структурной атрофии желез: |
77,6 |
89,7 |
68,2 |
83,3 |
||||
|
– ↓ плотности желез |
63,3 |
** |
67,2 |
** |
38,6 |
45,8 |
||
|
– кистозная трансформация |
46,9 |
75,9* |
** |
54,5 |
62,5 |
|||
|
Фавеолярная гиперплазия |
46,9 |
70,7* |
** |
52,3 |
54,2 |
|||
|
↓ толщины СОЖ |
24,5 |
25,9 |
** |
15,9 |
10,4 |
|||
Примечание: ПЯЭ – покровно-ямочный эпителий; ЖЭ – железистый эпителий; ПКГ – париетальноклеточная гиперплазия; ↓ – уменьшение; р<0,05 при сравнении: # –ПЯЭ и ЖЭ одной локализации; * – передней стенки и малой кривизны внутри группы; ** – с другой группой.
Таблица 4
Примечание: ЛФ – лимфоидные фолликулы; р<0,05 при сравнении: # – ПЯЭ и ЖЭ одной локализации; * – тела и антрального отдела внутри группы; ** – с другой группой.
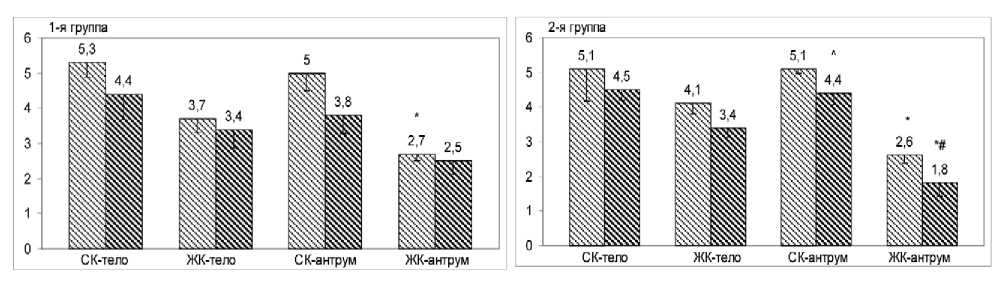
Таблица 5
Оценка выраженности дисрегенераторных изменений в СОЖ по условной 6-балльной шкале
** – соответствующих показателей в другой группе.
Обсуждение
Таким образом, независимо от возможных причинных факторов атрофия предстает как выраженный дис-регенераторный процесс с разнонаправленными нарушениями пролиферации и дифференцировки клеточных популяций СОЖ или дисрегуляторный процесс, вероятно, обусловленный разноуровневыми нарушениями регуляции регенерации. Последние могут быть тесно связаны с характером сопутствующей патологии, в частности дисплазией СТ (высокая частота ее признаков в обеих группах) – важнейшей интегративной системой организма и составляющей сосудисто-эпителио (паренхима-тозно)-стромальных отношений [3]. Дисбаланс в системе TGF- β – TGF β -R1 патогенетически также может быть связан с дисплазией СТ через участие TGF- β в морфогенезе СТ [2]. В качестве еще одного возможного эндогенного фактора метаболической, структурной и функциональной дезорганизации СОЖ может рассматриваться гиперэстрогенемия [9]. Все это значительно расширяет представления о пато- и морфогенетических вариантах
АП в СОЖ, традиционно ассоциирующегося лишь с его А (аутоиммунный) и В (бактериальный) типами [11].
Заключение
Список литературы Клиникохморфогенетические варианты атрофического поражения слизистой оболочки желудка
- Давыдовский И.В. Общая патология человека. -М.: Медицина, 1969. -559 с.
- Кадурина Т.И., Горбунова В.Н. Дисплазия соединительной ткани: руководство для врачей. -СПб.: Элси-СПб, 2009. -704 с.
- Казначеев В.П., Субботин М.Я. Этюды к теории общей патологии. -2-е изд. -Новосибирск: Наука, 2006. -256 с.
- Коваленко В.Л, Казачков Е.Л., Казимирова А.А. Значение некоторых ростовых факторов в патогенезе хронического гастрита у детей//Архив патологии. -2008. -№ 2. -С. 3-5.
- Наумова Л.А., Пальцев А.И., Беляева Я.Ю. Особенности клинико-морфологических проявлений атрофического процесса в желудке при отсутствии и наличии инфицированности H. pylori (I этап)//Экспериментальная и клиническая гастроэнтерология. -2005. -№ 2. -С. 22-28.
- Наумова Л.А., Пушкарев С.В. Соединительная ткань как система: отдельные клинические аспекты//Вестник СурГУ. Медицина. -2009. -№ 3. -С. 45-56.
- Наумова Л.А., Шевчишина О.Ф., Дятлова А.Ю. Отдельные аспекты структурных проявлений ассоциированного с дисплазией соединительной ткани атрофического процесса в слизистой оболочке желудка//Кубанский научный медицинский вестник. -2009. -№ 6 (111). -С. 60-62.
- Наумова Л.А., Пушкарев С.В. Атрофический процесс -клинико-морфологические аспекты (на примере поражения слизистых оболочек бронхов и желудка)//Вестник СурГУ. Медицина. -2010. -№ 5. -С. 98-114.
- Степанов Ю.М., Кушлинский Н.Е. Экспрессия рецепторов эстрогенов и простагландинов группы Е у больных атрофическим гастритом с предраковыми изменениями эпителия//Онкология. -2001. -Т. 3, № 1. -С. 16-8.
- Фролова И.И., Листергази Г.М., Радзинский В.Е. Иммуногистохимические исследования дискератоза и неопластических изменений экзоцервикса при гинекологической патологии//Архив патологии. -2002. -№ 6. -С. 23-6.
- Чернин В.В. Хронический гастрит. -Тверь: Триада, 2006. -304 с.
- Шехтер А.Б., Серов В.В. Воспаление, адаптивная регенерация и дисрегенерации (анализ межклеточных взаимодействий//Архив патологии. -1991. -№ 7. -С. 7-4.
- Blobe G.C., Shiemann, H.F., Lodish H.F. Role of transforming growth factor B in human disease//N. J. Med. -2000. -Vol. 342, No. 18. -P. 1350-358.
- Сoradini D., Casarsa C., Oriana S. Epithelial cell polarity and tumorogenesis: new perspectives for cancer detection and treatment//Acta Pharmacologica Sinica advance online publication 18 April 2011 [Электронный ресурс]. -URL: http://maciej.bioinfo.pl.
- Correa P. Helicobacter pylori and gastric carcinogenesis//Am. J. Surg. Pathol. -1995. -No. 19, Suppl. 1 -P. 37-3.
- Glasgow E., Mishra L. Transforming growth factor-в signaling and ubiquitinatinators in cancer//Endocrine#Related Cancer. -2007. -Vol. 1, No. 15 -P. 59-2.
- Herfs M., Hubert P., Khold N. Transforming growth factor upregulation reduces the density of Langerhance cells in Epithelial Methaplasia by affecting E-cadherin expression//Am. J. Pathol. -2008. -Vol. 172. -P. 1391-402.


